Recientemente ha surgido un importante interés en la epidemiología de las enfermedades inflamatorias intestinales. El presente artículo pretende revisar el método epidemiológico y los diferentes tipos de estudios epidemiológicos, mostrar las ventajas y limitaciones de cada uno de ellos, apoyado en ejemplos en el ámbito de la enfermedad inflamatoria intestinal, para intentar facilitar la comprensión y el análisis de estos estudios.
There has been renewed interest in the recent years, in the epidemiology of inflammatory bowel diseases. The aim of this article is present a review of the epidemiological method and the epidemiological studies, showing the strengths and limitations of each of them, with examples in the field of inflammatory bowel diseases in order to understand and analyse these types of studies.
El manejo de las enfermedades inflamatorias intestinales (EII) ha sufrido una profunda transformación en los últimos tiempos con la generalización de las consultas monográficas o de atención integral y la aparición de nuevos fármacos con posible impacto en la historia natural de la enfermedad. Quizás estos sean los motivos por los que se ha despertado un importante interés en la epidemiología de las EII. En esta revisión se pretende explicar el método epidemiológico y los diferentes tipos de estudios epidemiológicos con ejemplos en el ámbito de la EII, para intentar facilitar la comprensión y el análisis de estos estudios.
Epidemiología. Método epidemiológico. Estudios epidemiológicosLa Epidemiología es la rama de la Medicina que estudia la frecuencia, la distribución y los determinantes de estados y sucesos relacionados con la salud y enfermedad1. Como todo método científico, el método epidemiológico tiene 3fases. En primer lugar, observar o conocer la frecuencia y distribución de las enfermedades. A continuación, los patrones de frecuencia y distribución pueden dar lugar a hipótesis de asociación entre la enfermedad y un determinado factor. Finalmente, se diseña un estudio experimental para verificar o refutar la hipótesis planteada.
Los estudios epidemiológicos se clasifican en descriptivos o analíticos. Los estudios descriptivos valoran la frecuencia y la distribución de las enfermedades en las poblaciones, con relación a las variables de persona, lugar y tiempo. Estos pueden aportar indicios que contribuyan a generar hipótesis sobre asociaciones entre factores de exposición y estados de salud o enfermedad1,2. Los estudios analíticos valoran los determinantes de los estados de salud o enfermedad, comprobando o rechazando las hipótesis generadas por los estudios descriptivos, con el objetivo de identificar factores de riesgo o protectores de una enfermedad1,3. Entre los estudios descriptivos encontramos los estudios ecológicos, realizados sobre poblaciones, y las series de casos y estudios transversales, realizados sobre individuos. Los estudios analíticos pueden ser observacionales (estudios de casos y controles, estudios de cohortes) o intervencionistas (ensayos clínicos, ensayos de campo, ensayos comunitarios).
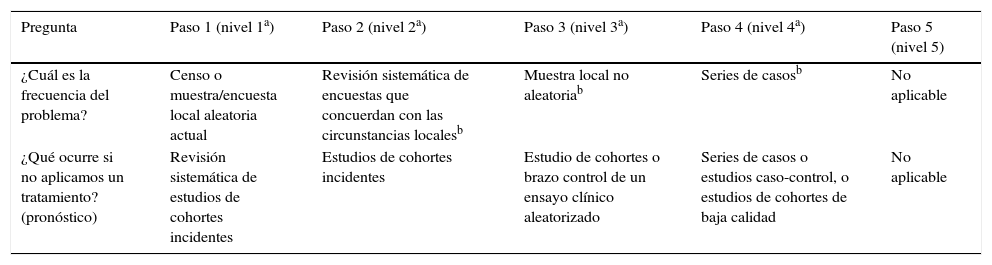
La mejor evidencia científica al analizar la frecuencia de una enfermedad se obtiene a partir de censos o de estudios sobre muestras aleatorias de la población general, y los estudios sobre cohortes de casos incidentes ofrecen la mejor evidencia para describir la historia natural o el pronóstico (tabla 1)4. Independientemente del nivel de evidencia, cada tipo de estudio tiene sus ventajas y limitaciones, que los hacen adecuados para diferentes escenarios. Finalmente, hay dos aspectos claves que influyen en la calidad de un estudio epidemiológico: hay que definir claramente la población de referencia sobre la que se van a extrapolar los resultados del estudio (estudios de base poblacional o de base hospitalaria)5 y los casos deben ser correctamente definidos, con una adecuada selección de las variables por las que se va a definir un proceso y de las escalas de medida que se van a utilizar6–8.
Clasificación de los estudios epidemiológicos según niveles de evidencia
| Pregunta | Paso 1 (nivel 1a) | Paso 2 (nivel 2a) | Paso 3 (nivel 3a) | Paso 4 (nivel 4a) | Paso 5 (nivel 5) |
|---|---|---|---|---|---|
| ¿Cuál es la frecuencia del problema? | Censo o muestra/encuesta local aleatoria actual | Revisión sistemática de encuestas que concuerdan con las circunstancias localesb | Muestra local no aleatoriab | Series de casosb | No aplicable |
| ¿Qué ocurre si no aplicamos un tratamiento? (pronóstico) | Revisión sistemática de estudios de cohortes incidentes | Estudios de cohortes incidentes | Estudio de cohortes o brazo control de un ensayo clínico aleatorizado | Series de casos o estudios caso-control, o estudios de cohortes de baja calidad | No aplicable |
Fuente: Adaptado de OCEBM4.
Los estudios ecológicos (o correlacionales) utilizan datos de poblaciones para comparar la frecuencia de enfermedad entre diversos grupos durante un mismo período, o en un mismo grupo durante períodos diferentes. Las variables de interés pueden ser la edad, el sexo y variables étnicas, socioeconómicas o geográficas1,8.
Su principal ventaja es que pueden realizarse rápidamente y con escasos costes, al basarse en información fácilmente disponible (censos, registros de mortalidad, registros de cáncer, datos de consumo de productos). Suelen ser el primer paso en la investigación de una posible relación entre una exposición y una enfermedad. La posibilidad de realizar un análisis de toda la población hace que sean útiles en el estudio de enfermedades raras1.
Las conclusiones de este tipo de diseño se refieren solo a las poblaciones y no a los individuos. No es posible extrapolarlas a la exposición del individuo y el riesgo de presentar la enfermedad (lo que se conoce como «falacia ecológica»). Los estudios ecológicos tampoco pueden controlar la presencia de variables de confusión1,2,6,8.
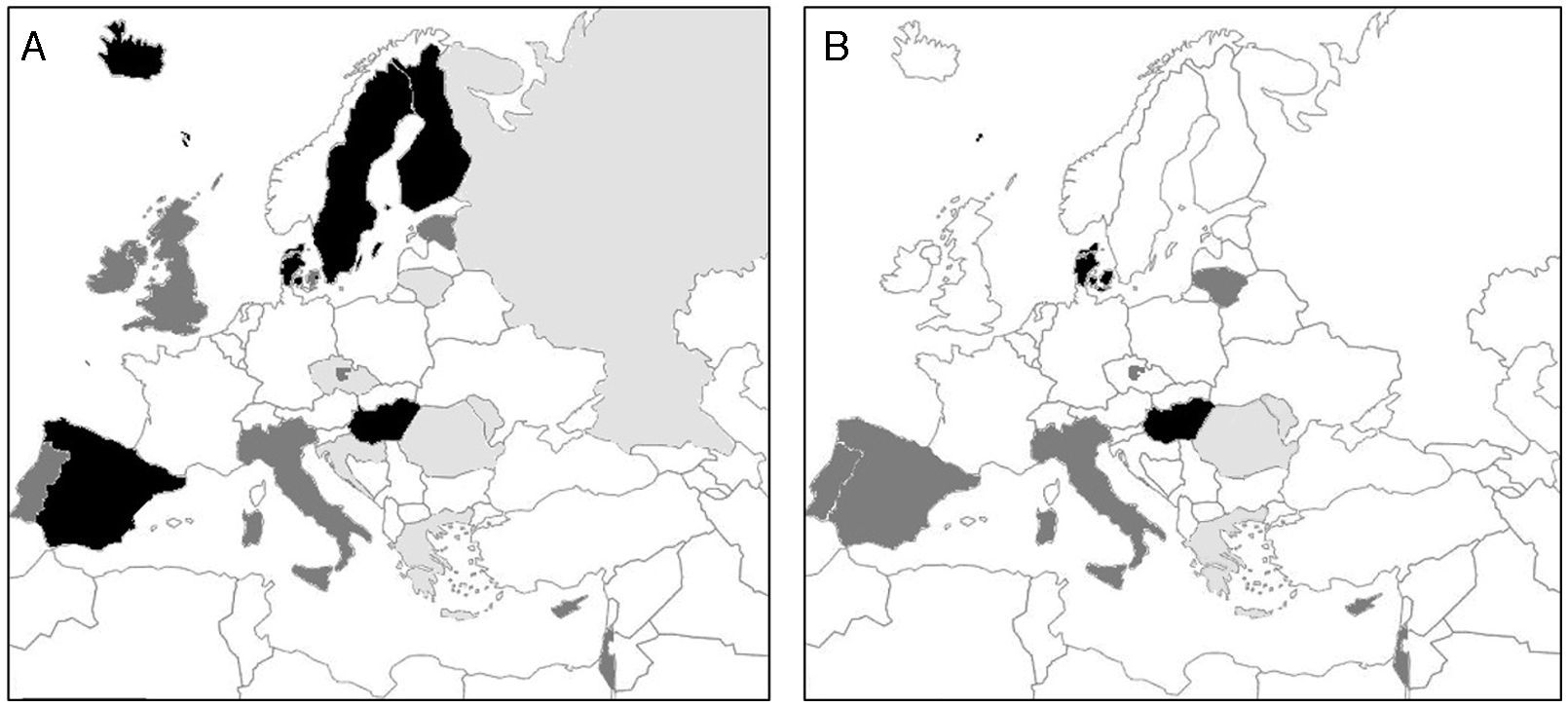
Un ejemplo de estudio ecológico es el estudio de incidencia de EII en Europa, estudio EpiCom. En este proyecto se identificaron todos los nuevos diagnósticos de EII en diferentes áreas geográficas y se crearon 2cohortes de casos incidentes, 2010 y 2011 (fig. 1)9,10. La población diana estaba bien definida y la definición de casos de EII fue uniforme en todos los centros. Así, se realizó una descripción de la incidencia en diferentes zonas geográficas. En la cohorte del año 2010 (31 centros de 22 países) se observó un gradiente este-oeste, de forma que en el oeste la incidencia era aproximadamente el doble que en el este (fig. 1A)9.
Estudios transversalesLos estudios transversales (estudios de prevalencia o en inglés «cross-sectional studies») valoran simultáneamente la exposición y la enfermedad en una población bien definida en un momento determinado1,6,8.
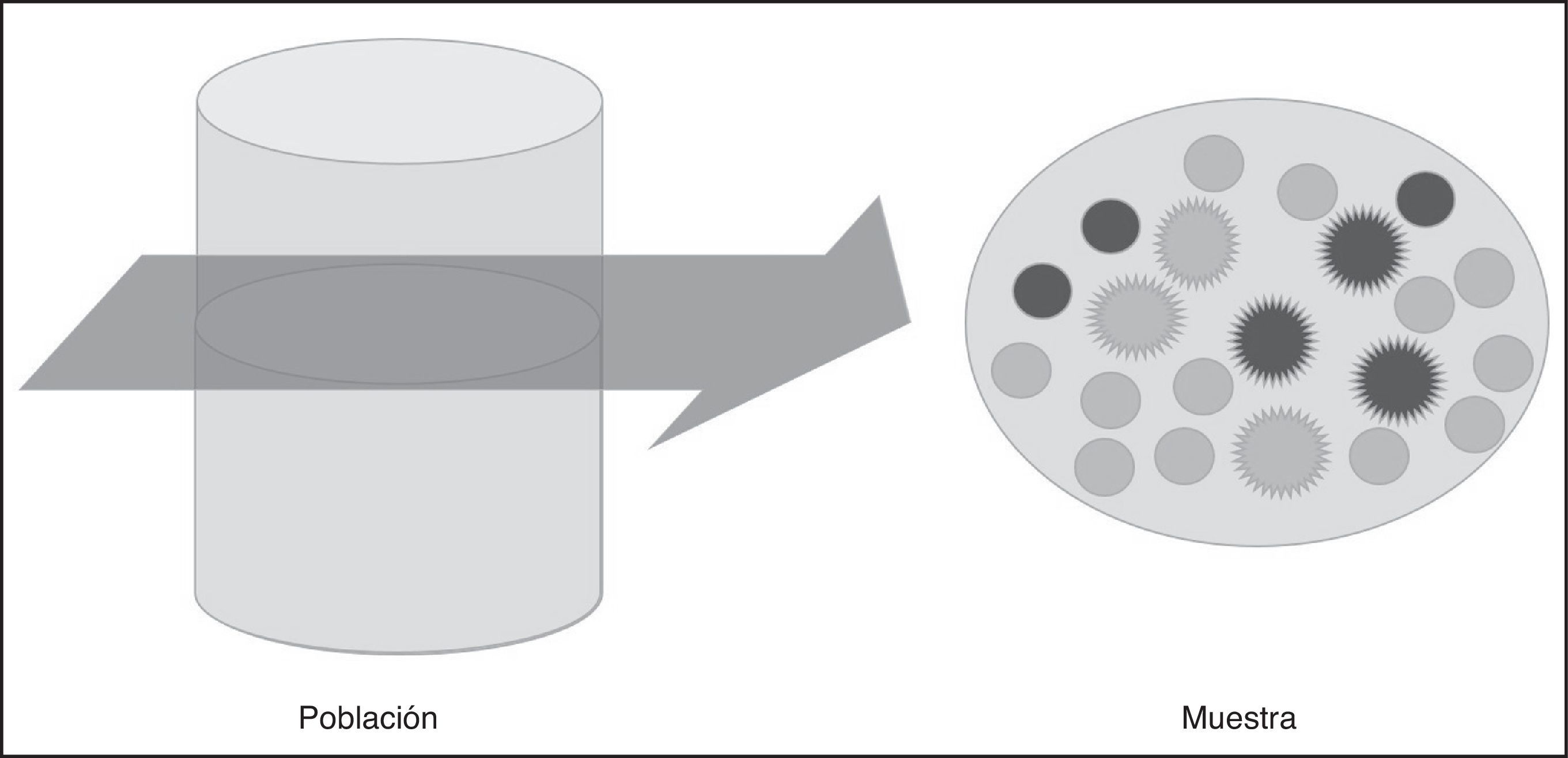
En estos estudios se selecciona una muestra de la población y se analiza la frecuencia de un factor de riesgo y de la enfermedad. Posteriormente, se compara la prevalencia de la enfermedad entre aquellos con el factor de riesgo y los que no lo presentan (fig. 2).
Además de definir correctamente la población de referencia y la definición de los casos, un punto crítico en el diseño de los estudios transversales es la selección de la muestra, que debe ser representativa de la población de referencia.
Son estudios fáciles de ejecutar y relativamente poco costosos. Permiten conocer la prevalencia de enfermedades y de factores de riesgo, incluso estudiar varias enfermedades y factores de riesgo de forma simultánea. Además, son útiles para valorar el estado de salud de una comunidad para determinar sus necesidades2,6,8.
Sin embargo, debido a la medición simultánea del factor de riesgo y de la enfermedad, no permite conocer la secuencia temporal de los acontecimientos y, como consecuencia, no es posible determinar si la exposición precedió a la enfermedad o viceversa. Por esto, únicamente pueden utilizarse como base para formular hipótesis sobre causalidad. Por lo mismo, tampoco permiten diferenciar entre factores de riesgo y factores pronósticos. No son útiles para el estudio de enfermedades raras o de corta duración, con baja prevalencia, ya que, al seleccionar la muestra, el número de casos puede ser tan pequeño que imposibilite el análisis. Por último, la posibilidad de sesgos de selección o de recuerdo (en inglés, «recall bias») es moderada-alta, lo que refuerza la importancia de una correcta definición de los casos y de las variables que se utilizarán para su medida1,2,6,8.
Andreu et al., a partir de la base ENEIDA (www.eneida.org), realizaron un estudio transversal sobre las características de la EII familiar en comparación con la EII esporádica11. Como muestra se seleccionaron todos los pacientes con diagnóstico de colitis ulcerosa (CU) y enfermedad de Crohn (EC) incluidos en la base ENEIDA. La EII familiar (factor de riesgo) se asoció a una edad de diagnóstico más temprana y a un mayor porcentaje de manifestaciones extraintestinales (patrones de enfermedad), y la EC familiar presentaba más frecuentemente un comportamiento penetrante y enfermedad perianal.
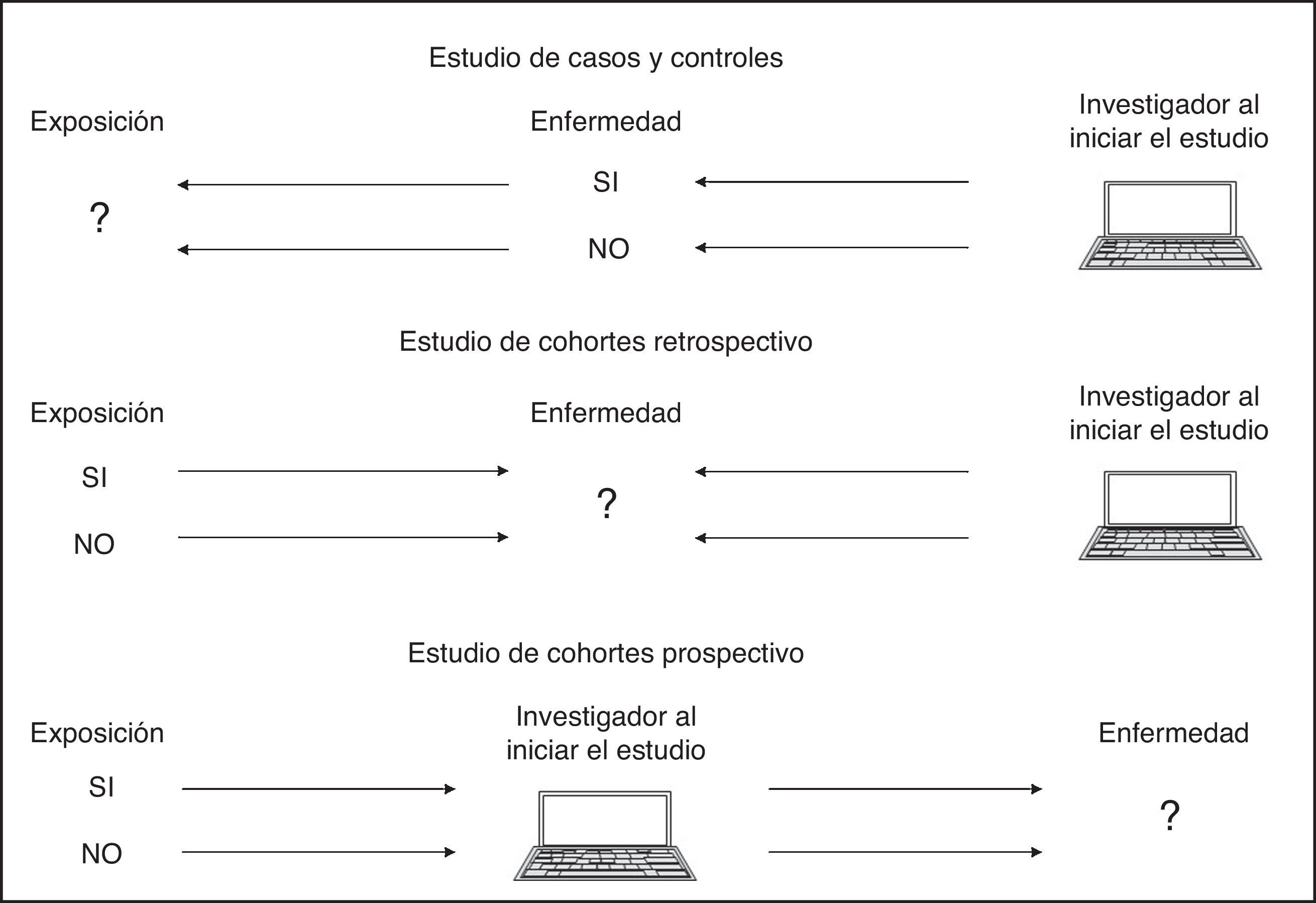
Estudios analíticosEstudios de casos y controlesSe trata de estudios observacionales longitudinales retrospectivos en los que se identifica a personas con una enfermedad (casos) y se comparan con un grupo control apropiado que no tenga la enfermedad (controles), para evaluar la relación entre un factor de exposición y la aparición de la enfermedad6,12. Para estudiar esta relación se compara la frecuencia de exposición a un factor en los casos y la frecuencia de exposición al factor en los controles (fig. 3). El resultado de esta comparación se conoce como «odds ratio» (OR), que nos dice cuánto más frecuente ha sido la exposición a un factor de riesgo en los casos que en los controles. Conceptualmente es diferente al riesgo relativo, pero numéricamente se aproxima a este, sobre todo en enfermedades raras12–14.
Los puntos claves a la hora de diseñar un estudio de casos y controles son la definición de casos, la selección de controles y las fuentes de información sobre la exposición y la enfermedad6,7,12,13. Respecto a la selección de casos, es fundamental establecer de forma clara y explícita la definición de enfermedad, los criterios de inclusión y los criterios de exclusión y, preferiblemente, deberían seleccionarse casos incidentes (de nuevo diagnóstico), ya que los casos prevalentes pueden haber cambiado sus hábitos en relación con la exposición (por ejemplo, si queremos valorar la asociación entre enfermedad inflamatoria y dieta, los casos prevalentes pueden haber cambiado sus hábitos dietéticos tras el diagnóstico de la enfermedad); también es posible que los casos prevalentes sean los supervivientes de los casos incidentes y la supervivencia puede estar influida por la exposición al factor de riesgo (por lo que el porcentaje de casos que tuvieron exposición factor de riesgo estaría infraestimada). La función del grupo control es estimar la proporción de exposición a un factor de riesgo en un grupo que no tiene la enfermedad, debe ser representativo de la población de donde provienen los casos y debe haber tenido el mismo riesgo de exposición al factor en estudio. Por último, las fuentes de información deben ser fiables, con las variables correctamente definidas y recogidas.
Los estudios de casos y controles son útiles para estudiar enfermedades poco comunes o con latencia prolongada. Permiten analizar múltiples factores de riesgo en una misma enfermedad. Se realizan con relativa rapidez y con costes bajos, ya que pueden realizarse con pocos individuos. La fuente de información suele ser accesible (registros, historias clínicas…). Por último, no implican ningún riesgo para los participantes12,13.
Sin embargo, no permiten valorar la incidencia de una enfermedad ni un estudio detallado de los factores causales y, en ocasiones, no puede establecerse claramente la relación temporal entre la exposición y la enfermedad. Además, el riesgo de que se produzcan sesgos es elevado: sesgos de información si las fuentes no son completas, si las variables no están correctamente definidas, o si depende de la memoria del sujeto; sesgo de selección si los casos no están correctamente definidos o los controles no son adecuados7,12,13.
En 2007, Terdiman et al. publicaron un estudio de casos y controles para valorar el efecto del tratamiento con 5-aminosalicilatos (5-ASA) en el riesgo de desarrollar cáncer colorrectal (CCR) en pacientes con EII15. Identificaron los casos de CCR a partir de 2 bases de datos con información sobre diagnósticos, procedimientos y tratamientos farmacológicos. Por cada caso de CCR se seleccionaron de forma aleatoria 20 controles sin CCR, apareados por edad, sexo y año de diagnóstico del caso índice, y se analizaron diferentes variables que incluían diagnóstico de EII, tipo de EII, colonoscopias, hospitalizaciones o consultas médicas en el año previo a la inclusión y tratamiento farmacológico recibido (5-ASA, antiinflamatorios no esteroideos, esteroides o inmunosupresores). Los casos con CCR habían recibido más frecuentemente 5-ASA que los pacientes sin CCR (1,2 vs. 0,4%; OR 3,35; IC 95%: 2,91-3,86). Como se ha comentado, los estudios de casos y controles tienen limitaciones a la hora de establecer una relación causal entre un factor y una enfermedad, y en este trabajo podría deducirse que la asociación entre el consumo de 5-ASA y el desarrollo de CCR es una relación causal, pero también se observó que el diagnóstico de EII previo al CCR era más frecuente en los casos que en los controles (EC: 1,0 vs. 0,1%; OR 6,60: IC 95 5,56-7,82; CU: 1,3 vs. 0,2%; OR 6,72; IC 95%: 5,79-7,81), lo que justifica la asociación entre 5-ASA y CCR.
Un reciente estudio realizado sobre la base ENEIDA ha analizado la incidencia de displasia y CCR en pacientes con CU y sus factores de riesgo16. Se incluyeron los pacientes con CU a los que se había realizado al menos una colonoscopia durante el seguimiento; los casos fueron los pacientes diagnosticados de neoplasia avanzada (displasia de alto grado o CCR) y se tomó como controles a los pacientes sin neoplasia avanzada. Como factores de riesgo independientes se identificaron la colangitis esclerosante primaria (OR 10,90; IC 95%: 3,75-31,76), la colitis extensa (OR 2,10; IC 95%: 1,01-4,38), el diagnóstico de CU a mayor edad (OR 2,23; IC 95%: 1,03-4,83) y la apendicectomía previa al diagnóstico de CU (OR 2,66; IC 95%: 1,06-6,71). Como factores protectores se identificaron la exposición a tiopurinas (OR 0,21; IC 95%: 0,06-0,74) y el participar en un programa de cribado de CCR (OR 0,33; IC 95%: 0,16-0,67). En este estudio el tratamiento con 5-ASA no se relacionó con el riesgo de neoplasia avanzada, pero esta falta de asociación podría justificarse por un amplio uso de 5-ASA en la población de estudio (90%) o por sesgos de información, ya que la base ENEIDA no incluía datos importantes como la duración ni la dosis de tratamiento.
Estudios de cohortesEn este tipo de estudio los individuos se clasifican en 2grupos (cohortes) en función de la presencia o ausencia de exposición a un factor. En el momento de la clasificación todos están libres de la enfermedad de interés y son seguidos durante un período de tiempo para observar la frecuencia de aparición del fenómeno que nos interesa (fig. 3). Son estudios observacionales longitudinales y pueden ser prospectivos o retrospectivos. Los estudios prospectivos se inician antes de la aparición de la enfermedad (en ocasiones antes de la exposición al riesgo) y en los retrospectivos la enfermedad ya ha tenido lugar, pero los pacientes estaban previamente definidos por la exposición al factor de riesgo6,17,18.
Con este tipo de estudios podemos calcular la incidencia de la enfermedad en los expuestos al factor de riesgo y en los no expuestos, y la relación entre ambas incidencias se conoce como riesgo relativo («hazard ratio» en los estudios de supervivencia)19. Cuando la cohorte es homogénea en la exposición al factor de riesgo, el grupo control puede ser una cohorte no expuesta o puede realizarse una comparación con las tasas derivadas de estadísticas vitales (por ejemplo, registros poblacionales de tumores)17. En estos casos, la razón de incidencia se ajusta por edad y sexo, lo que da lugar a la razón estandarizada de incidencia (en inglés «standardized incidence ratio», SIR) o de mortalidad (en inglés «standardized mortality ratio», SMR)19.
Algunos de los puntos clave de un estudio de cohortes son similares a los estudios de casos y controles, pero hay algunos aspectos peculiares que conviene considerar. Tanto los expuestos como los no expuestos deben estar en riesgo (mayor o menor) de desarrollar la enfermedad. La exposición al factor de riesgo debe estar correcta y claramente definida. Los controles (no expuestos) deben ser lo más similares posible a los expuestos, salvo en la exposición al factor de riesgo. Las enfermedades en estudio deben definirse claramente antes de que se desarrollen y esta definición debe ser estable durante el tiempo que dure el estudio. Por último, hay que evitar las pérdidas de seguimiento18.
Los estudios de cohortes permiten describir la incidencia y la historia natural de una enfermedad y establecen la secuencia temporal entre la exposición a un factor de riesgo y la aparición de una enfermedad. Con estos estudios se mide adecuadamente la exposición al factor de riesgo y es posible estudiar diferentes efectos de un mismo factor de riesgo. Por último, son útiles para estudiar el efecto de exposiciones raras6,17,18.
Por contra, necesitan un tamaño muestral elevado y un tiempo de observación prolongado para la obtención de resultados. Su coste es elevado y son de difícil ejecución. Pueden verse influidos por la pérdida de seguimiento de los pacientes y por cambios en los criterios diagnósticos de una enfermedad. Esto hace que no sean adecuados para estudiar enfermedades poco frecuentes o con latencia larga6,17,18.
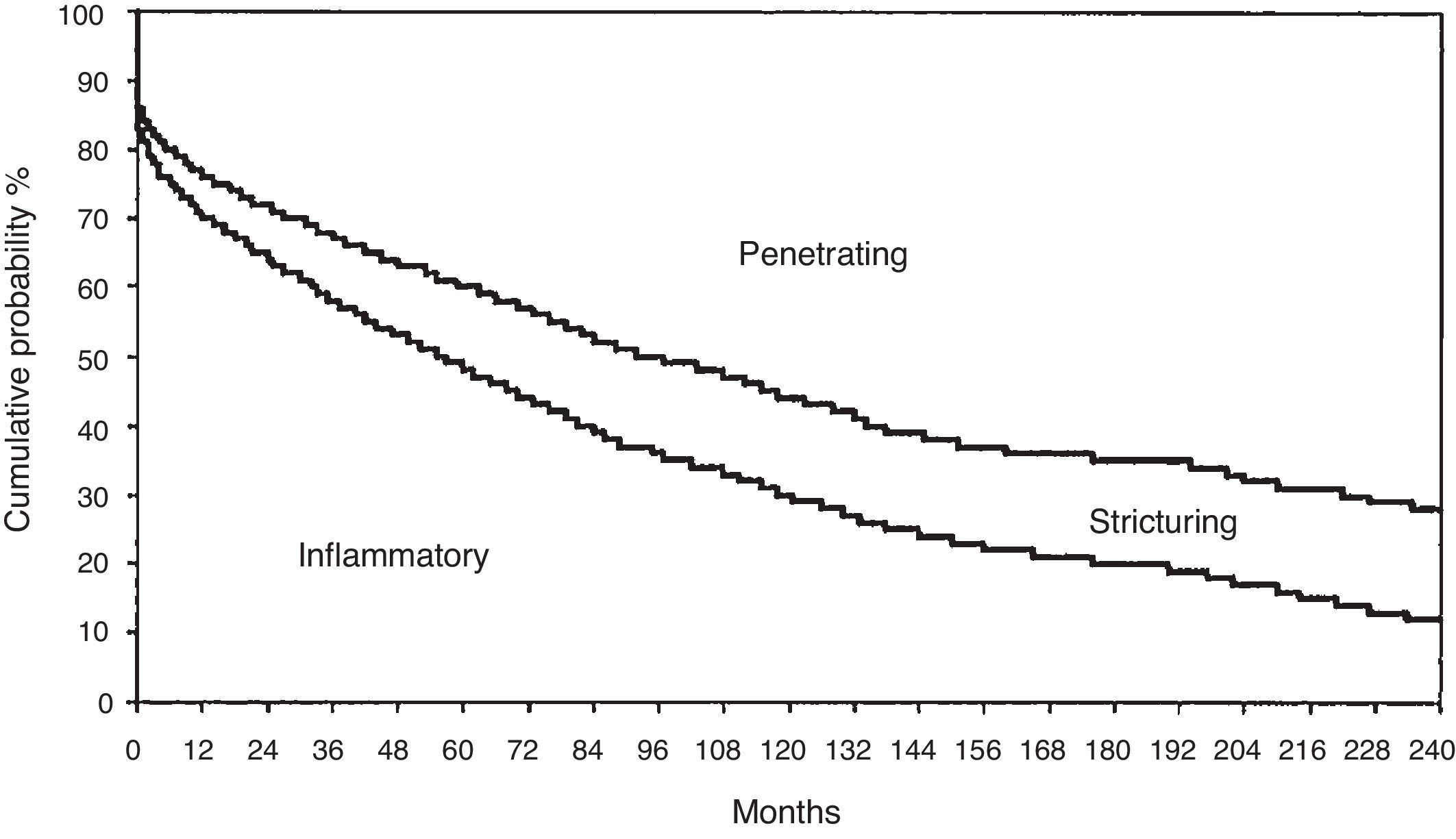
Un ejemplo de estudio de cohortes retrospectivo es el trabajo de Cosnes et al.20, que describe la evolución a largo plazo de la EC. En este estudio se siguió una cohorte de 2002 pacientes con EC y se analizó la aparición de complicaciones (estenosis o fístula/perforación), lo que permitió conocer la evolución de la enfermedad (fig. 4).
Evolución a largo plazo del patrón de la enfermedad en pacientes con enfermedad de Crohn.
Fuente: Reproducido de Cosnes et al.20. Copyright 2002, con autorización de Wolters Kluwer Health, Inc.
Un tipo especial de estudio de cohortes es el estudio de cohortes de casos incidentes (en inglés, «inception cohort study»). En este caso la cohorte es un grupo de pacientes seleccionados en el momento del inicio o al diagnóstico de la enfermedad21. Permite conocer la historia natural de la enfermedad, comparar el desenlace (hospitalización, cirugía, mortalidad) de esta con la población de referencia y realizar estudios anidados. Los estudios anidados utilizan a los participantes en la cohorte incidente, en los que las características basales están bien definidas, y el seguimiento prospectivo reduce la posibilidad de sesgos de selección o de información; los estudios anidados pueden ser de cohortes prospectivos, retrospectivos o de casos y controles.
En estos estudios los pacientes pueden reclutarse en la población general o en hospitales. Las cohortes de base poblacional ofrecen la mejor evidencia científica sobre la historia natural de una enfermedad, porque abarcan desde los casos leves hasta los más graves, aunque hay que tener en cuenta que al hablar de «poblacional» es frecuente que los pacientes se seleccionen en asistencia primaria y que se pierdan pacientes con síntomas leves que no consultan o aquellos con una enfermedad fulminante que fallecen antes de poder buscar asistencia (situación excepcional en EII). Las cohortes de base hospitalaria se centran en un grupo de pacientes con mayor gravedad y su pronóstico puede ser peor, pero si nuestro ámbito de trabajo es el hospital, la información que podemos obtener de ellos puede ser más útil que la que ofrezca una cohorte poblacional.
En las cohortes de casos incidentes un aspecto muy problemático es la pérdida de seguimiento de los sujetos en estudio, lo que limita seriamente las conclusiones del estudio.
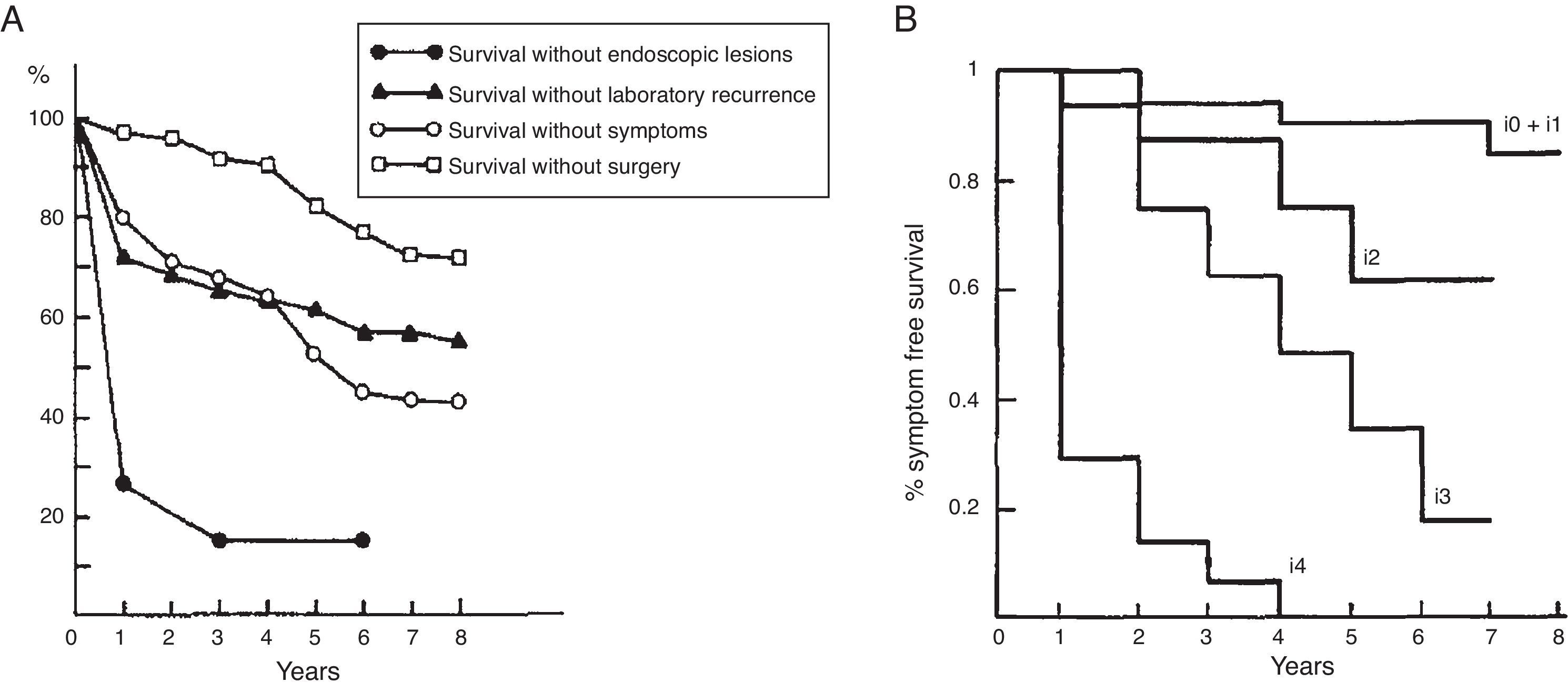
Un ejemplo de estudio de cohortes de casos incidentes es el trabajo de Rutgeerts et al., que valora la recurrencia posquirúrgica en pacientes con EC22. Se incluyeron 89 pacientes operados por enfermedad de Crohn activa. Esta cohorte puede considerarse una cohorte de casos incidentes, pues los pacientes se incluyen inmediatamente después de la resección quirúrgica, con unos criterios de inclusión claramente establecidos, y se realiza un seguimiento prospectivo preestablecido. Aunque se trata de una cohorte de base hospitalaria, este trabajo ha tenido un gran impacto, ya que ha permitido conocer la historia natural de la recurrencia posquirúrgica y la importancia de la recurrencia endoscópica como predictor de la recurrencia clínica (fig. 5).
Recurrencia posquirúrgica. A) Curvas de Kaplan-Meyer de supervivencia libre de recurrencia quirúrgica, clínica, biológica o endoscópica tras la intervención quirúrgica. B) Recurrencia clínica en función de la gravedad de las lesiones en la ileocolonoscopia un año tras la intervención quirúrgica.
Fuente: Reproducido de Rutgeerts et al.22. Copyright 1990, con autorización de Elsevier.
En el estudio EpiCom se está realizando el seguimiento de 2cohortes de casos incidentes (años 2010 y 2011) de base poblacional, que permitirá conocer la evolución de la enfermedad en la época de los fármacos biológicos con el mayor nivel de evidencia posible. Sin embargo, es un buen ejemplo para ilustrar las dificultades y limitaciones de este tipo de estudios. En la cohorte 2010 no se observaron diferencias en el porcentaje de pacientes con EC intervenidos quirúrgicamente entre los países del este y del oeste de Europa en el seguimiento a un año (16 vs. 12%, respectivamente)23 ni a los 3 años (18 vs. 16%, respectivamente)24. En cambio, en la cohorte del año 2011 las tasas de cirugía fueron significativamente diferentes entre los países del este y del oeste en el primer año de seguimiento (24 vs. 7%, respectivamente; p<0,001)25 y al tercer año (28 vs. 11%; p=0,02)26. Estas diferencias entre ambas cohortes pueden justificarse por el hecho de que en la cohorte de 2011 no participaron los países escandinavos, Reino Unido ni Irlanda, en los que tradicionalmente se han descrito mayores tasas de cirugía que en los países del sur de Europa27. Otro problema que queda de manifiesto en estos estudios es la pérdida de seguimiento de los pacientes: en la cohorte de 2010 la pérdida de seguimiento de pacientes con EC a los 3 años fue del 36,4% y en la cohorte de 2011 del 54%, lo que puede limitar la extrapolación de datos a otras poblaciones.
ConclusiónLos estudios epidemiológicos son útiles para investigar posibles causas, factores de riesgo y la historia natural de las enfermedades, y cada tipo de estudio aporta una información diferente con una utilidad particular, con sus ventajas e inconvenientes. Los aspectos fundamentales a la hora de diseñar o interpretar los estudios epidemiológicos son la correcta definición de la población de referencia sobre la que se desea extrapolar los resultados y de los criterios de selección de los casos y controles.
FinanciacionVicent Hernández disfrutó entre el 1 de junio de 2015 y el 31 de mayo de 2016 de una beca de intensificación a cargo del Projecto BIOCAPS, financiado por la Comisión Europea (FP-7-REGPOT 2012-2013-1, Grant agreement n.° FP7-316265).
Conflicto de interesesVicent Hernández ha recibido honorarios por actividades formativas de MSD, AbbVie, Ferring, Shire, Tillots y Otsuka; ha recibido ayudas de desplazamiento de MSD, AbbVie, Ferring, Faes Farma, Shire, Falk Pharma, Tillots, Otsuka y Takeda. Finalmente, ha recibido ayudas para la organización de cursos de MSD, AbbVie, Otsuka y Hospira Biologicals-Pfizer.