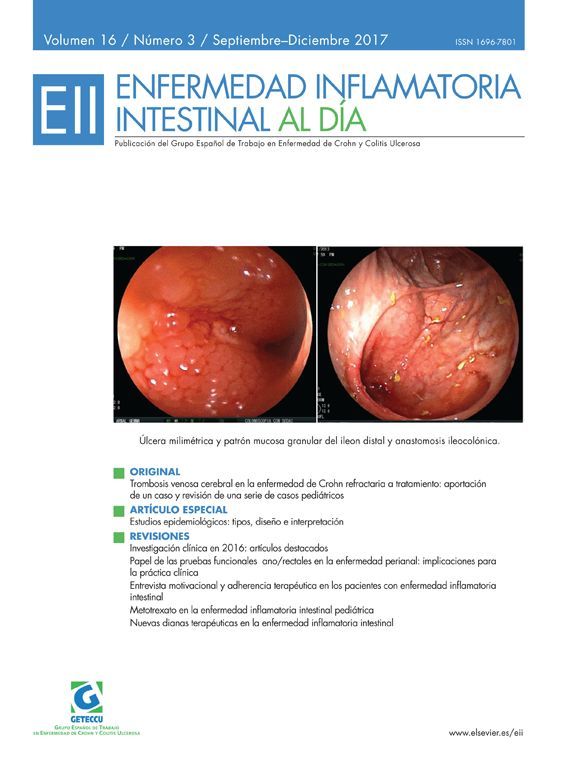
En la enfermedad de Crohn (EC), las estenosis inflamatorias y las posquirúrgicas ocasionan cuadros oclusivos difíciles de manejar. Suele ser necesario optimizar el tratamiento médico y realizar dilataciones endoscópicas, aunque en ocasiones el tratamiento definitivo es la cirugía.
El objetivo del estudio es evaluar la eficacia de la inyección local de infliximab en pacientes con EC con estenosis inflamatorias (primarias o de la anastomosis) en nuestro centro.
Material y métodosEstudio prospectivo de 17pacientes. Criterios de inclusión: EC con clínica oclusiva, con estenosis inflamatorias de menos de 5cm de longitud confirmadas por entero RM no franqueables con colonoscopio convencional. Se inyectaron 30mg de infliximab por sesión endoscópica en los 4 cuadrantes de la estenosis, con una media entre sesiones de 6semanas.
ResultadosDiecisiete pacientes: 12 hombres y 5 mujeres, con una edad media de 44,1años. Evolución media de la EC: 12,2años. Estenosis de la anastomosis: 64,7%; estenosis primarias: 35,3% (2 ileales, 2 colónicas, una pilórica y una estomal). El 88,2% seguían tratamiento biológico. Número medio de sesiones: 4 (rango 1-12). Se han realizado 3 dilataciones neumáticas. Respuesta completa: 35,3%; respuesta parcial: 41,1%; no respuesta: 23,5%. Los respondedores han mantenido la respuesta tras un seguimiento medio de 23,3meses. No se han registrado efectos secundarios.
ConclusiónLa inyección local de infliximab tópico en las estenosis de la EC puede ser una terapia complementaria a la dilatación endoscópica y una alternativa a la cirugía, segura y bien tolerada.
Inflammatory and postsurgical stenosis of Crohn's disease (EC) can cause occlusive symptoms difficult to manage. Optimizing medical treatment and endoscopic dilatation is usually necessary; although sometimes the definitive treatment is surgery. The objective of this study is to evaluate the efficacy of local infliximab injection in patients with Crohn's disease with inflammatory stenosis (primary or postsurgical) in our center.
Material and methods17patients were included prospectively. Inclusion criteria: Crohn's disease with occlusive symptoms, inflammatory stenosis less than 5cm length studied by MR, non permeable with normal colonoscopy. 30mg of infliximab were injected in each endoscopic session, in all 4 sides of stenosis. The sessions were repeated with a median of 6weeks.
Results17patients (12 male, 5 female). Median age: 44.1years old. Median evolution of disease: 12.2years. Stenosis of the anastomosis: 64.7%, primary stenosis: 35.3% (2 ileal, 2 colon, 1 pyloric, 1 stoma). 88.2% were treated with biological drugs. Median number of endoscopic sessions: 4, R (1-12). 3 pneumatic dilatation. Complete response: 35.3%; partial response: 41.1%; non response: 23.5%. Responders have maintain sustained response along a median follow up of 23.3months. No adverse events have been registered.
ConclusionTopical injection of infliximab in luminal stenosis of Crohn's disease can be a complementary therapy to endoscopic dilatation and an alternative for surgery; safe and well tolerated.
Los pacientes con enfermedad de Crohn (EC) luminal que presentan estenosis inflamatorias son un grupo de enfermos que puede ser difícil de manejar, y en ocasiones se necesita un abordaje terapéutico multidisciplinar que aplique distintos tratamientos tópicos y sistémicos.
A priori existen 2 grupos de estos pacientes: los nunca intervenidos, con una estenosis inflamatoria en la luz intestinal de distinta localización, y aquellos ya sometidos a una resección quirúrgica por su EC y que presentan una recurrencia poscirugía en forma de estenosis inflamatoria de la anastomosis.
Todos ellos suelen presentar episodios suboclusivos de repetición, a pesar de un tratamiento sistémico médico adecuado, que merman claramente su calidad de vida, requiriendo con frecuencia de la cirugía para solucionar el problema local1,2. Esto es especialmente importante en los casos de pacientes que ya han sido resecados con anterioridad.
El objetivo de este estudio es valorar si este grupo de enfermos, al margen de un tratamiento farmacológico sistémico, podrían beneficiarse de la inyección local de infliximab a nivel de la estenosis con el fin de evitar la opción quirúrgica.
Material y métodosSe incluyeron de forma prospectiva (desde mayo de 2012 hasta junio de 2015) 17 pacientes diagnosticados de EC, con cuadros suboclusivos de repetición secundarios a estenosis inflamatoria refractaria a terapia biológica.
A todos los pacientes se les realizó una entero RM para valorar la longitud de la estenosis. Los criterios de inclusión fueron: estenosis con componente inflamatorio evaluadas por entero RM (engrosamiento mural, hipercaptación y realce patológico, focos de hiperseñal rodeados de halo edematoso)3-5, tener una longitud inferior o igual a 5cm, y no ser franqueables con el colonoscopio (Olympus, serie 180, procesador EXERA II).
Las características de los pacientes de la serie se describen en la tabla 1.
Tabla descriptiva de los pacientes
| Pacientes (n=17) | |
|---|---|
| Edad media | 44,1 años. Rango (18-67) |
| Sexo | 12 hombres, 5 mujeres |
| Clasificación de Montreal | A1:1; A2: 15; A3: 1 L1: 9; L2: 6; L3: 1; L4: 1 B1: 12; B2: 1; B3: 4 EPA: 8 |
| Tratamiento biológico en el momento de la inclusión Infliximab Adalimumab Certolizumab Ustekinumab Tratamiento inmunomodulador Azatioprina Metotrexato | 2 10 2 1 2 2 |
| Evolución media de la enfermedad | 12,2 años |
| Estenosis de la anastomosis Estenosis primarias | 11 6 (2 íleon, 2 colon, 1 píloro, 1 estoma) |
La evolución media de la EC era de 12,2años.
Once de las estenosis (64,7%) eran de la anastomosis quirúrgica.
Previo al inicio del tratamiento endoscópico, 15 pacientes (88,2%) estaban en tratamiento biológico (2 pacientes con infliximab, 10 con adalimumab, 2 con certolizumab pegol y uno con ustekinumab). Los 2 restantes no estaban en tratamiento biológico, uno por presentar un antecedente reciente de melanoma cutáneo y el otro por haber presentado efectos adversos con infliximab y adalimumab.
Cinco pacientes (33%) estaban intensificados (uno con infliximab y 4 con adalimumab). Los 2 pacientes en tratamiento con certolizumab pegol seguían un mantenimiento con 200mg cada 15días, y el paciente en tratamiento con ustekinumab seguía una pauta de 45mg cada 15días.
El 23,5% de los pacientes llevaban tratamiento con inmunomoduladores (2 pacientes con metotrexato y otros 2 con azatioprina).
La exploración endoscópica se realizó —bajo sedación profunda— en el gabinete habitual de exploraciones, utilizando midazolam y propofol en bomba de perfusión target control infussion (TCI). Los pacientes fueron sedados por el anestesista o la enfermera de sedación de la unidad de endoscopias capacitada para tal fin.
Todos habían seguido previamente el protocolo estándar de preparación para colonoscopia habitual en nuestro centro (preparación intestinal con Moviprep® o Citrafleet®).
La preparación de la inyección de infliximab (Remicade®) se realizó en el servicio de farmacia de nuestro hospital, que identificó por paciente y lote el administrado. Una vez reconstituido el vial de infliximab (reconstitución del mismo en 10ml de agua bidestilada para inyección), se extrajeron 30mg, que fueron diluidos en 10ml de suero fisiológico, tendiendo a utilizar el remanente de los viales sobrantes preparados ese día. Un paciente recibió una dosis de 60mg, y 2 pacientes recibieron 2 dosis de 100mg de infliximab diluidos en 20cc de suero fisiológico.
Se accedía a la estenosis inflamatoria con el colonoscopio convencional y, utilizando una aguja de inyección interject contrast (Injection Therapy Neddle Catheter. Boston Scientific), se inyectaban intramucosa 30mg de infliximab repartidos en los 4 cuadrantes de las mismas.
En los casos que requirieron dilatación por persistencia de la clínica obstructiva, esta se realizó bajo control endoscópico y radiológico utilizando una sonda balón de dilatación neumática con guía (CRE Wireguided Balloon Dilatation Catehter. Boston Scientific), dilatando un minuto de forma progresiva desde 10 hasta 15mm de diámetro máximo.
Se definió la respuesta al tratamiento de la siguiente manera:
- 1.
Respuesta completa: pacientes en los que desapareció la clínica oclusiva y la estenosis se franqueó con el colonoscopio.
- 2.
Respuesta parcial: pacientes en los que desapareció o mejoró la clínica oclusiva y la estenosis no pudo ser franqueada con el colonoscopio, pero mejoró el componente inflamatorio de la misma.
- 3.
No respuesta: pacientes sin mejoría.
De todos ellos se evaluaron eventuales efectos secundarios derivados del procedimiento endoscópico y de la inyección local de infliximab.
ResultadosSe evaluaron 17 pacientes: 12 hombres y 5 mujeres, con una edad media de 44,1años (rango 18-67años). El tiempo medio de seguimiento fue de 23,3meses.
El número medio de sesiones endoscópicas realizadas por paciente fue de 4 (rango 1-12), separadas entre ellas una media de 6 semanas (rango 4-12).
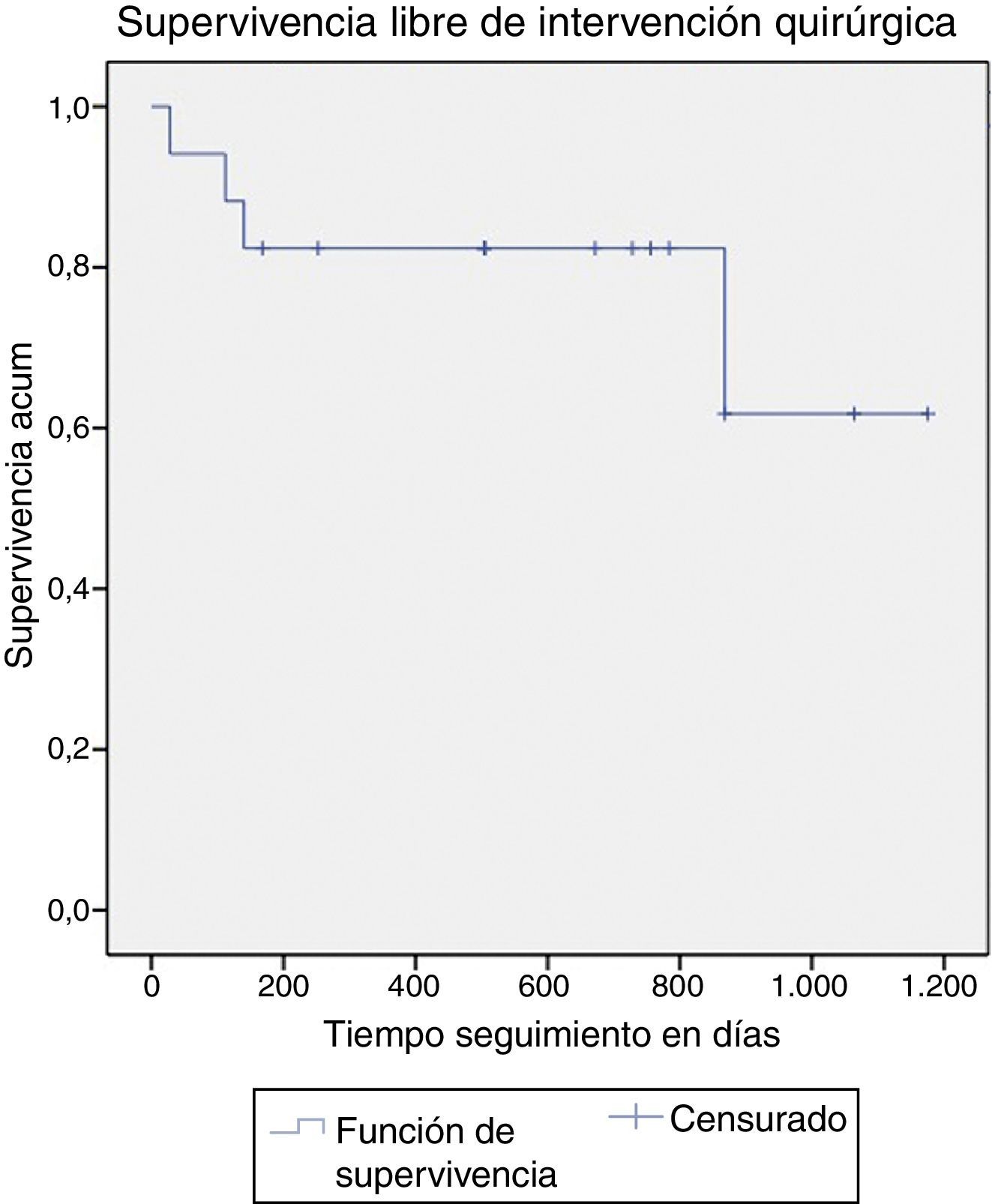
El 76,4% de los pacientes respondieron a la inyección local de infliximab, siendo la respuesta completa en el 35,3% de los casos y parcial en el 41,1%; el 23,5% no respondieron al tratamiento tópico con infliximab y fueron intervenidos (tabla 2 y fig. 1).
A lo largo del seguimiento, en 7 pacientes se intensificó el tratamiento anti-TNF y en 8 se cambió el tratamiento biológico (4 a otro anti-TNF y 4 a otro biológico con un mecanismo de acción diferente, el ustekinumab).
No se registraron efectos secundarios locales ni sistémicos con la administración de infliximab tópico. No hubo ninguna complicación derivada del proceso endoscópico, y todas las exploraciones fueron bien toleradas por los enfermos.
Pacientes con respuesta completaDe los 6pacientes que respondieron de forma completa, 2 presentaban una estenosis de la anastomosis, 3 una estenosis luminal, y uno una estenosis a nivel del estoma.
El número medio de sesiones endoscópicas que se realizaron en estos pacientes fue de 5 (rango 1-12). En 2 de estos pacientes se realizaron 4 sesiones: 2 de 30mg y otras 2 posteriores de 100mg de infliximab por respuesta parcial, tras las cuales los pacientes obtuvieron respuesta completa, manteniendo la mejoría clínica y la permeabilidad de la estenosis. Un paciente requirió 7 sesiones endoscópicas a lo largo del seguimiento y no seguía tratamiento biológico por haber presentado un antecedente reciente de melanoma cutáneo.
Durante el seguimiento, en un paciente se intensificó el tratamiento biológico y en 2 se cambió de agente biológico, manteniendo la mejoría clínica y la permeabilidad de la estenosis en el último control.
Por tanto, en el 50% de estos pacientes, la inyección local de infliximab induce la respuesta completa sin necesidad de modificar la pauta del tratamiento biológico.
Pacientes con respuesta parcialDe los 7 pacientes con respuesta parcial, 2 (28,5%) presentaban una estenosis luminal y 5 (71,4%) una estenosis de la anastomosis, de los que 3 requirieron dilatación de la misma con balón neumático y, posteriormente, inyección local de infliximab intralesional. El número medio de sesiones en los pacientes de este grupo fue de 5 (rango 2-12). Tres de los pacientes fueron cambiados de tratamiento biológico a lo largo del seguimiento, 2 de ellos a un fármaco con otro mecanismo de acción (ustekinumab).
Pacientes sin respuestaLos 4 pacientes que se intervinieron estaban ya operados y presentaban estenosis de la anastomosis. Dos pacientes se intervinieron tras no objetivar mejoría tras 3 y 5 sesiones endoscópicas, respectivamente. Un paciente no experimentó mejoría tras una sesión endoscópica y se intervino de urgencia al ingresar por oclusión intestinal.
Todos seguían tratamiento con adalimumab antes del inicio del tratamiento endoscópico (3 de ellos intensificados con 40mg semanales). En 2 de los pacientes el tratamiento con adalimumab no se modificó a lo largo del seguimiento. Al último paciente se le cambió el tratamiento con adalimumab por certolizumab coincidiendo con el inicio de las sesiones endoscópicas. Tras 2 sesiones de inyección de infliximab tópico y habiendo transcurrido 16semanas desde el cambio de tratamiento biológico, el paciente no experimentó ninguna mejoría clínica ni endoscópica, realizándose finalmente la tercera resección ileal segmentaria.
Por tanto, globalmente, esta intervención endoscópica ha sido eficaz en el 72,2% de los pacientes, que han mantenido la respuesta completa o parcial tras una media de seguimiento de 23,3meses. Al mismo tiempo que se han realizado las sesiones de inyección de infliximab tópico sobre las estenosis, o durante el seguimiento, al 22,2% de los pacientes se les ha intensificado el tratamiento biológico, y al 16,6% se les ha cambiado a otros nuevos fármacos biológicos no anti-TNF.
En las figuras 2 y 3 se muestra una curva de supervivencia libre de intervenciones quirúrgicas y libre de nuevas intervenciones endoscópicas, respectivamente.
DiscusiónEn la EC las estenosis inflamatorias y las derivadas de la cirugía son un problema real en la práctica clínica, que ocasionan a los pacientes cuadros suboclusivos de repetición a pesar de los tratamientos médicos de los que disponemos.
Las estenosis en la enfermedad inflamatoria intestinal son el resultado de la respuesta cicatricial a la inflamación crónica de la pared intestinal con fibrosis, que produce un estrechamiento de la luz intestinal6,7. La estenosis luminal es más frecuente en la EC que en la colitis ulcerosa, dada su afectación transmural. Pueden aparecer en cualquier parte del tracto digestivo, pero son más habituales en el íleon terminal, la anastomosis ileocolónica y en el marco cólico8. En la EC las estenosis más frecuentes son las posquirúrgicas, a nivel de la anastomosis ileocolónica8.
Representan un reto en el manejo terapéutico, que generalmente requiere la participación conjunta medicoquirúrgica. Suele ser necesario optimizar los tratamientos biológicos y realizar dilataciones endoscópicas, aunque a veces el tratamiento definitivo es el quirúrgico.
Existen muy pocas evidencias acerca de la utilidad de la inyección de fármacos en las estenosis de la EC.
Con el objetivo de disminuir la inflamación y, consecuentemente, la fibrosis secundaria de las estenosis en la EC, se han publicado los resultados de algunos estudios evaluando distintos tratamientos tópicos. Los corticoides han sido los más utilizados. Si bien algunas series con triamcinolona o con betametasona tras dilatación con balón encontraban mejoría en un porcentaje de pacientes superior al 80%9,10, un estudio controlado con placebo tras dilatación endoscópica, que incluía a 13pacientes, no encontró reducción del tiempo hasta una nueva dilatación, e incluso se observó tendencia hacia una peor evolución en los pacientes tratados con inyección de esteroides11.
Se han realizado algunos estudios evaluando la eficacia de la inyección de infliximab tópico en la enfermedad perianal. Poggioli et al.12 incluyeron 15pacientes con fístulas perianales complejas a los que se les inyectó sobre las mismas infliximab (15-21mg), consiguiendo su resolución en 10pacientes. La inyección intraarticular de infliximab ha mostrado su eficacia en la artritis reumatoide y en la artritis inflamatoria aguda13,14. Partiendo de estas observaciones, se ha sugerido que la inyección directa de infliximab en una estenosis luminal puede mejorar el grado de inflamación, con la consiguiente mejoría del edema de la submucosa, permitiendo una dilatación de la luz intestinal.
Publicaciones recientes han valorado la inyección de infliximab en las estenosis mediante endoscopia. Swaminath15 recoge una pequeña serie de 3pacientes con EC refractarios a tratamiento médico (infliximab intravenoso) en los que la dosis utilizada fue de 90-120mg repartidos en 10mg por inyección. Se inyectó infliximab circunferencialmente sobre las 3 estenosis. Todos presentaron mejoría durante 4-7meses y no requirieron nuevas actuaciones sobre las estenosis. En la serie publicada por Biancone16 se incluyeron 8pacientes con recurrencia posquirúrgica a los que se les realizó inyección local de infliximab en las lesiones de la mucosa perianastomótica, con una dosis media de 30mg por sesión. En 3 de los 8pacientes se observó una mejoría endoscópica, manteniéndose en remisión durante el periodo de seguimiento (rango 14-21meses desde la inyección).
Recientemente en el año 2014 se ha comunicado una serie del grupo de Hendel et al.17 en la que se incluyeron 6 pacientes con estenosis inflamatorias en EC. Todos ellos fueron tratados con dilatación endoscópica mediante balón, con posterior inyección de 40mg de infliximab; en 5 de ellos se consiguió mejoría clínica y endoscópica sin necesidad de nueva inyección en los siguientes 6meses.
No existen estudios controlados que evalúen la eficacia de la inyección local de infliximab en las estenosis inflamatorias de la EC. Nuestra serie de 17pacientes expresa la realidad del difícil manejo de este tipo de enfermos. Más de la mitad han sido ya intervenidos y presentan una estenosis de la anastomosis. Son pacientes que, a pesar de recibir tratamiento biológico, tienen una mala calidad de vida por la clínica oclusiva que presentan. Probablemente este grupo de pacientes se podría beneficiar además de algún tratamiento local sobre la estenosis. En nuestra serie, paralelamente al inicio de las sesiones de inyección local de infliximab, o durante el seguimiento, se ha intensificado o cambiado el tratamiento biológico al 38,8% de los pacientes, optimizando así al máximo el tratamiento médico que siguen.
ConclusionesLa inyección local de infliximab sobre las estenosis inflamatorias ha demostrado en nuestra serie ser útil en más del 70% de nuestros pacientes, al desaparecer o mejorar su clínica oclusiva. Esta mejoría se ha mantenido a lo largo de todo el seguimiento y, por tanto, se ha obviado la cirugía en un porcentaje importante de enfermos.
Esta aproximación terapéutica requiere del trabajo conjunto de gastroenterólogos, endoscopistas y cirujanos. Es una técnica segura y bien tolerada, sin haber objetivado efectos secundarios ni complicaciones derivadas de la misma, y probablemente sea de utilidad en este escenario clínico tan concreto como complejo.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.