Actualizar las recomendaciones sobre la profilaxis postexposición ocupacional y no ocupacional, facilitando su uso apropiado desde el punto de vista asistencial.
MétodosEste documento ha sido consensuado por un panel de expertos de la SPNS, de GESIDA, de la SEMST y de diferentes sociedades científicas relacionadas, tras revisar los resultados de eficacia y seguridad de ensayos clínicos, estudios de cohortes y de farmacocinética publicados en revistas biomédicas (PubMed y Embase) o presentados a congresos, y diferentes guías clínicas. La fuerza de la recomendación y la gradación de su evidencia se basan en los criterios del sistema GRADE.
ResultadosSe han elaborado unas recomendaciones para la valoración del riesgo de transmisión en los diferentes tipos de exposición; de las situaciones en las que debe recomendarse la profilaxis postexposición; de las circunstancias especiales a tener en cuenta; de las pautas de antirretrovirales, con su inicio y duración; del seguimiento precoz de la tolerancia y adherencia del tratamiento; del seguimiento posterior de las personas expuestas, independientemente de que hayan recibido profilaxis postexposición o no, y de la necesidad del apoyo psicológico.
ConclusionesEn este documento se actualizan las recomendaciones previas respecto a la profilaxis postexposición ocupacional y no ocupacional, tanto en adultos como en niños.
This consensus document is an update of occupational and non-occupational prophylaxis guidelines in HIV-patients, promoting appropriate use of them, from the standpoint of care.
MethodsThis document has been approved by expert panel of SPNS, GESIDA, SEMST and different scientific societies related, after reviewing the results of efficacy and safety clinical trials, cohort and pharmacokinetic studies published in biomedical journals (PubMed and Embase) or presented at conferences and different guidelines. The strength of the recommendation and gradation of their evidence are based on the GRADE system.
ResultsWe have developed recommendations for assessing the risk of transmission in different types of exposure situations in which post-exposure prophylaxis should be recommended, special circumstances to consider, patterns of antiretroviral with the start and duration of early monitoring of tolerance and adherence to treatment, the subsequent monitoring of exposed persons regardless of whether they received post-exposure prophylaxis or not, and the need of psychological support.
ConclusionsThese new guidelines updated previous recommendations regarding occupational post-exposure prophylaxis and non-occupational, in adults and children.
La profilaxis postexposición (PPE) puede ser una medida secundaria para prevenir la infección por el virus de la inmunodeficiencia humana (VIH) cuando la prevención primaria ha fallado. La PPE se aconseja en personas con una exposición de riesgo al virus de la inmunodeficiencia humana (VIH) esporádica y excepcional.
Este documento de consenso sobre las recomendaciones de las PPE ocupacional y no ocupacional pretende ser un documento técnico para los profesionales sanitarios. Su principal objetivo es facilitar el uso apropiado de la PPE. Para ello, se han elaborado unas recomendaciones para la valoración del riesgo de transmisión en los diferentes tipos de exposición, de las situaciones en las que debe recomendarse la PPE, de las circunstancias especiales a tener en cuenta, de las pautas de antirretrovirales (ARV) con su inicio y duración, del seguimiento precoz de la tolerancia y adherencia del tratamiento, del seguimiento posterior de las personas expuestas independientemente de que hayan recibido PPE o no, y de la necesidad del apoyo psicológico.
El documento va dirigido a todos los profesionales que trabajan en la práctica clínica en el ámbito de la infección por VIH.
Para la elaboración de este documento se constituyó un grupo de expertos compuesto por especialistas en medicina interna-infectología, medicina del trabajo, medicina preventiva, pediatría y medicina de urgencias y emergencias, con experiencia en el ámbito de la infección por VIH, actuando 3 miembros del panel como coordinadores. Cada miembro del panel ha aceptado participar de forma voluntaria y altruista.
Cada redactor realiza una revisión de la evidencia científica (última revisión febrero de 2015) disponible de cada uno de los aspectos que se incluyen en el documento y, con ella, escribe su capítulo que es discutido y revisado por los revisores asignados. Una vez compilado el documento, se remite a todos los miembros del panel para su discusión. Posteriormente, se realiza una reunión de consenso de todo el panel y se somete a la revisión externa, exponiéndose durante un periodo de tiempo en la web de las entidades promotoras para que los y las profesionales a los que va dirigido y cualquier persona interesada pueda sugerir matices o cambios, decidiendo el panel a posteriori su inclusión o no.
Para la valoración de la calidad de la evidencia y la graduación de las recomendaciones se ha utilizado el sistema Grading of Recommendations of Assessment Development and Evaluations (GRADE)1.
Para la elaboración de los capítulos se ha realizado una búsqueda bibliográfica en las siguientes bases de datos: Medline, Pubmed, UpToDate,Web of Science, Registro Cochrane y MD Consult, incluyendo artículos desde el año 2000 a 2014. También se han consultado las últimas guías clínicas de la Secretaría del Plan Nacional sobre el Sida; CDC Guidelines; New York State Department of Health AIDS Institute; World Health Organization.
Transmisión ocupacional: VIH, VHB, VHCRiesgo y fundamentosEl riesgo de transmisión de VIH, virus de la hepatitis C (VHC) y virus de la hepatitis B (VHB) en una exposición ocupacional (EO) existe, y difiere en función al fluido al que se exponga el profesional. Para el VIH, estudios prospectivos realizados en trabajadores sanitarios han estimado el riesgo medio de transmisión después de una exposición percutánea a sangre en un 0,3% (IC95%: 0,2-0,5%)2. El riesgo de transmisión después de una exposición a otros fluidos o tejidos no se ha cuantificado, pero es probable que sea considerablemente inferior al del contacto con sangre.
La incidencia media de seroconversión después de una exposición percutánea con una fuente positiva al VHC es del 1,8% (rango: 0-7%)3.
La infección accidental por el VHB constituye un riesgo ocupacional bien establecido para los profesionales sanitarios si no están vacunados frente a este virus. El riesgo de adquirir una infección por VHB, ante un accidente percutáneo en personal no vacunado, depende de los marcadores de la persona de la que procede la sangre o el fluido corporal. En estudios realizados en trabajadores sanitarios con exposición percutánea a sangre contaminada por el VHB el riesgo de transmisión es al menos del 30% si el paciente fuente es Ag HBs positivo con Ag HBe positivo y menor del 6% si el Ag HBe es negativo2.
La PPE se plantea como una estrategia de prevención biomédica2,3. Sin ninguna duda, la mejor forma de prevenir la transmisión ocupacional es evitar la exposición. Para ello, cada institución debería promover la asignación de recursos para:
- a)
La educación y el entrenamiento de todo el personal en las precauciones universales. Incluyendo la vacunación frente a VHB (artículo 8 del Real Decreto 664/1997 sobre protección de los trabajadores contra riesgos relacionados con la exposición a agentes biológicos durante el trabajo) y la gestión adecuada de residuos, que se deben seguir ante cualquier situación de riesgo de contacto con líquidos potencialmente contaminados, como sangre o cualquier fluido o tejido contaminado con sangre, semen, flujo vaginal, líquido cefalorraquídeo, sinovial, pleural, peritoneal, pericárdico o amniótico.
- b)
Disponer de los materiales necesarios para actuar como barrera (guantes, mascarillas, batas y gafas protectoras), así como contenedores de material desechable potencialmente contaminado y dispositivos de seguridad (implantados en varias comunidades autónomas, por trasposición de la Directiva 2010/32/UE del Consejo, de 10 de mayo de 2010, que aplica el Acuerdo Marco para la prevención de las lesiones causadas por instrumentos cortantes y punzantes en el sector hospitalario y sanitario).
- c)
Garantizar el asesoramiento y la asistencia las 24h del día con disponibilidad de diagnóstico serológico preferiblemente en menos de 2h para el VIH y siempre antes de las 72h; para el virusB y C, lo antes posible y siempre antes de las 96h (ver algoritmos de actuación).
- d)
Facilitar el acceso a la medicación en los casos necesarios en los plazos establecidos.
- e)
Establecer los protocolos de seguimiento adecuados.
- f)
Disponer de profesionales encargados de la atención y seguimiento de los casos de EO (servicios de prevención de riesgos laborales, unidades de infecciosas, urgencias).
- g)
Establecer criterios de notificación centralizada para crear un registro a través de los Servicios de Prevención de Riesgos Laborales (SPRL) y valorar la eficacia de las intervenciones.
El trabajador ha de recibir asistencia urgente, y para ello acudirá inmediatamente al servicio de salud laboral en horario laboral y al servicio de urgencias en horario no laboral, donde se le entregará un informe de la asistencia recibida, reflejando las lesiones que ha sufrido. Debe comunicarlo al responsable inmediato para que haga el parte de accidente que posteriormente se enviara a la mutua, con independencia de que se le atienda en el servicio de salud laboral o en urgencias.
En heridas cutáneas (punciones, cortes), salpicaduras a piel no íntegra, se recomienda:
- a)
Lavado con agua y jabón.
- b)
Dejar fluir la sangre.
- c)
Desinfectar la herida con un antiséptico (povidona yodada, gluconato de clorhexidina).
- d)
Cubrir con un apósito impermeable.
En salpicaduras a mucosas (conjuntiva, etc.) se recomienda lavado con agua abundante o suero fisiológico.
En ningún caso se aplicarán agentes cáusticos. No se recomienda «exprimir», porque induce hiperemia, que puede aumentar el riesgo de adquirir la infección
Evaluación del riesgo de trasmisión ocupacional del VIHEl riesgo de trasmisión tras una EO depende de múltiples factores, como son la situación serológica del trabajador, el tipo de exposición, la cantidad de virus presente en el inóculo y el estado virológico de la fuente, así como del tiempo transcurrido desde la exposición4.
Existen varios estudios que demuestran que la exposición a elevadas cargas virales se asocia a mayor riesgo de transmisión de la infección5,6. Por este motivo, en los periodos de elevada viremia como son las fases de infección aguda o las fases avanzadas de la enfermedad, si la fuente no está recibiendo tratamiento antirretroviral (TAR), el riesgo de trasmisión es mayor.
Por otro lado, la exposición a fluidos corporales de pacientes con infección por el VIH y carga viral indetectable no elimina por completo el riesgo de transmisión, aunque lo hace muy improbable, siendo necesario el seguimiento y la valoración de la PPE7.
Tipos de exposición ocupacionalLas exposiciones percutáneas son más eficientes en la transmisión del VIH que las mucosas. El CDC estima que el riesgo promedio de seroconversión del VIH después de una EO percutánea es aproximadamente del 0,3% (IC95%: 0,2 a 0,5%), lo que supone 3 infecciones por cada 1.000 incidentes2. Tras la exposición de mucosas, el riesgo se reduce al 0,09% (IC95%: 0,006 a 0,5%), siendo incluso menor cuando el contacto es con piel no intacta7.
Con respecto a los factores relacionados con el accidente, este dependerá:
a) De la profundidad del pinchazo:
- 1.
Inoculación accidental superficial: erosión.
- 2.
Profundidad intermedia: aparición de sangre.
- 3.
Inoculación accidental profunda.
Cuanto mayor sea la profundidad, mayor será el riesgo de transmisión.
b) Del tipo de material utilizado:
- 1.
Aguja hueca: mayor riesgo que con las agujas de sutura, ya que estas últimas solo presentan una fina lámina de fluido en la superficie de la aguja.
- 2.
Aguja maciza o bisturí.
El riesgo aumenta de forma concomitante con el aumento de diámetro de la aguja8,9, de los factores de barrera (el uso de guantes disminuye el 50% el volumen inyectado), del tipo y condición del epitelio o de la superficie expuesta (la piel sana intacta es una excelente barrera y presenta poco o ningún riesgo).
Finalmente, el riesgo se relaciona directamente con el tipo de fluido al que se ha expuesto el trabajador, siendo el de mayor riesgo la sangre visible en el dispositivo. Otros fluidos con elevado potencial infeccioso que requieren evaluación precisa son la sangre, el semen y las secreciones vaginales. No se conoce el potencial infeccioso del líquido cefalorraquídeo (LCR); los líquidos serosos y el líquido amniótico presentan un potencial infeccioso desconocido. Vómitos, heces, saliva, sudor, lágrimas, orina y esputo no tienen riesgo significativo, excepto si tienen sangre visible9.
Características de la fuenteEs fundamental conocer la situación serológica del paciente fuente contactando con su médico responsable. Si esta no se sabe o no se puede conocer, se debe realizar un estudio serológico completo previa solicitud de consentimiento verbal o por escrito, que consistiría en: VHB, solicitar el antígeno (Ag) HBs; VHC, si es positivo, considerar medir la carga viral; VIH, si es positivo, medir la carga viral.
Lo recomendable es disponer de los resultados serológicos del VIH preferiblemente antes de transcurrir 2h tras la exposición. Las técnicas disponibles hoy día aseguran resultados con excelente sensibilidad y especificidad en menos de 30min10, y aportan información esencial acerca de la necesidad de iniciar o continuar la PPE. No obstante, la administración de PPE no debería posponerse hasta la disposición de los resultados de la serología del caso fuente, y se debe suspender si esta es negativa.
No existen datos publicados de ningún caso de transmisión ocupacional en el periodo ventana de la infección por VIH.
En el caso de que el paciente fuente tenga infección por el VIH conocida, es fundamental conocer la carga viral, el tipo de TAR (si lo recibe), así como la historia farmacológica y los motivos de cambio de tratamiento (resistencias o intolerancia) del paciente9,11,12.
Si no se puede conocer la situación serológica de la fuente, se la considerará como de alto riesgo9,11,12.
Características del trabajadorSe debe realizar una serología completa en la persona expuesta tras la exposición, para determinar su estatus serológico frente al VIH, al VHC y al VHB (anti-HBs, anti-HBc, AgHBs), salvo que ya sea positivo conocido. Además se realizará una analítica básica que incluya hemograma, función renal y hepática. Para la serología del VIH se recomienda realizar una prueba de cuarta generación (incluye la detección de anticuerpos y de antígeno P24).
Consideraciones previas a la profilaxis postexposiciónAntes de considerar el uso de la PPE es necesario tener en cuenta si la persona expuesta acude antes de 72h tras la exposición y recabar toda la información sobre la persona fuente. Con independencia de si se realiza o no PPE, todos los procedimientos e intervenciones deben estar claramente recogidos.
Si la PPE está indicada se recomienda iniciarla lo antes posible tras la EO, preferiblemente en las primeras 24h y siempre dentro de las primeras 72h9. No se recomienda iniciar PPE si han pasado más de 72h desde la EO.
Las recomendaciones generales para la profilaxis postexposición ocupacional (PPEO) se recogen en la tabla 1. En general se recomienda realizar PPE cuando el riesgo de transmisión es alto; cuando el riesgo no es alto, se debe valorar individualmente cada caso, y cuando el riesgo es despreciable o nulo, no se recomienda.
Recomendaciones generales de PPEO
| Tipo de exposición | Tipo de material | Recomendación |
|---|---|---|
| Percutánea | SangreaRiesgo muy altoRiesgo altoRiesgo no altoLíquido que contiene sangre, otros líquidos potencialmente infectantesb o tejidosOtros líquidos corporales no infectantes | Recomendar PPERecomendar PPERecomendar PPEdRecomendar PPEdNo recomendar PPE |
| Mucosas | SangreLíquido que contiene sangre, otros líquidos infecciososb o tejidosOtros líquidos corporales | Valorar individualmenteeValorar individualmenteeNo recomendar PPE |
| Piel alto riesgoc | SangreLíquido que contiene sangre, otros líquidos potencialmente infectantesb o tejidosOtros líquidos corporales no infectantes | Valorar individualmenteeValorar individualmenteeNo recomendar PPE |
Riesgo muy alto: accidente con gran volumen de sangre (pinchazo profundo con aguja utilizada en acceso vascular del paciente) y con carga viral VIH elevada.
Riesgo alto: accidente con alto volumen de sangre o accidente con sangre que contiene carga viral VIH elevada.
Riesgo no alto: accidente en el que no se da exposición a gran volumen de sangre ni a sangre con carga viral VIH elevada (pinchazo con aguja de sutura de paciente con carga viral baja o indetectable).
Incluye semen, secreciones vaginales, LCR y líquidos sinovial, pleural, peritoneal, pericárdico y amniótico.
Contactos cutáneos de alto riesgo cuando se trata de líquidos con carga viral VIH elevada, el contacto es muy prolongado, el área es extensa o hay zonas de piel no íntegra.
- 1.
Se necesita conocer la situación serológica frente al VIH del paciente fuente. Los resultados se han de conocer preferiblemente en las primeras 2h. Recomendación fuerte, alta calidad de la evidencia.
- 2.
En el caso de que el paciente fuente tenga infección por el VIH conocida, es fundamental conocer la carga viral, el régimen de TAR (si lo recibe), así como la historia farmacológica y los motivos de cambio de tratamiento (resistencias, intolerancia o toxicidad) del paciente. Recomendación fuerte, alta calidad de la evidencia. Si no se puede conocer la situación serológica del paciente fuente, se considerará como de alto riesgo. Recomendación fuerte, moderada calidad de la evidencia.
- 3.
La PPE ha de iniciarse lo antes posible tras la EO al VIH, preferiblemente en las primeras 24h y siempre dentro de las primeras 72h. Recomendación fuerte, moderada calidad de la evidencia. En las EO percutáneas a sangre con riesgo alto y muy alto se recomienda realizar PPE. Recomendación fuerte, moderada calidad de la evidencia.
- 4.
En las EO percutáneas a sangre con menor riesgo o a otros fluidos corporales potencialmente infectantes se recomienda realizar PPE, aunque si la carga viral de la fuente es indetectable se puede considerar no realizarla. Recomendación fuerte, baja calidad de la evidencia.
- 5.
En las EO con mucosas o con piel de alto riesgo a sangre y a otros fluidos corporales potencialmente infectantes se recomienda realizar PPE, aunque si la carga viral de la fuente es indetectable se puede considerar no realizarla. Recomendación débil, baja calidad de la evidencia.
- 6.
En las EO a fluidos corporales no infectantes no se recomienda realizar PPE. ecomenRdación fuerte, baja calidad de la evidencia.
- 7.
LA PPE debe interrumpirse si se confirma que el paciente fuente es VIH negativo. Recomendación fuerte, baja calidad de la evidencia.
El VIH comparte las vías de transmisión con el VHB y el VHC, por lo que se deberá realizar la valoración de la situación con respecto a ambos tipos de hepatitis. El VHC no se transmite de manera eficaz a través de exposición laboral; como ya se ha dicho, la incidencia media de seroconversión después de un contacto con sangre de un paciente VHC positivo es del 1,8%3, y es muy rara la transmisión a través de las membranas mucosas. El VHB, como se ha comentado previamente, sí se transmite con frecuencia si el trabajador expuesto no está vacunado.
La evaluación de la exposición de riesgo es la misma que para el VIH en cuanto a la forma y el tipo de exposición. Es fundamental evaluar, de forma correcta, la presencia de la infección en el paciente fuente. Si se desconoce el estado serológico, se debe realizar una extracción de sangre para realizar una serología previa solicitud de consentimiento informado, y poder tener acceso a los resultados en un periodo mínimo de tiempo10-13. No es necesaria la determinación de la carga viral del VHB o del VHC de forma sistemática. Solo estaría indicado en el caso de que el paciente se encuentre en situación de inmunodepresión avanzada o presente otras enfermedades que se asocien con la posibilidad de un resultado falso negativo de la serología. Si el paciente no da el consentimiento para la realización de las determinaciones serológicas, sea desconocido o no pueda realizarse, debe considerarse la fuente como infectada8.
Además se debe evaluar la susceptibilidad del trabajador expuesto, con la determinación de serología del VHC, del VHB si no está vacunado y del anti-HBs si está vacunado y se desconocía previamente o está inmunodeprimido. Se considera que es susceptible de infección por el VHB cuando el trabajador no está vacunado y cuando, estando vacunado, presente un título de anti-HBs<10mUI/ml14.
No existe una profilaxis efectiva frente al VHC, pues la cinética viral demuestra que para que el tratamiento sea eficaz debe haber ya una infección establecida. Por eso es importante el seguimiento de estos pacientes para poder diagnosticar cuanto antes una posible infección aguda por el VHC, en cuyo caso el tratamiento puede ser más eficaz.
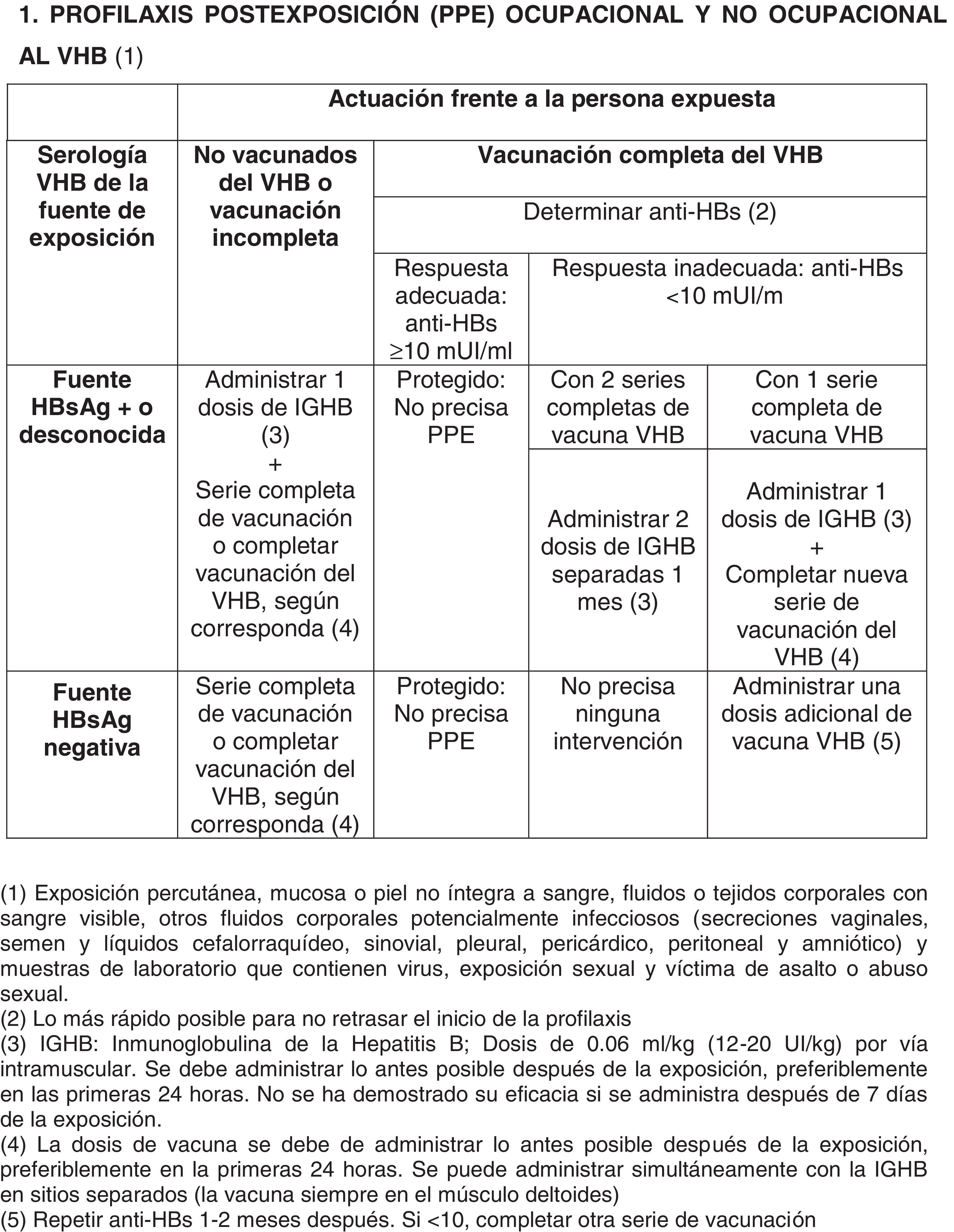
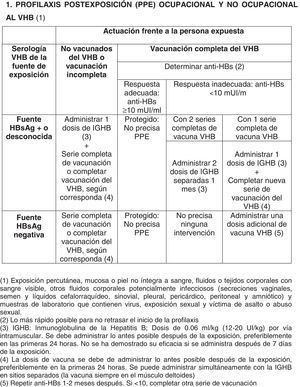
En la tabla 2 se expone el protocolo de actuación y la PPE frente al VHB.
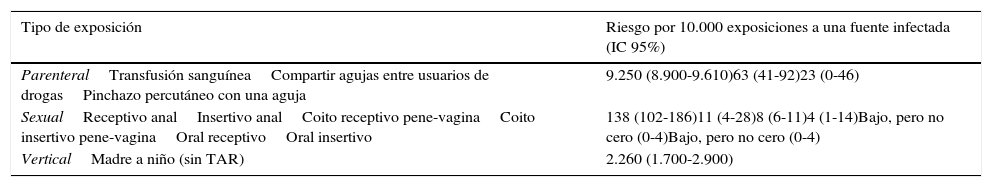
Probabilidad, estimada por acto, de adquirir la infección por VIH de una fuente infectada, según la ruta de exposición
| Tipo de exposición | Riesgo por 10.000 exposiciones a una fuente infectada (IC 95%) |
|---|---|
| ParenteralTransfusión sanguíneaCompartir agujas entre usuarios de drogasPinchazo percutáneo con una aguja | 9.250 (8.900-9.610)63 (41-92)23 (0-46) |
| SexualReceptivo analInsertivo analCoito receptivo pene-vaginaCoito insertivo pene-vaginaOral receptivoOral insertivo | 138 (102-186)11 (4-28)8 (6-11)4 (1-14)Bajo, pero no cero (0-4)Bajo, pero no cero (0-4) |
| VerticalMadre a niño (sin TAR) | 2.260 (1.700-2.900) |
Exposición a VHB y/o VHC:
- 1.
En el caso del VHB, la actuación y la PPE dependen de la situación tanto del paciente fuente como de la persona expuesta (ver algoritmo de actuación). Recomendación fuerte, moderada calidad de la evidencia.
- 2.
Si la pauta de vacunación frente al VHB es correcta no debe efectuarse seguimiento, salvo por las posibles implicaciones legales. En estos casos debe realizarse estudio serológico frente al VHB al inicio y a los 6 meses. Recomendación fuerte, baja calidad de la evidencia.
- 3.
En el caso del VHC no existe una PPE eficaz, por lo que debe asegurarse un diagnóstico precoz de una posible infección aguda en la persona expuesta, para poderla tratar cuanto antes. Recomendación fuerte, muy baja calidad de la evidencia.
El riesgo y los fundamentos de la transmisión percutánea no ocupacional son similares a los de la transmisión ocupacional, excepto por la frecuente dificultad para identificar la fuente de exposición que caracteriza a la exposición no ocupacional (ENO). Por este motivo, en este apartado nos centraremos en la transmisión sexual.
La ENO se define como el contacto por vía sexual o percutánea, de manera accidental, con sangre y/u otros fluidos biológicos potencialmente infectados de VIH fuera del ámbito ocupacional o perinatal15.
Evaluación del riesgo de transmisión no ocupacional del VIHLa transmisión del VIH puede realizarse únicamente por exposición a fluidos potencialmente infectantes. El mayor riesgo de transmisión es por sangre o fluidos que contengan sangre visible. También se consideran potencialmente infectantes el semen, las secreciones vaginales, los líquidos cefalorraquídeo, pleural, pericárdico, peritoneal y amniótico, y la leche materna. No se consideran infectantes la orina, las heces, la saliva, el vómito, las secreciones nasales, las lágrimas, el sudor ni el esputo, si no contienen sangre visible.
La probabilidad de transmisión del VIH dependerá fundamentalmente del tipo de exposición, del estado de la persona fuente, de la cantidad de virus en el inóculo y del individuo expuesto.
Teniendo en cuenta todos estos factores se pueden establecer diversos grados de riesgo que pueden modificarse por los factores concurrentes anteriormente citados. Cuando nos referimos a relaciones sexuales, estas se consideran con riesgo potencial cuando no se ha utilizado o se ha hecho mal uso del preservativo. El tipo de exposición se describe desde el punto de vista del expuesto.
- 1.
Riesgo considerable, si se cumplen las 3 condiciones siguientes:
- a)
Exposición de recto, vagina, ojos, boca u otras membranas mucosas, piel no intacta o contacto percutáneo
- b)
con fluidos potencialmente infectantes
- c)
y fuente VIH positiva.
En estos casos se recomienda que la persona expuesta realice profilaxis postexposición no ocupacional (PPENO).
- a)
- 2.
Riesgo a valorar individualmente, si se cumplen las 3 condiciones siguientes:
- a)
Exposición de recto, vagina, ojos, boca u otras membranas mucosas, piel no intacta o contacto percutáneo
- b)
con fluidos potencialmente infectantes
- c)
y fuente con estado frente a VIH desconocido.
La probabilidad de infectarse por VIH cuando el estado de la fuente es desconocido puede estimarse multiplicando la probabilidad de que la persona sea positiva por la probabilidad de que se transmita.
Como se ha comentado, en la ENO no siempre es posible conocer si la fuente de exposición tiene infección por el VIH. Esta es la razón por la que la PPENO se recomienda si la fuente tiene alta probabilidad de estar infectada por el VIH16:
- a)
Hombre que tiene sexo con hombres (HSH),
- b)
usuario de drogas por vía parenteral (UDVP),
- c)
trabajador del sexo,
- d)
agresor sexual,
- e)
antecedentes de ingreso en centros penitenciarios, o
- f)
un individuo procedente de un país con una prevalencia de VIH superior al 1% (Haití, Bahamas, Jamaica, Belice, Trinidad y Tobago, Estonia, Rusia, Tailandia y África subsahariana).
- a)
- 3.
Riesgo despreciable:
- a)
Cualquier tipo de exposición con fluidos no considerados como potencialmente infectantes, independientemente del estado de la fuente respecto al VIH.
- b)
Cualquier tipo de exposición con cualquier tipo de fluido si la fuente es VIH negativo.
En estos casos no se recomienda realizar PPENO.
- a)
- 4.
Sin riesgo considerable:
- a)
Besos.
- b)
Mordedura sin solución de continuidad.
- c)
Arañazo superficial con objeto afilado, incluidas las agujas abandonadas en la calle.
- d)
Fluidos infectantes sobre piel intacta (0%).
- a)
En estas exposiciones no está indicado realizar PPENO.
Tipos teóricos de exposición no ocupacionalEn el momento actual, la exposición por vía sexual es, con diferencia, la causa más frecuente de ENO, siendo la relación anal receptiva la exposición que mayor riesgo tiene17,18. Otras exposiciones de riesgo alto serían la transfusión sanguínea (en el momento actual su riesgo es casi inexistente al realizarse cribado sistemático de serología del VIH en todos los donantes), seguida del uso compartido de jeringas entre UDVP y la exposición percutánea con aguja.
En lo que a las relaciones sexuales se refiere, se considera que la exposición sexual es de riesgo en el caso de que se haya practicado sin preservativo o con rotura o mal uso del mismo. El riesgo de infección aumenta de forma considerable en el caso de relaciones sexuales traumáticas, con violencia, ante la presencia de lesiones genitales y/o infecciones de transmisión sexual (ITS), sangrado o menstruación durante la relación, o la existencia de una carga viral del VIH elevada en sangre y/o fluidos15,16.
Evaluación del riesgo según la vía de contagio (sexual, parenteral). El cálculo del riesgo de transmisión depende de la prevalencia de la infección VIH en la población a la que pertenece la persona fuente y del riesgo estimado del tipo de exposición19 (tabla 2). En las tablas 3-5 se detalla el riesgo estimado de las diferentes exposiciones15,16.
Riesgo estimado de infección tras exposición sexual con fuente VIH+, sin uso de preservativo, rotura o mal uso del mismo
| Riesgo considerable (0,8-3%) | Riesgo bajo (0,05-0,8%) | Riesgo mínimo (0,01-0,05%) | Riesgo despreciable/nulo (< 0,01%) |
|---|---|---|---|
| Recepción anal con eyaculación | Recepción vaginal con o sin eyaculaciónRecepción anal sin eyaculaciónPenetración analPenetración vaginalSexo orogenital con eyaculación | Sexo orogenital sin eyaculaciónSexo orogenital femenino | BesosCariciasMasturbaciónContacto con secreciones con piel íntegra |
Riesgo estimado de infección tras exposición sexual con fuente VIH desconocido, sin uso de preservativo, rotura o mal uso del mismo
| Riesgo bajoa (0,05-0,8%) | Riesgo mínimoa (0,01-0,05%) | Riesgo despreciable/nulo (< 0,01%) |
|---|---|---|
| Recepción anal con eyaculación | Recepción anal sin eyaculaciónRecepción vaginal con o sin eyaculaciónPenetración analPenetración vaginalSexo oral con o sin eyaculaciónSexo orogenital femenino | BesosCariciasMasturbaciónContacto con secreciones con piel integra |
Riesgo estimado de infección por VIH tras diferentes tipos de exposición parenterales con fuente VIH+ o desconocido
| Riesgo considerable (0,8-3%) | Riesgo bajo (0,05-0,8%) | Riesgo mínimo (0,01-0,05%) |
|---|---|---|
| Compartir jeringuillas o agujas usadasPinchazo profundo o con abundante sangrado con jeringa, de forma inmediata tras uso por fuente desconocida | Uso de jeringuilla de origen desconocidoPinchazo superficial tras uso por caso fuenteContacto abundante con sangre del caso fuente con mucosas del sujeto afecto | Compartir resto de material de inyección (recipiente, cuchara, algodón, filtro, etc.)Pinchazo accidental con poco sangrado con aguja de jeringa de procedencia desconocida |
Junto a las circunstancias antes detalladas se hace preciso tener en cuenta las circunstancias que impliquen un aumento del riesgo de transmisión. Estas serían16,19,20:
La infectividad de la persona fuente: la infección aguda por VIH, la enfermedad avanzada con niveles bajos de CD4+ (<350célulasl/ml) o eventos sida si la fuente no está recibiendo TAR, así como la presencia de una carga viral del VIH>5.000copias/ml.
La presencia de sangrado, menstruación, úlceras sangrantes o ITS.
Con anterioridad ya se han comentado otras circunstancias en las que se recomienda valorar la PPENO (HSH, UDVP, etc.). Todo ello justifica que la valoración del riesgo deba ser individualizada.
Consideraciones previas a la profilaxis postexposiciónAntes de considerar el uso de la PPE es preciso tener en cuenta si la persona expuesta acude antes de 72h tras la exposición, recabar toda la información sobre la persona fuente y valorar si existe la capacidad de seguimiento clínico de la persona expuesta. Con independencia de si se realiza o no PPE, todos los procedimientos e intervenciones deben estar claramente recogidos.
Tras la exposición accidental, las heridas y la piel expuesta deben ser lavadas con agua y jabón. Por su parte, tras un pinchazo accidental, nunca debe exprimirse la zona del pinchazo.
Así mismo, las personas que sufren una exposición accidental deben ser evaluadas lo antes posible para valorar si está indicada la PPE.
Al igual que en la PPEO, si la PPENO está indicada se recomienda iniciarla lo antes posible tras la ENO, preferiblemente en las primeras 24h y siempre dentro de las primeras 72h21. No se recomienda iniciar PPE si han pasado más de 72h desde la ENO.
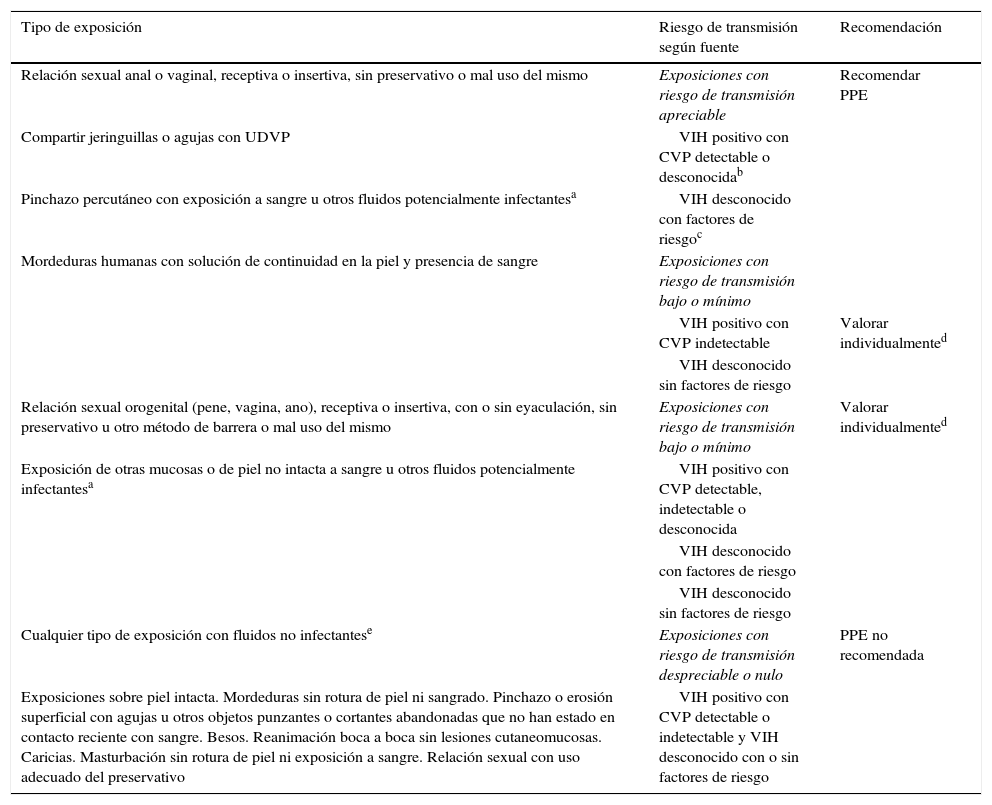
Las recomendaciones generales sobre PPENO se recogen en la tabla 6. En general se recomienda realizar PPE cuando el riesgo de transmisión es apreciable; cuando el riesgo es bajo o mínimo se debe valorar individualmente cada caso, y cuando el riesgo es despreciable o nulo, no se recomienda.
Recomendaciones de profilaxis postexposición no ocupacional (PPENO)
| Tipo de exposición | Riesgo de transmisión según fuente | Recomendación |
|---|---|---|
| Relación sexual anal o vaginal, receptiva o insertiva, sin preservativo o mal uso del mismo | Exposiciones con riesgo de transmisión apreciable | Recomendar PPE |
| Compartir jeringuillas o agujas con UDVP | VIH positivo con CVP detectable o desconocidab | |
| Pinchazo percutáneo con exposición a sangre u otros fluidos potencialmente infectantesa | VIH desconocido con factores de riesgoc | |
| Mordeduras humanas con solución de continuidad en la piel y presencia de sangre | Exposiciones con riesgo de transmisión bajo o mínimo | |
| VIH positivo con CVP indetectable | Valorar individualmented | |
| VIH desconocido sin factores de riesgo | ||
| Relación sexual orogenital (pene, vagina, ano), receptiva o insertiva, con o sin eyaculación, sin preservativo u otro método de barrera o mal uso del mismo | Exposiciones con riesgo de transmisión bajo o mínimo | Valorar individualmented |
| Exposición de otras mucosas o de piel no intacta a sangre u otros fluidos potencialmente infectantesa | VIH positivo con CVP detectable, indetectable o desconocida | |
| VIH desconocido con factores de riesgo | ||
| VIH desconocido sin factores de riesgo | ||
| Cualquier tipo de exposición con fluidos no infectantese | Exposiciones con riesgo de transmisión despreciable o nulo | PPE no recomendada |
| Exposiciones sobre piel intacta. Mordeduras sin rotura de piel ni sangrado. Pinchazo o erosión superficial con agujas u otros objetos punzantes o cortantes abandonadas que no han estado en contacto reciente con sangre. Besos. Reanimación boca a boca sin lesiones cutaneomucosas. Caricias. Masturbación sin rotura de piel ni exposición a sangre. Relación sexual con uso adecuado del preservativo | VIH positivo con CVP detectable o indetectable y VIH desconocido con o sin factores de riesgo |
Sangre, fluidos que contengan sangre visible, semen, secreciones vaginales, líquidos cefalorraquídeo, pleural, pericárdico, peritoneal, sinovial, amniótico, y leche materna.
HSH, UDVP, trabajador del sexo, agresor sexual, antecedentes de ingreso en centros penitenciarios y natural de un país con una prevalencia de VIH superior al 1% (Haití, Bahamas, Jamaica, Belice, Trinidad y Tobago, Estonia, Rusia, Tailandia y África subsahariana).
Valorar individualmente cada caso. En general se recomienda iniciar PPE si la fuente es VIH+ con CVP detectable o desconocida, o si es VIH desconocido con factores de riesgo. Si la fuente es VIH+ con CVP indetectable o si es VIH desconocido sin factores de riesgo, se puede considerar no realizar PPE dado que el riesgo de transmisión es muy bajo.
- 1.
Las personas que sufren una exposición accidental deben ser evaluadas lo antes posible para valorar si está indicada la PPE. Recomendación fuerte, moderada calidad de la evidencia.
- 2.
Tras la exposición accidental, las heridas y la piel expuesta deben ser lavadas con agua y jabón. Por otra parte, tras un pinchazo accidental nunca debe exprimirse la zona del pinchazo. Recomendación fuerte, moderada calidad de la evidencia.
- 3.
Cuando se produce una exposición al VIH, con independencia de si se realiza o no PPE, todos los procedimientos e intervenciones deben estar claramente recogidos. Recomendación fuerte, moderada calidad de la evidencia.
- 4.
Se recomienda iniciar PPENO lo antes posible tras la exposición, preferiblemente en las primeras 24h y no más tarde de las 72h. Recomendación fuerte, moderada calidad de la evidencia.
- 5.
Se recomienda realizar PPENO en las exposiciones con riesgo apreciable (tabla 6). Recomendación fuerte, baja calidad de la evidencia.
- 6.
Se recomienda valorar individualmente la necesidad de PPENO en las exposiciones con riesgo bajo o mínimo (tabla 6). En general se recomienda iniciar PPENO si la fuente es VIH+ con CVP detectable o desconocida, o si es VIH desconocido con factores de riesgo. Si la fuente es VIH+ con CVP indetectable o si es VIH desconocido sin factores de riesgo, se puede considerar no realizar PPENO, dado que el riesgo de transmisión es muy bajo. Recomendación débil, baja calidad de la evidencia.
- 7.
No se recomienda realizar PPENO en las exposiciones con riesgo nulo o despreciable (tabla 6). Recomendación fuerte, baja calidad de la evidencia.
- 8.
La PPENO debe interrumpirse si se confirma que la persona fuente es VIH negativo. Recomendación fuerte, baja calidad de la evidencia.
La evaluación del riesgo en la exposición percutánea no ocupacional es similar al de la EO, excepto por la frecuente dificultad para identificar la fuente de exposición que caracteriza a la ENO. Además, habrá que considerar el riesgo de transmisión por vía sexual del VHB y del VHC en las ENO.
En lo que respecta al VHB, habrá que conocer el estado de la fuente y el estado de inmunidad del sujeto expuesto y vacunar o utilizar gammaglobulina anti-VHB en caso necesario. En los pacientes no inmunizados frente al VHB o que desconozcan su estado inmunológico, la decisión de vacunar no debe demorarse hasta disponer de la serología anti-HBs.
Cada vez se describen con mayor frecuencia casos de transmisión de VHC tras relaciones sexuales, sobre todo en HSH20,21. Además, no existe una profilaxis efectiva frente al VHC, pues la cinética viral demuestra que para que el tratamiento sea eficaz debe haber ya una infección establecida. Por eso es importante el seguimiento de estos pacientes para poder diagnosticar cuanto antes una posible infección aguda por el VHC, en cuyo caso el tratamiento puede ser más eficaz.
RECOMENDACIONES- 1.
En el caso del VHB, la actuación depende de la situación tanto del paciente fuente como de la persona expuesta. Recomendación fuerte, moderada calidad de la evidencia.
- 2.
Si la pauta de vacunación VHB es correcta, no debe efectuarse seguimiento salvo por las posibles implicaciones legales. En estos casos debe realizarse estudio serológico frente al VHB al inicio y a los 6 meses. Recomendación fuerte, baja calidad de la evidencia.
- 3.
En cuanto al VHC, en estos momentos no se dispone de ninguna medida eficaz de PPE, por lo que las recomendaciones deben ir dirigidas a un diagnóstico precoz de una posible infección aguda en la persona expuesta, para poderla tratar cuanto antes. Recomendación fuerte, muy baja calidad de la evidencia.
Tras la exposición por vía sexual hay que tener en cuenta la posibilidad de transmisión de otras ITS (como sífilis, gonococo y clamidia), que depende de la prevalencia en la comunidad, del tipo de exposición, de la presencia de traumatismo y del número de personas fuente.
Se aconseja instaurar tratamiento empírico tras la exposición, dado que ninguna prueba diagnóstica es capaz de identificar una ITS en el momento de la agresión22. No obstante, siempre deben realizarse los procedimientos diagnósticos adecuados sin tener en cuenta los síntomas. También se debe realizar un test de embarazo.
En agresiones sexuales se aconseja instaurar una pauta de tratamiento empírico triple con una dosis única de ceftriaxona (la dosis recomendada es de 250mg i.m.) más metronidazol 2g v.o. más azitromicina 1g v.o. o doxiciclina 100mg cada 12h durante 7días16,22,23. Con esta pauta se tratarían las infecciones por clamidia, sífilis, gonococo y tricomonas. Con posterioridad se remitirán a la consulta de ginecología en caso necesario.
En la exposición parenteral es conveniente conocer, además del estado serológico vacunal de la persona expuesta con respecto al VHB, los antecedentes de vacunación frente al tétanos, para vacunar o usar una dosis de recuerdo, o de gammaglobulina en caso necesario24. Así mismo se valorará la indicación de vacunar de la hepatitisA.
RECOMENDACIONES- 1.
Tras una exposición por vía sexual se han de descartar, además del VIH, otras ITS, realizando los procedimientos diagnósticos adecuados. Recomendación fuerte, alta calidad de la evidencia.
- 2.
En las agresiones sexuales se aconseja instaurar una pauta de tratamiento empírico triple (ceftriaxona más metronidazol más azitromicina o doxiciclina). Recomendación fuerte, moderada calidad de la evidencia.
La PPE frente al VIH está indicada en cualquier momento durante el embarazo siempre que haya existido exposición significativa. Se deben tener en cuenta los riesgos que en esta población podría tener el TAR, especialmente durante el primer trimestre de gestación, por lo cual siempre se deben consultar las guías actualizadas sobre TAR en embarazo25,26. Respecto a la profilaxis de VHB, se debe actuar según protocolo de actuación en la población general.
RECOMENDACIÓN- 1.
En el caso de exposición de riesgo a VIH en una mujer gestante, se deben seguir las mismas recomendaciones de PPE que en las no gestantes. Recomendación fuerte, baja calidad de la evidencia.
Se deben tener en cuenta las connotaciones medicolegales de toda agresión sexual y aplicar los protocolos establecidos.
Se estima que el riesgo de transmisión sexual de VIH puede ser mayor en víctimas de violación por laceraciones genitales y/o anales producidas durante la misma1. Si bien existen pocos datos acerca de la prevalencia de infección por VIH entre personas con cargos de violación, en todos los casos en que esta exista se debe recomendar la PPE. Las pautas y los tiempos de inicio de la PPE deben seguir los mismos criterios que en otros contactos sexuales de riesgo27,28.
Se aconseja instaurar una pauta de tratamiento antibiótico empírico en dosis única para evitar otras ITS.
RECOMENDACIONES- 1.
Se recomienda la PPE frente al VIH a las víctimas de agresión sexual cuando exista exposición significativa, definida como contacto directo de semen, fluidos vaginales o sangre del asaltante con vagina, pene, ano o boca de la víctima, aunque no exista daño macroscópico visible. Recomendación fuerte, baja calidad de la evidencia.
- 2.
Se recomienda la PPE en los casos de rotura de la integridad de la piel o membranas mucosas de la víctima si han entrado en contacto con sangre, semen o fluidos vaginales del asaltante, así como en mordeduras que presenten sangre visible. Recomendación fuerte, baja calidad de la evidencia.
A toda persona que haya sido evaluada tras una EO o una ENO, con independencia de que se realice PPE o no, debe ofrecérsele un plan de seguimiento clínico y analítico, información y apoyo psicológico.
En el momento inicial se realizarán las siguientes determinaciones:
- -
Analítica general, que incluya hemograma completo y bioquímica (perfil renal y hepático).
- -
Serología del VIH, VHB y VHC.
- -
Serología de sífilis y cribado de otras ITS en las exposiciones sexuales.
- -
Test del embarazo en mujeres en las exposiciones sexuales.
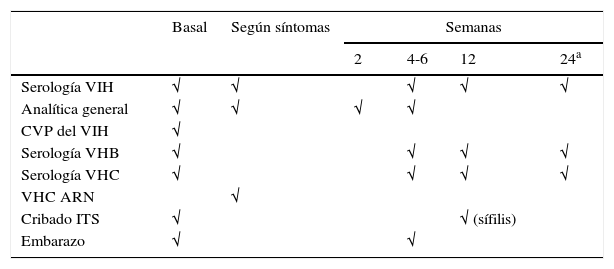
El inicio de la PPE al VIH nunca debe demorarse hasta disponer de los resultados. Si posteriormente se confirma que la fuente es VIH negativa, se suspenderá la PPE. El seguimiento de estos pacientes es de 24semanas15,16. La única excepción es la realización de una nueva serología frente al VIH a las 48semanas en el caso de sufrir una infección por el VHC tras la exposición a una fuente coinfectada por el VIH-VHC16. En los laboratorios donde dispongan de determinación combinada de antígeno/anticuerpo para VIH de cuarta generación, el seguimiento podría reducirse a la determinación basal, 6semanas y 4meses postexposición. Las pruebas a realizar, así como sus controles, se detallan en el cronograma de la tabla 7.
Cronograma del seguimiento
| Basal | Según síntomas | Semanas | ||||
|---|---|---|---|---|---|---|
| 2 | 4-6 | 12 | 24a | |||
| Serología VIH | √ | √ | √ | √ | √ | |
| Analítica general | √ | √ | √ | √ | ||
| CVP del VIH | √ | |||||
| Serología VHB | √ | √ | √ | √ | ||
| Serología VHC | √ | √ | √ | √ | ||
| VHC ARN | √ | |||||
| Cribado ITS | √ | √ (sífilis) | ||||
| Embarazo | √ | √ | ||||
Por otro lado, las personas que han sufrido una exposición accidental deben ser informadas sobre los signos y/o síntomas de la infección aguda por el VIH. En este caso se realizará una carga viral del VIH, con independencia del tiempo transcurrido desde la exposición accidental. Los pacientes que inicien PPE, además, deben ser informados de los efectos secundarios del tratamiento ARV, de las posibles interacciones medicamentosas, y de la necesidad de tener una buena adherencia al mismo.
Así mismo, durante el periodo de seguimiento, sobre todo durante las primeras 12semanas, la persona expuesta deberá evitar una posible transmisión secundaria del VIH o de otras infecciones, utilizando siempre el preservativo en las relaciones sexuales, no compartiendo jeringuillas, evitando el embarazo y las donaciones de sangre, semen…
RECOMENDACIONES- 1.
Si en el seguimiento se utiliza una prueba de antígeno/anticuerpos de cuarta generación para el VIH (incluye la detección del antígeno p24), este puede concluir 4meses después de la exposición. Si no se dispone de ensayos de cuarta generación, el seguimiento concluye normalmente 6meses después de una exposición al VIH. Recomendación fuerte, alta calidad de la evidencia.
- 2.
Del mismo modo, se debe aconsejar sobre medidas de prevención secundarias (uso de anticonceptivos de barrera, evitar las donaciones de sangre o derivados, tejidos o semen, el embarazo o la lactancia) para prevenir la transmisión secundaria, en especial durante las primeras 6-12semanas tras la exposición. Recomendación fuerte, alta calidad de la evidencia.
Las pautas de elección para la PPE consisten en la combinación de 2 inhibidores de la transcriptasa inversa análogos de nucleósidos/nucleótidos (ITIAN) asociados a un tercer fármaco antirretroviral (FARV) de otra familia9,21.
Por su mejor tolerancia y administración una vez al día, se considera que los 2 ITIAN preferentes son tenofovir/emtricitabina9,21 (TDF/FTC) coformulados (un comprimido al día). Como alternativa, se puede utilizar zidovudina/lamivudina (ZDV/3TC) coformulados (un comprimido 2 veces al día) si no se quiere usar TDF (por ejemplo en personas con enfermedad renal). El uso de abacavir no se recomienda por el riesgo de reacción de hipersensibilidad a dicho fármaco, al no poder tener disponible el HLA-B*5701 en la persona expuesta al iniciar la PPE.
Como tercer fármaco se puede utilizar un inhibidor de la proteasa potenciado con ritonavir (IP/r) o un inhibidor de la integrasa (INI)9,21, dado que la probabilidad de exposición a virus resistente a estos FARV es muy escasa. Entre los diferentes IP/r disponibles, al igual que en las guías de tratamiento ARV29, los preferidos son darunavir/ritonavir (DRV/r, 800/100mg/día) o atazanavir/ritonavir (ATV/r 300/100mg/día), y como alternativa, lopinavir/ritonavir (LPV/r, 2 comprimidos 2 veces al día). Como INI se recomienda utilizar raltegravir (RAL, un comprimido 2 veces al día), por su buena tolerancia, escasas interacciones farmacológicas y mayor experiencia30. Con otros INI, como elvitegravir/cobicistat (EVG/COBI) y dolutegravir (DTG), todavía no existe suficiente experiencia, por lo que en la actualidad se deben considerar solo como fármacos alternativos. En cuanto al uso de IP/r o RAL, las guías más recientes sobre PPE9,21 prefieren RAL por mejorar la adherencia y la tolerancia, así como por tener escaso riesgo de interacciones30, a pesar de que hay que administrarlo 2 veces al día.
En general no se recomienda el uso en las pautas preferentes de inhibidores de la transcriptasa inversa no nucleósidos (ITINN) de primera generación, efavirenz (EFV) y nevirapina (NVP), como tercer fármaco9,21, por sus efectos adversos y mayor riesgo de resistencias primarias. Por su mejor tolerancia, rilpivirina (RPV) y etravirina (ETR) podrían ser una alternativa. En un estudio reciente se han comunicado buenos resultados con RPV, pero no existe experiencia con ETR en PPE.
En los casos en que el paciente fuente de la exposición tenga resistencias conocidas o sospechadas (fracasos virológicos previos) a alguno o varios de los FARV de las pautas preferentes recomendadas en la PPE, o que la persona expuesta tenga posibles contraindicaciones para el uso de alguno de ellos, se recomienda consultar con un experto en infección por VIH para seleccionar la pauta más adecuada en estos casos, sin que ello suponga una demora en el inicio de la PPE (se puede iniciar la pauta recomendada y que el experto la revise y la ajuste lo antes posible, preferiblemente en menos de 24-72h).
RECOMENDACIONES- 1.
Se recomienda utilizar TDF/FTC con RAL como pauta preferente, tanto en PPE ocupacional como no ocupacional. Recomendación fuerte, moderada calidad de la evidencia.
- 2.
Como pautas alternativas se pueden utilizar TDF/FTC con DRV/r, ATV/r, DTG, EVG/COBI o RPV, tanto en PPE ocupacional como no ocupacional. Recomendación débil, baja calidad de la evidencia.
Aunque la duración óptima de la PPE no se conoce, basándonos en los resultados de estudios en modelos animales31 y transmisiones ocupacionales32, se recomienda una pauta de 28días de duración9,21,24.
RECOMENDACIONES- 1.
Se recomienda una pauta de 28 días de duración del tratamiento para la PPE. Recomendación fuerte, baja calidad de la evidencia.
- 2.
Se recomienda una re-evaluación sobre adherencia y toxicidades a las 72h de iniciar la PPE. Recomendación fuerte, baja calidad de la evidencia.
Una vez iniciada la PPE, se recomienda una re-evaluación del paciente dentro de las 72h posteriores a la exposición. En este momento se pueden obtener nuevos datos sobre la misma, aclarar riesgos y beneficios, modificar o ajustar la pauta de PPE, asegurar una adecuada adherencia y manejar síntomas asociados a efectos secundarios. Posteriormente se recomiendan controles clínicos al menos cada 2 semanas hasta completar la pauta de PPE9,21,24.
El seguimiento será el mismo en la PPEO y PPENO, si bien en el caso de las exposiciones sexuales debe realizarse, además, el cribado de otras ITS (sífilis, gonococo, clamidia)9,21,24.
Toxicidad e interaccionesLa toxicidad del TAR es un problema de gran relevancia que condiciona la adherencia a él. A esto hay que añadir la existencia de posibles interacciones farmacológicas derivadas de la administración previa o concomitante de otros fármacos, que pueden reducir el beneficio de la PPE o aumentar la posibilidad de efectos adversos.
En el caso de observar una toxicidad o un efecto adverso que pueda limitar el éxito de la PPE, se debe valorar la modificación de la pauta o el uso de tratamientos que minimicen estos efectos adversos (por ejemplo, antieméticos).
A la hora de seleccionar la PPE, existen diferentes guías29,33 y páginas web34,35 en las que pueden consultarse los principales efectos secundarios de los FARV empleados y el riesgo de interacciones.
Abordaje psicológicoEs recomendable que el clínico valore en la visita de prescripción de la PPE la necesidad de proporcionar apoyo psicológico en función del nivel de ansiedad o preocupaciones que presente el paciente. Si el nivel de angustia es elevado, se corre el riesgo de que la transmisión de información resulte inútil, ya que el estado emocional del paciente puede dificultar la comprensión de las instrucciones a seguir, incidiendo finalmente en que la adherencia al tratamiento no sea la adecuada. Si nos hallamos ante una agresión sexual será indispensable la derivación al centro de salud mental de referencia de la persona afectada y una adecuada monitorización de la adherencia, ya que se ha mostrado inadecuada en el contexto de las agresiones sexuales.
Respecto a la PPEO, el clínico debería proporcionar toda la información que sea necesaria para resolver las dudas que se planteen. Aunque no es lo habitual, si la ansiedad o angustia es muy elevada y puede interferir en sus actividades laborales, será necesaria la derivación a especialistas en salud mental.
Por lo que respecta a niños y adolescentes, el clínico valorará la necesidad de derivar al equipo de salud mental que corresponda en función de la ansiedad o de las preocupaciones que presente la familia o el niño. También puede considerarse la derivación de la familia a alguna entidad que aborde estos temas y que disponga de profesionales cualificados. Si se trata de una agresión sexual demostrada, la derivación para intervención psicológica por parte de profesionales especializados en este campo será indispensable. En el adolescente, es importante que el clínico utilice en las entrevistas un lenguaje y un estilo cercanos, con el fin de crear un clima de confianza y cercano que permita obtener informaciones veraces.
Profilaxis postexposición en niños y adolescentesLa sistemática a llevar a cabo en la atención de un niño o adolescente con una exposición potencial o confirmada al VIH es la siguiente:
- 1.
Limpiar la puerta de entrada: herida (cutánea o mucosa), mucosa expuesta (oral, genital, ocular).
- 2.
Determinar si es necesaria la PPE para VIH.
- 3.
Notificar a los padres o tutores legales.
- 4.
En caso de sospecha o confirmación de abuso sexual, notificar a las autoridades judiciales correspondientes y asegurar un examen físico forense por personal adecuadamente formado y acreditado.
- 5.
En caso de no disponer de capacidad necesaria, remitir al niño al centro médico con capacidad adecuada para evaluación y atención integral.
- 6.
Realizar prueba serológica basal de VIH.
- 7.
Evaluar riesgo para otros patógenos transmisibles.
- 8.
Evaluación analítica basal.
- 9.
Iniciar tratamiento profiláctico con ARV, si está indicado, de forma ideal en las primeras 6h, y siempre antes de las 72h siguientes a la exposición (ver más adelante).
- 10.
Iniciar tratamiento o profilaxis para otros patógenos si está indicado (ver más adelante).
- 11.
Establecer calendario y contenido de seguimiento.
Evaluación analítica basal:
- -
Recuento sanguíneo complete.
- -
Pruebas de función hepatica.
- -
Evaluar el estado de vacunación contra VHB y tétanos.
- -
Serología VHC.
- -
En caso de sospecha o confirmación de abuso sexua, realizar pruebas para el diagnóstico de:
- •
Gonorrhea, sífilis y clamidia.
- •
VHB, VHS y VPH.
- •
Vaginosis bacteriana y tricomoniasis.
- •
La situación más habitual es con gran diferencia el pinchazo accidental con aguja de origen desconocido. En estos casos no hay que hacer profilaxis ARV.
Las mordeduras suceden con frecuencia entre los niños. No obstante, los niveles de VIH en saliva son muy bajos, por lo que el riesgo de transmisión del VIH es inapreciable, siempre y cuando la piel se mantenga íntegra. Son muy pocos los casos documentados de posible transmisión por este mecanismo36-38.
En cualquier caso, una mordedura que da lugar a exposición de sangre, tanto para la persona mordida como para el mordedor, puede ser indicación de PPE.
RECOMENDACIÓN- 1.
Si un niño VIH negativo muerde a una persona VIH+ o es mordido por una persona VIH+ con pérdida de la integridad de la piel, debe recibir PPE frente a VIH. Recomendación fuerte, baja calidad de la evidencia.
El abuso sexual por parte de un adolescente o adulto infectado, aunque estadísticamente es menos frecuente que en adultos, entraña un mayor riesgo de transmisión viral en niños debido a su mayor vulnerabilidad anatómica, a los traumatismos, a una mucosa vaginal y anal más fina, a ectopia cervical, etc. Por tanto, el riesgo, en caso de penetración confirmada, puede ser mayor que el derivado de estudios en adultos, sobre todo en niños pequeños y en caso de producción de lesiones importantes (desgarros, etc.).
No hay estudios que demuestren que la PPE en pediatría sea eficaz, y se comprende la dificultad para llevar a cabo dichos estudios.
Tratamiento profiláctico frente al VIH en niños y adolescentes.Salvo los adolescentes, en los que se puede llevar a cabo una pauta idéntica a la de los adultos, los niños deben recibir una pauta adaptada a esta edad, teniendo en cuenta el estado de aprobación para la edad pediátrica de los FARV recomendados en la PPE en adultos, así como la disponibilidad de suspensión para niños que no pueden ingerir comprimidos o cápsulas39.
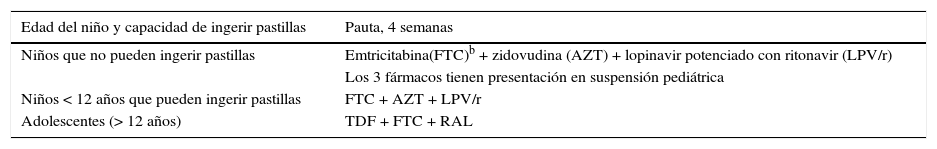
Por estas razones, y para unificar la profilaxis en la edad pediátrica, la pauta recomendada se refleja en la tabla 8.
Pautas recomendadas en la profilaxis postexposición en la edad pediátricaa
| Edad del niño y capacidad de ingerir pastillas | Pauta, 4 semanas |
|---|---|
| Niños que no pueden ingerir pastillas | Emtricitabina(FTC)b + zidovudina (AZT) + lopinavir potenciado con ritonavir (LPV/r) |
| Los 3 fármacos tienen presentación en suspensión pediátrica | |
| Niños < 12 años que pueden ingerir pastillas | FTC + AZT + LPV/r |
| Adolescentes (> 12 años) | TDF + FTC + RAL |
Calculando las dosis por peso, si se alcanza la dosis del adolescente se puede valorar administrar alguno de los fármacos en cápsulas/comprimidos. LPV/r tiene la presentación en comprimido pediátrico de 100mg; puede valorarse su empleo, dado las dificultades para la ingesta de lopinavir en suspensión, debido al fuerte sabor a etanol.
En caso de que el niño no esté bien vacunado, o esté vacunado pero presente serología (anti-HBs) negativa, se recomienda vacunación e inmunoglobulina específica frente al VHB por vía i.m., a ser posible en las primeras 72h16,40.
RECOMENDACIONES- 1.
Se debe seguir la misma sistemática diagnóstica que en el adulto. Recomendación fuerte, baja calidad de la evidencia.
- 2.
En caso de que esté indicado, se recomienda una pauta de 28días de duración del tratamiento para la PPE, preferentemente en las primeras 6h tras la exposición, y siempre en las primeras 72h. Recomendación fuerte, baja calidad de la evidencia.
- 3.
La PPE en adolescentes (>12años) se puede llevar a cabo en una pauta idéntica a la de los adultos. Recomendación fuerte, baja calidad de la evidencia.
- 4.
La PPE en niños menores de 12años debe consistir en emtricitabina (FTC) + zidovudina (AZT) + lopinavir potenciado con ritonavir (LPV/r). En niños que no pueden ingerir pastillas se administrarán estos fármacos en suspensión pediátrica. Recomendación fuerte, baja calidad de la evidencia.
La realización de este documento ha sido financiada con fondos propios de la SPNS.
Declaración de conflicto de interesesCon el fin de evitar y/o minimizar los posibles conflictos de intereses, las personas que forman el panel de expertos/as han realizado una declaración formal de intereses. En esta declaración parte de los/as autores/as han recibido financiación para participar en congresos y para la realización de investigaciones, así como han recibido pagos como ponentes por parte de instituciones públicas y laboratorios farmacéuticos. Estas actividades no afectan a la claridad del presente documento por no entrar en conflicto de intereses lo recomendado con los honorarios y/o ayudas recibidas. Cabe resaltar que con respecto a los fármacos en el documento, solamente se habla de principio activo y no de marca comercial.
Conflicto de interesesEsperanza M. Alonso Jiménez declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
José Ramón Blanco declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en los laboratorios Abbvie, Boehringer-Ingelheim, Bristol-Myers Squibb, Gilead Sciences, GlaxoSmithKline, Janssen, Merck y ViiV Healthcare; ha recibido compensación económica por charlas de Abbvie, Boehringer-Ingelheim, Bristol-Myers Squibb, Gilead Sciences, GlaxoSmithKline, Janssen, Merck y ViiV Healthcare, así como pagos por desarrollos de presentaciones educacionales para Gilead Sciences y Bristol-Myers Squibb.
Carlos Dueñas declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Marina Fernández Escribano declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Carmina Fumaz declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener ningún conflicto de intereses.
Federico García declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría y ha recibido compensación económica por charlas en los laboratorios Gilead Sciences, ViiV, Abbvie y Roche Diagnostica.
Pedro González de Castro declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Raúl González Montero declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener conflicto de intereses.
José Antonio Iribarren declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en los laboratorios Abbvie y Janssen-Cilag, ha recibido becas de investigación clínica de laboratorios Abbvie, Bristol-Myers Squibb, Gobierno Vasco, FIPSE y FISS, ayudas para asistencia a congresos de Abbvie, Gilead, Janssen-Cilag y ViiV, y ha participado en actividades educativas, charlas o simposios patrocinados por Abbvie, Bristol-Myers Squibb, Gilead, Merck, Novartis Janssen, Pfizer y ViiV.
Juan Emilio Losa declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Fernando Lozano declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría para Abbvie, Bristol-Myers Squibb, Gilead Sciences, GlaxoSmithKline, Janssen, Merck-Sharp & Dome, Pfizer, Roche Pharmaceuticals y ViiV Healthcare, y ha recibido compensación económica por charlas de Abbvie, Bristol-Myers Squibb, Gilead Sciences, GlaxoSmithKline, Janssen, Merck-Sharp & Dome, Pfizer y ViiV Healthcare.
Oscar Miró declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
David Moreno declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Enriqueta Muñoz Platon declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Enrique Ortega declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Rosa Polo Rodríguez declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Declara no tener conflicto de intereses.
Jesús Sanz Sanz declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en los laboratorios Abbvie, Bristol-Myers Squibb, Gilead Sciences, Janssen, Merck, ViiV Healthcare y Boehringer-Ingelheim; ha recibido compensación económica por charlas de Abbvie, Bristol-Myers Squibb, Gilead Sciences, Janssen, Merck, ViiV Healthcare y Boehringer-Ingelheim, y ha recibido pagos por desarrollo de presentaciones educacionales para ViiV Healthcare.
Ignacio Santos declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
M. Jesús Tellez declara no haber recibido ninguna ayuda ni subvención relacionada con este documento. Ha efectuado labores de consultoría en los laboratorios Abbvie, Bristol-Myers Squibb, Gilead Sciences y Janssen; ha recibido compensación económica por charlas de Gilead Sciences y Janssen
M. Victoria Vals Jiménez declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
M. Luisa Valle Robles declara no haber recibido ninguna ayuda ni subvención relacionada con este documento.
Comité de Redacción
Rosa Polo Rodriguez. Especialista en Medicina Interna. Secretaría del Plan Nacional sobre el Sida. Madrid.
Fernando Lozano. Especialista en Medicina Interna. Unidad Clínica de Enfermedades Infecciosas y Microbiología. Hospital Universitario de Valme. Sevilla.
Pedro González de Castro. Especialista en Medicina del Trabajo. Presidente de la Sociedad Española de Medicina del Trabajo.
Esperanza M. Alonso Jiménez. DUE, Presidenta de la Federación Española de Enfermería del Trabajo (FEDEET).
Oscar Miró. Especialista en Medicina Interna. Servicio de Urgencias del Hospital Clínic. Barcelona.
José Ramón Blanco. Especialista en Medicina Interna. Departamento de Enfermedades Infecciosas/VIH. Hospital San Pedro CIBIR. Logroño.
David Moreno. Especialista en Pediatría. Infectología Pediátrica. Hospital Regional Universitario de Málaga.
Carlos Dueñas. Especialista en Medicina Interna. Unidad de Enfermedades Infecciosas/VIH. Hospital Universitario de Burgos.
Enriqueta Muñoz Platón. Especialista en Medicina Preventiva. Servicio de Medicina Preventiva. Complejo Hospitalario de Toledo.
Marina Fernández Escribano. Especialista en Medicina del Trabajo. Servicio de Prevención de Riesgos Laborales. Hospital Ramón y Cajal. Madrid.
Jesús Sanz Sanz. Especialista en Medicina Interna. Unidad de Enfermedades Infecciosas/VIH. Hospital Universitario de La Princesa. Madrid.
Carmina Fumaz. Especialista en Psicología Clínica. Hospital de Día de VIH. Hospital Unversitario Germans Trias i Pujol. Badalona. Barcelona.
Ignacio Santos. Especialista en Medicina Interna. Unidad de Enfermedades Infecciosas/VIH. Hospital Universitario de La Princesa. Madrid.
Federico García. Especialista en Microbiología y Parasitología Clínicas. Servicio de Microbiología. Complejo Hospitalario Universitario de Granada.
M. Jesús Téllez. Especialista en Medicina Interna. Unidad de Enfermedades Infecciosas/VIH. Hospital Universitario Clínico San Carlos. Madrid.
Raúl González Montero. Especialista en Pediatría. Infectología Pediátrica. Hospital San Juan. Alicante.
M. Victoria Vals Jiménez. Especialista en Medicina del Trabajo. Servicio de Prevención de Riesgos Laborales. Área de Salud de Segovia.
Juan Emilio Losa. Especialista en Medicina Interna. Unidad de Enfermedades Infecciosas/VIH. Hospital Universitario Fundación Alcorcón. Alcorcón. Madrid.
Mª Luisa Valle Robles. Especialista en Medicina del Trabajo. Servicio de Prevención de Riesgos Laborales. Área de Salud de Segovia.
José Antonio Iribarren. Especialista en Medicina Interna. Unidad de Enfermedades Infecciosas/VIH. Hospital de Donosti. San Sebastián.
Enrique Ortega. Especialista en Medicina Interna. Unidad de Enfermedades Infecciosas/VIH. Hospital General Universitario. Valencia.