Dada la asociación entre tuberculosis (TB) e infección por VIH, la realización del Mantoux está indicada en todo paciente infectado con VIH. Este artículo analiza la frecuencia de no realización de la prueba de la tuberculina y sus factores asociados en una cohorte de infectados con VIH.
Pacientes y métodosEntre 2000–2002 se identificó en 10 hospitales a todos los pacientes infectados con VIH y no seguidos previamente, de forma regular, en consultas específicas. Se recogió información de la historia clínica sobre realización del Mantoux y otras variables. Se calculó el porcentaje de no realización del Mantoux y los factores asociados mediante la utilización como medida de asociación de la odds ratio (OR) y su intervalo de confianza (IC) del 95%. Para el análisis multivariante se ajustó un modelo de regresión logística.
ResultadosMil doscientos cuarenta y dos pacientes cumplieron criterios de inclusión y a 185 pacientes no se les realizó el Mantoux (el 17,6% de aquéllos en los que estaba indicado). La probabilidad de no realización del Mantoux fue mayor en usuarios de drogas (OR: 2,6; IC del 95%: 1,1–6,5) y menor entre los desempleados (OR: 0,6; IC del 95%: 0,3–1,0), aquéllos con más de 200 CD4 (CD4 200–499: OR: 0,5; IC del 95%: 0,3–0,9; CD4 ≥500: OR: 0,3; IC del 95%: 0,2–0,6) y los contactos con enfermos tuberculosos (OR: 0,2; IC del 95%: 0,1–0,5).
ConclusionesEl porcentaje de no realización del Mantoux es bastante elevado. La no realización del Mantoux parece asociarse con las expectativas del médico, tanto sobre el resultado de la prueba como sobre la correcta cumplimentación del tratamiento preventivo anti-TB por el paciente.
Tuberculin skin testing (TST) for tuberculosis (TB) is recommended for all patients with HIV infection because of the known relationship between these two conditions. In this report we analyze the incidence and variables associated with non-prescription of TST in a cohort of HIV-infected people.
Patients and methodsLongitudinal study conducted between 2000 and 2002 at 10 HIV hospital-based clinics. All HIV-infected patients who had not been regularly followed-up previously in dedicated clinics were identified. Data about TST and other variables related to TB were obtained from the clinical records. We calculated the percentage of patients who did not undergo TST and the associated factors, using odds ratios (ORs) and the 95% CI to investigate associations. A multivariate logistic regression analysis was performed.
ResultsA total of 1242 patients met the inclusion criteria. TST was not performed in 185 patients (17.6% of those eligible). The fact of being an intravenous drug abuser was associated with a higher probability of TST non-prescription (OR: 2.6, 95% CI 1.1–6.5), whereas being unemployed (OR: 0.6, 95% CI 0.3–1.0), having a CD4 cell count >200 (CD4 200–499: OR 0.5, 95% CI 0.3–0.9. CD4≥500: OR 0.3, 95% CI 0.2–0.6), and contact with persons with TB (OR 0.2, 95% CI 0.1–0.5) were associated with a lower probability.
ConclusionsIn this study, the percentage of TST non-prescription was quite high. The results suggest that TST non-prescription in this population is related to the clinicians’ expectations regarding the results of the test and the patients’ adherence to treatment for latent TB infection.
España ocupa el segundo lugar en incidencia tanto de tuberculosis (TB) como de sida entre los países de Europa occidental1,2 y ambas enfermedades están muy relacionadas. Año tras año la TB es la principal enfermedad indicativa de sida en nuestro país (el 28,8% en el período 2003–2006)3 a diferencia de los países de nuestro entorno, en los que la enfermedad que más frecuentemente conduce al diagnóstico de sida es la neumonía por Pneumocystis jiroveci2.
Existen evidencias de que el tratamiento de la infección tuberculosa latente (TITL) en los infectados por el VIH es una estrategia beneficiosa tanto para el paciente como para la comunidad, lo que contribuye así al control global de la TB. A nivel individual, disminuye el riesgo de desarrollar TB activa4, reduce la morbimortalidad de los individuos coinfectados5,6 y evita las complicaciones del tratamiento simultáneo de ambas enfermedades7; a nivel comunitario se disminuye el riesgo de transmisión de TB8.
El estudio “Aspectos operacionales y adherencia a quimioprofilaxis antituberculosa en sujetos VIH positivos” se puso en marcha en 1999 y sus objetivos fueron caracterizar a la población diana para la realización de quimioprofilaxis antituberculosa en sujetos VIH positivos y estimar la proporción de pacientes coinfectados por TB/VIH a los que se les prescribe, inician y finalizan el TITL, así como los factores relacionados con cada uno de estos hechos. El objetivo último era mejorar la escasa información existente en nuestro país sobre todos estos aspectos, a pesar de la importancia de la coinfección TB/VIH como problema de salud pública. Los resultados acerca de la prevalencia de infección tuberculosa y de TB actual o pasada en estos pacientes a la entrada del estudio ya se han publicado9.
En este artículo se presentan los resultados sobre la no realización de la prueba de Mantoux a la entrada en el estudio, así como los factores asociados con este hecho.
Material y métodosEntre marzo del 2000 y febrero del 2003 se identificó una cohorte de pacientes infectados con VIH y no seguidos previamente de forma regular en una consulta específica de infección por VIH, que solicitaron asistencia en los 10 hospitales participantes en el estudio. Se definió como “paciente no seguido regularmente” a todo aquel que cumplía alguna de las 2 condiciones siguientes: a) persona que acudía por primera vez a una consulta relacionada con el VIH, y b) persona que habiendo recibido atención sanitaria en relación con la infección por VIH, no se había atendido en una consulta específica para el VIH en los 2 años previos. La información sobre si se había realizado o no la prueba de la tuberculina a la entrada al estudio y otras variables clinicoepidemiológicas de interés se obtuvieron a partir de la historia clínica. Puesto que la normativa española recomienda la técnica de Mantoux para la realización de esta prueba y ésta suele ser la práctica habitual en nuestro país, en este artículo utilizaremos indistintamente los términos prueba de tuberculina y Mantoux10.
Para mejorar la validez y la consistencia de la información se elaboró un cuestionario estandarizado y un manual para la recogida de datos, y se realizaron reuniones de entrenamiento con los responsables del estudio en los diferentes hospitales. Una descripción más detallada de la metodología se ha publicado anteriormente9.
En el análisis de datos se calculó el porcentaje de sujetos de estudio a los que no se les había realizado el Mantoux y sus intervalos de confianza (IC) del 95%, tanto en el global del estudio como estratificado por diversas variables. Para evaluar la asociación entre variables cualitativas, se empleó el test de χ2. Se utilizó la odds ratio (OR) y su IC del 95% como medida de asociación y se realizó un análisis multivariante de regresión logística de acuerdo con la estrategia de modelización de Hosmer y Lemeshow11 para evaluar los factores relacionados con la no realización de la prueba de la tuberculina. El análisis estadístico se realizó mediante el programa STATA (versión 10.0)12.
Resultados- (a)
Características de los sujetos de estudio
Un total de 1.242 enfermos cumplieron los criterios de inclusión del estudio. Los sujetos fueron mayoritariamente hombres (74,7%), de nacionalidad española (87,6%) y con una edad media de 36 años (DE: 8,5). El 52,5% no tenía estudios o había realizado sólo estudios primarios y un alto porcentaje de los sujetos (39,5%) se encontraba en situación de desempleo. El uso de drogas por vía parenteral (UDVP) actual o previo fue la práctica de riesgo más común para la infección por VIH (53,0%), seguida de las relaciones heterosexuales (28,6%) y homo/bisexuales no protegidas (15,6%), y por otros mecanismos o no constaba información (2,8%). Respecto a la situación clínica a la entrada en el estudio, el 39% de los enfermos presentaba más de 55.000copias/ml de carga viral y el 36% menos de 200CD4/μl. En relación con la TB, 184 pacientes (14,8%) referían antecedentes de contacto previo con un enfermo tuberculoso y 216 pacientes (17,4%) presentaban escara posvacunación9.
- (b)
Candidatos a screening de la infección tuberculosa latente (ITL) y realización de prueba de la tuberculina
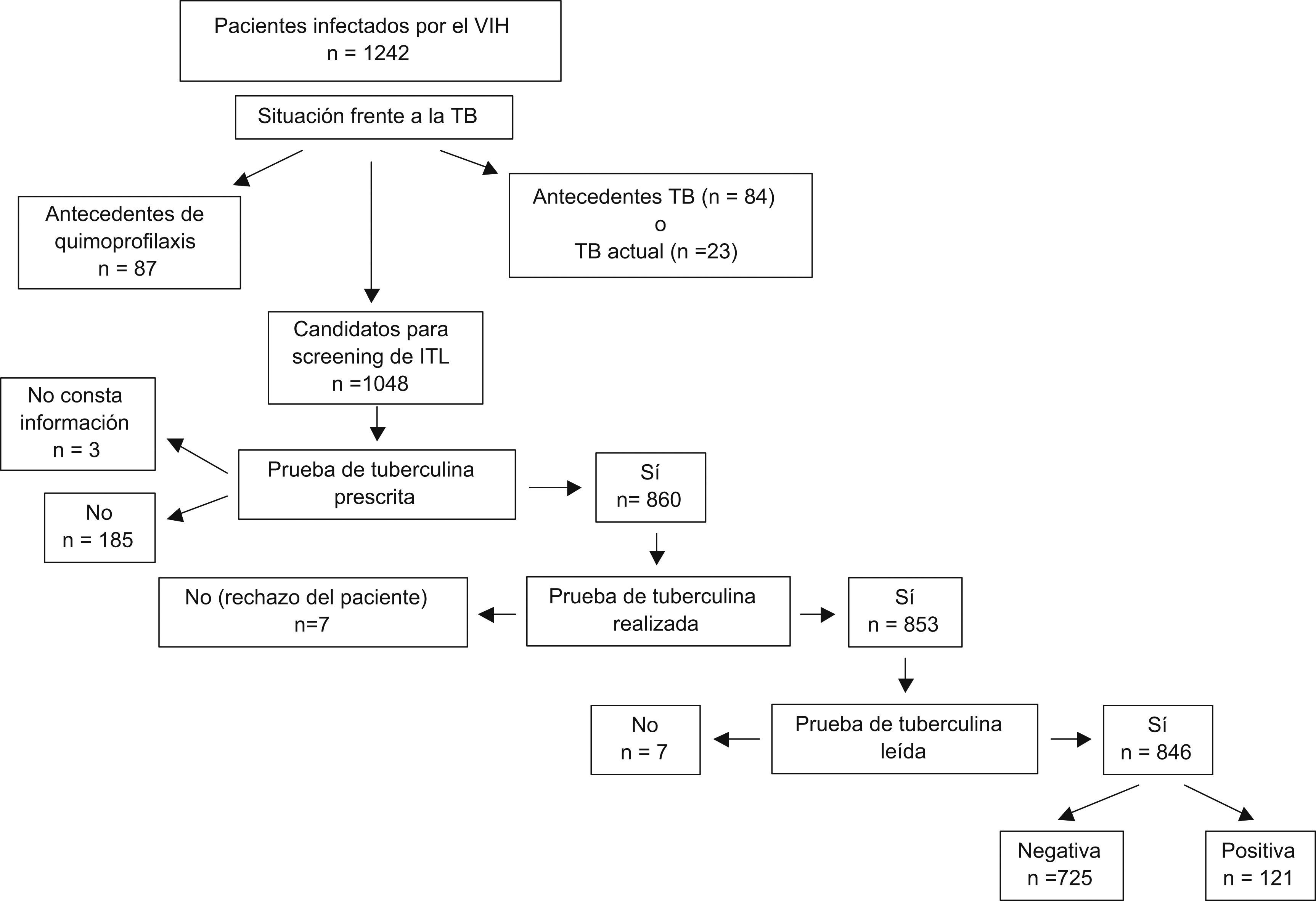
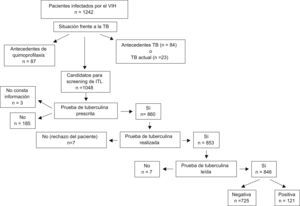
En la evaluación diagnóstica inicial, de los 1.242 pacientes incluidos en el estudio, se encontró que 84 (6,8%) habían presentado TB en el pasado, 23 (1,8%) la presentaban en ese momento, 87 (7,0%) tenían antecedentes de quimioprofilaxis antituberculosa y los 1.048 restantes eran candidatos a screening de la ITL9. De entre estos últimos, se prescribió la prueba de la tuberculina a 860 (82,1%), no se les prescribió la prueba a 185 (17,6%) y en 3 casos (0,3%) no constaba información. Un total de 7 sujetos rechazó la prueba, por lo que finalmente ésta se realizó a 853 casos, de los que 7 no acudieron a la lectura (fig. 1). Así, pues, la prueba tuberculínica se prescribió y se realizó en 853 pacientes y no se prescribió en 185 pacientes, lo que supone un 81,4 y un 17,6%, respectivamente, de los 1.048 candidatos al screening de la ITL. Las características de los pacientes a los que no se les realizó la prueba de la tuberculina se muestran en las tablas 1 y 2.
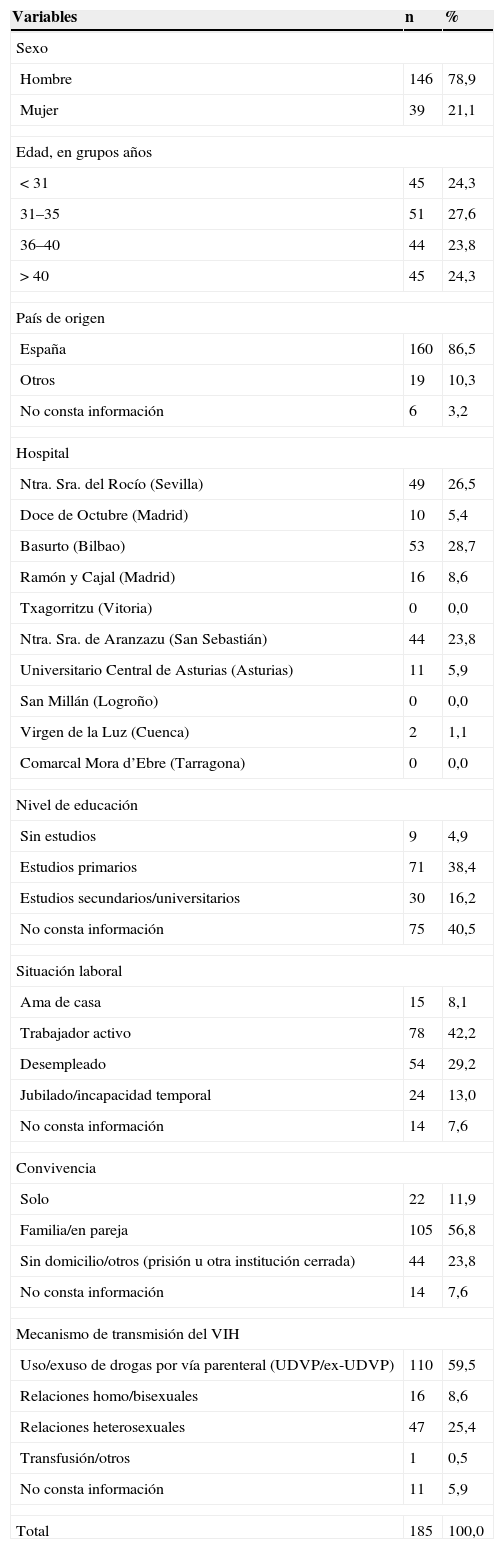
Tabla 1.Características sociodemográficas de los sujetos a los que no se les realizó la prueba de la tuberculina
Variables n % Sexo Hombre 146 78,9 Mujer 39 21,1 Edad, en grupos años < 31 45 24,3 31–35 51 27,6 36–40 44 23,8 > 40 45 24,3 País de origen España 160 86,5 Otros 19 10,3 No consta información 6 3,2 Hospital Ntra. Sra. del Rocío (Sevilla) 49 26,5 Doce de Octubre (Madrid) 10 5,4 Basurto (Bilbao) 53 28,7 Ramón y Cajal (Madrid) 16 8,6 Txagorritzu (Vitoria) 0 0,0 Ntra. Sra. de Aranzazu (San Sebastián) 44 23,8 Universitario Central de Asturias (Asturias) 11 5,9 San Millán (Logroño) 0 0,0 Virgen de la Luz (Cuenca) 2 1,1 Comarcal Mora d’Ebre (Tarragona) 0 0,0 Nivel de educación Sin estudios 9 4,9 Estudios primarios 71 38,4 Estudios secundarios/universitarios 30 16,2 No consta información 75 40,5 Situación laboral Ama de casa 15 8,1 Trabajador activo 78 42,2 Desempleado 54 29,2 Jubilado/incapacidad temporal 24 13,0 No consta información 14 7,6 Convivencia Solo 22 11,9 Familia/en pareja 105 56,8 Sin domicilio/otros (prisión u otra institución cerrada) 44 23,8 No consta información 14 7,6 Mecanismo de transmisión del VIH Uso/exuso de drogas por vía parenteral (UDVP/ex-UDVP) 110 59,5 Relaciones homo/bisexuales 16 8,6 Relaciones heterosexuales 47 25,4 Transfusión/otros 1 0,5 No consta información 11 5,9 Total 185 100,0 UDVP: uso de drogas por vía parenteral; VIH: virus de la inmunodeficiencia humana.
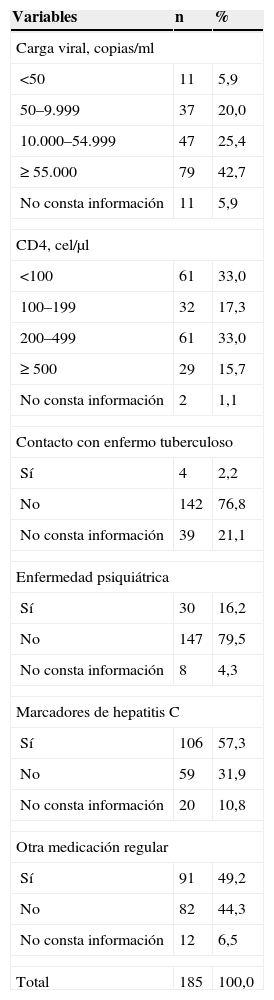
Tabla 2.Características clínicas de los sujetos a los que no se les realizó la prueba de la tuberculina
Variables n % Carga viral, copias/ml <50 11 5,9 50–9.999 37 20,0 10.000–54.999 47 25,4 ≥ 55.000 79 42,7 No consta información 11 5,9 CD4, cel/μl <100 61 33,0 100–199 32 17,3 200–499 61 33,0 ≥ 500 29 15,7 No consta información 2 1,1 Contacto con enfermo tuberculoso Sí 4 2,2 No 142 76,8 No consta información 39 21,1 Enfermedad psiquiátrica Sí 30 16,2 No 147 79,5 No consta información 8 4,3 Marcadores de hepatitis C Sí 106 57,3 No 59 31,9 No consta información 20 10,8 Otra medicación regular Sí 91 49,2 No 82 44,3 No consta información 12 6,5 Total 185 100,0 - (c)
Factores asociados con la no realización de la prueba de la tuberculina
Para examinar la proporción de no realización de la prueba según otras variables de interés, se analizaron los 1.038 casos en los que la realización o no del Mantoux dependió exclusivamente del criterio médico, y se excluyó del análisis a los pacientes que rechazaron la prueba y a aquéllos en los que no constaba información al respecto.
La no realización de la prueba fue superior en los pacientes españoles (17,8%), en personas con estudios primarios (16,8%), en jubilados/personas en situación de incapacidad laboral (28,9%) y en aquellos que no tenían domicilio fijo o residían en instituciones cerradas (21,4%). Al estratificar por variables clínicas, la no realización del Mantoux fue mayor en los pacientes que habían adquirido el VIH a través del uso de drogas intravenosas respecto a aquéllos en los que el mecanismo de transmisión fue sexual (el 21,2% por el UDVP frente al 15,2% en heterosexuales y el 9,0% en homo/bisexuales) y fue menor conforme se incrementa el nivel de CD4. Además, el Mantoux se realizó con menor frecuencia cuando: a) no había antecedentes de contacto con un enfermo tuberculoso; b) los pacientes presentaban marcadores de la hepatitis C o enfermedad psiquiátrica, y c) los sujetos tomaban otra medicación de forma regular (tablas 3 y 4).
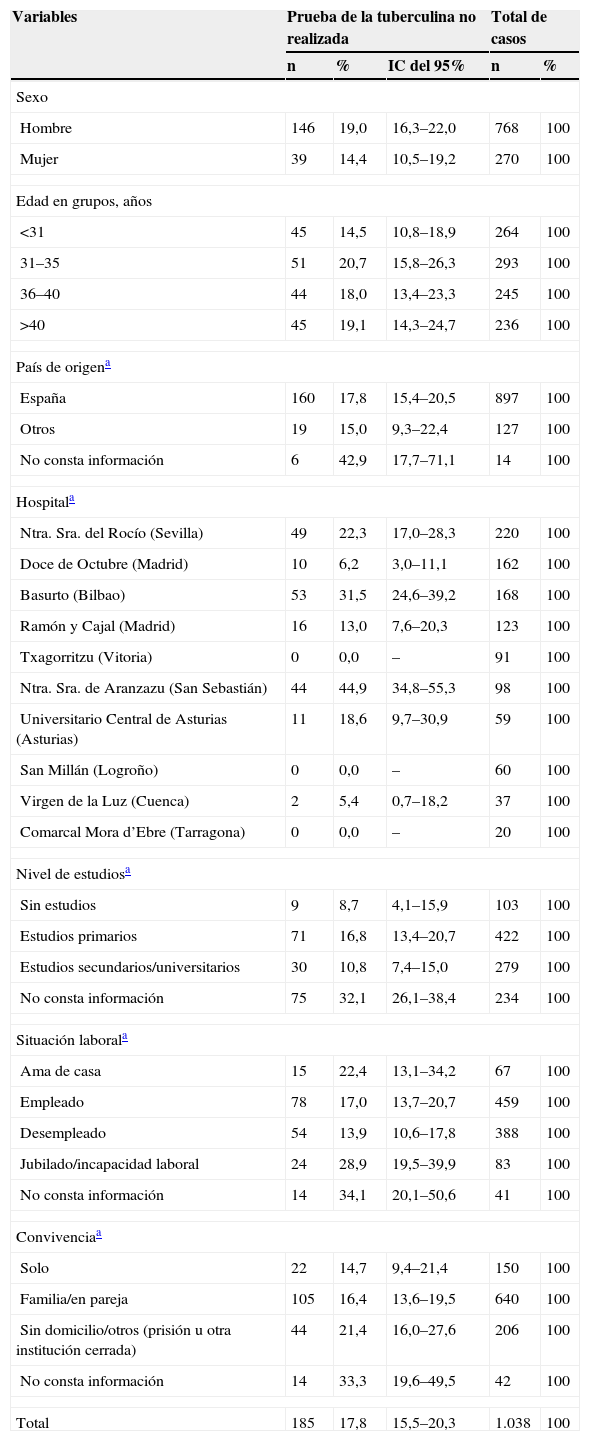
Tabla 3.Prevalencia (%) e intervalo de confianza del 95% de no realización de la prueba de la tuberculina según variables sociodemográficas
Variables Prueba de la tuberculina no realizada Total de casos n % IC del 95% n % Sexo Hombre 146 19,0 16,3–22,0 768 100 Mujer 39 14,4 10,5–19,2 270 100 Edad en grupos, años <31 45 14,5 10,8–18,9 264 100 31–35 51 20,7 15,8–26,3 293 100 36–40 44 18,0 13,4–23,3 245 100 >40 45 19,1 14,3–24,7 236 100 País de origena España 160 17,8 15,4–20,5 897 100 Otros 19 15,0 9,3–22,4 127 100 No consta información 6 42,9 17,7–71,1 14 100 Hospitala Ntra. Sra. del Rocío (Sevilla) 49 22,3 17,0–28,3 220 100 Doce de Octubre (Madrid) 10 6,2 3,0–11,1 162 100 Basurto (Bilbao) 53 31,5 24,6–39,2 168 100 Ramón y Cajal (Madrid) 16 13,0 7,6–20,3 123 100 Txagorritzu (Vitoria) 0 0,0 – 91 100 Ntra. Sra. de Aranzazu (San Sebastián) 44 44,9 34,8–55,3 98 100 Universitario Central de Asturias (Asturias) 11 18,6 9,7–30,9 59 100 San Millán (Logroño) 0 0,0 – 60 100 Virgen de la Luz (Cuenca) 2 5,4 0,7–18,2 37 100 Comarcal Mora d’Ebre (Tarragona) 0 0,0 – 20 100 Nivel de estudiosa Sin estudios 9 8,7 4,1–15,9 103 100 Estudios primarios 71 16,8 13,4–20,7 422 100 Estudios secundarios/universitarios 30 10,8 7,4–15,0 279 100 No consta información 75 32,1 26,1–38,4 234 100 Situación laborala Ama de casa 15 22,4 13,1–34,2 67 100 Empleado 78 17,0 13,7–20,7 459 100 Desempleado 54 13,9 10,6–17,8 388 100 Jubilado/incapacidad laboral 24 28,9 19,5–39,9 83 100 No consta información 14 34,1 20,1–50,6 41 100 Convivenciaa Solo 22 14,7 9,4–21,4 150 100 Familia/en pareja 105 16,4 13,6–19,5 640 100 Sin domicilio/otros (prisión u otra institución cerrada) 44 21,4 16,0–27,6 206 100 No consta información 14 33,3 19,6–49,5 42 100 Total 185 17,8 15,5–20,3 1.038 100 IC: intervalo de confianza.
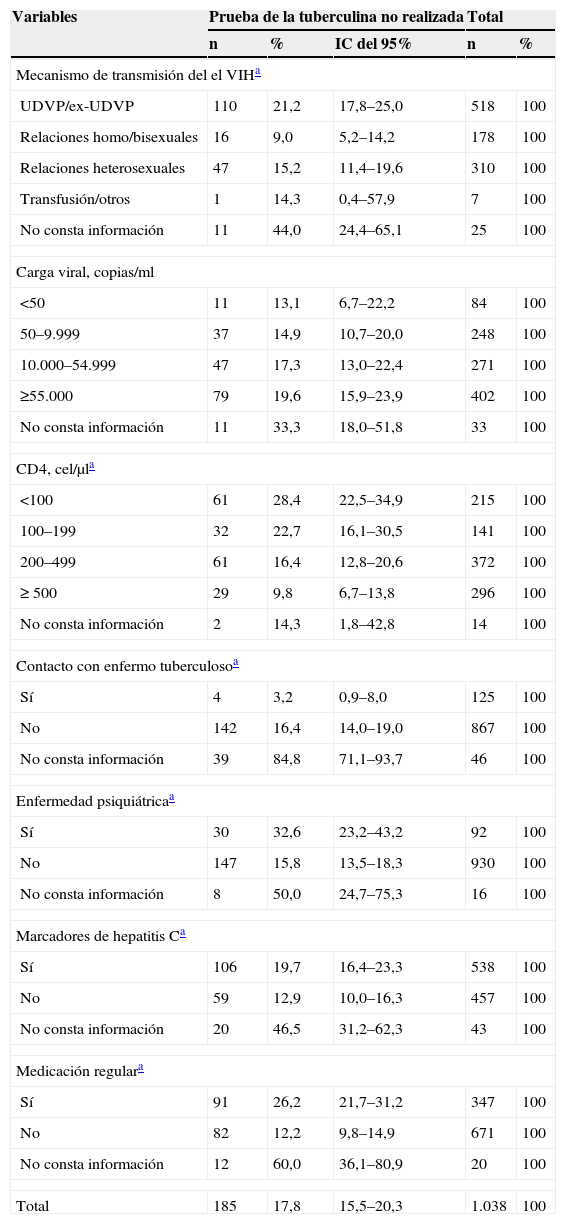
Tabla 4.Prevalencia (%) e intervalo de confianza del 95% de no realización de la prueba de la tuberculina según variables clínicas
Variables Prueba de la tuberculina no realizada Total n % IC del 95% n % Mecanismo de transmisión del el VIHa UDVP/ex-UDVP 110 21,2 17,8–25,0 518 100 Relaciones homo/bisexuales 16 9,0 5,2–14,2 178 100 Relaciones heterosexuales 47 15,2 11,4–19,6 310 100 Transfusión/otros 1 14,3 0,4–57,9 7 100 No consta información 11 44,0 24,4–65,1 25 100 Carga viral, copias/ml <50 11 13,1 6,7–22,2 84 100 50–9.999 37 14,9 10,7–20,0 248 100 10.000–54.999 47 17,3 13,0–22,4 271 100 ≥55.000 79 19,6 15,9–23,9 402 100 No consta información 11 33,3 18,0–51,8 33 100 CD4, cel/μla <100 61 28,4 22,5–34,9 215 100 100–199 32 22,7 16,1–30,5 141 100 200–499 61 16,4 12,8–20,6 372 100 ≥ 500 29 9,8 6,7–13,8 296 100 No consta información 2 14,3 1,8–42,8 14 100 Contacto con enfermo tuberculosoa Sí 4 3,2 0,9–8,0 125 100 No 142 16,4 14,0–19,0 867 100 No consta información 39 84,8 71,1–93,7 46 100 Enfermedad psiquiátricaa Sí 30 32,6 23,2–43,2 92 100 No 147 15,8 13,5–18,3 930 100 No consta información 8 50,0 24,7–75,3 16 100 Marcadores de hepatitis Ca Sí 106 19,7 16,4–23,3 538 100 No 59 12,9 10,0–16,3 457 100 No consta información 20 46,5 31,2–62,3 43 100 Medicación regulara Sí 91 26,2 21,7–31,2 347 100 No 82 12,2 9,8–14,9 671 100 No consta información 12 60,0 36,1–80,9 20 100 Total 185 17,8 15,5–20,3 1.038 100 IC: intervalo de confianza; UDVP: uso de drogas por vía parenteral; VIH: virus de la inmunodeficiencia humana.
En el análisis multivariante se evaluaron todas aquellas variables que habían sido significativas en el bivariante y las que, sin serlo, tenían interés epidemiológico. En este proceso se eliminaron del modelo final las variables no significativas que estuvieran relacionadas con otras ya incluidas en el modelo, ya que de lo contrario se hubieran producido problemas en la estimación del modelo debido a la colinealidad; por esta razón, se ha eliminado la variable convivencia.
En el modelo ajustado, la probabilidad de no realización del Mantoux fue mayor en los UDVP (OR: 2,6; IC del 95%: 1,1–6,5). Por el contrario, la probabilidad de no realización de Mantoux fue menor en los pacientes desempleados (OR: 0,6; IC del 95%: 0,3–1,0), en los que referían antecedentes de contacto con un enfermo tuberculoso (OR: 0,2; IC del 95%: 0,1–0,5) y cuando el nivel de CD4 era superior a 200cel/μl (CD4 entre 200–499: OR: 0,5; IC del 95%: 0,3–0,9; CD4≥500: OR: 0,3; IC del 95%: 0,2–0,6) (tabla 5).
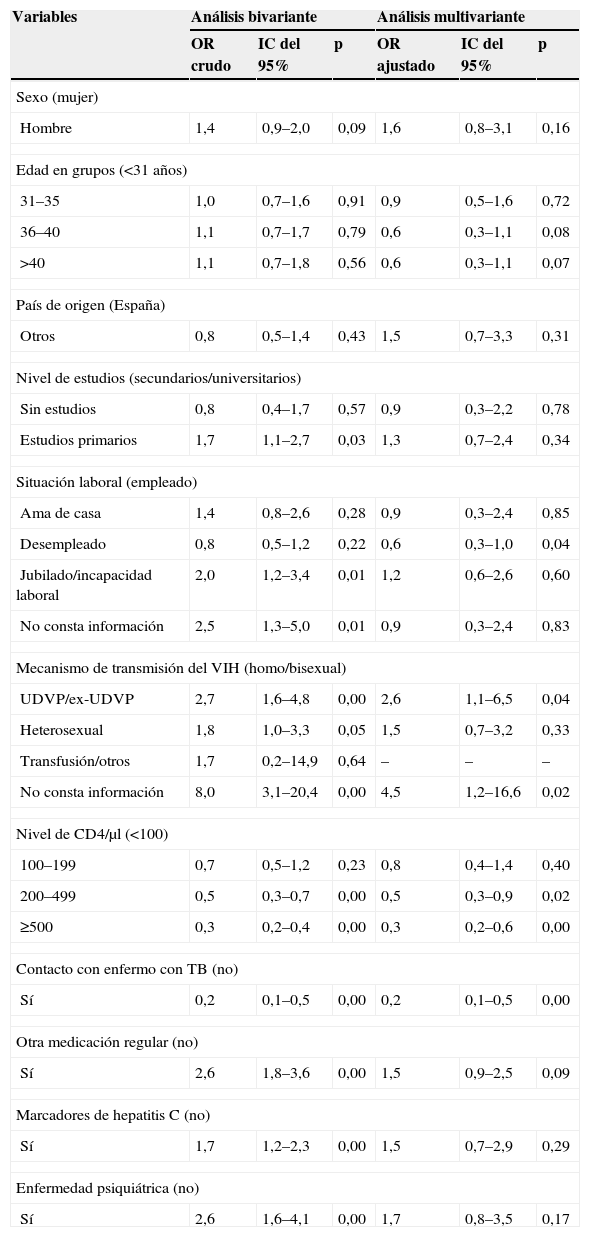
Tabla 5.Variables asociadas con la no realización de la prueba de la tuberculina. Odds ratio crudo, odds ratio ajustado e intervalos de confianza del 95% (n = 1.038)
Variables Análisis bivariante Análisis multivariante OR crudo IC del 95% p OR ajustado IC del 95% p Sexo (mujer) Hombre 1,4 0,9–2,0 0,09 1,6 0,8–3,1 0,16 Edad en grupos (<31 años) 31–35 1,0 0,7–1,6 0,91 0,9 0,5–1,6 0,72 36–40 1,1 0,7–1,7 0,79 0,6 0,3–1,1 0,08 >40 1,1 0,7–1,8 0,56 0,6 0,3–1,1 0,07 País de origen (España) Otros 0,8 0,5–1,4 0,43 1,5 0,7–3,3 0,31 Nivel de estudios (secundarios/universitarios) Sin estudios 0,8 0,4–1,7 0,57 0,9 0,3–2,2 0,78 Estudios primarios 1,7 1,1–2,7 0,03 1,3 0,7–2,4 0,34 Situación laboral (empleado) Ama de casa 1,4 0,8–2,6 0,28 0,9 0,3–2,4 0,85 Desempleado 0,8 0,5–1,2 0,22 0,6 0,3–1,0 0,04 Jubilado/incapacidad laboral 2,0 1,2–3,4 0,01 1,2 0,6–2,6 0,60 No consta información 2,5 1,3–5,0 0,01 0,9 0,3–2,4 0,83 Mecanismo de transmisión del VIH (homo/bisexual) UDVP/ex-UDVP 2,7 1,6–4,8 0,00 2,6 1,1–6,5 0,04 Heterosexual 1,8 1,0–3,3 0,05 1,5 0,7–3,2 0,33 Transfusión/otros 1,7 0,2–14,9 0,64 – – – No consta información 8,0 3,1–20,4 0,00 4,5 1,2–16,6 0,02 Nivel de CD4/μl (<100) 100–199 0,7 0,5–1,2 0,23 0,8 0,4–1,4 0,40 200–499 0,5 0,3–0,7 0,00 0,5 0,3–0,9 0,02 ≥500 0,3 0,2–0,4 0,00 0,3 0,2–0,6 0,00 Contacto con enfermo con TB (no) Sí 0,2 0,1–0,5 0,00 0,2 0,1–0,5 0,00 Otra medicación regular (no) Sí 2,6 1,8–3,6 0,00 1,5 0,9–2,5 0,09 Marcadores de hepatitis C (no) Sí 1,7 1,2–2,3 0,00 1,5 0,7–2,9 0,29 Enfermedad psiquiátrica (no) Sí 2,6 1,6–4,1 0,00 1,7 0,8–3,5 0,17 Las categorías de referencia se muestran entre paréntesis. Modelo multivariante ajustado por hospital.
IC: intervalo de confianza; OR: odds ratio; TB: tuberculosis; UDVP: uso de drogas por vía parenteral; VIH: virus de la inmunodeficiencia humana.
En este estudio se presentan datos sobre realización del test tuberculínico y los factores asociados con este hecho en un número importante de personas infectadas por VIH identificadas en 10 hospitales españoles situados en un ámbito geográfico muy amplio. En España hay poca información de este tipo13, a pesar de que la prevalencia de ITL en infectados por VIH es alta9 y, por tanto, el screening y el tratamiento de la ITL en estas personas debería ser una prioridad.
El porcentaje de no realización de la prueba de la tuberculina en este estudio fue del 17,6% de aquéllos en los que estaba indicada. Esta cifra es inferior a la referida en estudios retrospectivos realizados en Estados Unidos14–16 (donde la no realización osciló entre el 36 y el 54%) y al 31% encontrado en un estudio prospectivo en Suiza17; sin embargo, es superior al 11% publicado en un estudio de cohortes realizado en Italia18.
Un hecho que cabe destacar es la baja proporción de pacientes que rechazan hacerse la prueba o no acuden a su lectura (0,8%) en comparación con las cifras halladas en otros estudios. En el estudio italiano, por ejemplo, el 10% de los enfermos rechazó hacerse la tuberculina y de aquéllos a los que se les realizó, el 7% no acudió a la lectura18. En Nueva York, el 11% de las personas a las que se les practicó una prueba de tuberculina no acudió para su lectura16.
En este estudio se observa, como cabía esperar, una menor probabilidad de no prescripción y realización del Mantoux en personas que refieren un contacto con un enfermo de TB y también en aquellas que están desempleadas. Asimismo, la no realización del Mantoux fue menor cuando la cifra de CD4 superaba los 200cel/μl, un resultado similar al encontrado en otros estudios16; estos hallazgos, al igual que los de otros autores que han comunicado la menor realización de la prueba cuando hay un diagnóstico de sida18 o cuando se ha prescrito medicación antirretroviral17, parecen reflejar la dificultad de los clínicos para interpretar resultados negativos del Mantoux en situaciones de inmunodepresión grave, razón por la que ni siquiera solicitan la prueba cuando anticipan esta circunstancia. Aunque desde hace tiempo existen pruebas que, en teoría, permitirían evaluar la presencia de anergia, no están indicadas para la toma de decisiones clínicas en el caso de la ITL19,20; en cuanto a los nuevos test desarrollados para la detección de la ITL21, si bien algunos estudios indican que son más sensibles que el test tuberculínico en personas inmunodeprimidas22–24, precisan todavía de estudios adicionales para evaluar la interpretación de los resultados indeterminados a niveles de CD4 inferiores a 100 células25,26 así como los resultados discordantes con la prueba de la tuberculina22,24,26.
Los pacientes con UDVP tuvieron mayor probabilidad de que no se les realizara el Mantoux, al igual que en la cohorte de Suiza17; esto se debe, probablemente, a la sospecha de mala adherencia al tratamiento de la ITL si el resultado de la prueba fuera positivo y fuera necesario indicarlo. Sin embargo, un ensayo clínico realizado en Alicante27, así como estudios observacionales internacionales28,29, muestra buenos resultados del tratamiento de la ITL en estos pacientes, en términos de reducción de la incidencia de TB. Todos estos estudios se han realizado dentro de programas de mantenimiento de metadona y a través de tratamientos directamente observados (TDO), lo que refuerza el cumplimiento del tratamiento.
En conclusión, nuestros resultados muestran un porcentaje no desdeñable de no realización de la prueba de la tuberculina para descartar ITL en pacientes infectados por el VIH, a pesar de que en España se recomienda realizar el Mantoux a todos estos pacientes en la evaluación diagnóstica inicial20.
La no realización del Mantoux parece estar relacionada con las expectativas de los médicos que deben prescribirlo, tanto en cuanto al resultado de la prueba como a la probabilidad de que el paciente complete el tratamiento para la ITL. A pesar de la amplia introducción del tratamiento antirretroviral de gran actividad (TARGA) en nuestro país y del impacto positivo que ha tenido en la TB, los datos indican que hay que reforzar otras intervenciones para mejorar el control de la TB en pacientes infectados por el VIH. Entre ellas, habría que destacar el TDO en el contexto de los programas de mantenimiento con metadona para los pacientes con UDVP y las medidas de apoyo social para que las personas en situación desfavorable puedan cumplir con el tratamiento de forma adecuada.
FinanciaciónEste trabajo ha contado con financiación de la Fundación para la Investigación y la Prevención del Sida en España (FIPSE) (exp: 3041/99)
Este trabajo ha contado con financiación de la Fundación para la Investigación y la Prevención del Sida en España (FIPSE) (exp: 3041/99).