Valorar la utilidad de una herramienta informática integrada en el programa de historia clínica de urgencias en el momento del triaje, para detectar de forma precoz pacientes con sepsis grave, y su posible repercusión en reducir las cifras de mortalidad en los pacientes atendidos.
MétodoEl estudio constaba de 2 muestras comparativas. La selección de pacientes se realizó de forma retrospectiva en los 2 grupos utilizando los códigos CIE-9 al alta de urgencias y hospitalaria 038.9, 995.91 para la sepsis, 995.92 para sepsis grave y 785.52 para shock séptico. La muestra denominada «alarmas» constaba de los pacientes estudiados tras implantar el sistema de alarmas de sepsis en el sistema informático de urgencias. Se definieron 2 tipos de alarmas, una de gravedad y otra de alerta en función de las constantes vitales alteradas. La muestra histórica, denominada «sin alarmas», constaba de pacientes atendidos en el servicio de urgencias durante el año previo a la implantación del sistema de alarmas.
ResultadosEl porcentaje de cumplimiento del paquete de tratamiento de la sepsis fue mayor en la muestra de alarmas, comparativamente con la muestra sin alarmas, respectivamente, para los hemocultivos 96,3% frente a 80,9% (p<0,001), antibiótico menor a 1h 62,9% frente a 39,3% (p<0,001), determinación de ácido láctico 91,4% frente a 77,9% (p<0,001) y la aplicación de volumen adecuado 57,7% frente a 54,3% (p=0,54). La mortalidad durante el ingreso se redujo en términos absolutos del 25% de la muestra sin alarmas al 13,6% en la muestra con alarmas. La supervivencia a los 30 días fue mayor en la muestra de alarmas (log rank=0,004).
ConclusionesUn sistema electrónico de identificación de pacientes con sepsis permite una mayor precocidad en la actuación, un cumplimiento mejor de las medidas básicas y por tanto una disminución de la estancia y la mortalidad.
The objective of this study was to assess the usefulness of a software tool integrated into the medical electronic history at the time of emergency triage. The aim was the early detection of patients with severe sepsis, and the potential impact of this software tool on reducing the mortality rate in patients treated.
MethodThe study consisted of two comparative samples. Patient selection was performed retrospectively into two groups using ICD-9 codes from the hospital and emergency department discharge reports. The codes were 038.9, 995.9 and 995.92 for sepsis, and 785.52 for severe sepsis and septic shock. The sample called «alarms» consisted of patients studied after implementing the sepsis alarm system in the Emergency Department computer system. There were two types of alarms, a serious one and an alert one depending on the on vital signs defined. The historical sample called «no alarms» consisted of patients seen in the Emergency Department during the year before the introduction of the alarm system.
ResultsThe compliance rate of the sepsis treatment package was higher in the «alarms» sample, compared to the sample without alarms, with blood cultures, 96.3% versus 80.9% (P<.001), antibiotic treatment in less than one hour, 62.9% vs. 39.3% (P<.001), determination of lactic acid, 91.4% vs. 77.9% (P<.001), and applying appropriate volume, 57.7% vs 54.3% (P=.052), respectively. The hospital mortality was reduced in absolute terms from 25% in the sample without alarms to 13.6% in the sample with alarms. Survival at 30 days was higher in the sample with alarms (Log Rank=.004).
ConclusionsThere were no studies that evaluated the effectiveness of an alarm system in our literature search. An electronic identification system for patients with sepsis allows acting earlier, better compliance with basic measures, and a reduction in hospital stay and mortality.
Las infecciones constituyen un 14,3% de las urgencias hospitalarias en nuestro país1. De todas ellas un 6,3% cumplen criterios diagnósticos de sepsis1. Se estima que se presentan unos 50.000-100.000 casos de sepsis/año, de los cuales un 30% evolucionarán a cuadros de sepsis grave (SG) o shock séptico (SS). La mortalidad en ambos casos es muy elevada, siendo del 20-25% en la SG y del 45% en el caso de SS2. Además, en los últimos años su incidencia ha aumentado a una tasa anual del 8-13%, tanto en Europa como en Estados Unidos, lo que se relaciona con factores como aumento de la edad de la población, incremento de la realización de técnicas invasivas, estados de inmunodepresión por fármacos, enfermos tratados con quimioterapia, etc.3–6.
A esta prevalencia se une la complejidad en su diagnóstico, ya que es una enfermedad difícil de identificar. Ante una infección grave, el organismo, presenta una respuesta sistémica inespecífica, con unos signos y síntomas muy generales y que con facilidad conducen a confusión y a error diagnóstico. Esta ausencia de criterios clínicos y diagnósticos bien definidos han dificultado el avance en el conocimiento clínico-epidemiológico de esta entidad. De hecho, han sido precisas varias conferencias internacionales de consenso para definir el concepto de sepsis7.
Con el enfoque actual, la SG y el SS pertenecen al grupo de enfermedades tiempo-dependiente, entendiendo como tales aquellas en las que un retraso en el diagnóstico o en el tratamiento influye negativamente en la evolución. Así pues, los servicios de urgencias pasan a tener un papel crucial tanto en la detección precoz como en el inicio del tratamiento de la SG/SS8. Para garantizar una asistencia ajustada al factor tiempo se han creado unos códigos, cuya activación se basa en datos clínicos, como es el caso del código ictus o el código dolor torácico. Estos códigos han demostrado disminuir la morbimortalidad al priorizar la asistencia y el tratamiento.
La Comunidad de Aragón utiliza el programa informático denominado Puesto clínico hospitalario (PCH). Se decidió integrar la activación del código de sepsis grave (CSG) a través de los parámetros que se obtienen en el momento de triaje de una forma automática dentro del propio programa informático. De esta manera, se buscaba alertar de forma precoz al personal sanitario (personal facultativo y de enfermería) de los posibles casos de SG y SS.
El objetivo de nuestro estudio fue comparar el comportamiento de los enfermos detectados por el sistema de alarma e incluidos en el CSG, con respecto a una muestra del año previo, para determinar la utilidad real de esta nueva herramienta.
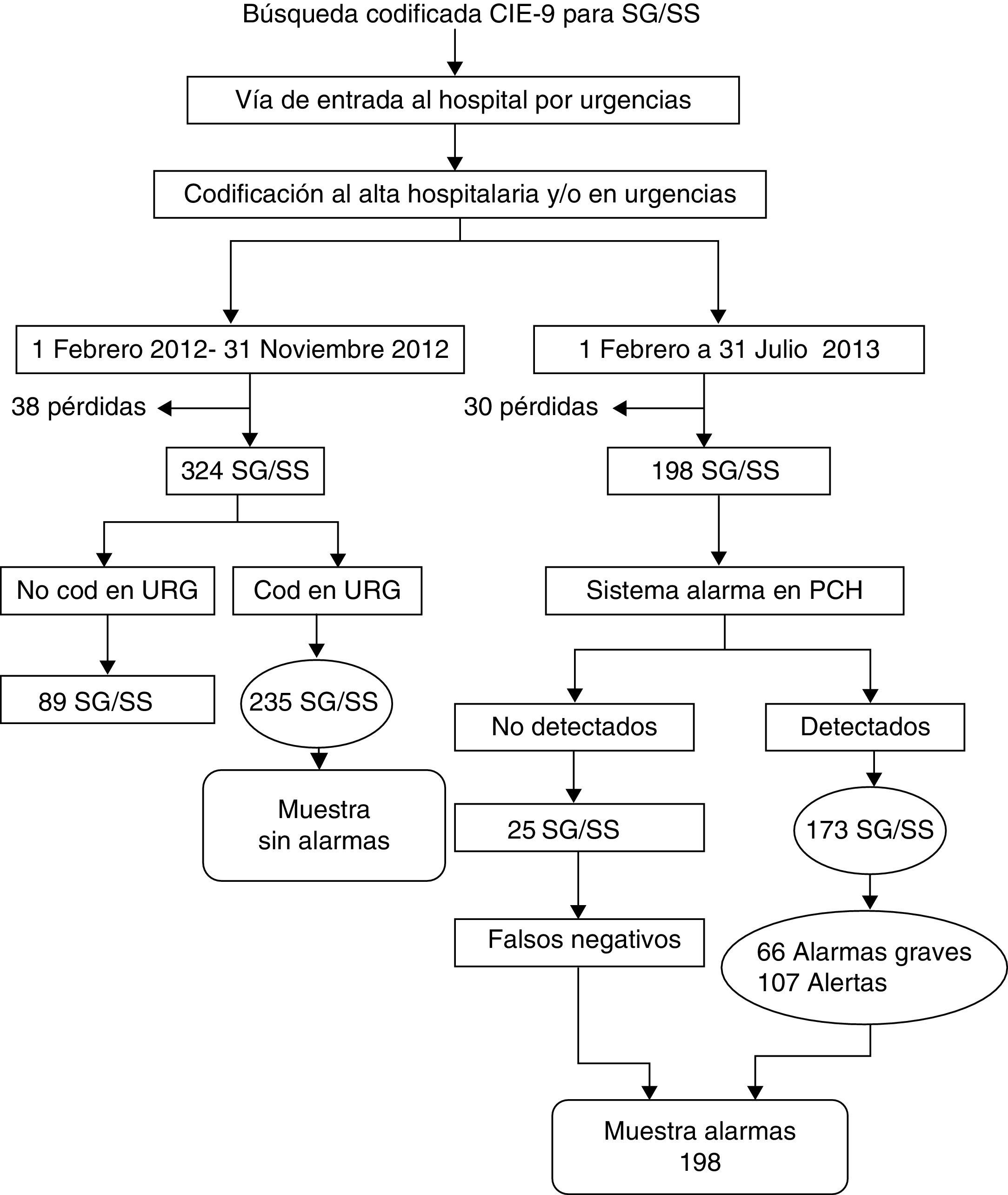
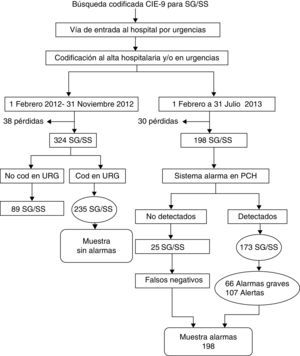
MétodosEstudio cuasi-experimental con control histórico tras la implantación de un sistema automático de detección de sepsis en el triaje realizado en el Servicio de Urgencias del Hospital Royo Villanova de Zaragoza. La selección de pacientes (fig. 1) se realizó de forma retrospectiva en los 2 grupos utilizando los códigos CIE-9 al alta de urgencias y hospitalaria 038.9, 995.91 para la sepsis, 995.92 para SG y 785.52 para SS, utilizando como periodos de tiempo para el grupo «alarmas» del 1 de febrero al 31 de julio de 2013 y para el grupo «sin alarmas» del 1 febrero de 2012 al 31 de noviembre 2012.
La formación que recibió el personal sanitario en los 2 periodos del estudio fue equivalente: tríptico resumen de la campaña sobrevivir a la sepsis (SSC), sesiones clínicas periódicas y jornada formativa autonómica de un día.
Aplicación de alarmas en el momento del triajePara la activación de las alarmas informáticas se tomó la definición de sepsis según la conferencia de consenso ACCP/SCCM (Bone et al., 1999) y la posterior actualización de la definición en la siguiente conferencia de consenso SCCM/ESICM/ACC/ATS/SIS (Levy et al., 2003)7, formando parte del algoritmo los siguientes parámetros: presión arterial sistólica<90mmHg, taquicardia (>90/min), fiebre (>38°C) o hipotermia (<36°C), taquipnea (>30/min), hipoxemia (saturación de O2<90%), hiperglucemia (>140mg/dl, en ausencia de haber respondido afirmativamente al apartado de diabetes), así como la presencia de 2 circunstancias, la sospecha de infección y la alteración del estado mental. Tanto los aparatos de medida como el personal de triaje no sufrieron modificaciones a lo largo del periodo de estudio.
Siguiendo la definición de sepsis se constituyó el algoritmo de alarmas para que hubiera una advertencia visual automática desde el programa al introducir las constantes de la siguiente manera: a) alteración de 2 parámetros cualquiera que no sean hipotensión (alerta); b) alteración de 2 parámetros, siendo uno de ellos hipotensión (alarma grave); c) alteración de 3 o más parámetros (alarma grave).
Cuando el paciente cumplía criterios de alerta o alarma grave se activaba de forma automática una alarma visual manifestada de las siguientes formas: a) mediante un desplegable que se mostraba a la enfermería de triaje. En él se recomendaba la activación del CSG y la aplicación del antibiótico en menos de 1h; b) mediante la coloración verde en el listado general de enfermos pendientes de ser atendidos por el médico, buscando un contraste visual que alertaba al facultativo sobre un paciente que debía ser atendido de forma prioritaria; c) en la historia clínica del enfermo aparecía una «pestaña» específica de sepsis en la que se recogía información útil para su manejo (protocolo de actuación de la Campaña Sobrevivir a la Sepsis [SSC], descripción de los paquetes de medidas a seguir [bundles], antibiótico empleado en<1h, cumplimiento de variables hemodinámicas, criterios de disfunción orgánica [bilirrubina, creatinina, ácido láctico, INR, recuento de plaquetas, hipotensión, hipoxemia, oliguria]) y limitación del esfuerzo terapéutico.
Tras los pasos anteriores el facultativo que atendía al paciente era finalmente quien determinaba si realmente era un «caso» para proseguir con el Código sepsis o no. Es decir, los casos de SRIS detectados en triaje alertaban para que el médico identificara de forma precoz si era causado por una infección o no, de la misma forma que las alertas obtenidas a través de la sospecha de infección más otro parámetro debían ser ratificadas como «caso» por el médico responsable. En cualquier caso, siempre era el facultativo el que indicaba qué medidas terapéuticas se iban a realizar.
Cuando se detectaba una alarma de gravedad el programa asignaba de forma automática un nivel de triaje ii. La asignación de este nivel se realizaba con independencia del valor obtenido por el programa web_e_pat (SET). Era posible obtener un nivel de triaje más alto en el SET y posteriormente que el sistema de alarmas asignara un nivel de mayor gravedad en función de las constantes.
Los pacientes detectados por este sistema de alarmas en el servicio de urgencias, de manera automática, generaban desde el sistema un mensaje de correo electrónico a una dirección de correo corporativa con los datos del enfermo y del ingreso.
Criterios de exclusiónComo criterios de exclusión comunes para ambas muestras fueron: pacientes que no cumplían criterios de SG/SS. No recogido en la historia clínica al menos un 60% de los datos requeridos; pacientes trasladados a otros centros hospitalarios tras una primera valoración en el servicio de urgencias y que no se pueda acceder vía digital a su historia; pacientes atendidos en pediatría; pacientes que no accedan al servicio de urgencias mediante el triaje inicial. Las historias clínicas fueron revisadas por 3 adjuntos y únicamente se incluyeron aquellos casos que cumplían los criterios definidos para los 3 facultativos (las historias excluidas aparecen como pérdidas en la figura 1).
Tamaño muestralSe estimó el tamaño muestral necesario para obtener una mortalidad del 15% en el grupo de alarmas, mientras que en el grupo sin alarmas se esperaba una mortalidad del 25% basándonos en los resultados del estudio de Shapiro et al.9 tras implantar un protocolo de atención de sepsis en urgencias. Además de esta diferencia, se consideró una potencia del 80% y un error alfa del 5% con hipótesis bilateral, obteniendo un tamaño necesario por grupo de 140 pacientes.
Variables analizadasLa variable resultado principal fue exitus al ingreso y en menos de 30 días. Se analizaron variables demográficas (sexo, edad) y variables de comorbilidad (EPOC, cirrosis, cáncer, sida, diabetes, inmunosupresores, quimioterapia, insuficiencia renal, portador de sonda vesical, índice Barthel, índice de Charlson). Variables clínicas: hipotensión —PAS<90mmHg o PAM <70 mmHg—, hopoxemia —PaO2/FiO2<300—, renal: creatinina >2mg/dl; hiperbilirrubinemia: bilirrubina total>4mg/dl. Trombocitopenia: plaquetas<100.000/mm3. Coagulopatía: aPTT>60seg, hiperlactacidemia>4mmol/l. Índice SOFA. Variables microbiológicas: foco, origen epidemiológico, microorganismo en bacteriemias. Variables de proceso: porcentaje de cumplimiento de los Bundles de la SSC, tiempos de actuación, niveles de triaje y tiempo de estancia media (días). Bundles: determinación del ácido láctico en la primera atención; extracción de hemocultivos antes del antibiótico; aplicación del antibiótico en la primera hora; aplicación de volumen (30ml/kg) en la primera hora en los casos de hipotensión o hiperlactacidemia. Tiempos de actuación: a) tiempo entre urgencias y médico (tiempo en minutos desde que el paciente es triado hasta que es valorado por el médico, es decir, excluye tiempo de admisión y tiempo de triaje); b) tiempo entre urgencias y prescripción (tiempo en minutos desde que el paciente es triado hasta que el médico pauta un antibiótico como orden médica); c) tiempo antibiótico entre urgencias y enfermera (tiempo en minutos desde que el paciente es triado hasta que la enfermera le aplica el antibiótico pautado por el médico); d) tiempo antibiótico entre atención médica y prescripción (tiempo de decisión del médico en minutos para pautar el antibiótico, es decir, desde que el médico valora al enfermo cuánto tiempo emplea en decidir la orden médica del antibiótico). Los niveles de prioridad fueron los definidos por el Sistema español de triaje (SET)10.
Análisis estadísticoSe describieron los resultados mediante estadísticos de tendencia central (media) y dispersión (desviación típica) para las variables cuantitativas y porcentajes para las variables cualitativas. Para el análisis bivariante se emplearon los test de la Chi cuadrado para la asociación entre variables cualitativas y la «t» de Student o la U de Mann-Whitney para las cuantitativas (según criterios de normalidad: cuando el test de Kolmogorov-Smirnov era significativo se utilizó el test no paramétrico de la U de Mann-Whitney).
Se obtuvieron curvas de supervivencia para éxitus menor o igual a 30 días con el método de Kaplan-Meier, analizando las diferencias mediante el test de rangos logarítmicos. Finalmente se realizó un análisis multivariante mediante la regresión de Cox (test de Wald) para ajustar por diversas variables de los pacientes y su relación con la presencia de efecto adverso. Las covariables se seleccionaron en función de su disponibilidad y el análisis bivariante previo.
En la aplicación de las pruebas se ha utilizado la hipótesis bilateral, y la significación estadística de la diferencia se consideró a partir de valores p inferiores a 0,05. Los intervalos de confianza incluidos fueron del 95% (IC 95%).
Para el análisis estadístico se utilizó el programa epidemiológio EPIDAT 3.1 y programa SPSS versión 20.0. Por último, se consiguió la aprobación favorable por el Comité ético de investigación clínica de Aragón (CEICA).
ResultadosDurante el periodo de alarmas se atendieron 23.424 urgencias de adultos. Hubo 3.181 ingresos, de los que 198 fueron por SG/SS (6,22%), la alarma de sepsis se activó correctamente en 173 casos (25 falsos negativos), sensibilidad del 87% (IC 95%: 81,93-91,66%). La alarma se activó en 162 ingresos no debidos a SG/SS. La especificidad de la alarma para SG/SS fue 94,56% (IC 95%: 93,64-95,32%), con un valor predictivo positivo de 51,64% (IC 95%: 46,15-57,11%) y negativo de 99,11% (IC 95%: 98,69-99,4%). Por tanto, la muestra en el grupo de alarmas se compuso de 198 casos. En el periodo sin alarmas se atendieron 38.313 urgencias con 5.245 ingresos, donde se codificaron 235 ingresos de SG/SS (4,48%) (fig. 1).
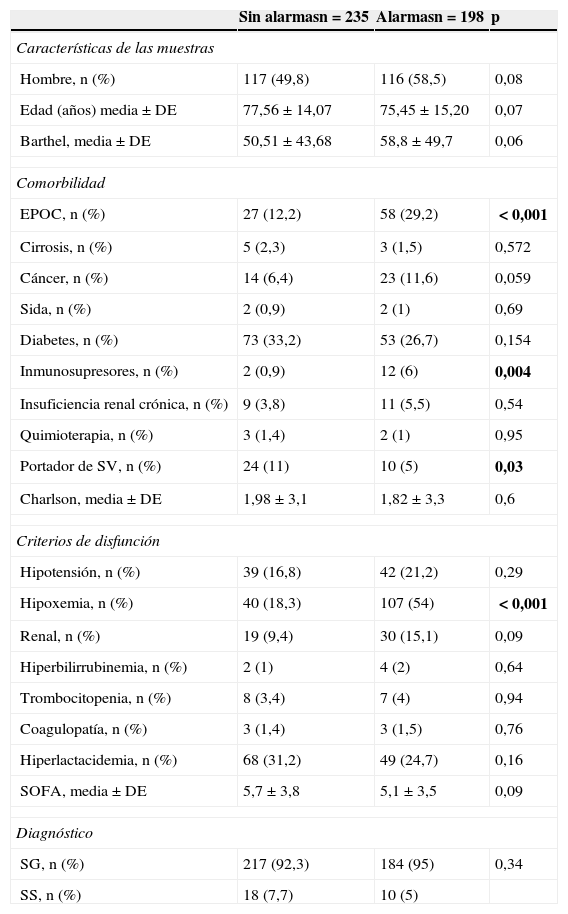
La muestra de alarmas presentó mayor morbilidad en cuanto a EPOC e inmunosupresión frente a la de sin alarmas y mayor Barthel (tabla 1). En la muestra sin alarmas había más casos significativos de portadores de sonda vesical que en la muestra de alarmas. El resto de los factores (quimioterapia, cirrosis, cáncer, insuficiencia renal, sida y diabetes) no arrojaron diferencias estadísticamente significativas.
Comparación entre la muestra de alarmas y sin alarmas
| Sin alarmasn=235 | Alarmasn=198 | p | |
|---|---|---|---|
| Características de las muestras | |||
| Hombre, n (%) | 117 (49,8) | 116 (58,5) | 0,08 |
| Edad (años) media±DE | 77,56±14,07 | 75,45±15,20 | 0,07 |
| Barthel, media±DE | 50,51±43,68 | 58,8±49,7 | 0,06 |
| Comorbilidad | |||
| EPOC, n (%) | 27 (12,2) | 58 (29,2) | <0,001 |
| Cirrosis, n (%) | 5 (2,3) | 3 (1,5) | 0,572 |
| Cáncer, n (%) | 14 (6,4) | 23 (11,6) | 0,059 |
| Sida, n (%) | 2 (0,9) | 2 (1) | 0,69 |
| Diabetes, n (%) | 73 (33,2) | 53 (26,7) | 0,154 |
| Inmunosupresores, n (%) | 2 (0,9) | 12 (6) | 0,004 |
| Insuficiencia renal crónica, n (%) | 9 (3,8) | 11 (5,5) | 0,54 |
| Quimioterapia, n (%) | 3 (1,4) | 2 (1) | 0,95 |
| Portador de SV, n (%) | 24 (11) | 10 (5) | 0,03 |
| Charlson, media±DE | 1,98±3,1 | 1,82±3,3 | 0,6 |
| Criterios de disfunción | |||
| Hipotensión, n (%) | 39 (16,8) | 42 (21,2) | 0,29 |
| Hipoxemia, n (%) | 40 (18,3) | 107 (54) | <0,001 |
| Renal, n (%) | 19 (9,4) | 30 (15,1) | 0,09 |
| Hiperbilirrubinemia, n (%) | 2 (1) | 4 (2) | 0,64 |
| Trombocitopenia, n (%) | 8 (3,4) | 7 (4) | 0,94 |
| Coagulopatía, n (%) | 3 (1,4) | 3 (1,5) | 0,76 |
| Hiperlactacidemia, n (%) | 68 (31,2) | 49 (24,7) | 0,16 |
| SOFA, media±DE | 5,7±3,8 | 5,1±3,5 | 0,09 |
| Diagnóstico | |||
| SG, n (%) | 217 (92,3) | 184 (95) | 0,34 |
| SS, n (%) | 18 (7,7) | 10 (5) | |
En negrita se expresan los datos que alcanzan nivel de significación estadística.
EPOC: enfermedad pulmonar obstructiva crónica; SV: sonda vesical; SOFA: Sequential Organ Failure Assessment, escala de fracaso multiorgánico.
Las 2 muestras presentaron una distribución superponible en cuanto a criterios de disfunción orgánica, a excepción de la hipoxemia (p<0,001) que fue más prevalente en el grupo de alarmas.
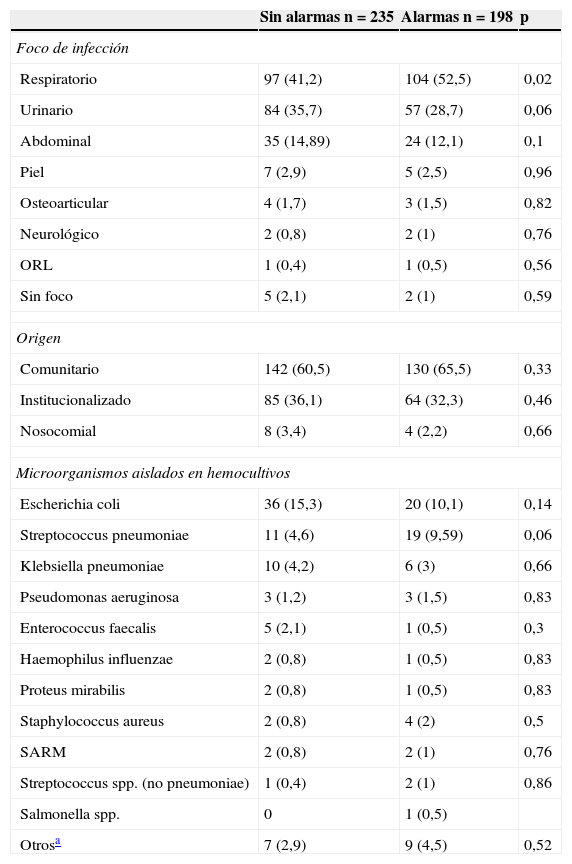
El foco más frecuente es el respiratorio en ambas muestras, con mayor prevalencia en el grupo de alarmas (p=0,02), donde el foco urinario presentó menor frecuencia (p=0,06) (tabla 2). El perfil bacteriológico fue superponible, Escherichia coli fue el microorganismo más frecuentemente aislado en los hemocultivos de ambas muestras (p = 0,14).
Perfil microbiológico
| Sin alarmas n=235 | Alarmas n=198 | p | |
|---|---|---|---|
| Foco de infección | |||
| Respiratorio | 97 (41,2) | 104 (52,5) | 0,02 |
| Urinario | 84 (35,7) | 57 (28,7) | 0,06 |
| Abdominal | 35 (14,89) | 24 (12,1) | 0,1 |
| Piel | 7 (2,9) | 5 (2,5) | 0,96 |
| Osteoarticular | 4 (1,7) | 3 (1,5) | 0,82 |
| Neurológico | 2 (0,8) | 2 (1) | 0,76 |
| ORL | 1 (0,4) | 1 (0,5) | 0,56 |
| Sin foco | 5 (2,1) | 2 (1) | 0,59 |
| Origen | |||
| Comunitario | 142 (60,5) | 130 (65,5) | 0,33 |
| Institucionalizado | 85 (36,1) | 64 (32,3) | 0,46 |
| Nosocomial | 8 (3,4) | 4 (2,2) | 0,66 |
| Microorganismos aislados en hemocultivos | |||
| Escherichia coli | 36 (15,3) | 20 (10,1) | 0,14 |
| Streptococcus pneumoniae | 11 (4,6) | 19 (9,59) | 0,06 |
| Klebsiella pneumoniae | 10 (4,2) | 6 (3) | 0,66 |
| Pseudomonas aeruginosa | 3 (1,2) | 3 (1,5) | 0,83 |
| Enterococcus faecalis | 5 (2,1) | 1 (0,5) | 0,3 |
| Haemophilus influenzae | 2 (0,8) | 1 (0,5) | 0,83 |
| Proteus mirabilis | 2 (0,8) | 1 (0,5) | 0,83 |
| Staphylococcus aureus | 2 (0,8) | 4 (2) | 0,5 |
| SARM | 2 (0,8) | 2 (1) | 0,76 |
| Streptococcus spp. (no pneumoniae) | 1 (0,4) | 2 (1) | 0,86 |
| Salmonella spp. | 0 | 1 (0,5) | |
| Otrosa | 7 (2,9) | 9 (4,5) | 0,52 |
Datos expresados en n (%).
SARM: Staphyllococcus aureus resistente a meticilina.
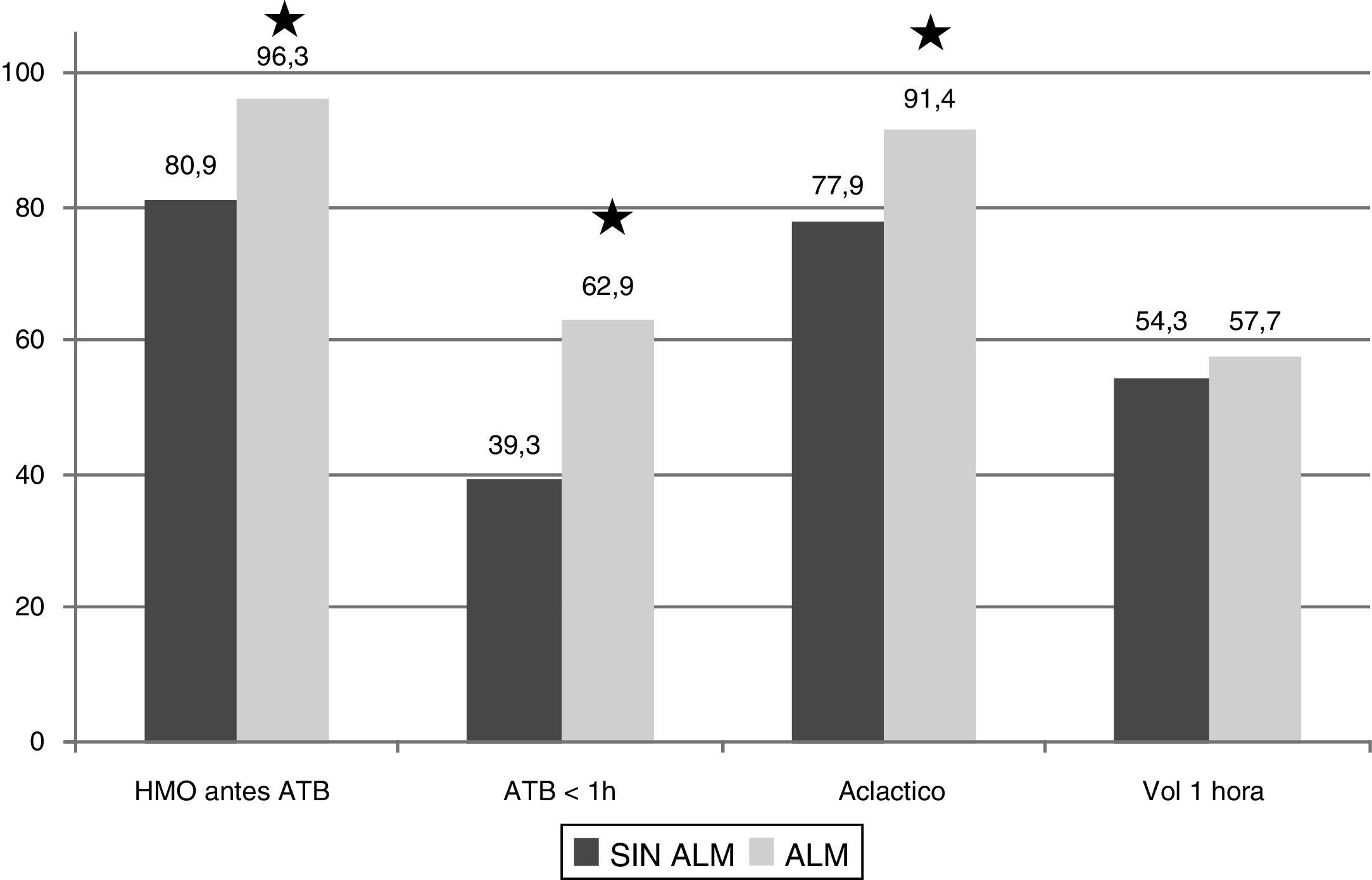
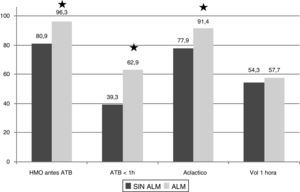
La figura 2 muestra comparativamente el porcentaje de cumplimiento del paquete de las 3 primeras horas, antes y después del sistema de alarmas. El porcentaje de cumplimiento fue mayor en todos los aspectos, tanto en la extracción de hemocultivos, como en la aplicación del antibiótico en la primera hora, la determinación del ácido láctico o en la aplicación de 30ml/kg de volumen en los casos necesarios (hipotensión o hiperlactacidemia). Sin embargo, la significación estadística solo se alcanza en los 3 primeros, siendo el valor de p respectivamente <0,001, <0,001, <0,001 y 0,54.
Diferencias en la aplicación del paquete de tratamiento entre las distintas muestras. Porcentaje de cumplimiento.
Ác. láctico: ácido láctico; ATB: antibioterapia; H: hora; HMO: hemocultivos; Vol: volumen. ★Significación estadística p<0,05. Sin ALM: muestra sin alarmas; ALM: muestra con alarmas.
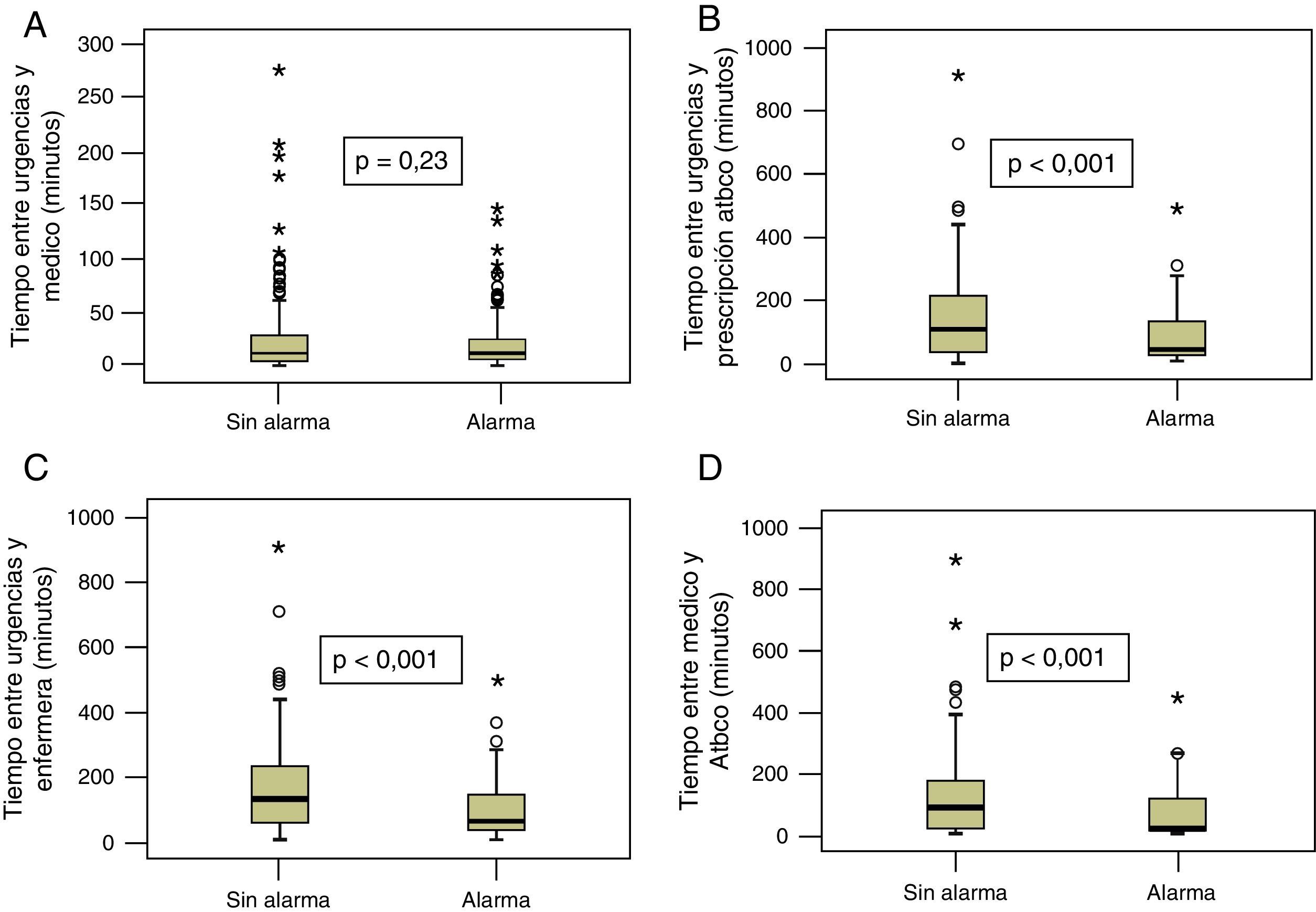
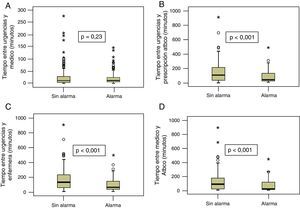
La mediana de tiempo desde el triaje hasta la atención médica (fig. 3A) fue 11min (rango intercuartílico 4-28min) para la muestra sin alarmas. Con alarmas la mediana fue de 10min (rango intercuartílico 3-24min). La mediana de tiempo hasta la prescripción de antibiótico fue 101min (rango intercuartílico 34-208min) sin alarmas y de 39min (rango intercuartílico 22-129min) para la muestra con alarmas (fig. 3B). En el caso del tiempo hasta la atención de enfermería fue sin alarmas mediana 130min (rango intercuartílico 60-231min) y con alarmas mediana 63min (rango intercuartílico 38-146min) (fig. 3C). La mediana de tiempo de decisión de antibiótico fue 84min (rango intercuartílico 16-175min) sin alarmas y 18min (rango intercuartílico 9-113) con alarmas (fig. 3D).
La estancia total incluyendo exitus en el grupo sin alarma fue 12,21±13,78 ([IC 95%] 9,71-23,94) y en el grupo de alarma 10,31±9,45 ([IC 95%] 8,9-11,56) (p=0,09). La estancia hospitalaria excluyendo exitus<30 días fue 13,56±14,77 ([IC 95%] 11,40-15,71) para la muestra sin alarmas y 10,55±10,01 ([IC 95%] 8,89-12,19) para la muestra de alarmas, p=0,01.
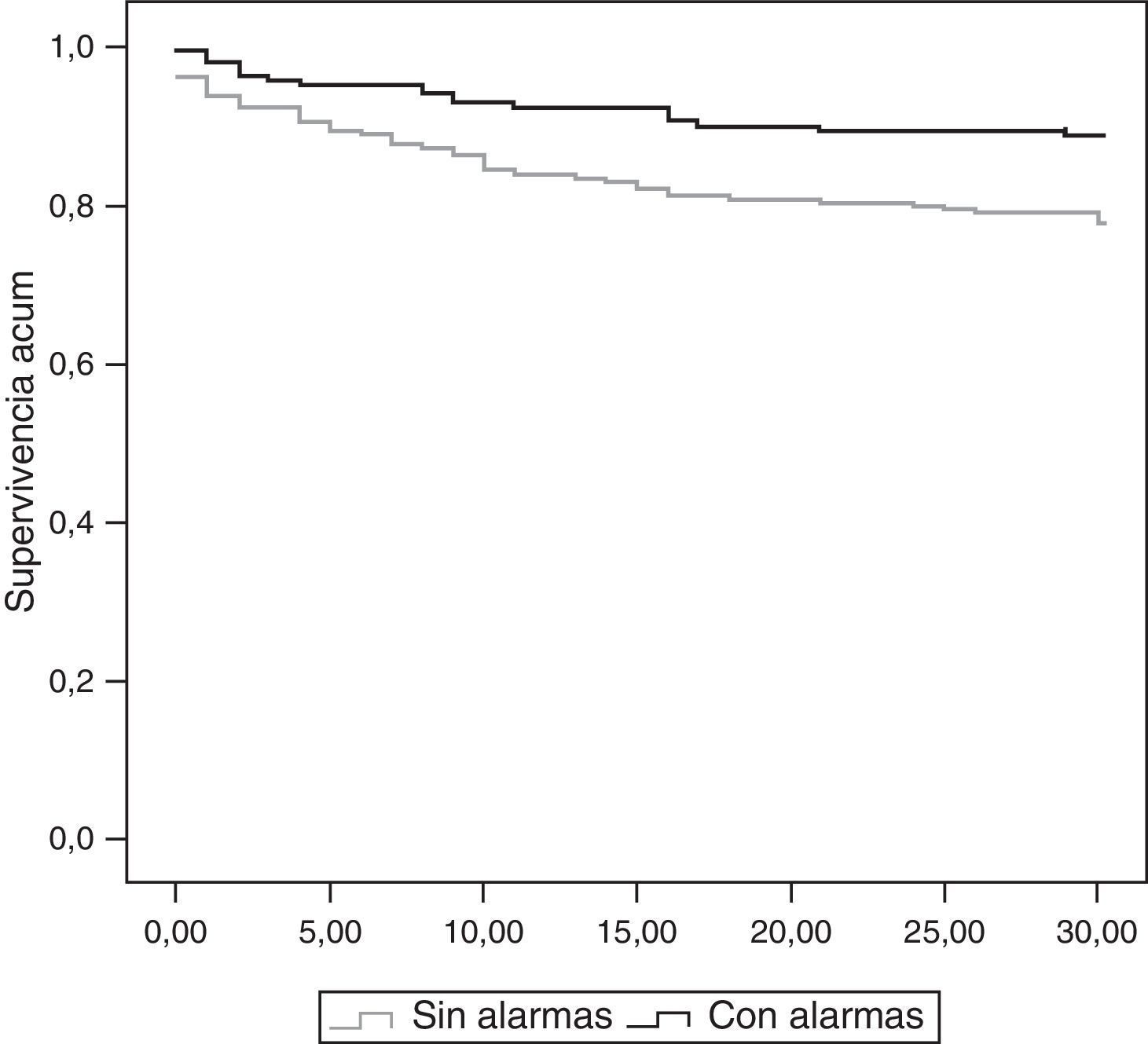
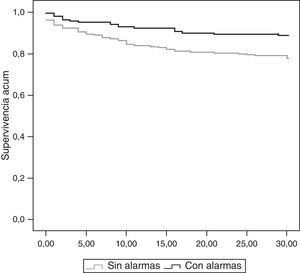
La mortalidad durante el ingreso fue del 25% de la muestra sin alarmas por 13,6% en la muestra con alarmas (p=0,004). La supervivencia a los 30 días fue mayor en la muestra de alarmas (fig. 4), obteniendo un HR 2,028 ([IC 95%] 1,24-3,313) (p=0,005) de mortalidad a los 30 días de la muestra «sin alarmas» frente a «con alarmas». En la muestra con alarmas la activación de una alarma de gravedad determinó un riesgo HR=3,8 ([IC 95%] 1,44-10,07) de mortalidad a los 30 días frente a la de activación de una alerta (p=0,003).
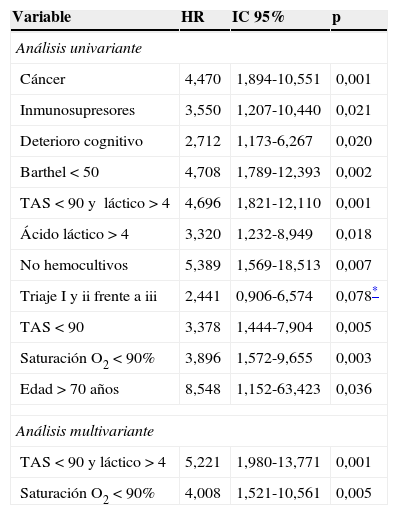
Los factores que influyeron en la mortalidad en el análisis tanto univariante como multivariante se exponen en la tabla 3. Los pacientes que eran portadores de sonda vesical o EPOC no arrojaron diferencias significativas de mortalidad en el análisis univariante.
Resumen de variables significativas
| Variable | HR | IC 95% | p |
|---|---|---|---|
| Análisis univariante | |||
| Cáncer | 4,470 | 1,894-10,551 | 0,001 |
| Inmunosupresores | 3,550 | 1,207-10,440 | 0,021 |
| Deterioro cognitivo | 2,712 | 1,173-6,267 | 0,020 |
| Barthel<50 | 4,708 | 1,789-12,393 | 0,002 |
| TAS<90 y láctico>4 | 4,696 | 1,821-12,110 | 0,001 |
| Ácido láctico>4 | 3,320 | 1,232-8,949 | 0,018 |
| No hemocultivos | 5,389 | 1,569-18,513 | 0,007 |
| Triaje I y ii frente a iii | 2,441 | 0,906-6,574 | 0,078* |
| TAS<90 | 3,378 | 1,444-7,904 | 0,005 |
| Saturación O2<90% | 3,896 | 1,572-9,655 | 0,003 |
| Edad>70 años | 8,548 | 1,152-63,423 | 0,036 |
| Análisis multivariante | |||
| TAS<90 y láctico>4 | 5,221 | 1,980-13,771 | 0,001 |
| Saturación O2<90% | 4,008 | 1,521-10,561 | 0,005 |
No hay estudios, en nuestra búsqueda bibliográfica, que valoren la efectividad de un sistema de alarmas tras su aplicación, pero sí muchos estudios que aportan información en relación con el cumplimiento del paquete de tratamiento propuesto por la SSC11 y que en definitiva se asocia con una reducción de la mortalidad. El mejor cumplimiento de medidas fundamentales, como la extracción de hemocultivo, la aplicación del antibiótico en las 3 primeras horas y la determinación del ácido láctico en la serie de alarmas son los responsables fundamentales de la menor mortalidad de esta serie, en consonancia con los resultados de la SSC, datos que son significativos respecto a la muestra del año previo. De esta forma se obtuvo una reducción de mortalidad en términos absolutos del 11,3% al ingreso y una mayor supervivencia a los 30 días de forma significativa, siendo el NNT de 8.
Comparado con otros estudios como el ABISS Edusepsis (Ferrer et al.12), nuestro estudio obtiene mejores resultados que el ABISS en relación con la determinación de lactato (50%) y la extracción de hemocultivos antes de antibiótico (62%) y resultados similares en la aplicación del antibiótico o volumen. Sin embargo, respecto a la muestra control, Ferrer et al. solo obtienen significación estadística en los 2 primeros. También hay que puntualizar que en el ABISS los datos provienen de la UCI (por tanto sepsis de todo el hospital) y en nuestro estudio se limita a urgencias, de ahí que sus tasas de mortalidad por sepsis grave sean muy superiores a las nuestras.
Aguirre13, en el Hospital del Mar, realiza un estudio con 40 pacientes que proceden de la implantación de un código sepsis y exclusivamente de urgencias. Los datos de cumplimiento del paquete de tratamiento son similares a nuestros resultados. La mortalidad absoluta final que obtuvieron fue del 17%, superior a la nuestra (13,6%). En cuanto a la administración del antibiótico, en el estudio de Aguirre el 90% lo habían recibido en las primeras 2h y el 72,5% en la primera hora, tal y como se recomienda actualmente en el documento de consenso de las Sociedades Españolas de Medicina de Urgencias y Emergencias, y de Medicina Intensiva8. En la serie de Kumar et al.14 el antibiótico era administrado en las primeras 6h en solo un 50% de los casos, y cada hora de retraso se tradujo en un aumento estimado de la mortalidad de un 7,6%, si bien era para shock. Nuestro sistema de alarmas obtuvo 62,9% de casos en la primera hora y 92% en las 3 primeras horas, datos superponibles. Otros autores tienen resultados similares: Nguyen 90,3% en las primeras 4h15, Shapiro 98% en las primeras 6h9 y Gao 74% en la primera hora16.
Por otro lado, la sensibilidad que presenta la herramienta informática es próxima al 90%. Esta elevada sensibilidad conlleva un aumento en la codificación de los casos y por tanto una mayor prevalencia de ingresos por SG/SS en el periodo de alarmas, sin que implique un aumento real de casos. La utilización de herramientas estandarizadas de screening precoz, terapias guiadas por objetivos y bundles de tratamiento conlleva implícita una mayor diligencia de los facultativos en la codificación de los procesos sépticos17. De forma paralela, el sistema de alarmas ha demostrado un valor predictivo positivo igual a 51,64%, lo que lleva implícito un incremento en el número de falsos positivos. En este sentido, destacar en primer lugar que el porcentaje de activación de las alarmas de forma global es bajo (1,43%) en comparación con el número de pacientes atendidos, y en segundo lugar respecto a los ingresos totales los falsos positivos representaron menos del 5% del total de ingresos. Por tanto, no ha supuesto ningún obstáculo en el normal funcionamiento diario del servicio.
De forma adicional, el sistema de alarmas ha conseguido mejorar todos los tiempos; alcanzaron la significación 3 de los 4 tiempos expuestos. Esto es indicativo de que el sistema de alertas agiliza objetivamente la atención de estos pacientes y la aplicación del antibiótico. Este hecho, implica otro factor determinante en la mejoría de los resultados respecto a la muestra histórica.
En el análisis multivariante la hipoperfusión (marcada por la hipotensión y/o la hiperlactacidemia) y la insuficiencia respiratoria son los 2 factores de nuestra serie que asocian mayor mortalidad. El sistema de alarmas facilita de forma automática la detección de la hipotensión y de la desaturación, lo que redunda en una mejor detección de las variables susceptibles de mayor mortalidad.
Apoyándonos en los resultados favorables, se ha logrado una reducción significativa en la estancia media de 2 días de media (excluyendo exitus<30 días). En Aragón el coste hospitalario diario por hospitalización es de 685 euros18, con lo que se estima en 698.000 euros de ahorro anuales solo en términos de hospitalización. Si bien hay que apuntar, que el diseño del estudio no fue evaluar el coste sanitario y el resultado es fruto de una extrapolación a un periodo más largo, por lo que además existen otros costes indirectos que no se han calculado.
Como limitaciones del estudio consideramos que puede haber influido en la reducción de mortalidad global del episodio cambios en la práctica médica habitual durante el ingreso del paciente que no controlamos, y que debido a la progresiva concienciación en nuestro medio de la atención al paciente séptico por las sucesivas jornadas y campañas formativas puede también haber redundado en un beneficio en la atención global. El diseño tampoco ha permitido evaluar las posibles consecuencias del aumento de sensibilidad, como la prescripción inadecuada de antibióticos de amplio espectro, la solicitud de pruebas innecesarias o el retraso en la atención de otras enfermedades no sepsis.
En resumen, este estudio aporta una herramienta innovadora, integrada en el propio sistema informático de urgencias y que se perfila como útil en la reducción de la mortalidad de los pacientes con sepsis. La ausencia de sistemas de detección automática en urgencias implica un riesgo 2,02 veces mayor de muerte a los 30 días que si se dispone de este sistema (p=0,005).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Este trabajo ha recibido financiación procedente de la beca 2013 de la Sociedad de Enfermedades Infecciosas del Norte (SEINORTE).