Durante el período 2001–2005 se llevó a cabo el tercer estudio de resistencia a los fármacos antituberculosos de primera línea en Castilla y León, España, en casos nuevos de tuberculosis (TB).
MétodosSe estudiaron 918 cepas de Mycobacterium tuberculosis procedentes de pacientes virus de la inmunodeficiencia humana negativos correspondientes a 6 hospitales que atienden al 46,7% del total de la población de la comunidad, y se utilizó el método de las proporciones en medio sólido.
ResultadosLa proporción de resistencias (resistencia primaria) fue del 4,2% y la resistencia simple (monorresistencia) fue del 2,6%. El 1,2% fueron resistentes a estreptomicina; el 3,2% a isoniacida (I); el 0,3% a rifampicina (R); el 0,1% a etambutol, y el 0,5% a pirazinamida, y se observó una cepa (0,1%) multirresistente (resistencia a I y a R). No hubo diferencias significativas con los estudios previos.
ConclusionesLa incidencia de resistencia primaria y de multirresistencia en la Comunidad de Castilla y León es baja, asimismo, la resistencia a I es aceptable. Consecuentemente, la pauta de tratamiento de la TB puede incluir solamente a los 3 fármacos (R, I y etambutol). Es conveniente, de acuerdo con los programas de control de la TB, realizar estudios de resistencia a los fármacos antituberculosos para optimizar las pautas de tratamiento.
During 2001–2005, a regional anti-tuberculosis drug resistance survey was conducted in Castilla y León, Spain, in newly treated HIV negative tuberculosis (TB) patients.
MethodsA total of 918 Mycobacterium tuberculosis strains were studied (one strain per patient) from six hospitals corresponding to 46.7% of the total population of Castilla y León, using the proportion method on solid medium.
ResultsPrimary drug resistance was 4.2% (streptomycin 1.2%, isoniazid 3.2%, rifampin 0.3%, ethambutol 0.1% and pyrazinamide 0.5%). Mono-resistance was observed in 24 (2.6%) and resistance to both isoniazid and rifampin (multi-drug resistance) was detected in one case (0.1%). These results were not statistically significant compared to previous studies in the same Community.
ConclusionThe incidence of primary drug resistance in the surveyed area was low, including isoniazid, allowing new anti-tuberculosis treatment with the standardised three-drug regimen to be started. Regular surveillance of drug resistance is recommended by the TB control programme in representative patient populations to optimize treatment regimens.
A pesar de los avances observados en los últimos años con relación a la precocidad en el diagnóstico, la tuberculosis (TB) continúa siendo un importante problema de salud pública con una incidencia a nivel mundial de 9 millones de casos nuevos.
Asimismo, los cambios socioeconómicos, que en algunos casos están agudizándose entre los diferentes países, provocan movimientos migratorios, los que van acompañados de un lastre de enfermedades infecciosas reemergentes que se implantan en los países de acogida. Este panorama se complica si los países de origen contemplan una incidencia alta de TB resistente, multirresistente (MDR) y extremadamente MDR.
España no es ajena a este problema, y se ha declarado según datos oficiales (Red Nacional de Vigilancia Epidemiológica) para 2005 una tasa global de TB de 18,02/100.000 habitantes, aunque la OMS la estima en 27/100.000 habitantes.
De ahí que las autoridades sanitarias españolas hayan propiciado la elaboración de un nuevo documento1 que propone unos «criterios básicos para el control de la TB» y reafirma la conveniencia del conocimiento a nivel nacional de los resultados de las pruebas de sensibilidad a los fármacos antituberculosos.
En Castilla y León y con el objetivo de conocer los niveles de resistencia primaria (RP) entre los casos primarios de TB se propició una serie de estudios de colaboración entre diversos hospitales en los quinquenios 1991–19952 y 1996–20003. Este tercer trabajo de colaboración muestra, asimismo, la proporción de resistencias a los fármacos antituberculosos de Mycobacterium tuberculosis aislados de pacientes, todos ellos casos nuevos, diagnosticados en el período 2001–2005 en la Comunidad de Castilla y León. La similitud en la recogida de datos posibilita conocer la evolución de esta durante 15 años.
Material y métodosEn el presente estudio se contempló disponer de un tamaño muestral representativo del área, en el que cada cepa procedía de un paciente diferente (casos nuevos), y se contó con la colaboración de laboratorios acreditados para la realización de las pruebas de susceptibilidad. No fue necesario disponer de consentimiento para la realización de este estudio ni existió ningún conflicto de intereses.
DefinicionesSe evaluó la resistencia a estreptomicina (S), a isoniacida (I), a rifampicina (R) y a etambutol (E). La RP o resistencia a algún fármaco se define como la que se presenta en cepas de M. tuberculosis procedentes de pacientes sin una historia previa de tratamiento. La monorresistencia es la resistencia a un solo fármaco. Las cepas con MDR son aquellas que presentan al menos resistencia a I y a R.
Centros participantes y recogida de datosEn este estudio de colaboración participaron 6 hospitales de la Comunidad de Castilla y León pertenecientes a la red del Sacyl, los que atendían a una población de 1.177.637 habitantes (el 46,7% del total de la comunidad). El tamaño muestral necesario para calcular la proporción de resistencias de M. tuberculosis con un intervalo de confianza del 95% se estimó en 918 casos, y se asumió una precisión del 1%, una proporción esperada del 4,0% y una población total de 2.200 casos nuevos de TB en el período4. El período de estudio abarcó desde el 1 de enero de 2001 hasta el 31 de diciembre de 2005 (5 años).
Aislamiento e identificación de Mycobacterium tuberculosisSe estudiaron 918 cepas de M. tuberculosis procedentes de diferentes pacientes (virus de la inmunodeficiencia humana negativo) correspondientes a los diagnósticos bacteriológicos realizados en los centros participantes. Cada muestra se procesó de acuerdo con los protocolos propios de cada laboratorio, se utilizó o bien N-acetil L-cisteina-sosa o lauril sulfato sódico, y se procedió a la inoculación de los viales líquidos correspondientes a los sistemas de detección continua (Bact-Alert 3D [Biomerieux®, Francia] o Bactec MGIT960 [Becton Dickinson®, EE. UU.]). Algunos laboratorios inocularon paralelamente el medio sólido de Lowestein-Jensen. Para la identificación se utilizó el kit Accuprobe M. tuberculosis complex culture confirmation (Biomerieux®, Francia). Finalmente, las cepas frescas se remitían al laboratorio de referencia para la realización de las pruebas de susceptibilidad, previa confirmación de la identidad de estas.
Laboratorio de referenciaLas pruebas de susceptibilidad a los fármacos antituberculosos se realizaron en el Laboratorio de Referencia Nacional (Dra. M.S. Jiménez del Instituto de Salud Carlos III de Majadahonda, Madrid), y se utilizó el método convencional de las proporciones5. Se consideró a una cepa como resistente cuando se observó un crecimiento de colonias mayor o igual al 1% a las concentraciones críticas de los fármacos utilizados (4mg/l de S; 0,2mg/l de I; 40mg/l de R; 2mg/l de E, y 200mg/l de pirazinamida) con respecto al crecimiento control.
Análisis estadísticoLos casos de TB con cepas resistentes se estratificaron usando las categorías siguientes: RP, monorresistencia, resistencia a I y MDR por años. No se tuvieron en cuenta para estos cálculos los resultados observados frente a pirazinamida. Las proporciones se compararon con la prueba del chi cuadrado mediante la utilización del sistema Epidat (versión 3.1 para Windows, Xunta de Galicia-OPS/OMS, España). Se calculó, asimismo, el intervalo de confianza del 95% para las proporciones. Un valor de p<0,05 se consideró estadísticamente significativo.
ResultadosSe realizaron pruebas de susceptibilidad a los fármacos antituberculosos a un total de 918 cepas de M. tuberculosis aisladas de pacientes diferentes que no presentaban historia previa de tratamiento. De ellas, 39 (4,2%) fueron resistentes a algún fármaco (RP); 11 a S (1,2%); 30 a I (3,2%); 3 a R (0,3%), y una a E (0,1%). La resistencia simple o la monorresistencia se observó en 24 cepas (2,6%) y en una cepa (0,1%) se observó MDR (tabla 1). De 425 cepas testadas, el 0,5% mostró resistencia a pirazinamida.
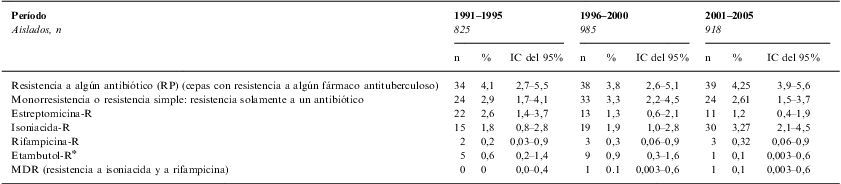
Resistencia primaria de Mycobacterium tuberculosis aislados de pacientes con virus de la inmunodeficiencia humana negativos a los fármacos antituberculosos en 3 períodos en la Comunidad de Castilla y León
| Período | 1991–1995 | 1996–2000 | 2001–2005 | ||||||
| Aislados, n | 825 | 985 | 918 | ||||||
| n | % | IC del 95% | n | % | IC del 95% | n | % | IC del 95% | |
| Resistencia a algún antibiótico (RP) (cepas con resistencia a algún fármaco antituberculoso) | 34 | 4,1 | 2,7–5,5 | 38 | 3,8 | 2,6–5,1 | 39 | 4,25 | 3,9–5,6 |
| Monorresistencia o resistencia simple: resistencia solamente a un antibiótico | 24 | 2,9 | 1,7–4,1 | 33 | 3,3 | 2,2–4,5 | 24 | 2,61 | 1,5–3,7 |
| Estreptomicina-R | 22 | 2,6 | 1,4–3,7 | 13 | 1,3 | 0,6–2,1 | 11 | 1,2 | 0,4–1,9 |
| Isoniacida-R | 15 | 1,8 | 0,8–2,8 | 19 | 1,9 | 1,0–2,8 | 30 | 3,27 | 2,1–4,5 |
| Rifampicina-R | 2 | 0,2 | 0,03–0,9 | 3 | 0,3 | 0,06–0,9 | 3 | 0,32 | 0,06–0,9 |
| Etambutol-R* | 5 | 0,6 | 0,2–1,4 | 9 | 0,9 | 0,3–1,6 | 1 | 0,1 | 0,003–0,6 |
| MDR (resistencia a isoniacida y a rifampicina) | 0 | 0 | 0,0–0,4 | 1 | 0.1 | 0,003–0,6 | 1 | 0,1 | 0,003–0,6 |
IC: intervalo de confianza; MDR: multirresistencia; R: cepas resistentes; RP: resistencia primaria.
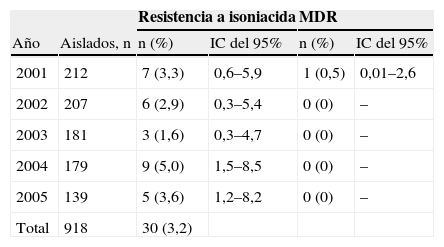
La misma tabla 1 muestra la evolución de la RP durante los 3 períodos de estudio en la Comunidad de Castilla y León. Por otra parte, durante estos 5 años no se ha observado un incremento en la resistencia a I, y no han sido significativas las diferencias observadas (tabla 2). Solamente en el año 2001 se observó una cepa con MDR.
Resistencia de Mycobacterium tuberculosis a isoniacida y multirresistencia en el período de estudio
| Resistencia a isoniacida | MDR | ||||
| Año | Aislados, n | n (%) | IC del 95% | n (%) | IC del 95% |
| 2001 | 212 | 7 (3,3) | 0,6–5,9 | 1 (0,5) | 0,01–2,6 |
| 2002 | 207 | 6 (2,9) | 0,3–5,4 | 0 (0) | – |
| 2003 | 181 | 3 (1,6) | 0,3–4,7 | 0 (0) | – |
| 2004 | 179 | 9 (5,0) | 1,5–8,5 | 0 (0) | – |
| 2005 | 139 | 5 (3,6) | 1,2–8,2 | 0 (0) | – |
| Total | 918 | 30 (3,2) | |||
IC: intervalo de confianza; MDR: multirresistencia.
El plan para la prevención y el control de la tuberculosis en España1 contempla como desafío, entre otros, la «detección de las resistencias a los fármacos antituberculosos». Como se apuntó anteriormente3, el conocimiento periódico de los niveles de resistencia en la Comunidad de Castilla y León facilitó la aplicación de los esquemas terapéuticos más adecuados, y se sumó positivamente a las medidas de lucha adoptadas en esta comunidad; se observó un descenso de la morbilidad, hecho contrastado por las autoridades sanitarias4 en sus estudios de vigilancia. Así, se puede constatar cómo desde la puesta en marcha del Programa de Prevención y Control de la Tuberculosis en la Comunidad de Castilla y León en 1998, la incidencia de casos de TB fue disminuyendo en esta con unas tasas comprendidas entre 18,5–14,42/100.000 habitantes entre los años 2001–2005, respectivamente. Por esto, de los datos expuestos en este trabajo de colaboración, se extrae una RP en esta comunidad que puede considerarse baja (4,25%), y se observa solamente una MDR en todo el quinquenio. Al comparar los 3 períodos, se constata que los datos de RP se mantienen muy similares, sin significación alguna, incluyendo asimismo a aquellos valores observados de resistencia a I (p>0,05). Solamente se observó una diferencia significativa en la resistencia a E entre los períodos 1996–2000 y 2001–2005. En este estudio no se incluyeron los datos correspondientes a los pacientes con enfermedad tuberculosa coinfectados por el virus de la inmunodeficiencia humana. La razón de tal hecho es que el número de pacientes coinfectados ha ido disminuyendo paulatinamente en los últimos años en esta comunidad, y los centros participantes han comunicado solamente 37 casos nuevos.
En España existe un interés por el conocimiento de las RP a M. tuberculosis, y se ponen de relieve en diversas publicaciones nacionales e internacionales que sitúan principalmente los niveles de resistencia a I como condicionantes de la pauta terapéutica inicial. Así, Jiménez, Casal y el Grupo Español de Micobacteriología (GEM) publicaron en 20086 los resultados de una encuesta a nivel nacional en la que se analizaron 965 cepas, de las que el 93,3% procedía de pacientes no tratados previamente. La RP observada fue del 8,3%, casi el doble que en nuestra población de estudio, y fue, asimismo, superior la resistencia en I con el 4,9% de cepas resistentes y con el 1,3% de cepas con MDR.
Al seguir una secuencia cronológica en cuanto al estudio de resistencias antibióticas a M. tuberculosis en períodos similares al del presente estudio, Calpe et al7 sitúan la resistencia a I en el 1,5% y a R en el 0,3% en un estudio sobre 459 cepas aisladas en un período que abarcó de 1987–2001 realizado en el Área 15 de la Comunidad de Valencia. Castilla et al8 en la Comunidad de Navarra y para un período de 14 años (1993–2006) observan una resistencia del 5,4%, aunque también se contabilizaron en este caso aquellos pacientes previamente tratados. En el período 1995–2006, García-Zamalloa y Arrizabalaga9 estudian 584 casos de un área sanitaria de Guipúzcoa, y presentan una resistencia a I del 1,4%, sin observar ninguna MDR. Dorronsoro et al10 para el período 1996–2003 estudian 475 casos en Navarra y publican una resistencia a I del 8% con una MDR del 3%. Ruiz et al11 estudian 158 casos del área de Lorca para el período 1999–2004 y sitúan la resistencia a I en el 5,3%, mientras que Aragó et al12 para el período 1999–2004 en el área de Sagunto y con 77 casos observan una RP del 12,1% y las resistencias a S, a I, a R y a E en el 3, el 3, el 3 y el 4,5%, respectivamente. Superiores son las cifras aportadas por Aznar et al13 en el Área 2 de Madrid que estudian 244 casos durante 5 años (2001–2004) con el 15,2% de cepas resistentes y una resistencia a I del 7,4%. En Castilla y León, Sáez-González et al14 publican una resistencia en el área sanitaria de Salamanca del 8,7% para I y del 8,3% para R con un 4,17% de MDR para el período 1992–2001. En León, Remacha et al15 observan una resistencia global del 6,5 y del 5% a I.
De lo expuesto se observa una variabilidad en los niveles de resistencia a lo largo de la geografía nacional, en ocasiones, derivada de la dificultad del conocimiento de la historia a fármacos de los pacientes, como se apunta en algún trabajo15. Aun al contar con la realidad de estos problemas, se reconoce que la morbilidad de la TB es diferente desde tiempos pasados en las distintas regiones españolas. Por esto es conveniente realizar estudios precisos que permitan situar realmente este problema y planes que propicien y protocolicen un rápido diagnóstico así como una detección precoz de aquellos casos con MDR. En Castilla y León, de acuerdo con las directrices del documento1 y habida cuenta de que la resistencia a I es inferior al 4% de los casos, el tratamiento de la TB en aquellos pacientes que no se han tratado previamente, es decir, casos nuevos, podría basarse en el triple tratamiento inicial (I+R+pirazinamida) durante 2 meses y continuar los 4 meses siguientes con I y R.
En conclusión, los datos de resistencias observadas en Castilla y León son aceptables, con una tendencia a un ligero incremento no significativo de estas, no es necesaria la utilización de un cuarto fármaco y con una incidencia de MDR escasa. Esta situación es la consecuencia de un diagnóstico de la enfermedad lo más precoz posible, de un seguimiento próximo de la evolución de esta y de la colaboración que el mismo paciente ofrece.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
Agradecemos la colaboración prestada en la revisión de los datos estadísticos del Dr. M. González-Sagrado de la Unidad de Investigación del Hospital Universitario Río Hortega de Valladolid.