La azitromicina constituye una alternativa antibiótica en la diarrea bacteriana. Existen pocos datos en España de sensibilidad a azitromicina de enteropatógenos.
MétodosSe determinaron las CMI de azitromicina por E-test en aislados de Salmonella no typhi (SNT), Shigella y Yersinia de los últimos 3años (2010-2012). También se estudió la sensibilidad a los antibióticos habitualmente utilizados en la clínica diarreica mediante un método de microdilución.
ResultadosDe las 139 cepas de SNT, Shigella y Yersinia, 138 tuvieron una CMI≤16mg/l de azitromicina. En adultos, el 14,7 y el 40,6% de las cepas de SNT y Shigella, respectivamente, mostraron resistencia al menos a 2 de los siguientes antibióticos: amoxicilina, cotrimoxazol y ciprofloxacino. En población pediátrica, el 10% de los aislados de SNT y el 28,6% (2/7) de Shigella presentaron resistencia combinada a amoxicilina y cotrimoxazol.
ConclusionesLa azitromicina sería una elección antibiótica útil en el tratamiento de diarrea bacteriana en nuestro medio.
Azithromycin represents an alternative option to treat bacterial diarrhea when the antibiotic therapy is indicated. Little is known regarding the susceptibility to azithromycin in enteropathogens in Spain.
MethodsThe MICs of azithromycin were determined by E-test against Salmonella non-typhi (SNT), Shigella and Yersinia isolates collected over the last three years (2010-2012). In addition, the susceptibility to other antibiotics usually used to treat gastrointestinal diseases was determined in these isolates by using a microdilution method.
ResultsA total of 139 strains of SNT, Shigella and Yersinia were studied. All of them, except one strain, had a MIC≤16mg/L of azithromycin. In the adult population, 14.7% and 40.6% of SNT and Shigella isolates, respectively, were resistant to at least 2 of following antibiotics: amoxicillin, trimethoprim-sulfamethoxazole and ciprofloxacin. In the pediatric population, 10% of SNT clinical isolates and 28.6% (2/7) of Shigella isolates were resistant to amoxicillin and trimethoprim-sulfamethoxazole.
ConclusionsIn our experience, azithromycin would be a useful antibiotic alternative to treat bacterial diarrhea.
La diarrea infecciosa es la segunda causa de morbimortalidad en el mundo, aunque no es así en países desarrollados. El aumento de enteropatógenos resistentes a los antimicrobianos complica la elección del tratamiento antibiótico y requiere la actualización de los patrones de sensibilidad antibiótica.
La gran variabilidad en cuanto a la prevalencia de patógenos específicos según la región geográfica, la edad del paciente y la época estacional hacen necesarias unas guías prácticas que ayuden a manejar la clínica diarreica (rehidratación, datos epidemiológicos, tratamiento antibiótico si procede…). En estas guías la azitromicina constituye una alternativa antibiótica en aquellos casos en los que la administración de un antimicrobiano está indicada, pudiendo ser especialmente útil en niños, en los que las quinolonas no se aconsejan y donde pautas más cortas de tratamiento aseguran un mejor cumplimiento, o en situaciones en las que la bacteria aislada sea resistente a antibióticos de primera elección.
Las guías IDSA de 2001 mencionan la azitromicina como tratamiento de shigelosis en pacientes inmunocompetentes1. En una revisión reciente de DuPont2, la azitromicina es un tratamiento de elección de la salmonelosis no tifoidea y de la shigelosis en niños, mientras que en adultos aparece como una alternativa a fluoroquinolonas y ceftriaxona en diarrea causada por Shigella y Salmonella no typhi (SNT).
Debido a la escasez de datos en España sobre la sensibilidad a la azitromicina en enteropatógenos, el objetivo de nuestro estudio es evaluar la actividad in vitro de este antibiótico en aislados recientes de SNT, Shigella y Yersinia, además de actualizar la información de resistencias a antibióticos de primera línea en los microorganismos mencionados.
Material y métodosHemos llevado a cabo un estudio de las concentraciones mínimas inhibitorias (CMI) de azitromicina en un conjunto elegido al azar de enteropatógenos aislados de diferentes pacientes en los últimos 3años (2010-2012) en el área de influencia del Hospital Universitario de Getafe. Se incluyen 39 aislados del género Shigella, 64 del género Salmonella distintos de Salmonella typhi y 36 de Yersinia enterocolitica. Se utilizó agar Mueller-Hinton (bioMérieux S.A.) y tiras de E-test de azitromicina (bioMérieux S.A.). El inóculo bacteriano se ajustó al 0,5 de McFarland.
También aportamos la sensibilidad de nuestras cepas a amoxicilina, cefotaxima, cotrimoxazol, ácido nalidíxico y ciprofloxacino obtenida durante el proceso habitual de laboratorio mediante un método de microdilución (Wider, Francisco Soria Melguizo S.A.). Los resultados se interpretaron según los criterios clínicos de EUCAST del año 20133 y las reglas expertas, excepto en el caso de azitromicina, que se usó el punto de corte epidemiológico (CMI≤16mg/l) para Salmonella y Shigella.
Para analizar los datos de sensibilidad se clasifica a los sujetos en población adulta, n=79 (56,83%) y pediátrica (≤14años), n=60 (43,16%).
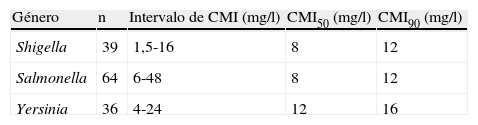
ResultadosLos valores de CMI de azitromicina en los 3 géneros bacterianos causantes de diarrea se resumen en la tabla 1.
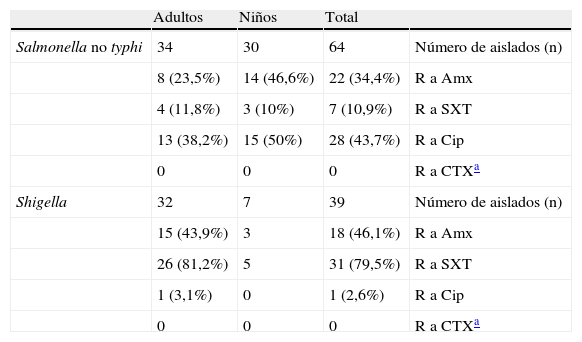
En la tabla 2 se muestran los resultados conseguidos al evaluar en SNT y Shigella la actividad antimicrobiana de otros antibióticos probados. El 43,7% de las cepas de Salmonella fueron resistentes a ácido nalidíxico (CMI>16mg/l) y tuvieron CMI de ciprofloxacino >0,12mg/l. En población pediátrica, 3 aislados de 30 (10%) presentaron resistencia combinada a amoxicilina y cotrimoxazol en SNT. Por el contrario, 5 aislados de los 34 (14,7%) de adultos fueron resistentes al menos a 2 de los siguientes antibióticos: amoxicilina, cotrimoxazol y ciprofloxacino.
Porcentajes de resistencia a antibióticos de primera línea en aislados de SNT y Shigella
| Adultos | Niños | Total | ||
| Salmonella no typhi | 34 | 30 | 64 | Número de aislados (n) |
| 8 (23,5%) | 14 (46,6%) | 22 (34,4%) | R a Amx | |
| 4 (11,8%) | 3 (10%) | 7 (10,9%) | R a SXT | |
| 13 (38,2%) | 15 (50%) | 28 (43,7%) | R a Cip | |
| 0 | 0 | 0 | R a CTXa | |
| Shigella | 32 | 7 | 39 | Número de aislados (n) |
| 15 (43,9%) | 3 | 18 (46,1%) | R a Amx | |
| 26 (81,2%) | 5 | 31 (79,5%) | R a SXT | |
| 1 (3,1%) | 0 | 1 (2,6%) | R a Cip | |
| 0 | 0 | 0 | R a CTXa |
Amx: amoxicilina; Cip: ciprofloxacino; CTX: cefotaxima; R: resistencia; SXT: cotrimoxazol.
En Shigella, de los 7 aislados de niños, solo 2 (28,6%) mostraron resistencia simultánea a amoxicilina y cotrimoxazol. En el caso de los adultos, el 40,6% presentaban resistencia combinada a 2 o más antibióticos.
Nuestros resultados con Yersinia enterocolitica son bien diferentes a los expuestos anteriormente con las otras especies; la mayoría de los aislados (63,8%) se obtuvieron de heces en niños, frente al 36,11% en adultos. Todos mostraron sensibilidad a ciprofloxacino y cotrimoxazol. Sin embargo, no se obtuvo ningún aislado sensible a amoxicilina, debido a que todas las cepas pertenecían al serotipo O:3, el cual produce una β-lactamasa cromosómica que hidroliza ampicilina y cefalosporinas de primera y segunda generación.
DiscusiónEn el laboratorio de nuestro servicio de Microbiología, cuando se identifica un enteropatógeno causante de diarrea se suele realizar un antibiograma. Muchos de los sistemas comerciales no incluyen azitromicina entre los antibióticos a probar. Por esta razón, nuestro objetivo fue evaluar si los aislados recientes de SNT, Shigella y Yersinia tienen CMI de este antibiótico propias de los fenotipos sin mecanismos de resistencia, condición previa indispensable para que la azitromicina suponga una alternativa en la terapéutica de la diarrea bacteriana.
En la actualidad, ninguno de los más importantes comités del antibiograma (CLSI y EUCAST) ha propuesto puntos de corte clínicos que permitan interpretar los valores de CMI de azitromicina en especies de Salmonella, Shigella y Yersinia. Tan solo EUCAST hace referencia a un punto de corte epidemiológico (CMI≤16mg/l) en aislados de Salmonella typhi3. En el caso de Shigella existen trabajos recientes en los que se hace referencia al mismo punto de corte epidemiológico4.
Según nuestra experiencia, el 98,5% de las cepas de SNT y el 100% de las de Shigella tenían CMI de azitromicina ≤16mg/l, lo que supone que la azitromicina podría ser una elección antibiótica útil.
Estudios realizados en SNT frente a azitromicina en varios países europeos concluyen que la gran mayoría de los aislados presentan valores de CMI comprendidos entre 4 y 8mg/l5,6. También hay que mencionar un brote de Shigella que tuvo lugar en Los Ángeles (California) en el año 2012, donde el 32,5% de los aislados ensayados mostraron sensibilidad disminuida a la azitromicina (CMI>16mg/l) como consecuencia de la expresión de un gen de localización plasmídica, mphA, responsable de la resistencia a macrólidos7. En nuestra experiencia, una única cepa de SNT presentó una CMI=48mg/l.
En cuanto al resto de antibióticos frente a estos enteropatógenos, trabajos realizados en España mostraron un 35% de resistencia a ácido nalidíxico en aislados de SNT en los primeros años del sigloxxi8, que podría ser equiparable a nuestros resultados (43,7%). En Europa se ha estado observando un aumento de la resistencia a este antibiótico en Salmonella, que ha pasado entre los años 2000-2004 del 14 al 20%, según la Red de Vigilancia Enter-net International9. Otros trabajos llevados a cabo en España pocos años después demuestran un porcentaje de resistencia a amoxicilina (35%) y cotrimoxazol (6,6%) en SNT muy similar a los obtenidos en nuestro estudio10.
Como conclusión final, 137 de las 139 cepas de Salmonella, Shigella y Yersinia de nuestro trabajo presentaron una CMI≤16mg/l de azitromicina, por lo que podría usarse como tratamiento de elección o alternativo con la ventaja de poder pautarla como dosis única al día, favoreciendo la adherencia al tratamiento del paciente. Por ello, su incorporación a sistemas comerciales para el estudio de sensibilidad antibiótica de enteropatógenos resultaría muy útil.
En un futuro próximo resultaría interesante recoger los datos obtenidos en otros centros de España para actualizar los resultados referentes a la azitromicina y a la resistencia antimicrobiana a otros fármacos de primera línea.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.