El cidofovir es un antiviral que inhibe la ADN-polimerasa de diferentes virus. Ha sido utilizado en infecciones originadas por el virus del papiloma humano.
MétodosEstudio retrospectivo descriptivo en el que se incluyó a pacientes con verrugas anogenitales resistentes a terapias convencionales sobre las que se aplicó cidofovir crema.
ResultadosSe trataron 9 pacientes inmunocompetentes, con respuesta completa en 6 y parcial en 3.
ConclusiónEl cidofovir podría ser una alternativa útil, aunque se precisan más estudios que establezcan su mejor posología y su coste-eficacia.
Cidofovir is an antiviral agent which inhibits the DNA polymerase of different viruses. Its use has been described for papillomavirus infections.
MethodsDescriptive retrospective study, including patients with difficult to treat anogenital warts who were treated with cidofovir cream.
ResultsNine immunocompetent patients were treated, where 6 of them had a complete response and 3 of them a partial response.
ConclusionCidofovir cream could be a useful therapeutic alternative, although further studies are required to establish the best dosage and its cost-effectiveness.
La infección por el virus del papiloma humano (VPH) es la infección de transmisión sexual (ITS) más frecuente1. Respecto al tratamiento de las verrugas anogenitales (VAG), se han empleado diferentes modalidades terapéuticas; entre ellas, tratamientos ablativos (crioterapia, láser, electrocoagulación o ácido tricloroacético), otros que actúan interrumpiendo la división celular (podofilotoxina tópica, interferón y 5-fluorouracilo intralesionales), o bien modificando la respuesta inmune como el imiquimod tópico2, aunque muchos pacientes no responden a estos tratamientos.
El cidofovir es un potente antiviral análogo citidínico aprobado para el tratamiento de retinitis causada por citomegalovirus en pacientes infectados por el virus de la inmunodeficiencia humana (VIH) y se ha utilizado recientemente en el tratamiento de infecciones causadas por VPH, incluyendo algunos casos de VAG2-10. El objetivo de nuestro estudio fue evaluar la eficacia y la seguridad del cidofovir tópico para el tratamiento de VAG.
MétodosSe realizó un estudio retrospectivo descriptivo en el que entre julio de 2008 y julio de 2011 se incluyó a pacientes adultos y niños con VAG de difícil tratamiento por el número de lesiones, por su localización o por su resistencia a otras terapias convencionales.
Tras ser aprobado en nuestro hospital su uso fuera de ficha técnica (y firmando el paciente un consentimiento informado), se prescribió la aplicación de cidofovir 1 o 3% en crema sin oclusión sobre las verrugas una o 2 veces al día.
En la evaluación de la eficacia al tratamiento se consideró respuesta completa a la desaparición total de las verrugas, respuesta parcial a la disminución en el número y/o tamaño de las mismas, y como sin respuesta cuando no existió disminución en el número y/o tamaño de estas en la revisión efectuada un mes después. En caso de respuesta parcial, se ofreció al paciente (si toleraba bien la irritación originada) continuar aplicando la crema hasta un máximo de 12 semanas. Se consideró recurrencia de las lesiones a la detección clínica de nuevas VAG durante el seguimiento. Además se anotó cualquier tipo de reacción adversa.
ResultadosSe trataron 9 pacientes con edades comprendidas entre 5 y 36 años, 5 de ellos varones (tabla 1). Todos eran inmunocompetentes. Dos eran diabéticos y otro presentaba infección por virus de la hepatitis C. Ninguno estaba infectado por el VIH. Cinco (todos adultos) habían sido diagnosticados de otras ITS. De los varones, 2 presentaban verrugas únicamente en el pene, otro en el pene y en la región perianal, otro en el área inguinoescrotal, y otro únicamente perianales. De las mujeres, una presentaba lesiones únicamente en la vulva, otra en la vulva y en la región perianal, y otras 2 solo perianales. Todos los pacientes habían sido previamente tratados con al menos 2 terapias convencionales (aunque sin respuesta satisfactoria). Ocho habían recibido tratamiento con imiquimod tópico, 6 con crioterapia, 4 con podofilotoxina tópica y 4 mediante electrocuretaje. La pauta de tratamiento osciló entre 3 y 7 días a la semana durante 1-12 semanas, realizándose un seguimiento mínimo de 2 meses.
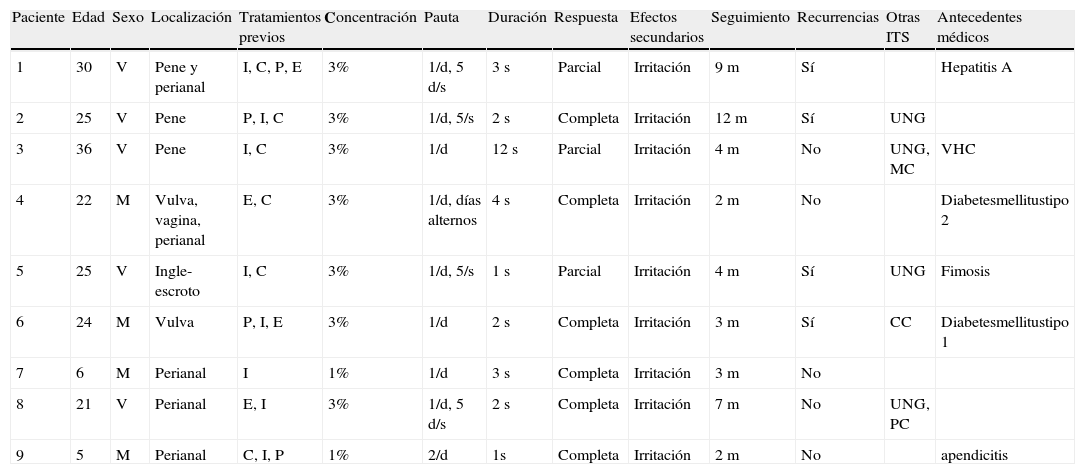
Casos tratados con cidofovir en este estudio
| Paciente | Edad | Sexo | Localización | Tratamientos previos | Concentración | Pauta | Duración | Respuesta | Efectos secundarios | Seguimiento | Recurrencias | Otras ITS | Antecedentes médicos |
| 1 | 30 | V | Pene y perianal | I, C, P, E | 3% | 1/d, 5d/s | 3 s | Parcial | Irritación | 9m | Sí | Hepatitis A | |
| 2 | 25 | V | Pene | P, I, C | 3% | 1/d, 5/s | 2 s | Completa | Irritación | 12m | Sí | UNG | |
| 3 | 36 | V | Pene | I, C | 3% | 1/d | 12 s | Parcial | Irritación | 4m | No | UNG, MC | VHC |
| 4 | 22 | M | Vulva, vagina, perianal | E, C | 3% | 1/d, días alternos | 4 s | Completa | Irritación | 2m | No | Diabetesmellitustipo 2 | |
| 5 | 25 | V | Ingle-escroto | I, C | 3% | 1/d, 5/s | 1 s | Parcial | Irritación | 4m | Sí | UNG | Fimosis |
| 6 | 24 | M | Vulva | P, I, E | 3% | 1/d | 2 s | Completa | Irritación | 3m | Sí | CC | Diabetesmellitustipo 1 |
| 7 | 6 | M | Perianal | I | 1% | 1/d | 3 s | Completa | Irritación | 3m | No | ||
| 8 | 21 | V | Perianal | E, I | 3% | 1/d, 5d/s | 2 s | Completa | Irritación | 7m | No | UNG, PC | |
| 9 | 5 | M | Perianal | C, I, P | 1% | 2/d | 1s | Completa | Irritación | 2m | No | apendicitis |
C: crioterapia; CC: cervicitis por clamidia; d: días; E: electrocuretaje; I: imiquimod crema; ITS: infección de transmisión sexual; m: meses; MC: molluscum contagiosum; P: podofilotoxina crema; PC: proctitis por clamidia; s: semanas; UNG: uretritis no gonocócica.
Todos los pacientes obtuvieron respuesta al tratamiento, que fue completa en 6 pacientes y parcial en los 3 restantes. De los que obtuvieron respuesta completa, solo 2 presentaron recurrencias, siendo en uno de estos casos finalmente resueltas mediante electrocuretaje y en el otro mediante podofilotoxina crema. Los pacientes que obtuvieron respuesta parcial finalmente abandonaron el tratamiento por la irritación asociada, siendo las lesiones residuales tratadas y finalmente resueltas combinando crioterapia e imiquimod crema en un caso, en otro caso mediante la aplicación de crioterapia y el último con el uso de podofilotoxina crema. El único efecto adverso fue la aparición de irritación local (en todos los pacientes), que tras la retirada del tratamiento se resolvió sin secuelas.
DiscusiónLos tratamientos para las VAG no están exentos de efectos secundarios y de una alta tasa de recurrencia3. Tienen como objetivo eliminar las lesiones causadas por el VPH, aunque no reducen la carga viral2,4. El cidofovir actúa inhibiendo de forma competitiva la ADN-polimerasa de diferentes virus (VPH, poxvirus, herpesvirus y adenovirus)3,7,9,10. Se ha empleado para el tratamiento de VAG tanto en adultos2-6,8-10 como en niños3,7. En la literatura se han descrito aproximadamente 90 pacientes con VAG tratados con cidofovir de forma tópica2-4,6-10 o intralesional5. La mayoría son casos aislados, aunque existen algunas series de casos a nivel internacional, y la más amplia es la publicada por Coremans et al.4, con 27 pacientes. En España solo se ha descrito un caso en un paciente inmunodeprimido6. El efecto adverso descrito con mayor frecuencia en el uso tópico del cidofovir es la irritación local8, tal y como ocurrió en nuestros casos, aunque se publicó un caso aislado de nefrotoxicidad en un trasplantado renal, tras la aplicación tópica de cidofovir probablemente en relación con su insuficiencia renal previa, su aplicación al 4%, el propilenglicol como excipiente y la excoriación del área tratada, incrementando su absorción10.
Debido a la ausencia de ensayos clínicos de doble ciego controlado, no existe consenso respecto a la concentración más oportuna a usar del producto (1-3% generalmente), su esquema de aplicación (1-2 veces al día, con o sin oclusión) y la duración óptima de este tratamiento, por lo que son precisos más estudios para poder definirlos. Incluso se ha descrito la utilidad de la aplicación del producto de forma intermitente (aunque sin definir la duración), considerándose por sus autores como la más eficaz, propugnando estos que antes de lograr una resolución completa de las VAG, la regresión continúa después de la interrupción del tratamiento; de esta forma se evitaría prolongar la duración y, por tanto, el desarrollo de erosiones y úlceras9. Algunos autores defienden que con cidofovir 1-3% 2 veces al día se obtenían mejores resultados en lesiones cutáneas, mientras que su aplicación una vez al día podría ser más oportuna para áreas más delicadas como labios, encías y genitales8. El único caso pediátrico descrito en la literatura7 (aparte de los nuestros3) fue tratado con cidofovir 1% con resolución completa, razón por la cual se decidió en nuestros pacientes pediátricos el uso a esta misma concentración.
La principal limitación de este tratamiento es su elevado coste. Aunque no hemos realizado la evaluación de los costes, se calcula que en nuestro medio 10g de crema, que deberían ser suficientes para el tratamiento de varias verrugas durante un mes, equivalen a unos 300euros.
Nuestro estudio muestra una buena respuesta al tratamiento con cidofovir tópico tanto al 1 como al 3%, y la irritación es aparentemente similar en todos los casos. Igualmente, se obtuvo buena respuesta mediante la aplicación de la crema tanto una vez como 2 veces al día. La crema fue aplicada a diario en 4 casos (3 con respuesta completa, una respuesta parcial), en otros 4 casos 5días/semana (2 con respuesta completa, 2 con respuesta parcial), y en un caso, a días alternos, con respuesta completa, por lo que aparentemente no pareció haber diferencias evidentes entre estas en la respuesta al tratamiento. Además, respecto a la duración del tratamiento, la máxima fue de 12 semanas, en un caso en que además solo se obtuvo respuesta parcial, si bien en el resto de casos este no se aplicó por más de 4 semanas.
Por tanto, teniendo en cuenta nuestros resultados y los de los estudios existentes (tabla 2), parece evidente que el cidofovir tópico podría ser una alternativa terapéutica útil por su eficacia y seguridad en el manejo de pacientes tanto inmunocompetentes como inmunodeprimidos con VAG persistentes, resistentes a otras terapias convencionales o de difícil tratamiento por su localización y/o número, y podríamos concluir que aunque estas diferentes concentraciones (1 y 3%) y posologías (aplicación 1 o 2 veces al día, a diario, 5 veces/semana o incluso a días alternos) podrían ser válidas, por razones económicas podría plantearse comenzar el tratamiento con una concentración del 1% aplicada una sola vez al día, 5 días a la semana, por un máximo de 6 semanas seguidas, si bien se precisan más estudios que confirmen su utilidad, su estabilidad y que definan mejor su posología y su coste-eficacia. Por último, recordar que es fundamental la firma de un consentimiento informado por el paciente y la aprobación de su uso por la comisión de Farmacia del hospital, al tratarse de una indicación fuera de ficha técnica y con escasos estudios disponibles hasta el momento.
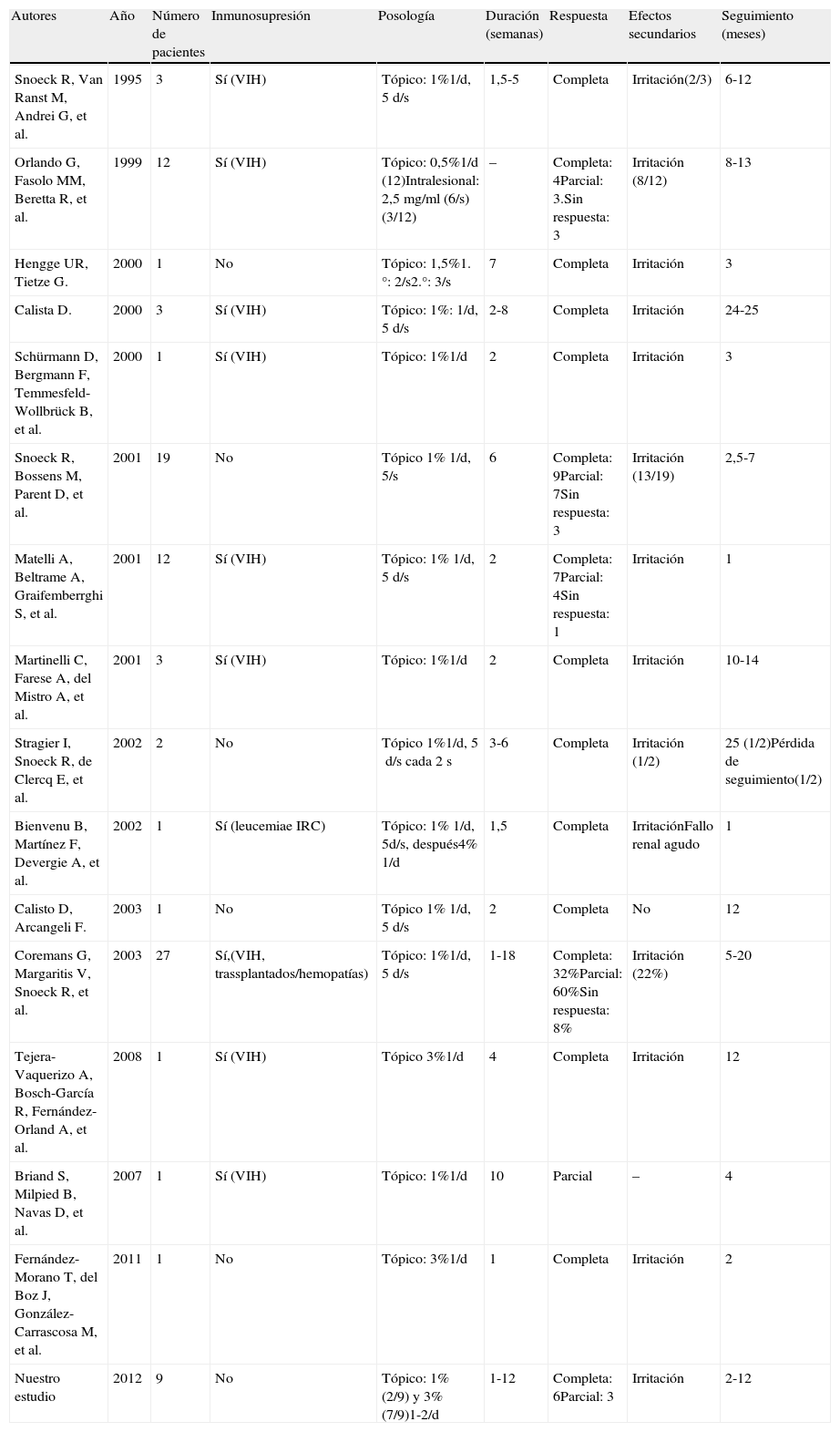
Estudios publicados para el tratamiento de verrugas anogenitales con cidofovir
| Autores | Año | Número de pacientes | Inmunosupresión | Posología | Duración (semanas) | Respuesta | Efectos secundarios | Seguimiento (meses) |
| Snoeck R, Van Ranst M, Andrei G, et al. | 1995 | 3 | Sí (VIH) | Tópico: 1%1/d, 5d/s | 1,5-5 | Completa | Irritación(2/3) | 6-12 |
| Orlando G, Fasolo MM, Beretta R, et al. | 1999 | 12 | Sí (VIH) | Tópico: 0,5%1/d (12)Intralesional: 2,5mg/ml (6/s) (3/12) | – | Completa: 4Parcial: 3.Sin respuesta: 3 | Irritación (8/12) | 8-13 |
| Hengge UR, Tietze G. | 2000 | 1 | No | Tópico: 1,5%1.°: 2/s2.°: 3/s | 7 | Completa | Irritación | 3 |
| Calista D. | 2000 | 3 | Sí (VIH) | Tópico: 1%: 1/d, 5d/s | 2-8 | Completa | Irritación | 24-25 |
| Schürmann D, Bergmann F, Temmesfeld-Wollbrück B, et al. | 2000 | 1 | Sí (VIH) | Tópico: 1%1/d | 2 | Completa | Irritación | 3 |
| Snoeck R, Bossens M, Parent D, et al. | 2001 | 19 | No | Tópico 1% 1/d, 5/s | 6 | Completa: 9Parcial: 7Sin respuesta: 3 | Irritación (13/19) | 2,5-7 |
| Matelli A, Beltrame A, Graifemberrghi S, et al. | 2001 | 12 | Sí (VIH) | Tópico: 1% 1/d, 5d/s | 2 | Completa: 7Parcial: 4Sin respuesta: 1 | Irritación | 1 |
| Martinelli C, Farese A, del Mistro A, et al. | 2001 | 3 | Sí (VIH) | Tópico: 1%1/d | 2 | Completa | Irritación | 10-14 |
| Stragier I, Snoeck R, de Clercq E, et al. | 2002 | 2 | No | Tópico 1%1/d, 5d/s cada 2 s | 3-6 | Completa | Irritación (1/2) | 25 (1/2)Pérdida de seguimiento(1/2) |
| Bienvenu B, Martínez F, Devergie A, et al. | 2002 | 1 | Sí (leucemiae IRC) | Tópico: 1% 1/d, 5d/s, después4% 1/d | 1,5 | Completa | IrritaciónFallo renal agudo | 1 |
| Calisto D, Arcangeli F. | 2003 | 1 | No | Tópico 1% 1/d, 5d/s | 2 | Completa | No | 12 |
| Coremans G, Margaritis V, Snoeck R, et al. | 2003 | 27 | Sí,(VIH, trassplantados/hemopatías) | Tópico: 1%1/d, 5d/s | 1-18 | Completa: 32%Parcial: 60%Sin respuesta: 8% | Irritación (22%) | 5-20 |
| Tejera-Vaquerizo A, Bosch-García R, Fernández-Orland A, et al. | 2008 | 1 | Sí (VIH) | Tópico 3%1/d | 4 | Completa | Irritación | 12 |
| Briand S, Milpied B, Navas D, et al. | 2007 | 1 | Sí (VIH) | Tópico: 1%1/d | 10 | Parcial | – | 4 |
| Fernández- Morano T, del Boz J, González- Carrascosa M, et al. | 2011 | 1 | No | Tópico: 3%1/d | 1 | Completa | Irritación | 2 |
| Nuestro estudio | 2012 | 9 | No | Tópico: 1% (2/9) y 3% (7/9)1-2/d | 1-12 | Completa: 6Parcial: 3 | Irritación | 2-12 |
d: días; IRC: insuficiencia renal crónica; s: semanas.
Los autores declaran no tener ningún conflicto de intereses.