La gastroenteritis infecciosa continúa siendo un problema de salud pública. La etiología bacteriana es la responsable de la mayoría de los casos graves. En nuestro país, Campylobacter y Salmonella son los géneros bacterianos más prevalentes, mientras que Yersinia y Shigella son mucho menos frecuentes. La mayoría de los casos suelen ser autolimitados y, en general, el tratamiento antibiótico no está indicado, salvo en pacientes con factores de riesgo de infección grave y en shigelosis. Ciprofloxacino, cefalosporinas de tercera generación, azitromicina, ampicilina, cotrimoxazol y doxiciclina son los fármacos más recomendados. El patrón de sensibilidad de las diferentes bacterias determina la elección del tratamiento antibiótico más adecuado. El objetivo de esta revisión es analizar la situación, las novedades y la evolución de la resistencia y la multirresistencia en estos 4 enteropatógenos.
Infectious gastroenteritis remains a public health problem. The most severe cases are of bacterial origin. In Spain, Campylobacter and Salmonella are the most prevalent bacterial genus, while Yersinia and Shigella are much less frequent. Most cases are usually self-limiting and antibiotic therapy is not generally indicated, unless patients have risk factors for severe infection and shigellosis. Ciprofloxacin, third generation cephalosporins, azithromycin, ampicillin, cotrimoxazole and doxycycline are the most recommended drugs. The susceptibility pattern of the different bacteria determines the choice of the most appropriate treatment. The aim of this review is to analyse the current situation, developments, and evolution of resistance and multidrug resistance in these 4 enteric pathogens.
La gastroenteritis infecciosa continúa siendo un problema de salud pública. La etiología bacteriana, menos prevalente que la vírica, es responsable de la mayoría de los episodios graves1.
El tratamiento antibiótico de la diarrea infecciosa de etiología conocida, así como su tratamiento empírico, deben considerarse en casos concretos con el fin de acortar la duración de la enfermedad, disminuir la transmisión y prevenir la aparición de complicaciones1. Por ello resulta fundamental el conocimiento de los patógenos más habituales, así como su perfil de sensibilidad antibiótica.
En nuestro medio, Campylobacter y Salmonella son los agentes etiológicos más frecuentes, seguidos de lejos por Yersinia y Shigella2, razón por la cual nos centraremos en el presente trabajo en las últimas novedades en antibióticos relacionadas con estos patógenos.
Salmonella enterica no typhiLos cuadros de gastroenteritis por Salmonella enterica no typhi (SNT) son habitualmente leves y autolimitados; el uso de antibióticos no está recomendado e incluso puede prolongar el estado de portador1,3. Sin embargo, en pacientes con factores de riesgo de bacteriemia, diarrea grave o signos de infección sistémica, el tratamiento de elección incluye una fluoroquinolona oral o azitromicina para casos de enteritis, y cefalosporinas de tercera generación, aztreonam o ciprofloxacino en bacteriemia o infección localizada4.
Los serotipos Enteritidis y Typhimurium suponen más del 80% de los aislados obtenidos en la práctica clínica2. A nivel mundial y en España, el serotipo Enteritidis ha sido el predominante desde hace tiempo. Sin embargo, en los últimos años se está observando un cambio, con cifras superiores para el serotipo Typhimurium5–8. La importancia de esta modificación radica en el perfil de sensibilidad, pues el serotipo Typhimurium se relaciona con mayores tasas de resistencia y multirresistencia antibiótica6,9.
La resistencia a ampicilina y amoxicilina-clavulánico en SNT se atribuye a β-lactamasas plasmídicas clásicas, entre las que TEM-1, PSE-1 y OXA-1 son las más frecuentes, aunque las 2 últimas parecen quedar más limitadas al serotipo Typhimurium6,10,11.
Según datos europeos, aproximadamente el 26% de las cepas de SNT son resistentes a ampicilina, con variaciones entre el 0-59% según el área geográfica12. Las cifras en España son superiores a la media europea, por encima del 30%5,6,8,13. La resistencia a amoxicilina-clavulánico se encuentra en aumento en España, aunque se mantiene en cifras bajas, con datos inferiores al 1% en 2001-2003 y en torno al 7-16% en los últimos años5–7.
Se han descrito numerosas cepas de SNT portadoras de β-lactamasas de espectro extendido (BLEE), así como de cefamicinasas, donde la más frecuente es CMY-25,8,10,14–17. En España, las cifras de resistencia a ceftriaxona son inferiores al 0,5%8,9,15. En EE. UU., en 2012 el 3% de las cepas era resistente18. Algunos estudios demuestran que el serotipo Virchow representa un alto porcentaje de las cepas productoras de BLEE, principalmente CTX-M-98,15.
De forma excepcional se han notificado carbapenemasas del tipo KPC, OXA-48, NDM y VIM16,19–21. Dada su capacidad de diseminación y la dificultad que en algunos casos supone su detección fenotípica, pueden convertirse en una amenaza en el futuro. La resistencia a carbapenemas en Salmonella se ha asociado también a otros mecanismos, como producción de una cefamicinasa y pérdida de porinas, así como a la pérdida de expresión de la porina OmpC durante el tratamiento con ertapenem22,23.
La resistencia a cotrimoxazol en España se mantiene constante en la última década, oscilando entre el 5 y el 13%6,7,9,13.
En cuanto a las fluoroquinolonas, la resistencia de alto nivel, definida hasta hace poco como CMI>1mg/L o CMI≥4mg/L por EUCAST y CLSI, respectivamente, continúa siendo excepcional, hecho que podría atribuirse al coste biológico que le supone a la bacteria y que limitaría su supervivencia en ausencia de presión selectiva24.
Merece especial atención la expansión en la última década del serotipo Kentucky con resistencia de alto nivel a ciprofloxacino (CMI>1mg/L). Le Hello et al.16 describen entre 2002 y 2010 una tendencia ascendente en el número de aislamientos en Europa y África. Pese a que las cifras absolutas no son elevadas, resulta preocupante su diseminación geográfica y evolución temporal; también la mayor tasa de hospitalización en comparación con cepas de este mismo serotipo sensibles a ciprofloxacino. Todas pertenecían al complejo clonal ST198, aislado en pollos y pavos de diferentes países africanos, atribuyéndose a estos animales la posible fuente de infección. La resistencia se debía a una doble mutación en gyrA y a una mutación en parC. A ello se suma la aparición desde 2009 de cepas que además han adquirido diferentes β-lactamasas, con resistencia a cefalosporinas de amplio espectro y carbapenemas. Entre las enzimas descritas se encuentran las BLEE CTX-M-1 y CTX-M-15, la cefamicinasa CMY-2 y las carbapenemasas VIM-2 y OXA-4816,25,26.
El fenotipo que predomina actualmente se caracteriza por presentar resistencia de alto nivel a ácido nalidíxico y sensibilidad disminuida a ciprofloxacino (CMI=0,12-1mg/L). La mayoría presentan una única mutación en gyrA27; este fenotipo se relaciona con una baja respuesta clínica y un incremento de la mortalidad en pacientes con infecciones sistémicas tratados con fluoroquinolonas28. Por otro lado, encontramos cepas sensibles a ácido nalidíxico y con sensibilidad disminuida a ciprofloxacino por mecanismos de resistencia plasmídicos asociados a los genes qnr y aac-6′-Ib-cr29–31. Aunque aún se desconoce el impacto clínico que puede tener este fenotipo, la sensibilidad disminuida a ciprofloxacino parece ser el factor más importante para predecir la respuesta al tratamiento32. La prevalencia de resistencia plasmídica es baja en EE. UU.33,34 y algo mayor en Europa y Asia29–31,35.
El método recomendado para evaluar e informar la sensibilidad a quinolonas en Salmonella, tanto por CLSI como por EUCAST, se basaba en la utilización de ácido nalidíxico como cribado. El descubrimiento de otros mecanismos de resistencia a quinolonas en este género ha hecho que deje de ser adecuado para inferir la resistencia en todos los casos. EUCAST desde 2014 y CLSI desde 2015 recomiendan para ello el uso de discos de 5μg de pefloxacino. Sin embargo, CLSI considera resistentes todas las cepas con CMI de ciprofloxacino≥1mg/L, a diferencia de EUCAST, cuyo punto de corte ha bajado a 0,06mg/L36,37.
Con respecto a la azitromicina, Martin-Pozo et al.13 encuentran que el 98,4% (63/64) de las cepas de SNT presentaban una CMI por debajo del punto de corte epidemiológico de EUCAST (CMI≤16mg/L). De igual forma, solo el 1,9% (24/1.237) de las cepas estudiadas por Gunell et al.38 tenían una CMI≥32mg/L, y la mayoría se encontraban comprendidas entre 4-8mg/L. En la serie de Müller et al.39 (N=125) ninguna presentó resistencia a azitromicina.
El fenómeno de multirresistencia, definido como resistencia a 3 o más grupos de antimicrobianos, es en la actualidad un aspecto preocupante por ir en aumento y limitar las opciones de tratamiento. Tal es el caso del fagotipo DT104 del serotipo Typhimurium, cuyo perfil de resistencia más común es ampicilina, cloranfenicol, estreptomicina, sulfamidas y tetraciclina (ACSSuT), y que empezó a extenderse ya desde mediados de los años 80 por todo el mundo40. De Toro et al.6 observan un elevado porcentaje de resistencia a ASSuT, fundamentalmente en este serotipo. En la mayoría de los aislamientos resistentes a ampicilina, encontraron fenotipos de multirresistencia, siendo los patrones más habituales ASSuT y AACSTCSu (AC: amoxicilina-clavulánico). Soler et al.9 encontraron que el 74% (896/1.211) de los aislamientos de principios de la última década del serotipo Typhimurium eran resistentes a 4 o más antibióticos y solo un 13,5% (163/1.211) resultaron sensibles a todos los antibióticos evaluados. Solo el 18,5% (387/2.092) de las cepas estudiadas por Pardos de la Gandara et al.8 eran sensibles a todos los antibióticos analizados, y se encontró un fenotipo de multirresistencia en todas las cepas productoras de BLEE. La asociación de diferentes familias de β-lactamasas localizadas en plásmidos conjugativos incrementa la resistencia y la capacidad de diseminación. Como ejemplos encontramos asociaciones de CTX-M-14 con OXA-1, y de CTX-M-9 con SHV-1215. Aún más preocupante es la presencia simultánea de CMY-2 y OXA-48 en el serotipo Kentucky ST198-X1, resistente, a su vez, a ciprofloxacino16.
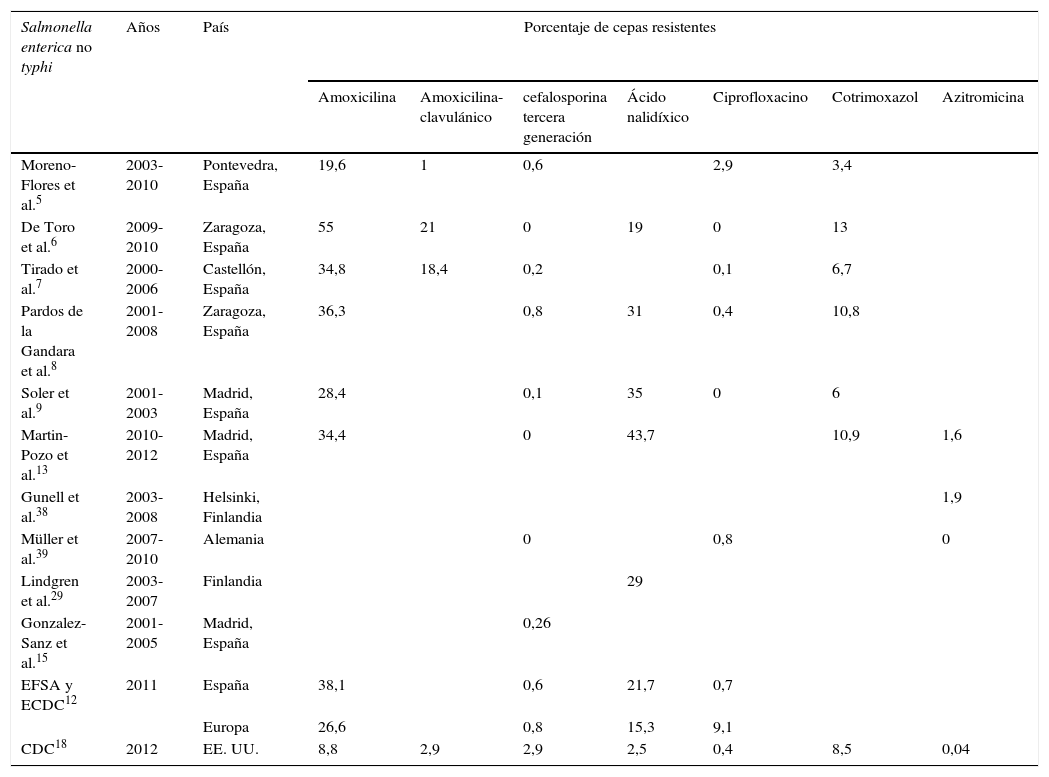
Los datos analizados (tabla 1) muestran hasta la fecha bajas tasas de resistencia a los antibióticos considerados de elección, fundamentalmente en el caso de cefalosporinas de tercera generación y azitromicina. Con respecto a las quinolonas, la resistencia de alto nivel a ciprofloxacino sigue siendo excepcional; no así la resistencia a ácido nalidíxico. Además, la instauración del nuevo sistema de cribado permite realizar un análisis más exhaustivo de la resistencia a este grupo de antimicrobianos y guiar así el tratamiento antibiótico de forma adecuada.
Tantos por ciento de resistencia en Salmonella enterica no typhi
| Salmonella enterica no typhi | Años | País | Porcentaje de cepas resistentes | ||||||
|---|---|---|---|---|---|---|---|---|---|
| Amoxicilina | Amoxicilina-clavulánico | cefalosporina tercera generación | Ácido nalidíxico | Ciprofloxacino | Cotrimoxazol | Azitromicina | |||
| Moreno-Flores et al.5 | 2003-2010 | Pontevedra, España | 19,6 | 1 | 0,6 | 2,9 | 3,4 | ||
| De Toro et al.6 | 2009-2010 | Zaragoza, España | 55 | 21 | 0 | 19 | 0 | 13 | |
| Tirado et al.7 | 2000-2006 | Castellón, España | 34,8 | 18,4 | 0,2 | 0,1 | 6,7 | ||
| Pardos de la Gandara et al.8 | 2001-2008 | Zaragoza, España | 36,3 | 0,8 | 31 | 0,4 | 10,8 | ||
| Soler et al.9 | 2001-2003 | Madrid, España | 28,4 | 0,1 | 35 | 0 | 6 | ||
| Martin-Pozo et al.13 | 2010-2012 | Madrid, España | 34,4 | 0 | 43,7 | 10,9 | 1,6 | ||
| Gunell et al.38 | 2003-2008 | Helsinki, Finlandia | 1,9 | ||||||
| Müller et al.39 | 2007-2010 | Alemania | 0 | 0,8 | 0 | ||||
| Lindgren et al.29 | 2003-2007 | Finlandia | 29 | ||||||
| Gonzalez-Sanz et al.15 | 2001-2005 | Madrid, España | 0,26 | ||||||
| EFSA y ECDC12 | 2011 | España | 38,1 | 0,6 | 21,7 | 0,7 | |||
| Europa | 26,6 | 0,8 | 15,3 | 9,1 | |||||
| CDC18 | 2012 | EE. UU. | 8,8 | 2,9 | 2,9 | 2,5 | 0,4 | 8,5 | 0,04 |
Yersinia enterocolitica (Y. enterocolitica) causa principalmente enterocolitis en niños en los meses de invierno, y más raramente adenitis mesentérica, ileítis terminal, septicemia (en personas con defectos inmunitarios) y artritis reactiva. Se asocia al consumo de agua y alimentos contaminados, principalmente carne de cerdo, que es su principal reservorio. En Europa los serotipos O:3 y O:9, y en raras ocasiones O:5,27 y O:8, causan infecciones en humanos, siendo O:3 el más habitual. El serotipo O:8 se detecta fundamentalmente en EE. UU.41.
La mayoría de los cuadros de enterocolitis son autolimitados y no requieren tratamiento antibiótico. De ser necesario, el fármaco de elección para la gastroenteritis es ciprofloxacino, y en infecciones sistémicas una cefalosporina de tercera generación asociada a gentamicina. Cotrimoxazol y doxiciclina son alternativas aceptadas4.
El principal mecanismo de resistencia a β-lactámicos en Y. enterocolitica es por producción de β-lactamasas cromosómicas, una penicilinasa constitutiva de la clase A (BlaA) y una cefalosporinasa inducible de clase C (BlaB) que no se inhibe con los inhibidores de β-lactamasas. Los genes de BlaA y BlaB se encuentran en la mayoría de las cepas, pero la expresión de una u otra depende del serotipo42,43. La expresión de ambas daría un perfil de resistencia a aminopenicilinas, carboxipenicilinas, cefalosporinas de primera generación, cefoxitina y amoxicilina-clavulánico. Pese a encontrarse en el cromosoma de prácticamente todas las cepas de Y. enterocolitica, la expresión de las 2 enzimas, una sola o ninguna atiende, entre otros posibles factores, a mutaciones puntuales44,45.
Actualmente la mayoría de las cepas se mantienen sensibles a un gran número de antibióticos, entre los que se encuentran cefalosporinas de tercera y cuarta generación, carbapenemas, aminoglucósidos y fluoroquinolonas. La tasa de resistencia a cotrimoxazol es inferior al 2%, y en el caso de las tetraciclinas no supera el 1%13,42–44,46.
Capilla et al.47 detectan un 23% de cepas del serotipo O:3 resistentes a ácido nalidíxico, de las que prácticamente todas presentaban una única mutación en gyrA con elevada heterogeneidad en las mutaciones observadas. Encuentran que la resistencia de alto nivel a ácido nalidíxico se asocia a la suma de una mutación en gyrA y la sobreexpresión de bombas de expulsión. La sensibilidad disminuida a ciprofloxacino, sin embargo, solo se asociaba a una mutación en gyrA; todas las cepas eran sensibles a ciprofloxacino según los puntos de corte actuales.
En nuestra experiencia observamos en los últimos años un incremento en la resistencia a ácido nalidíxico, del 13,5% en el período 2009-2011 al 32% en 2012-2015, y un aumento de cepas resistentes a cotrimoxazol (González-Torralba, manuscrito en preparación).
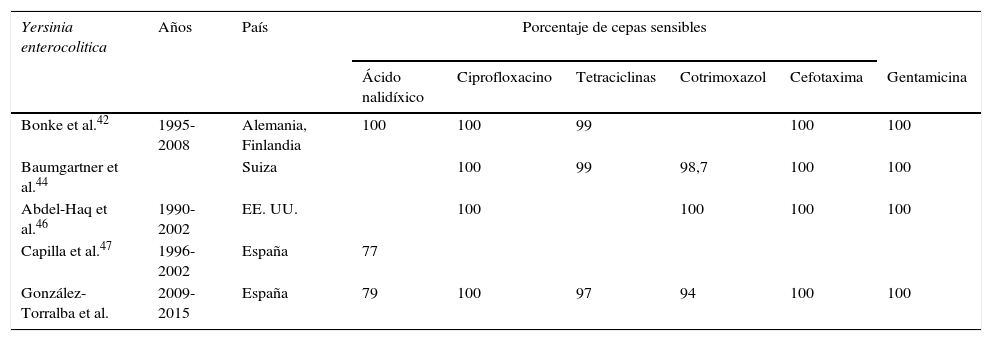
De acuerdo con los datos analizados (tabla 2), podemos concluir que los tratamientos de elección anteriormente mencionados siguen manteniendo por el momento una excelente actividad in vitro frente a Y. enterocolitica, aunque merece una especial atención el incremento en la resistencia a ácido nalidíxico por su posible implicación en la resistencia a fluoroquinolonas en un futuro.
Tantos por ciento de sensibilidad en Yersinia enterocolitica
| Yersinia enterocolitica | Años | País | Porcentaje de cepas sensibles | |||||
|---|---|---|---|---|---|---|---|---|
| Ácido nalidíxico | Ciprofloxacino | Tetraciclinas | Cotrimoxazol | Cefotaxima | Gentamicina | |||
| Bonke et al.42 | 1995-2008 | Alemania, Finlandia | 100 | 100 | 99 | 100 | 100 | |
| Baumgartner et al.44 | Suiza | 100 | 99 | 98,7 | 100 | 100 | ||
| Abdel-Haq et al.46 | 1990-2002 | EE. UU. | 100 | 100 | 100 | 100 | ||
| Capilla et al.47 | 1996-2002 | España | 77 | |||||
| González-Torralba et al. | 2009-2015 | España | 79 | 100 | 97 | 94 | 100 | 100 |
El número anual de gastroenteritis producidas por Shigella a nivel mundial alcanza los 165 millones de casos. Según el informe epidemiológico del año 2013 del ECDC48, en 2011 se notificaron 7.322 casos en Europa, mostrando un descenso paulatino desde 2007, en el que se produjeron 8.380.
La transmisión se realiza a través de alimentos o agua contaminada y por contacto directo entre personas. En los últimos años se ha hecho patente que la shigelosis en hombres que mantienen relaciones sexuales con hombres es básicamente una infección de transmisión sexual. Uno de los principales factores de riesgo asociados a la infección por Shigella es un viaje reciente a una zona endémica. Así, en Europa, aproximadamente el 60% de los pacientes adquirieron la infección en otros continentes, principalmente África y Asia48.
De las 4 especies que incluye el género Shigella, S. sonnei y S. flexneri son las que actualmente engloban la gran mayoría de casos49. Sin embargo, mientras que en los países poco desarrollados predomina S. flexneri, en los países con un mayor nivel de desarrollo S. sonnei es la mayoritaria. Así, en Europa, en 2011 S. sonnei se detectó en el 61% de los casos y S. flexneri en el 32%48. De forma similar, en países que han experimentado una evolución socioeconómica reciente, como Vietnam, se ha detectado un incremento de S. sonnei, del 29 al 78% entre 1995 y 200850.
Las manifestaciones clínicas de la infección por Shigella están determinadas principalmente por su serotipo. Mientras que S. sonnei suele asociarse con cuadros más leves de gastroenteritis, S. flexneri y sobre todo S. dysenteriae pueden producir casos graves. Las principales complicaciones son bacteriemia, cuadros neurológicos y síndrome hemolítico urémico.
El tratamiento antibiótico en la shigelosis reduce el riesgo de posibles complicaciones y acorta la duración de los síntomas y la excreción en las heces del microorganismo, y, por lo tanto, está indicado su empleo51. Es una medida fundamental para evitar la transmisión, especialmente en el caso de un brote, debido al bajo inóculo que necesita Shigella para producir una infección.
Actualmente el tratamiento empírico incluye como fármacos de primera línea las fluoroquinolonas (ciprofloxacino), la azitromicina y las cefalosporinas de tercera generación (ceftriaxona), que globalmente mantienen bajas tasas de resistencia. Como alternativas se encuentran la ampicilina y el cotrimoxazol4.
S. flexneri suele ser más resistente a ampicilina y presenta una mayor multirresistencia a los antibióticos que S. sonnei. Sin embargo, S. sonnei tiene una mayor probabilidad de ser resistente a cotrimoxazol que S. flexneri52–57.
La resistencia a la ampicilina comenzó a detectarse en la década de 1970, pocos años después de ser reconocida como el tratamiento de elección de la shigelosis58. Las mayores tasas de resistencia, que superan el 90%, se han detectado en China55,57 y en la India59. Diferentes estudios en otros países han encontrado un descenso paulatino durante los últimos años. Así, en EE. UU. la tasa de resistencia en 2003 alcanzó el 79%, reduciéndose al 25% en 201218. De igual forma, en Vietnam hubo un descenso del 75 al 48% en el período 1995-200850.
El cotrimoxazol surgió como tratamiento alternativo a la ampicilina, pero en pocos años las tasas de resistencia eran elevadas58. Hoy en día, en países como EE. UU. oscilan entre el 30 y el 50%, mientras que en China alcanzan el 70-80% y superan el 90% en la India18,55,57,60.
Tras la aparición de estos elevados niveles de resistencia frente a ambos fármacos comenzó a emplearse el ácido nalidíxico y posteriormente las fluoroquinolonas58. Los diferentes estudios muestran una gran heterogeneidad en las tasas de resistencia a quinolonas a nivel mundial. Gu et al.61 realizaron un metaanálisis comparando las tasas de resistencia en 2 localizaciones geográficas distintas (Europa-América y África-Asia) desde 1998 hasta 2009. En África-Asia la resistencia al ácido nalidíxico alcanzó un 64% en el año 2009, siendo 5 veces mayor que en 1998, y la resistencia a ciprofloxacino aumentó casi 50 veces, con una tasa final del 29%. En Europa-América no superó el 4% para ácido nalidíxico y el 0,6% para ciprofloxacino en todo el período, con pocos cambios. En el estudio NARMS, en EE. UU., el 4,5% de las cepas aisladas en 2012 fueron resistentes al ácido nalidíxico y el 2% a ciprofloxacino, con un incremento estadísticamente significativo de la resistencia al ácido nalidíxico desde 200318. En Alemania se han detectado cifras más elevadas de resistencia a ciprofloxacino (54%) en cepas de hombres que mantienen relaciones sexuales con hombres; la resistencia fue aún mayor en aquellos coinfectados con el VIH (66 vs. 24%)62. En la India las tasas de resistencia al ácido nalidíxico superan el 90% y son del 70-85% a fluoroquinolonas59,60. En China detectaron igualmente que más del 90% de los aislados fueron resistentes al ácido nalidíxico; aunque la resistencia global a ciprofloxacino fue del 11,6%, el análisis por especie mostró mayores tasas y una tendencia al alza en S. flexneri, con cifras que alcanzaron el 54% en 201157.
Otro de los fármacos de primera línea con posibilidad de administración por vía oral es la azitromicina. A pesar de que actualmente no existen puntos de corte clínicos para Shigella, se considera que aquellas cepas con CMI≥32mg/L presentan una disminución en la sensibilidad18. El mecanismo es la presencia del gen mphA, que produce una fosfotransferasa que inactiva al antibiótico63. La resistencia a este antibiótico en EE. UU. osciló entre el 3,1 y el 4,2% en 2011-201218. Estas cifras son similares a las comunicadas por Pons et al.53 entre 1995 y 2010 en una unidad de medicina tropical en España. Se ha detectado una mayor presencia de cepas con sensibilidad reducida a la azitromicina entre hombres que mantienen relaciones sexuales con hombres, principalmente los infectados por el VIH64–66. En los últimos años han comenzado a detectarse niveles más alarmantes de resistencia; en la India se alcanzan tasas del 34-49%59,60.
En el año 2001 se describió el primer caso de resistencia a cefalosporinas de tercera generación en Shigella67. Posteriormente se detectaron nuevos casos en Irán, India, Bangladesh, Vietnam e incluso en España54,68–71. Folster et al.72 estudiaron en EE. UU. 3.880 cepas de los años 1999-2007, de las que 6 eran productoras de BLEE; en 4 se detectó el gen blaCTX-M-15, y en las 2 restantes, el blaCTX-M-14. Actualmente en EE. UU. el nivel de resistencia a cefalosporinas de tercera generación permanece estable a niveles muy reducidos, un 1,1% en el año 201218. En la India, Ghosh et al.60 encontraron que el 1,9% de los aislados de S. flexneri fueron resistentes a cefalosporinas de tercera generación, mientras que no se detectó ninguna cepa resistente de S. sonnei. Sin embargo, en otro estudio de este país, en la bahía de Bengala, se detectó que entre los años 2006 y 2011 el 17% de las cepas fueron resistentes59. En China se han comunicado cifras de resistencia a cefotaxima del 28-30%55,57. Zhang et al.56 analizaron las cepas aisladas entre 2008-2012 y encontraron un 55,6% de resistencia a cefotaxima, la mayoría por producción de BLEE. En 2 aislados se identificó la presencia de AmpC. En Vietnam se ha detectado un importante aumento de cepas resistentes a cefalosporinas de tercera generación, del 1% en el año 2000 hasta el 23% en 2008 en un estudio50, y del 0 al 75% en otro realizado entre los años 2007 y 2009; el 94,5% fueron S. sonnei y se detectó la producción de CTX-M-15 en el 92% y de CTX-M-24 en el 8%73.
En el momento actual no se ha detectado la presencia de carbapenemasas en Shigella.
La resistencia a 3 clases de antibióticos en cepas de EE. UU. fue del 37%, a 4 clases, del 19%, y a 5, del 8%18. En Chile la multirresistencia en S. sonnei ha aumentado desde 1997; en 2008-2009 la totalidad de las cepas fueron resistentes al menos a ampicilina, cotrimoxazol, tetraciclina y cloranfenicol74. En cepas de hombres que mantienen relaciones sexuales con hombres con sensibilidad disminuida a la azitromicina, el 53% fueron resistentes a 5 o más clases de antibióticos y la corresistencia azitromicina-ciprofloxacino fue del 4%65. En la India se han descrito cepas resistentes a más de 10 antibióticos distintos en el 45% de los casos59, y en China se ha detectado multirresistencia en el 90% de las cepas estudiadas, siendo los patrones más frecuentes: ampicilina-tetraciclina-cotrimoxazol en el 70,8% de las cepas y ampicilina-cotrimoxazol-ciprofloxacino en el 24%55. En aislados resistentes a cefalosporinas de tercera generación de Vietnam, el 97% presentaba además resistencia a cotrimoxazol y tetraciclinas73. Se han detectado también cepas resistentes a fluoroquinolonas y a cefalosporinas de tercera generación, alcanzando niveles de hasta el 74% en aislados de S. flexneri56.
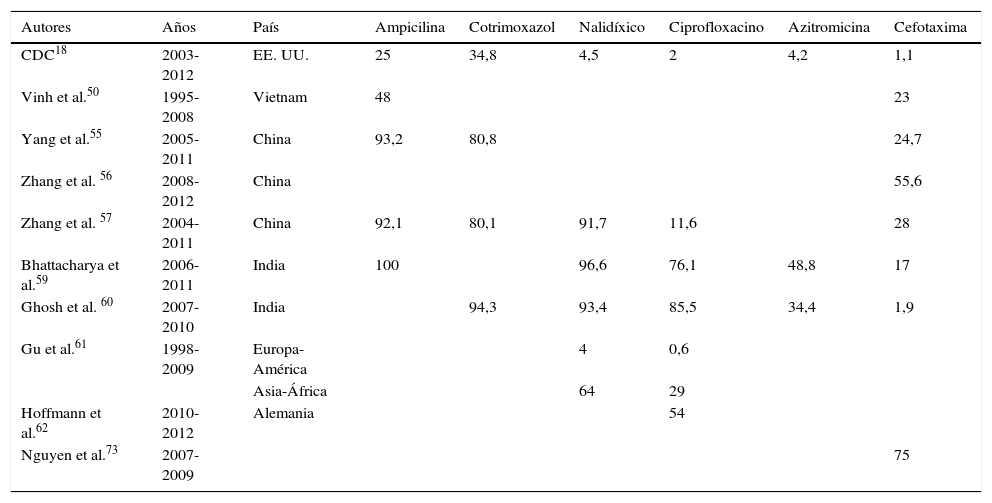
En Europa la infección por Shigella se asocia principalmente a viajes recientes a zonas endémicas. Debido a la gran variabilidad geográfica entre los diferentes patrones de resistencia (tabla 3) es fundamental conocer las características epidemiológicas del paciente para instaurar un tratamiento empírico adecuado. Actualmente no se han detectado resistencias frente a carbapenemas, y las cefalosporinas de tercera generación mantienen habitualmente unas tasas de resistencias bajas. Fluoroquinolonas y azitromicina son una alternativa como tratamiento por vía oral.
Tantos por ciento de resistencia en Shigella
| Autores | Años | País | Ampicilina | Cotrimoxazol | Nalidíxico | Ciprofloxacino | Azitromicina | Cefotaxima |
|---|---|---|---|---|---|---|---|---|
| CDC18 | 2003-2012 | EE. UU. | 25 | 34,8 | 4,5 | 2 | 4,2 | 1,1 |
| Vinh et al.50 | 1995-2008 | Vietnam | 48 | 23 | ||||
| Yang et al.55 | 2005-2011 | China | 93,2 | 80,8 | 24,7 | |||
| Zhang et al. 56 | 2008-2012 | China | 55,6 | |||||
| Zhang et al. 57 | 2004-2011 | China | 92,1 | 80,1 | 91,7 | 11,6 | 28 | |
| Bhattacharya et al.59 | 2006-2011 | India | 100 | 96,6 | 76,1 | 48,8 | 17 | |
| Ghosh et al. 60 | 2007-2010 | India | 94,3 | 93,4 | 85,5 | 34,4 | 1,9 | |
| Gu et al.61 | 1998-2009 | Europa-América | 4 | 0,6 | ||||
| Asia-África | 64 | 29 | ||||||
| Hoffmann et al.62 | 2010-2012 | Alemania | 54 | |||||
| Nguyen et al.73 | 2007-2009 | 75 |
Desde 2005 Campylobacter es el enteropatógeno con mayor número de casos declarados en la Unión Europea. En los últimos años se ha detectado un incremento de hasta el 14% en EE. UU.75–77.
Las infecciones en humanos se producen principalmente por las especies termotolerantes C. jejuni y C. coli. En Europa, de los 214.268 casos confirmados declarados en 2012, casi el 90% se asociaron a estas especies76.
El cuadro clínico de la mayoría de las infecciones son diarreas agudas autolimitadas. Sin embargo, pueden darse casos graves, prolongados o con recaídas, especialmente en los extremos de la vida, en inmunodeprimidos y en gestantes. Las manifestaciones extraintestinales, como la bacteriemia o la meningitis, y las complicaciones postinfecciosas (artritis reactiva, síndrome de Guillain-Barré) son raras.
Cuando está indicado el tratamiento antibiótico, eritromicina y azitromicina son los agentes terapéuticos de primera línea1. Entre las alternativas figuran fluoroquinolonas y tetraciclinas. En el caso de infección sistémica se debe tratar con imipenem solo o asociado a gentamicina4,78.
La resistencia a macrólidos se debe principalmente a mutaciones puntuales en el ARNr 23S, principalmente en las posiciones 2074 y 2075. Cuando las 3 copias del gen, que poseen tanto C. jejuni como C. coli, se ven afectadas, las CMI son elevadas79; se han descrito cepas que solo tenían 2 copias mutadas, con menores CMI de macrólidos80. Otros mecanismos incluyen mutaciones de las proteínas ribosomales L4 y L22, que se asocian con bajos niveles de resistencia, y las bombas de expulsión, principalmente CmeABC, que actúan sinérgicamente con las mutaciones de ARNr 23S para generar elevada resistencia78,79,81. Recientemente se ha detectado la presencia del gen ermB, que codifica una metilasa ribosomal82. En un estudio sobre 1.554 cepas, incluidas 10 de humanos, se encontró dicho gen en el 3,7%, principalmente en C. coli. Todas las cepas con ermB fueron resistentes a eritromicina, la mayoría con CMI>512mg/L, así como a clindamicina, ciprofloxacino y tetraciclinas. La distribución temporal evidencia una aparición reciente y con tendencia al aumento; además, se ha demostrado la transmisión horizontal de este gen entre C. coli y C. jejuni83.
A nivel mundial la tasa de resistencia a macrólidos permanece estable a niveles bajos. En Europa las cepas resistentes a eritromicina suponen el 1,4% en C. jejuni y el 15% en C. coli. En España las cifras son superiores, 3,3 y 27%, respectivamente12. En EE. UU. alcanzan el 2% para C. jejuni y el 9% para C. coli18. Las mayores tasas de resistencia a eritromicina en C. jejuni son del 6,4% y se han descrito en China84.
Uno de los principales problemas en el tratamiento de las infecciones por Campylobacter es el aumento de la resistencia a fluoroquinolonas y tetraciclinas detectado a nivel mundial. La resistencia a fluoroquinolonas se debe principalmente a mutaciones en la región determinante de resistencia a quinolonas del gen que codifica la subunidad gyrA de la ADN girasa. La mutación más frecuente implica el cambio de aminoácido Thr86Ile, que genera elevada resistencia a ácido nalidíxico y ciprofloxacino (CMI>16mg/L); otras mutaciones provocan el cambio de aminoácido Thr86Ala, lo que conlleva una elevada resistencia a ácido nalidíxico pero baja a ciprofloxacino. Además se han descrito alteraciones en el sistema de la bomba de expulsión CmeABC, que actúa sinérgicamente con otros mecanismos, produciendo un elevado nivel de resistencia a fluoroquinolonas79–81.
Las tasas de resistencia a fluoroquinolonas presentan un amplio intervalo entre países. En EE. UU., entre 1997 y 2011 el 25% de C. jejuni y el 34% de C. coli fueron resistentes a ciprofloxacino, con un incremento temporal del 12%18. En España las resistencias son especialmente elevadas, 84% en C. jejuni y 86% en C. coli12. Sin embargo, las tasas más altas se han comunicado en la India, 97%85, y en China, 98%84. Vlieghe et al.86 detectaron entre 1994 y 2006, en pacientes con antecedentes de viaje internacional, resistencia a norfloxacino en el 70% de las cepas de Asia, en el 60,6% de las de América Latina y en el 30% de las de África. El aumento temporal más marcado fue en el subcontinente Indio, del 29 al 78%.
La resistencia a tetraciclinas está mediada por la modificación del punto de unión al ribosoma mediante la producción de una proteína codificada en el gen tetO, que confiere CMI elevadas. Aunque normalmente es de origen plasmídico, también se han detectado en el cromosoma. Además intervienen mecanismos de bombas de expulsión, como CmeABC y CmeG79–81. En Europa, en 2012 se detectaron tasas de resistencia del 32%, siendo especialmente elevadas en España, con un 73%12.
Otros antibióticos susceptibles de emplearse como tratamiento son los aminoglucósidos y los β-lactámicos. Entre los primeros, las modificaciones enzimáticas, que disminuyen la afinidad por el sitio de unión en la subunidad 30S, son las que confieren resistencia. Se han descrito múltiples enzimas, normalmente plasmídicas, siendo la más frecuente tanto en C. jejuni como en C. coli una fosfotransferasa79.
Los mecanismos de resistencia a β-lactámicos son menos conocidos. Se ha detectado la presencia de β-lactamasas, incluyendo una de clase D que no se inhibe por ácido clavulánico, OXA-61. También se han descrito alteraciones en las porinas, así como la existencia de bombas de expulsión como CmeABC80.
Las resistencias a gentamicina y carbapenemas son excepcionales. Fernandez-Cruz et al.87 analizaron las bacteriemias por Campylobacter a lo largo de 23 años. Todos los aislados fueron sensibles a imipenem y el 94% a aminoglucósidos.
La aparición de resistencia a macrólidos es importante ya que se asocia con resistencia a fluoroquinolonas y a otros grupos de antibióticos. El 18% de C. jejuni y el 6,4% de C. coli de Europa fueron sensibles a todos los antibióticos probados, mientras que en España solo lo fueron el 1,6 y 0%, respectivamente. Se detectaron cepas multirresistentes (resistencia a más de 3 grupos de antibióticos) en el 24% de C. jejuni y el 35% de C. coli. El 1,4 y el 16%, respectivamente, presentaron corresistencia a eritromicina y ciprofloxacino12. Wang et al.83 encontraron que todos los aislados portadores de ermB eran resistentes, además, a fluoroquinolonas y tetraciclinas. Lehtopolku et al.88 detectaron un 1,1% de cepas resistentes a macrólidos, de las que el 95, el 74 y el 32% presentaban corresistencia a ciprofloxacino, tetraciclinas y amoxicilina/clavulánico, respectivamente. Debido a esta limitación del arsenal terapéutico diferentes estudios han analizado la utilidad de la tigeciclina como alternativa antibiótica. En el anterior encontraron que todas las cepas multirresistentes estudiadas fueron sensibles. Resultados similares se han descrito en los últimos años en Kuwait, España y Polonia89–92.
De igual forma, el aumento de las resistencias en Campylobacter determina la importancia de los pruebas de sensibilidad in vitro. A pesar de que fue reconocido como un patógeno humano desde 1972, el método de estudio de sensibilidad no se ha estandarizado hasta 2004. Mientras que CLSI37 recomienda como método de elección la dilución en agar o la microdilución en caldo, EUCAST ha estandarizado recientemente un método de difusión con discos36. Además, existen variaciones en los criterios empleados para interpretar los resultados, incluyendo puntos de corte diferentes para C. jejuni y C. coli, por lo que sería conveniente armonizar los criterios de interpretación de los aislados78.
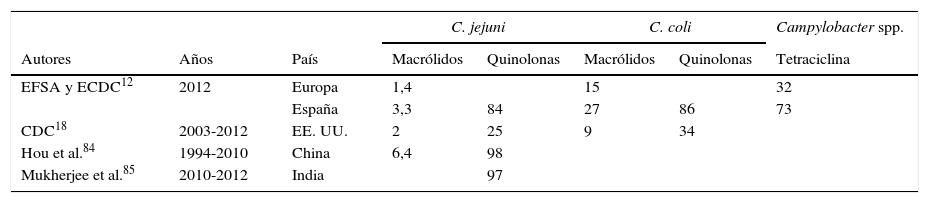
A pesar del aumento de la resistencia que se ha producido en los últimos años, los macrólidos se mantienen como la principal opción terapéutica frente a Campylobacter. Sin embargo, las alternativas por vía oral se encuentran limitadas debido a las actuales tasas de resistencia a quinolonas y tetraciclinas (tabla 4).
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.