Las infecciones de dispositivos de electroestimulación cardiaca conllevan un tratamiento intravenoso prolongado con las complicaciones derivadas de ello. En los pacientes con electroestimulación cardiaca, la bacteriemia por Staphylococcus aureus se asocia con una alta morbimortalidad1. El tratamiento antibiótico definitivo debe basarse en las recomendaciones para endocarditis. Es común el fracaso terapéutico2.
Presentamos un caso de bacteriemia por S. aureus sensible a meticilina (SAMS) en un paciente portador de un desfibrilador automático implantable (DAI) con tromboflebitis séptica yugular, tratado con dalbavancina. Este antibiótico ofrece ventajas posológicas y ha mostrado su actividad en bacteriemia y en infecciones de cuerpo extraño, aunque todavía no se ha aprobado su uso para estas indicaciones.
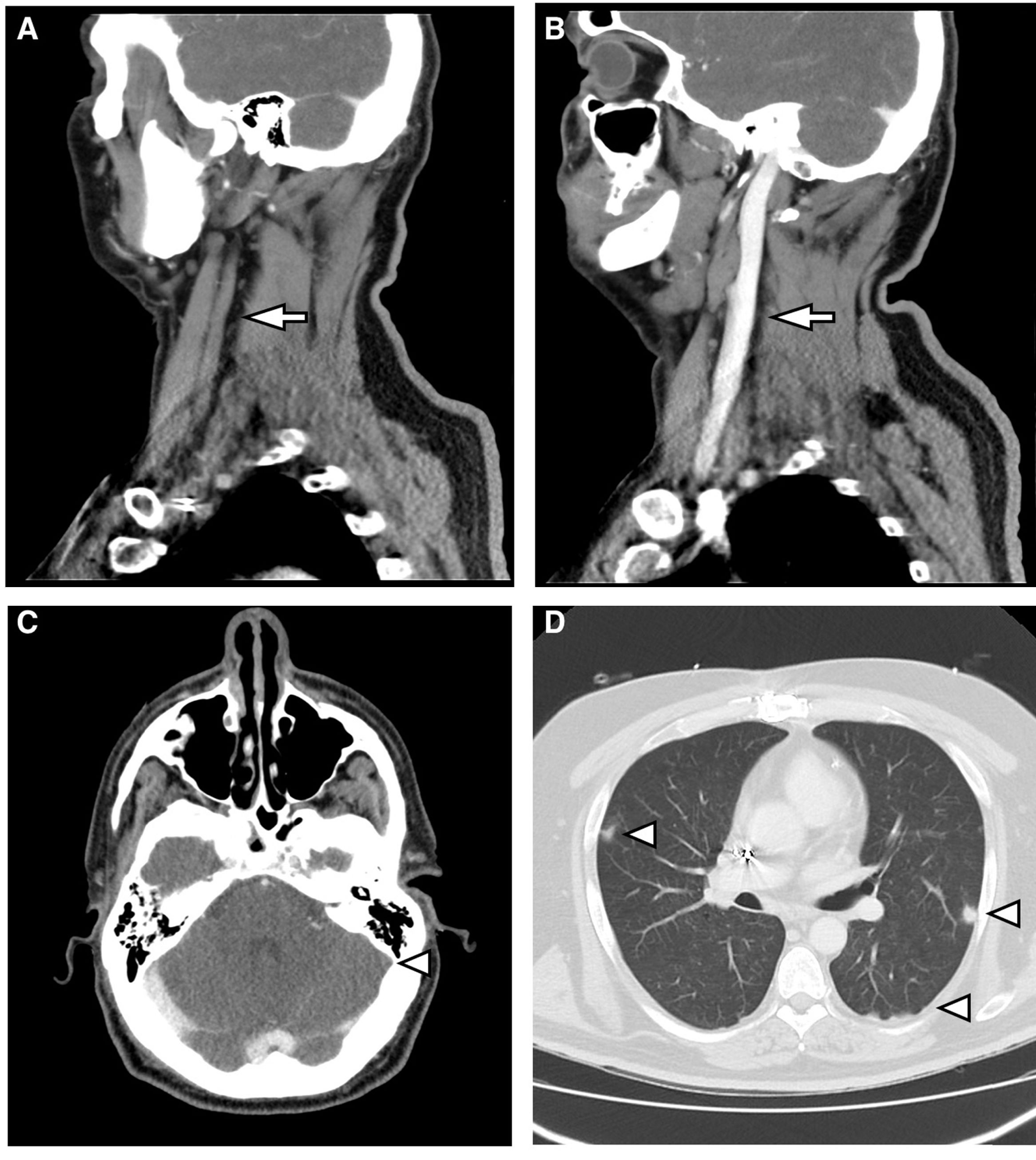
Se trata de un varón de 46 años hospitalizado para estudio de dolor torácico con antecedente de infarto agudo de miocardio hacía 6 meses y colocación de DAI por vía subclavia izquierda 2semanas antes del presente ingreso. El segundo día de hospitalización presentó episodio de fiebre de 39°C asociado a flebitis en vía venosa periférica. Se inició tratamiento con amoxicilina-clavulánico, pasando tras la primera dosis a 2g de cloxacilina intravenosa cada 6/h al objetivar en 2/2 hemocultivos crecimiento de SAMS. Se realizó ecocardiograma transtorácico y transesofágico que no mostró endocarditis ni infección del cable del DAI. Dada la bacteriemia por S. aureus, se solicitó valoración de retirada del dispositivo por Cardiología, que se desestimó inicialmente por considerar que existían riesgos derivados de la intervención que no se podrían asumir en nuestro centro. Tras 3 días de antibioterapia persistía la fiebre y se aisló de nuevo SAMS en hemocultivo, por lo que se asoció 10mg/kg de daptomicina cada 24h al tratamiento anterior. Se solicitó tomografía axial computarizada cervicotorácica que mostró hallazgos compatibles con trombosis de la vena yugular interna izquierda que se extendía al seno sigmoide y embolias sépticas pulmonares bilaterales (fig. 1). Se decidió suspender cloxacilina e iniciar cefazolina (2g/8h) para evitar al máximo la manipulación de la vía venosa, manteniendo daptomicina. Tras 3 días de tratamiento, el paciente presentó nuevo episodio de flebitis, con imposibilidad para canalizar nuevo acceso venoso periférico. Debido a la necesidad de antibioterapia intravenosa durante 6 semanas, dada la posibilidad de infección de cable del DAI y considerando la dificultad para el mantenimiento del acceso venoso, se decidió suspender el tratamiento e iniciar 1.500mg de dalbavancina cada 2 semanas, durante 6 semanas en total. Se realizó de forma ambulatoria, con excelente evolución clínica y analítica. Se solicitaron hemocultivos de control hasta la semana 12 postratamiento, que resultaron estériles, y se realizó PET-TAC al final del tratamiento, sin captación en el cable ni en las válvulas cardiacas, con disminución del tamaño de la trombosis y resolución completa de las lesiones pulmonares.
A) Reconstrucción sagital de TCMD con contraste intravenoso. Ausencia de flujo en la vena yugular interna izquierda (flecha). B) Se compara con la vena yugular interna contralateral bien replecionada (flecha). C) TCMD con contraste intravenoso. Ausencia de flujo en seno sagital (punta de flecha). D) TCMD con ventana de pulmón. Se observan múltiples nódulos parenquimatosos de distribución periférica (puntas de flecha).
La dalbavancina es un lipoglicopéptido aprobado para tratamiento de infecciones de piel y partes blandas. Ofrece ventajas posológicas dada su prolongada vida media3, permite su administración semanal intravenosa y existen estudios que muestran eficacia similar en pautas de dosis única de 1.500mg4. Si bien la única indicación aprobada por la FDA/EMEA es la infección de piel y partes blandas, existen datos que muestran su actividad a otros niveles. Un ensayo clínico de fase 2 en pacientes con bacteriemia relacionada con catéter mostró una tasa de éxito global de dalbavancina superior a la de vancomicina (87 vs. 50%)5. Hay estudios en modelos animales de endocarditis por S. aureus que muestran que dalbavancina presenta mayor actividad que teicoplanina y vancomicina6, y otros estudios muestran su actividad en infecciones de cuerpo extraño por S. aureus7 y en infecciones asociadas a dispositivos subcutáneos8. Trabajos recientes demuestran eficacia en la reducción in vitro de biofilms a concentraciones que pueden obtenerse fácilmente in vivo9, lo que apoya los hallazgos previos publicados del probable potencial de este fármaco en el tratamiento de las infecciones asociadas a dispositivos. En el caso de nuestro paciente, en el que de manera excepcional no se retiró el dispositivo, dalbavancina se ha mostrado eficaz en el control de la infección, sin efectos adversos. Gracias a la pauta utilizada se ha evitado el riesgo y el coste sanitario que hubiera supuesto un ingreso prolongado.
Queda de manifiesto el probable papel que este antibiótico puede jugar en las infecciones intravasculares y de cuerpo extraño, lo que abre nuevas opciones terapéuticas en el ámbito extrahospitalario, si bien se necesitan estudios que comprueben esta hipótesis.