Evaluar las tasas y la naturaleza de las complicaciones relacionadas con el catéter venoso central de acceso periférico (CVCAP o PICC) desde su inserción hasta su retirada.
MétodoEstudio observacional prospectivo. Se han incluido a todos los pacientes con edad superior a 14 años a los que se les insertó un CVCAP en una unidad de cuidados intensivos (UCI) polivalente durante el año comprendido entre el 1 de mayo de 2015 al 30 de abril de 2016. Variables estudiadas: datos demográficos, vena de inserción, indicación, unidad de cuidado, duración, complicaciones y factores relacionados, tasa de infección y motivo de retirada.
ResultadosSe insertaron 144 CVCAP, de los cuales 94 corresponden al grupo UCI (65,28%) y 50 (34,72%) al no-UCI. La complicación más importante fue la sospecha de infección: 17,36% (tasa de incidencia de 15,2 por 1.000 días de CVCAP). El total de infecciones confirmadas fue del 6,25% (5,5 por 1.000 días de CVCAP), siendo en el grupo UCI del 1,39% (1,2 por 1.000 días) y en el grupo no-UCI del 4,86% (4,2 por 1.000 días). Hubo 5 bacteriemias, todas en el grupo no-UCI (3 por 1.000 días). El germen más frecuente fue el Staphylococcus epidermidis (6 casos). La flebitis tuvo una incidencia del 9,03% (7,9 por 1.000 días de CVCAP).
ConclusionesEl CVCAP, eficaz dispositivo de acceso venoso central debido a la mínima incidencia de riesgos en la implantación y a sus ventajas respecto a los catéteres venosos centrales clásicos, es una técnica enfermera más.
To evaluate the rates and nature of the complications related to the Central Peripheral Access Catheter (CVCAP or PICC) from its insertion to its withdrawal.
MethodsProspective observational study. All patients older than 14 years of age with a PICC inserted in the polyvalent intensive care unit (ICU) during the period between May 1, 2015 and April 30, 2016 were included. Data collected included: demographic data, insertion details, reason for insertion and removal, maintenance unit, total dwell time, incidence of complications and related factors and infection rate.
Results144 PICCs were inserted, of which 94 corresponded to the ICU group (65.28%) and 50 (34.72%) to the non-ICU group. The most important complication was the suspicion of infection: 17.36% (rate of 15.2 per 1000 days of PICC). The total number of confirmed infections was 6.25% (5.5 per 1000 days of PICC), 1.39% (1.2 per 1000 days) being in the ICU group and 4.86% (4.2 per 1000 days) in the non-ICU group. There were 5 bacteraemias, all in the non-ICU group (3 per 1000 days). The most frequent germ was Staphylococcus epidermidis (6 cases). Phlebitis had an incidence of 9.03% (7.9 per 1000 days of PICC).
ConclusionsPICC, effective device for central venous access due to the minimal incidence of risks in implantation and to its advantages with regard to the classic central venous catheters, is a further nursing technique.
El catéter venoso central de acceso periférico es un acceso venoso central cada vez más empleado convirtiéndose en una práctica común entre las enfermeras que trabajan en las unidades de cuidados intensivos por sus múltiples usos e indicaciones.
¿Qué aporta?Este artículo describe los resultados de estos catéteres insertados por enfermeras, y demuestra que la tasa de complicaciones, aunque baja, no está exenta de riesgos para el paciente, especialmente cuando su mantenimiento se realiza en plantas de hospitalización.
¿Implicaciones del estudio?Este estudio ha detectado la necesidad de sensibilizar sobre el riesgo de infecciones relacionadas con estos catéteres, y puede servir para motivar a los hospitales a establecer indicaciones claras sobre su uso, que sirvan para mejorar la seguridad del paciente.
El catéter venoso central de acceso periférico (CVCAP), también denominado catéter central de inserción périférica (PICC en denominación anglosajona), es un tubo largo, flexible y delgado, habitualmente entre 4-7F en dependencia del número de luces, que se coloca a través de las venas basílica o cefálica, por encima de la flexura evitando la fosa ante-cubital. Puede ser de corta duración (poliuretano grado I) o de duración intermedia >6 meses (poliuretano grado III). Este catéter se inserta hasta llegar al 1/3 inferior de la vena cava superior (próximo a la unión venoatrial), y se utiliza para la administración de fluidos, productos sanguíneos o fármacos, así como para la monitorización hemodinámica o la extracción de muestras sanguíneas. Según los datos nacionales del programa de prevalencia de las infecciones nosocomiales en España (estudio EPINE-EPPS 2017) se considera que el 83,24% de los pacientes llevan un dispositivo intravascular, de los cuales el 10,41% es un catéter venoso central (CVC)1.
Numerosas guías y protocolos sobre la práctica clínica de la terapia intravenosa a través de catéteres percutáneos2–5, recomiendan el uso de accesos venosos centrales cuando la administración de terapia intravenosa va a tener una duración de más de 6 días, un pH<5 o >9, elevada osmolaridad >600mOsm/l, nutrición parenteral total (NPT), fármacos vesicantes o tratamiento por múltiples luces. A las indicaciones anteriores se podrían añadir los criterios de las enfermeras, habituadas a valorar a los pacientes, observar su árbol vascular y actualizar conocimientos mediante documentos de consenso3,6.
El campo de acción enfermera permite la implantación de dispositivos intravenosos centrales a través de las venas del antebrazo. Los CVCAP son unos dispositivos que cumplen las mismas funciones que una vía central. Estos dispositivos, de durabilidad garantizada, pueden ser implantados por enfermeras capacitadas y, además de preservar el sistema vascular del paciente y permitir también la posibilidad de realizar extracciones sanguíneas sin necesidad de material punzante7, ofrecen otra serie de ventajas sobre otros catéteres venosos centrales como un riesgo de punción arterial muy pequeño, de fácil compresión si se produce, o la ausencia de las complicaciones torácicas propias de las vías centrales de acceso a través de las subclavias o yugulares.
El uso de catéteres vasculares produce, en ocasiones, infecciones de tipo local o sistémico como la bacteriemia no complicada o complicada, manifestada por bacteriemia persistente, tromboflebitis séptica, endocarditis y otras complicaciones metastásicas como abscesos pulmonares, cerebrales, osteomielitis y endoftalmitis. Este tipo de complicaciones tiene una importante morbilidad y una mortalidad no despreciable, siendo la causa más frecuente que obliga a su retirada en cualquier tipo de dispositivo8–10. Por ello, y para evitar las complicaciones, es importante aplicar las indicaciones basadas en la evidencia11,12. Recientemente, en 2015, se publicó la Michigan Appropriateness Guide for Intravenous Catheters (MAGIC) que resume como seleccionar el dispositivo intravenoso con el riesgo más bajo que soporte más eficazmente el plan de tratamiento del paciente13.
Las bacteriemias relacionadas con los catéteres vasculares se encuentran entre las infecciones de mayor frecuencia adquiridas en el hospital. En el estudio EPINE-EPPS 20171, las bacteriemias relacionadas con catéter venoso central (BRCVC) representan el 34,36% del total de todas las bacteriemias, y disminuye al 26,41% cuando la bacteriemia se confirmada también por cultivo microbiológico de la punta del catéter. En el Estudio Nacional de Vigilancia de la Infección Nosocomial en la UCI (ENVIN-HELICS 2017)14 la BRCVC representa el 11,82% de todas las infecciones adquiridas en las unidades de cuidados intensivos (UCI).
Los programas de vigilancia para la prevención de las BRCVC, principalmente destinados a la aplicación sencilla de un grupo de medidas preventivas de eficacia demostrada, asociadas con unas campañas educativas dirigidas al personal y puestas en práctica en colaboración con las estructuras directivas de las instituciones, como la Bacteriemia Zero15, han tenido un impacto significativo en la reducción de las tasas de BRCVC en las UCI, como así lo demuestra los resultados de los 24 años de los estudios ENVIN-HELICS14. En el año 2001 la tasa de bacteriemias de origen desconocido y asociadas a un CVC se situaba en 3,7 episodios por 1.000 días de catéter16 y en el año 2017 estába en 2,93 episodios por 1.000 días de catéter (este año se han estudiado específicamente las bacteriemias con origen en CVC encontrando una incidencia de 1,58 episodios por 1.000 días de CVC)14.
En los catéteres vasculares, como en otros dispositivos, establecer programas de vigilancia implica conocer la patogenia de las infecciones relacionadas con el uso de estos catéteres (IRC). Los microorganismos pueden acceder a los mismos por la vía intraluminal o extraluminal. La adherencia de estos microorganismos y su incorporación formando biocapas ocasiona la colonización de los catéteres, con la posibilidad de desarrollar una diseminación hematógena17.
Existen 3 puntos importantes por donde pueden acceder los microorganismos a través de un CVCAP o cualquier otro tipo de dispositivo intravascular: la contaminación del producto de infusión, la contaminación de la conexión y del espacio intraluminal y la contaminación de la piel adyacente al lugar de su inserción y la superficie extraluminal18.
La contaminación del producto administrado es muy excepcional debido a los rigurosos controles a los que están sometidos estos productos. Solamente en las soluciones de NPT con lípidos preparados presentan un riesgo superior si no se han elaborado con las correspondientes medidas de seguridad8,9. La contaminación de la conexión y del espacio intraluminal es la segunda causa más común, especialmente cuando la duración supera las 2 semanas de implantación18,19. El acceso de los microorganismos desde la piel adyacente al lugar de inserción de los catéteres es el mecanismo patogénico más importante para la colonización de la superficie extraluminal, siendo posiblemente la única vía de llegada en los catéteres con menos de 8 días de inserción. La colonización por diseminación hematógena de un microorganismo originado en un foco distante es muy poco frecuente, observándose fundamentalmente en pacientes críticos con catéteres de larga duración o en enfermos afectos de enfermedades intestinales crónicas y portadores de dispositivos intravasculares para nutrición parenteral. Hay que pensar en esta posibilidad cuando, a pesar de la retirada del catéter, la infección es recidivante8,9,20.
El establecimiento de programas de vigilancia, como la Bacteriemia Zero15, han tenido un impacto significativo en la reducción de las complicaciones infecciosas, favoreciendo el incremento de la utilización de los CVCAP gracias a sus importantes ventajas como6,21,22:
- •
Es un producto enfermero rápido y menos costoso que los catéteres venosos centrales de acceso no periférico.
- •
Preserva el árbol vascular ya que evita múltiples pinchazos al paciente.
- •
Es menos invasivo que un CVC convencional y, al ser de inserción periférica, elimina el riesgo de neumotórax y/o hemotórax.
- •
Es una buena alternativa ante problemas de coagulación.
- •
Tiene los beneficios de cualquier vía central: posibilidad de tratamiento multilumen y administración de fármacos como quimioterapia, NPT, vesicantes y grandes volúmenes. También permite la monitorización hemodinámica y la extracción de muestras sanguíneas.
El objetivo general de este trabajo es evaluar las tasas y la naturaleza de las complicaciones relacionadas con el CVCAP, desde su inserción hasta su retirada.
MetodologíaDiseñoEstudio observacional prospectivo.
ÁmbitoEl ámbito de trabajo es un hospital de segundo nivel con un única UCI de carácter polivalente. Atiende a una población general de 105.600 personas según datos de tarjeta sanitaria individual de 2015. La enfermera inserta los CVCAP, tanto a los enfermos de la unidad como a los enfermos que desde las plantas de hospitalización lo precisan. El periodo de estudio fue del 1 de mayo de 2015 al 30 de abril de 2016.
SujetosSe han incluido en el estudio todos aquellos pacientes mayores de 14 años a los que se les ha insertado un CVCAP durante su ingreso en el hospital.
No se han incluido a los menores de 14 años porque a la población pediátrica de enfermos críticos o semicríticos de nuestro hospital es trasladada al hospital pediátrico de referencia. No se ha realizado exclusión por razones de sexo, servicio de pertenencia o motivo de la colocación del catéter.
En dependencia del cuidado posterior a la inserción se ha dividido a los pacientes en cuidado en la unidad (grupo UCI) y cuidado en plantas de hospitalización (grupo no-UCI).
El tamaño muestral se estimó en función de una incidencia esperada de IRC del 10%. Para una confianza del 95% y con una precisión del ±5%, resultaría una muestra mínima de 130 pacientes.
Para dotar al estudio de seguridad, y reducir al máximo las complicaciones infecciosas, las inserciones se realizaron teniendo en cuenta las recomendaciones del proyecto Bacteriemia Zero15, según el protocolo expuesto en la tabla 1.
Protocolo de inserción de un CVCAP en la unidad
| Solicitud previa a la inserción: hoja interconsulta de solicitud (para los enfermos del grupo no-UCI, consentimiento informado y pruebas de coagulación reciente |
| Información al paciente sobre la técnica a realizar |
| Monitorización del trazado electrocardiográfico y pulsioximetría |
| Posición del paciente: decúbito supino con el brazo en ángulo de 90° |
| Desinfección con clorhexidina acuosa (2%) respetando el tiempo de secado |
| Lavado quirúrgico de manos y uso de medidas de barrera: gorro, mascarilla, bata y guantes estériles |
| Campo estéril mediante sábana y paños estériles dejando campo desinfectado visible |
| Colocación de compresor estéril |
| Inserción del catéter con técnica Seldinger: punción con aguja y jeringa e introducción de guía metálica. Retirada de la aguja dejando solo la guía |
| Teniendo sólo la guía, inyección de anestésico local e introducción del dilatador a la vena a través de la guía |
| Se retira el dilatador y se introduce el CVCAP a través de la guía, vigilando en la monitorización la aparición de extrasístoles o arritmias. Retirada de la guía. Fijación provisional |
| Prueba de imagen para la comprobación de la ubicación de la punta del catéter. Recolocación si fuera necesario |
| Aspirar, comprobar refluido, lavado con 20ml de suero fisiológico con la técnica introducir —parar— introducir. Sellado con fibrilin |
| Limpieza de la zona, fijación adhesiva estéril definitiva para impedir movilizaciones del catéter y protección con gasas estériles |
| La primera cura se realizará a las 24h pudiendo usar entonces apósito transparente para dejar visible la zona de inserción |
CVCAP: catéter venoso central de acceso periférico; UCI: unidad de cuidados intensivos.
Se elaboró una ficha estructurada de recogida de datos y variables de los pacientes en la que se recopilaron los siguientes:
- •
Filiación del paciente: edad, sexo, especialidad procedente de la petición (UCI o no-UCI).
- •
Factores de riesgo relacionados con el paciente: coagulopatía, evidenciada por actividad de protrombina inferior al 50%, tiempo de tromboplastina parcial activado (TTPA) en más de 1,5 veces el control, y recuento plaquetario inferior a 100×109/l, neutropenia, expresada por un recuento absoluto de neutrófilos inferior a 0,5×109/l y necesidad de medidas de aislamiento.
- •
Catéter: localización (cefálica o basílica), número de punciones, recolocación tras Rx de comprobación, duración en días.
- •
Datos de la inserción: indicación del CVCAP (intento de otra localización, problemas anatómicos o tratamiento multilumen), uso preferente (necesidad de vía central, necesidad de NPT, administración de fármacos vesicantes y/o vasoactivos y monitorización hemodinámica,) y motivo de retirada (fin del tratamiento y/o alta del paciente, sospecha de infección —entendida como la presencia de fiebre, enrojecimiento y/o exudado del punto de inserción o la posibilidad de sepsis relacionada con el catéter—, flebitis, salida accidental, rotura o exitus).
- •
Complicaciones: agudas (relacionadas con la inserción) como la migración anómala de la punta del catéter tras la inserción, sangrado y arritmias; y tardías (relacionadas su cuidado hasta la retirada del catéter), flebitis y trombosis.
- •
Datos microbiológicos: cultivo de punta de catéter, hemocultivos de sangre periférica y resultados obtenidos.
- •
Confirmación de la infección diferenciando entre colonización del catéter con presencia de una a 14 unidades formadoras de colonias (UFC), infección asociada a catéter con presencia de 15 o más UFC, bacteriemia asociada a catéter, presencia de 15 o más UFC+hemocultivos positivos con el mismo germen, según el manual de definiciones y términos del estudio (ENVIN-HELIS)14.
Se realizó una descriptiva de los pacientes incluidos en el estudio, acerca de sus características epidemiológicas básicas y las relacionadas con aspectos relativos a su ingreso hospitalario.
Las tasas de incidencias de las complicaciones por 1.000 días de catéter se han calculado sobre el total de catéteres insertados, precisando los resultados con intervalos de confianza (IC) del 95%.
Se emplearon pruebas de significación para conocer los factores relacionados con la aparición de complicaciones, concretamente pruebas de Chi-cuadrado y comparaciones de medias con la t de Student.
Para dichas comparaciones se fijó un umbral de significación del 5%.
Los datos se han analizado con el paquete estadístico SPSS® 11.0.
Consideraciones éticasEsta investigación cumple con la legislación vigente en materia de protección de datos de carácter personal y el marco regulador de referencia para el desarrollo de proyectos de investigación en España y en la Unión Europea. En todo momento se mantuvieron las normas de buena práctica clínica y los principios éticos establecidos para la investigación en seres humanos en la Declaración de Helsinki y sus revisiones posteriores.
De acuerdo con los principios éticos, previamente a la recogida de datos se informó a los pacientes/familia sobre los objetivos del estudio, invitándoles a participar y obteniendo el consentimiento informado, en el que se explicitaba que los datos serían utilizados de manera agregada.
El protocolo de estudio fue aprobado por el Comité de Ética y la Dirección del Centro Hospitalario.
ResultadosSe recogieron datos de 144 pacientes a los que se les había insertado un CVAP. La media de edad fue de 65,15 (DE: ±14,58) años, siendo el 61,80% (n=89) varones y el 38,20% (n=55) mujeres.
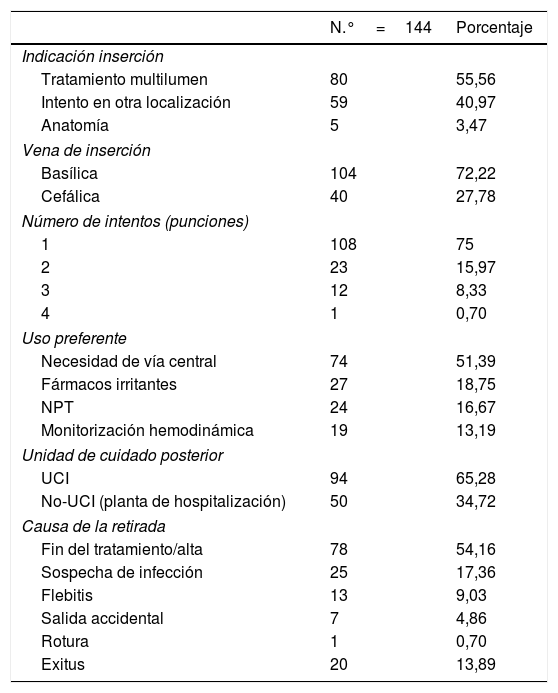
En la tabla 2 se describen los datos referentes a la inserción de los catéteres, unidad de cuidado posterior y causas de la retirada.
Datos referentes a la inserción de los catéteres, unidad de cuidado posterior y causa de la retirada
| N.°=144 | Porcentaje | |
|---|---|---|
| Indicación inserción | ||
| Tratamiento multilumen | 80 | 55,56 |
| Intento en otra localización | 59 | 40,97 |
| Anatomía | 5 | 3,47 |
| Vena de inserción | ||
| Basílica | 104 | 72,22 |
| Cefálica | 40 | 27,78 |
| Número de intentos (punciones) | ||
| 1 | 108 | 75 |
| 2 | 23 | 15,97 |
| 3 | 12 | 8,33 |
| 4 | 1 | 0,70 |
| Uso preferente | ||
| Necesidad de vía central | 74 | 51,39 |
| Fármacos irritantes | 27 | 18,75 |
| NPT | 24 | 16,67 |
| Monitorización hemodinámica | 19 | 13,19 |
| Unidad de cuidado posterior | ||
| UCI | 94 | 65,28 |
| No-UCI (planta de hospitalización) | 50 | 34,72 |
| Causa de la retirada | ||
| Fin del tratamiento/alta | 78 | 54,16 |
| Sospecha de infección | 25 | 17,36 |
| Flebitis | 13 | 9,03 |
| Salida accidental | 7 | 4,86 |
| Rotura | 1 | 0,70 |
| Exitus | 20 | 13,89 |
NPT: nutrición parenteral total; UCI: unidad de cuidados intensivos.
Teniendo en cuenta los resultados de la tabla 2 referentes al número de punciones, el valor de la media de las punciones fue de 1,35 (DE: ±0,66) y en el 75% (n=108) de los casos fue suficiente con un intento.
También se ha podido comprobar que existe relación entre la presencia de complicaciones y el número de punciones requeridas. Aquellos pacientes que presentaron algún tipo de complicación, el resultado indica que fueron sometidos a un mayor número de punciones, media 1,49 (DE: ±0,77), en comparación con los que no se complicaron, cuya media de punciones fue de 1,19 (DE: ±0,46). Y esta diferencia es estadísticamente significativa (p=0,005).
Los CVCAP han estado insertados un total de 1.647 días. La mediana referente al tiempo de inserción del catéter fue de 9 (RIC: 7-17) días.
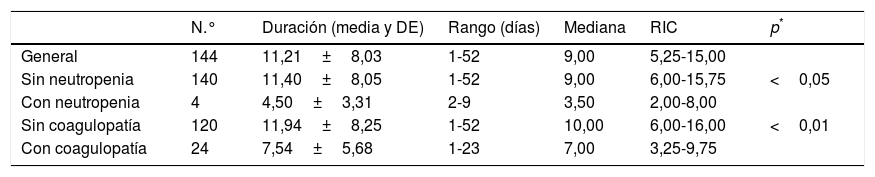
Entre las enfermedades asociadas a los enfermos antes de la inserción, 4 (2,77%) tenían neutropenia y 24 (16,67%) alteraciones de la coagulación. En la tabla 3 se muestra el análisis bivariante sobre la duración de los días del catéter en los pacientes con estas características.
Duración de los catéteres según enfermedad asociada
| N.° | Duración (media y DE) | Rango (días) | Mediana | RIC | p* | |
|---|---|---|---|---|---|---|
| General | 144 | 11,21±8,03 | 1-52 | 9,00 | 5,25-15,00 | |
| Sin neutropenia | 140 | 11,40±8,05 | 1-52 | 9,00 | 6,00-15,75 | <0,05 |
| Con neutropenia | 4 | 4,50±3,31 | 2-9 | 3,50 | 2,00-8,00 | |
| Sin coagulopatía | 120 | 11,94±8,25 | 1-52 | 10,00 | 6,00-16,00 | <0,01 |
| Con coagulopatía | 24 | 7,54±5,68 | 1-23 | 7,00 | 3,25-9,75 |
DE: desviación estándar; RIC: rango intercuartil.
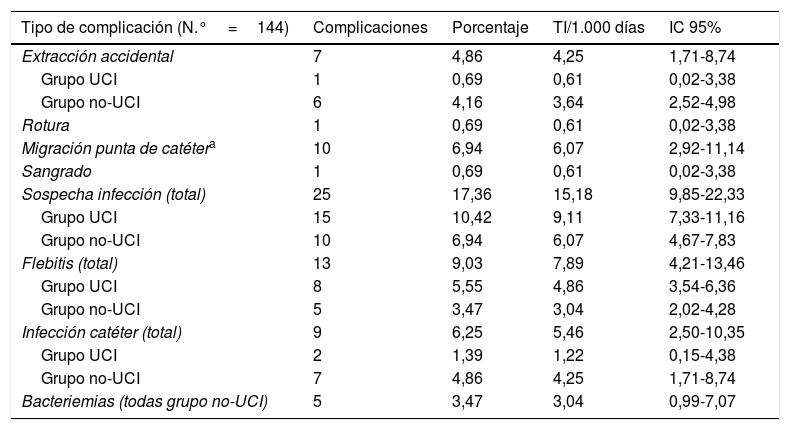
En la tabla 4 se muestran las complicaciones expresadas en porcentajes y tasas de incidencia por 1.000 días de catéter (TI/1.000) junto a los IC.
Complicaciones expresadas en porcentajes y en tasas de incidencias
| Tipo de complicación (N.°=144) | Complicaciones | Porcentaje | TI/1.000 días | IC 95% |
|---|---|---|---|---|
| Extracción accidental | 7 | 4,86 | 4,25 | 1,71-8,74 |
| Grupo UCI | 1 | 0,69 | 0,61 | 0,02-3,38 |
| Grupo no-UCI | 6 | 4,16 | 3,64 | 2,52-4,98 |
| Rotura | 1 | 0,69 | 0,61 | 0,02-3,38 |
| Migración punta de catétera | 10 | 6,94 | 6,07 | 2,92-11,14 |
| Sangrado | 1 | 0,69 | 0,61 | 0,02-3,38 |
| Sospecha infección (total) | 25 | 17,36 | 15,18 | 9,85-22,33 |
| Grupo UCI | 15 | 10,42 | 9,11 | 7,33-11,16 |
| Grupo no-UCI | 10 | 6,94 | 6,07 | 4,67-7,83 |
| Flebitis (total) | 13 | 9,03 | 7,89 | 4,21-13,46 |
| Grupo UCI | 8 | 5,55 | 4,86 | 3,54-6,36 |
| Grupo no-UCI | 5 | 3,47 | 3,04 | 2,02-4,28 |
| Infección catéter (total) | 9 | 6,25 | 5,46 | 2,50-10,35 |
| Grupo UCI | 2 | 1,39 | 1,22 | 0,15-4,38 |
| Grupo no-UCI | 7 | 4,86 | 4,25 | 1,71-8,74 |
| Bacteriemias (todas grupo no-UCI) | 5 | 3,47 | 3,04 | 0,99-7,07 |
Las tasas de incidencias están calculadas por 1.000 días de catéter (número del periodo de uso total de los catéteres: 1.647).
IC: intervalo de confianza del 95%; TI: tasa de incidencia; UCI: unidad de cuidados intensivos.
El número total de infecciones entre los catéteres insertados fue 9 (6,25%), correspondiendo 2 infecciones al grupo UCI (1,39%) y 7 al no-UCI (4,86%), es decir, el 22,22% de las infecciones por CVCAP se produjo en pacientes ingresados en la UCI y el 77,78% en el grupo no-UCI.
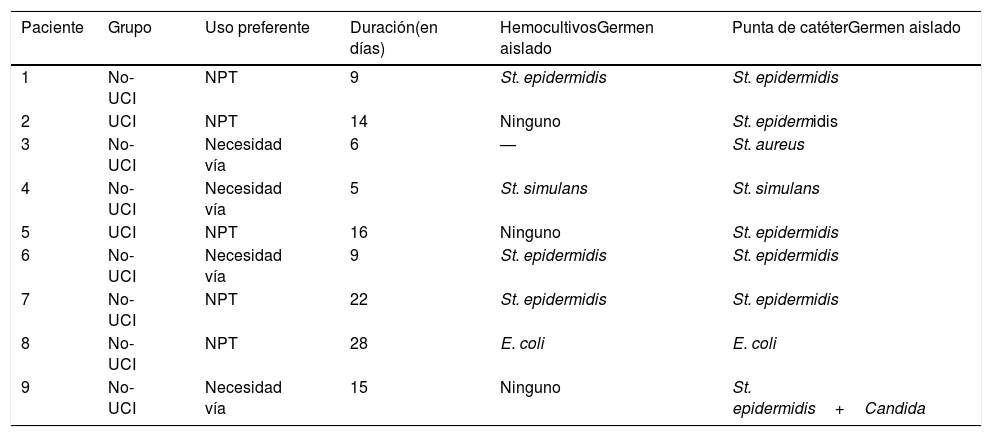
El microorganismo más frecuente de las IRC ha sido el Staphylococcus epidermidis. En la tabla 5 se muestra esta frecuencia, así como otros datos de interés relacionados con la IRC. Es importante resaltar que la NPT, como uso preferente de vía, ha estado presente en 5 (55,56%) de la IRC (n=9) y en 3 (60%) de todas las BRCVC (n=5), así como la diferencia de infecciones entre el grupo UCI y no-UCI (tabla 6).
Infección relacionada con catéter: datos referentes al grupo de cuidado, uso preferente, duración del catéter en días, germen responsable y cultivo de aislamiento (hemocultivos o en punta del catéter)
| Paciente | Grupo | Uso preferente | Duración(en días) | HemocultivosGermen aislado | Punta de catéterGermen aislado |
|---|---|---|---|---|---|
| 1 | No-UCI | NPT | 9 | St. epidermidis | St. epidermidis |
| 2 | UCI | NPT | 14 | Ninguno | St. epidermidis |
| 3 | No-UCI | Necesidad vía | 6 | — | St. aureus |
| 4 | No-UCI | Necesidad vía | 5 | St. simulans | St. simulans |
| 5 | UCI | NPT | 16 | Ninguno | St. epidermidis |
| 6 | No-UCI | Necesidad vía | 9 | St. epidermidis | St. epidermidis |
| 7 | No-UCI | NPT | 22 | St. epidermidis | St. epidermidis |
| 8 | No-UCI | NPT | 28 | E. coli | E. coli |
| 9 | No-UCI | Necesidad vía | 15 | Ninguno | St. epidermidis+Candida |
E: Escherichia; NPT: nutrición parenteral total; UCI: unidad de cuidados intensivos; St: Staphiloccocus.
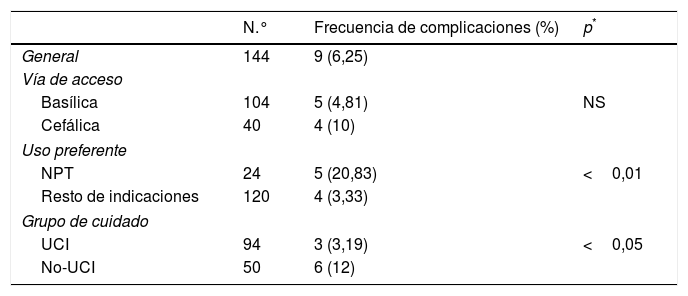
Factores relacionados con la aparición de infecciones
| N.° | Frecuencia de complicaciones (%) | p* | |
|---|---|---|---|
| General | 144 | 9 (6,25) | |
| Vía de acceso | |||
| Basílica | 104 | 5 (4,81) | NS |
| Cefálica | 40 | 4 (10) | |
| Uso preferente | |||
| NPT | 24 | 5 (20,83) | <0,01 |
| Resto de indicaciones | 120 | 4 (3,33) | |
| Grupo de cuidado | |||
| UCI | 94 | 3 (3,19) | <0,05 |
| No-UCI | 50 | 6 (12) | |
NPT: nutrición parenteral total; NS: no significativo; UCI: unidad de cuidados intensivos.
Hubo otros factores estudiados, relacionados con la aparición de infecciones, donde los subgrupos creados eran de un tamaño demasiado pequeño que su comparación resultó sin significación estadística, como las IRC entre pacientes con o sin neutropenia o entre los catéteres que necesitaron recolocación por mala posición inicial de la punta del catéter frente a los que no precisaron. Uno de los 4 pacientes neutropénicos presentó infección (25%), mientras que de los 140 que no lo eran se infectaron 8 (5,7%) (p=0,1). Con relación a los catéteres recolocados, de los 10 que necesitaron recolocación uno presentó infección (10%), mientras que los 134 que no precisaron recolocación se infectaron 8 (5,9%). Estas diferencias de porcentajes, aunque evidentes, no alcanzaron el umbral de significación estadística.
DiscusiónLas enfermeras que cuidan a pacientes en situación crítica se encuentran frecuentemente con problemas para la administración de tratamientos parenterales. La agresividad de algunos de los fármacos habituales como las aminas vasoactivas, los antibióticos, los antiarrítmicos como la amiodarona, etc., obligan en muchas ocasiones a la inserción de más de un catéter venoso periférico no central, y esto aumenta el riesgo de flebitis, extravasación y complicaciones23.
La cateterización venosa central clásica o convencional (CVCC) está ampliamente implantada en los centros hospitalarios desde hace muchos años y su uso no ha dejado de asociarse a complicaciones con riesgo vital para el paciente, prolongación de la estancia hospitalaria y aumento de los costes sanitarios24,25. Una gran alternativa a la CVCC es el CVCAP. Un estudio español de Gómez-Palomar y Miquel Pérez26 publicado en el año 2009 donde comparaba ambas cateterizaciones, concluía que se podía recomendar el uso de los CVCAP a las enfermeras capacitadas porque con una implantación totalmente aséptica y habilidad adquirida, era un sistema tan válido como el CVCC, con mínima incidencia de riesgos en la implantación y sin aumento complicaciones por su utilización. Otros trabajos han demostrado que reducen la carga de trabajo al médico y reducen los costes27,28. Estas ventajas, unidas a que los actuales CVCAP multilumen permiten simultáneamente la administración de diversos tratamientos, monitorización de la presión venosa central (PVC) y control analítico, hacen que sean una elección idónea en pacientes que precisen una vía central.
La flebitis como causa de retirada del catéter, que en este estudio ha sido estudiada independientemente, y no como sospecha de infección, para conocer realmente su incidencia, no deja de ser una entidad nosológica frecuente, relacionada con la infección y de etiología multifactorial. Su incidencia, en dependencia de la aplicación de protocolos, varía entre el 15,25 y el 2%23,29. Puede cursar como entidad propia o complicarse con una trombosis30. En los CVCAP, la más habitual es la mecánica, está relacionada con la zona de inserción del catéter, suele aparecer en los primeros 10 días de colocación y tiene relación con la obstrucción que provoca al flujo sanguíneo (más probable cuando los CVCAP superan el 50% de la luz venosa)31. En dependencia de la inflamación de la vena y, según los criterios visuales del VIP Score32,33, puede cursar con sintomatología clínica o sin ella. La ecografía, técnica de fácil uso, sirve para disminuir la incidencia de complicaciones en la inserción del CVCAP y para valorar la presencia de trombosis34-36.
La suma de la sospecha de infección con las flebitis ha supuesto, entre las causas de retirada, un resultado similar al encontrado por Seisdedos Elcuaz et al.37. Este resultado puede resultar llamativo cuando se compara con las infecciones confirmadas, pero una serie de estudios han demostrado que un porcentaje importante de catéteres retirados por sospecha de infección no tienen ninguna relación con el catéter38,39. Bouza et al.38, en una población de enfermos sin neutropenia, encontraron 204 casos susceptibles de estar relacionados con BRCVC, pero solo 28 (14%) estuvieron realmente relacionadas con el catéter, 27 (13%) no tenían ninguna relación con el catéter, 36 (18%) eran colonizaciones con hemocultivos negativos y el resto de los casos fueron negativos. Ferrer y Almirante18, nos recuerdan que sería necesario documentar y confirmar una infección por catéter antes de retirarlo. Para Rijnders et al.40, la presencia exclusiva de fiebre en enfermos con bajo riesgo de infección relacionada con el catéter, como los inmunocompetentes, sin cuerpo extraño intravascular, sin evidencia de infección en el foco de inserción, o de sepsis grave o shock séptico, bacteriemia o fungemia, no sería necesario retirar el catéter y se podría esperar a los resultados microbiológicos. Para estos mismos autores40, la presencia de un estado de shock o inestabilidad hemodinámica, la retirada temprana del catéter debe ser una prioridad. Sin embargo, en algunas circunstancias, los riesgos de una extracción inmediata del catéter (por ejemplo, coagulopatía con riesgo de diátesis hemorragia o dificultad para reemplazar el catéter), serían los médicos quienes tendrían que valorar la relación riesgos/beneficios. Pensamos que este mismo criterio de valoración se tendría que realizar en presencia de signos locales de infección con fiebre y sin bacteriemia acompañante.
Aunque entre las causas de retirada solo hay un caso de rotura del CVCAP, producido cuando se inyectaba contraste para realizar una tomografía axial computarizada (TAC), es importante recordar que esta exploración precisa de unos flujos superiores a los 5ml/s y no todos los CVCAP están preparados para esta velocidad. El reciente desarrollo de CVCP inyectables de alto flujo ha servido para superar estas limitaciones técnicas. Incluso en estos catéteres recomendamos, antes de la inyección del contraste, comprobar siempre la velocidad máxima de infusión y cual de las luces está habilitada para esta indicación. La extracción accidental encontrada en este estudio ha sido inferior a la encontrada por Grau et al. (8,9%)41. Posiblemente la diferencia radique en que todos los pacientes del estudio eran hospitalarios y los del estudio mencionado eran tanto hospitalarios como ambulatorios.
Safdar y Maki42, en un estudio similar realizado con la implantación de 215 CVCAP encontraron que la duración media de los CVCAP era de 11,3±19,8 días, cifra muy parecida a la media general encontrada en este estudio. El estudio también muestra que ha existido diferencia significativa cuando se ha comparado la duración entre pacientes con o sin neutropenia y con o sin coagulopatía, resultado lógico al tratarse de pacientes gravemente enfermos y con enfermedades subyacentes que los hacen más vulnerables a las infecciones y complicaciones43.
Aunque se ha teorizado que los CVCAP tienen una supuesta mayor seguridad y menor riesgo de infección que los CVCC no tunelizados porque la piel de la parte media-superior del antebrazo tiene una menor temperatura y densidad de bacterias que otras sitios de inserción del catéter venoso27,44, ensayos controlados que comparan ambas clases de catéter concluyen que los CVCAP utilizados en pacientes hospitalizados de alto riesgo están asociados con una tasa de BRCVC similar a los CVCC colocados en las venas subclavia o yugular interna (2 a 5 episodios por 1.000 días de catéteres), una duración media mayor y menor incidencia de trombosis22,42,45. La TI/1.000 infecciosa y de BRCVC de los resultados son acordes con la bibliografía comentada.
Las limitaciones iniciales de los CVCAP: caudales bajos, monitorización difícil de la PVC, falta de seguridad para los procedimientos de radiodiagnóstico, luz única, etc., se impusieron a las comentadas ventajas teóricas supuestas de los CVCAP y retrasaron la implantación de estos dispositivos como práctica común en las UCI. Hoy día nadie duda de que un CVCAP tiene una inserción fácil y segura durante su colocación en las venas periféricas del antebrazo, la ventaja de una ubicación central de la punta del catéter adecuada para todo tipo de soluciones con independencia de la osmolaridad y el pH, y que su indicación en mucho más apropiada en pacientes con alteración de la coagulación porque al facilitar la compresión y ser menor el traumatismo de inserción disminuye el riesgo de hemorragia21,22.
Aunque se han logrado avances significativos en la prevención de las BRCVC, estas infecciones continúan ocurriendo con TI/1.000 estimadas que van desde 1,3 en pacientes hospitalizados hasta 5,6 en las UCI de quemados46,47. En España, los estudios anuales ENVIN-HELICS han sido testigo de estos avances durante los últimos 24 años14,16.
Los resultados de este estudio muestran la diferencia de infecciones encontradas entre el grupo UCI y el no-UCI e indican que hay una necesidad de mejorar los cuidados de mantenimiento, especialmente en el grupo no-UCI. Haber encontrado que todas las BRCVC se dieran en el grupo no-UCI refuerza esta afirmación.
Muchas publicaciones muestran que la tasa de incidencia de BRCVC es mayor en la UCI que en las plantas de hospitalización34,43,45,46. Hay un interesante estudio de Ajenjo et al.43 sobre un total de 163 BRCVC tipo CVCAP (que se presentaron en 162 pacientes) con interesantes resultados y conclusiones. La utilización de los CVCAP fue mucho mayor el grupo UCI que en el grupo no-UCI (0,109 frente a 0,059 catéter/días por paciente-día. La TI/1.000 global encontrada de BRCVC fue de 3,13, observándose una mayor TI/1.000 de BRCVC en el grupo UCI frente al no-UCI (4,79 vs. 2,78), resultado lógico y acorde con que estas tasas de incidencia son mayores en el grupo UCI al tratarse de un grupo de pacientes gravemente enfermos, que pueden tener enfermedades subyacentes y otros factores de riesgo como catéteres múltiples, acceso más frecuente de catéteres, infusiones continuas, etc., que los hacen más vulnerables a la infección. Pero el análisis de estos resultados muestra otro interesante resultado y conclusión: de las 162 BRCVC, 44 (27%) correspondían al grupo UCI y el resto (73%) al grupo no-UCI. Es decir, las tasas de infección fueron considerablemente más altas entre los enfermos del grupo UCI que en los enfermos del grupo no-UCI, pero paradójicamente, el 73% de las infecciones se dieron en el grupo no-UCI, cifra similar a la obtenida en este estudio. Los hallazgos de este estudio en relación con las infecciones encontradas y la evolución de los resultados de los estudios ENVIN-HELICS14,16 demuestran que la aplicación rigurosa del protocolo de Bacteriemia Zero15 para la inserción y el mantenimiento del catéter ha tenido un impacto significativo en la reducción de las tasas de BRCV en las UCI, pero ponen de manifiesto que el cuidado de los CVCAP en las plantas de hospitalización no se realiza adecuadamente. En definitiva, para la prevención y el control de las infecciones relacionadas con el mantenimiento de los catéteres hacen falta estrategias multidisciplinarias, especialmente cuando su cuidado se va a realizar en unidades fuera de las UCI.
Coincidiendo con la bibliografía revisada, los estafilococos, en especial las especies coagulasa negativos como el Staphylococcus epidermidis y el Staphylococcus simulans, y en menor grado el Staphylococcus aureus, son los agentes etiológicos más frecuentes encontrados, seguidos de bacilos entéricos gram negativos y especies de Candida1,18,37,47,48,49. El Staphylococcus epidermidis es un microorganismo habitual de la piel y especialmente capacitado para colonizar catéteres vasculares, al segregar una sustancia adherente que facilita su unión a las superficies plásticas y forma una capa denominada biofilm que la protege de los mecanismos defensivos del huesped y favorece su multiplicación50. El crecimiento de Escherichia coli se dio en un paciente con NPT y que posteriormente fue diagnosticado e intervenido quirúrgicamente de un acceso intraabdominal. Este germen suele encontrase en pacientes con enfermedades intestinales, en tratamiento con NPT y puede dar lugar a infecciones recidivantes8,9,20.
La administración de NPT por el CVCAP, como por cualquier otro CVCC, conlleva un aumento del riesgo de bacteriemia y/o infección local48,51, y los resultados de este estudio coinciden con bibliografía previa.
El estudio presenta fortalezas y limitaciones. Como fortalezas están, por una parte, el poder comparar los cuidados de mantenimiento y su relación con la infección, una vez insertados todos los CVCAP en la UCI, entre el grupo UCI y no-UCI. Y por otra, en la forma de presentar las complicaciones. Salvo para la bacteriemia, las incidencias suelen expresarse en proporción al número de complicaciones encontradas sobre el total de CVCAP insertados, en vez de en tasas por 1.000 días de catéter. Creemos, al igual que otros autores34,52, que cuando se expresan las incidencias en porcentajes no se tiene en cuenta la duración de los catéteres. Puede ocurrir que 2 estudios presenten flebitis en el 3% de los 100 CVCAP insertados y sin embargo las tasas sean de 4,3/1.000 días de catéter si duran 7 días, y de 0,3/1.000 días de catéter si duran 90 días.
La mayor limitación es no haber descartado rutinariamente, mediante la ecografía e incluso una venografía de contraste, la posibilidad de una flebitis complicada con trombosis, aunque las flebitis que presentaron los pacientes fueron todas asintomáticas. Esta complicación es citada con frecuencia en la bibliografía especializada y va asociada a pacientes con importantes factores de riesgo12,43,53–56. Otra limitación, es haber realizado el estudio en un centro donde la rotación enfermera en las plantas de hospitalización es frecuente, por lo que sus resultados pudieran no ser necesariamente extrapolables a otros ámbitos.
La constante preocupación que existe sobre los problemas infecciosos relacionados tanto con la inserción de catéteres venosos periféricos como con los centrales6,57, garantizan nuevas investigaciones para continuar disminuyendo su incidencia. Con este estudio, los datos obtenidos nos sirven como punto de partida para identificar aspectos mejorables, establecer una estrategia mediante la creación de un grupo de trabajo con los servicios implicados que elabore y difunda un protocolo de consenso y, posteriormente, comparar los resultados de la aplicación del protocolo, fundamentalmente referidos al número de complicaciones, especialmente las infecciones, con los resultados que se han expuesto.
ConclusionesEl CVCAP es un dispositivo eficaz como acceso venoso central por la mínima incidencia de riesgos en la implantación, por no aumentar las BRCVC en los pacientes hospitalizados de alto riesgo cuando se comparan con los CVCC y por sus ventajas respecto a estos últimos catéteres, entre otras una mayor duración y una menor tasa de trombosis.
El CVCAP, considerado como la gran alternativa al CVCC, ha pasado a ser una técnica enfermera más. La alta probabilidad de éxito queda garantizada cuando lo implantan enfermeras capacitados.
En función de la evidencia obtenida en este estudio, parece clave sensibilizar a los profesionales sobre el riesgo de infecciones relacionadas con estos catéteres, mediante la organización de formación multidisciplinar en todo el hospital. De este modo, se podrá mejorar los procesos de inserción y mantenimiento, fomentar la prevención de infecciones, mejorar la seguridad de los pacientes y, con ello, reducir el gasto sanitario.
Conflicto de interesesNo existe ningún conflicto de intereses.
Al equipo de enfermería de la Unidad de Cuidados Intensivos del Hospital General San Jorge de Huesca, a Teo Lorente por su ayuda en el análisis estadístico y a Visi Ortega por su ayuda en la bibliografía.