Ginkgo biloba no retrasa el deterioro cognitivo en ancianos
Snitz BE, O'meara ES, Carlson MC, Arnol AM, Ives DG, Rapps R, et al. Ginkgo biloba preventing cognitive decline in older adults: a randomized trial. JAMA. 2009;302 (24):2263-70.
Pregunta de investigación. ¿Retrasa el deterioro cognitivo en ancianos el uso de Ginkgo biloba?
Método
Diseño. Ensayo clínico aleatorizado.
Aleatorización. Bloques permutados.
Enmascaramiento. Doble ciego.
Seguimiento. Media de seguimiento 6,1 años.
Ámbito. Cuatro ciudades de Estados Unidos.
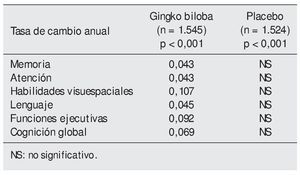
Pacientes. Un total de 7.709 elegidos, de 72 a 96 años. Se excluyen 4.640 y de los 3.069 incluidos, 1.545 reciben Ginkgo biloba y 1.524 placebo. No existen diferencia de edad, sexo, nivel educativo, etc., entre los dos grupos.
Criterios de inclusión y de exclusión. Se excluyeron pacientes con demencia prevalente o con una puntuación superior a 0,5 en la escala de la Clinical Dementia Rating, en tratamiento con warfarina, anticolinérgicos, antidepresivos, antipsicóticos, consumidores de Ginkgo biloba OTC, consumidores de vitamina E, hospitalizados por depresión en el último año o con terapia electroconvulsiva en los últimos 10 años, en tratamiento de Parkinson, o con niveles bajos de creatinina, hematocrito, plaquetas, vitamina B12, alergia a Ginkgo biloba o padecer enfermedad de pronóstico inferior a 5 años.
Intervenciones. Una dosis de 120 mg 2 veces al día de Ginkgo biloba en un grupo frente a placebo.
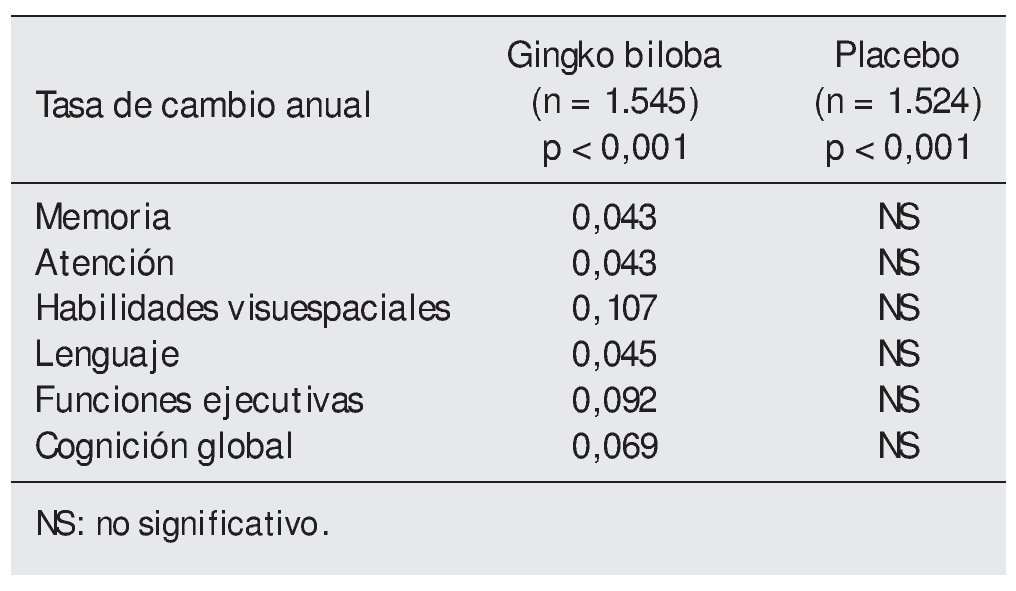
Variables resultado principal. Cambios en la función cognitiva medidos por distintas escalas: miniexamen del Estado Mental Modificado (3MSE), subescala cognitiva de la Escala para la Evaluación de la Enfermedad de Alzheimer (ADAS-Cog), y en dominios neuropsicológicos de memoria, atención, lenguaje, construcción visual espacial y funciones ejecutoras.
Diseño del análisis. Se reclutan 3.069 pacientes y se les solicita consentimiento informado. Se les distribuye en dos grupos (1.545 reciben Ginkgo biloba y 1.524 placebo). Se les pasan tests y cuestionarios periódicamente (3MSE cada 6 meses, ADAS-Cog anual). Cuando no se presentan se les realiza entrevista telefónica.
No hay diferencia entre los pacientes que abandonan el estudio entre un grupo u otro (39,35% de abandonos en grupo tratado y 36,34% en el grupo control-placebo). La adherencia al tratamiento fue similar entre un grupo y otro.
Resultados. No existe diferencia entre el grupo tratado con Ginkgo biloba y el tratado con placebo.
Conclusión de los autores. El tratamiento con Ginkgo biloba no retrasa el deterioro cognitivo en pacientes ancianos sanos ni en aquellos que presentaban un deterioro leve.
Fuente de financiación. Nacional Center for Complementary and Alternative Medicine, Nacional Institute on Aging y otros.
Comentario
En este subanálisis de un estudio previo "Ginkgo biloba for prevention of dementia"1 de los mismos autores, se demuestra que la raíz de Ginkgo biloba, usada para prevenir problemas asociados a la edad, no retrasa el deterioro cognitivo global, ni mejora dominios específicos de la cognición como la memoria, el lenguaje, la atención, las habilidades visoespaciales y las funciones ejecutivas.
La limitación principal del estudio es el abandono y la pérdida de pacientes, en torno al 40% en ambos grupos.
Los resultados obtenidos junto a la evidencia existente confirman que el extracto de Ginkgo biloba no debe utilizarse para el tratamiento del deterioro cognitivo leve ni como prevención del deterioro en personas ancianas sanas. No presenta mayor eficacia que el placebo.
Resultados
Mensaje para la práctica clínica. No hay que utilizar Ginkgo biloba con el propósito de retrasar el deterioro cognitivo en las personas ancianas.
Cumple 17 de los 22 criterios CONSORT.
Términos Mesh: Ginkgo biloba, cognitive decline, dementia.
Autores:
I. Elizondo López de Landache1, R. Escudero Merino2 y L. Braceras Izaguirre1
1Dirección de Farmacia. Gobierno Vasco.
2Distrito Sanitario Córdoba. Servicio Andaluz de Salud
Bibliografía
1. DeKosky ST, Williamson JD, Fitzpatrick AL, Kronmal RA, Ives DG, Saxton JA, et al. Ginkgo biloba for prevention of dementia: a randomized controlled trial. JAMA. 2008;300(19):2253-62.
Menos exacerbaciones asmáticas en los niños usando corticoides inhalados en vez de montelukast
Castro-Rodríguez JA, Rodrigo GJ. The role of inhaled corticosteroids and montelukast in children with mild-moderate asthma: results of a systematic review with meta-analysis. Arch Dis Child. Published online. 2009;doi:10.1136/adc.2009.169177.
Pregunta de investigación. ¿Con qué tratamiento prevenimos más exacerbaciones severas en niños y adolescentes asmáticos, con corticoides inhalados o con montelukast?
Métodos
Diseño. Metaanálisis de ensayos clínicos controlados. Fuente de datos. Medline, Embase y Cochrane Controlled Trials Register.
Selección y valoración de artículos. Ensayos clínicos prospectivos, aleatorizados y controlados publicados entre enero de 1966 y noviembre de 2009 de al menos 4 semanas de duración, en los que se comparan corticoides inhalados (CI) con montelukast (MON) o CI con la combinación de CI+MON en menores de 18 años con diagnóstico de asma leve o moderada desde hace al menos 6 meses.
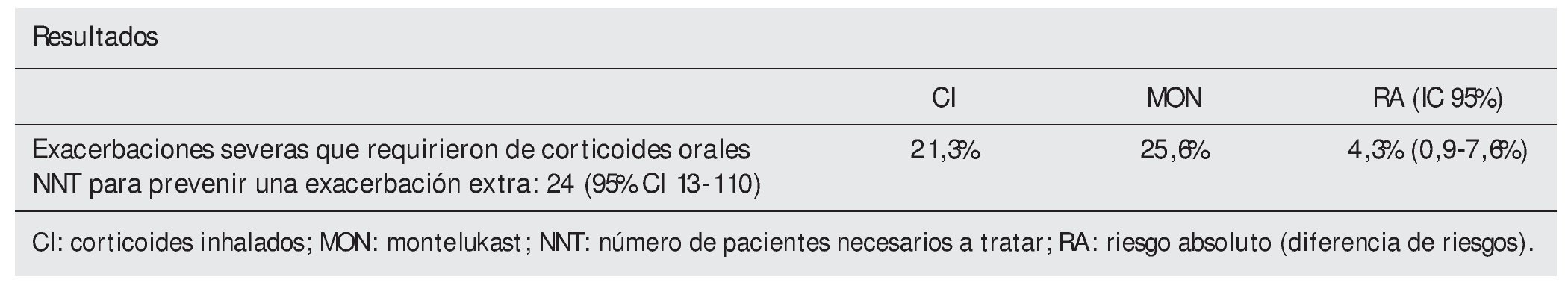
Variable resultado principal. Exacerbaciones severas, definidas como empeoramiento de los síntomas que requirió de corticoides orales.
Resultados. Dieciocho ensayos clínicos (3.757 pacientes) fueron seleccionados. Siete de los estudios (2.429 pacientes, edad media 9,7 años) evaluaban CI frente a MON en la variable principal.
Los pacientes tratados con CI mostraron mejores resultados que los tratados con MON en la variable principal (tabla) y en variables secundarias tales como función pulmonar, uso de medicación de rescate, síntomas y hospitalizaciones por exacerbaciones.
Entre CI y la terapia combinada CI+MON no se encontraron diferencias.
Conclusión de los autores. En niños y adolescentes con asma persistente leve/moderada, los CI en dosis bajas-medias (200-300 mcg de beclometasona) o equivalente fueron superiores a MON en la prevención de exacerbaciones que requirieron de corticoides orales. No hay suficientes datos para determinar si añadir MON a los CI mejora los resultados.
Fuente de financiación. No existe financiación externa.
Comentario
El asma es la enfermedad crónica de mayor prevalencia en la edad infantil, siendo su tendencia ascendente. Disminuye la calidad de vida de un elevado número de niños y familias por su morbilidad, evitable en muchos casos si se siguieran las recomendaciones. Numerosas guías de práctica clínica explicitan la necesidad de aumentar los conocimientos y habilidades de los profesionales que tratan el asma infantil para mejorar su manejo1.
El control de las exacerbaciones es primordial. Afectan a la calidad de vida de los niños, aumentan las necesidades de medicación de rescate y el consumo de recursos, tanto sanitarios (visitas a Urgencias, hospitalizaciones) como no sanitarios (falta de los niños a clase o de los padres al trabajo, problemas de integración en el niño, etc.), en ocasiones incluso suponen un riesgo vital2,3.
Los CI en dosis bajas-medias son el tratamiento más efectivo para el control del asma, mejoran la función pulmonar, sintomatología y calidad de vida, así como la frecuencia y severidad de las exacerbaciones. MON (el antileucotrieno usado en el asma infantil) es considerado una alternativa a los CI2,3. El atractivo de MON es su comodidad de uso vía oral, lo cual hace que se emplee en situaciones donde se debería usar un CI2.
Un metaanálisis llevado a cabo con anterioridad en adultos y niños ponía de manifiesto que se evitaban 4 exacerbaciones que requirieron de corticoides orales si en vez de montelukast se empleaban CI4. Aunque en la población pediátrica no permitía extraer conclusiones por ser el número de niños evaluados insuficiente5.
El metaanálisis que nos ocupa viene a confirmar lo que ya se apuntaba en algunos estudios específicamente hechos en niños: la importancia de usar CI en vez de MON como forma de evitar exacerbaciones severas.
La limitación más importante del estudio es la falta de poder estadístico para discernir otra cuestión de mucho interés: si realmente MON aporta algo a los CI como tratamiento adicional en los niños, dado que los resultados sólo provienen de dos estudios y no alcanzan la significación estadística.
En función de estos resultados, es difícil justificar la utilización de MON en lugar de un CI en el segundo escalón del asma infantil. Se debe promover la utilización de CI en niños de cualquier edad para disminuir el riesgo de crisis asmáticas y reducir el número de ingresos hospitalarios relacionados con el asma.
Mensaje para la práctica clínica. No hay ninguna justificación para usar MON en niños y adolescentes con asma leve o moderada. Los CI, salvo excepciones, se deberían usar siempre de primera elección. Especial importancia tiene también la adherencia y contar con un plan individualizado de manejo del asma por escrito.
Cumple 22 de los 27 criterios PRISMA.
Términos Mesh:asthma, children, corticosteroids, montelukast, exacerbations.
Autores:
J. Rodríguez Castilla, R. Fernández Urrusuno e I. Ferrer López
Servicio Andaluz de Salud
Bibliografía
1. Lora A, Praena M, Rodríguez J. Actualización del tratamiento del asma en niños mayores de 4 años. Form Act Pediatr Aten Prim. 2009;2(3):135-43.
2. Scottish Intercollegiate Guidelines Network and British Thoracic Society. British guideline on the management of asthma: a national clinical guideline. May 2008. Disponible en: http://www.sign.ac.uk/pdf/sign101.pdf
3. Global Strategy for asthma management and prevention (2009 update). Publications reviewed by the GINA Science Commitee. Disponible en: www.ginasthma.org
4. Cohen S, Taitz J, Jaffé A. Paediatric prescribing of asthma drugs in the UK: are we sticking to the guideline? Arch Dis Child. 2007;92(10):847-9.
5. Bloom D, Ermers M, Bont L, van Aalderen WMC, van Woensel JBM. Corticosteroides inhalados durante la bronquiolitis aguda para la prevención de las sibilancias posbronquiolíticas (Revisión Cochrane traducida). Biblioteca Cochrane Plus. 2007;1; nº 3.
Prevención primaria cardiovascular con estatinas: beneficio clínico real aún por confirmar
Brugts JJ, Yetgin T, Hoeks SE, Shepherd J, Westendorp RG, de Craen AJ, et al. The benefits of statins in people without established cardiovascular disease but with cardiovascular risk factors: meta-analysis of randomised controlled trials. BMJ. 2009;338; doi: 10.1136/bmj b2376
Pregunta de investigación. ¿Son eficaces las estatinas en pacientes sin enfermedad cardiovascular y con factores de riesgo en la reducción de la mortalidad y los accidentes cerebrovasculares (ACV) y coronarios?
Método
Diseño. Metaanálisis de ensayos clínicos aleatorizados (ECA).
Fuente de datos. Cochrane Central Register of Controlled Trials, Embase, Medline, DARE, ACP Journal Club.
Selección y valoración de artículos. ECA de tratamiento con estatinas (pravastatina, simvastatina, lovastatina, atorvastatina, rosuvastatina) frente a control (placebo, cuidados o tratamiento activo) y al menos un año de seguimiento, con variable principal de mortalidad y eventos cardiovasculares y con al menos un 80% de personas sin eventos cardiovasculares previos. Ensayos con puntuación JADAD superior o igual a 4.
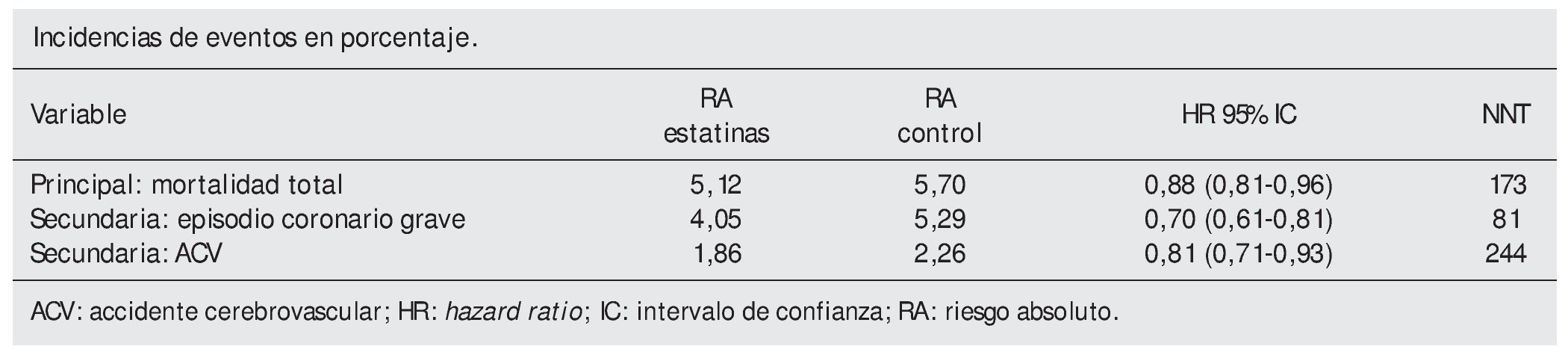
Variables resultado. Principal: muerte por cualquier causa. Secundarias: compuesta de eventos coronarios graves (muerte por enfermedad cardiaca e infarto de miocardio no mortal). Compuesta de ACV (ictus mortal y no mortal).
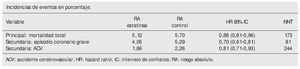
Resultados. Se incluyeron 10 ECA; 70.388 pacientes, (34% mujeres y 23 % diabéticos). Duración media de tratamiento 4,1 años (1,9-5,3). Edad media 63 años (55,3-75). Porcentaje de reducción media en colesterol 17%, en LDL: 26%, en TG: 9,3%. Aumento medio de HDL: 3,3%.
Conclusión de los autores. El uso de estatinas, en pacientes sin enfermedad cardiovascular establecida, pero con factores de riesgo, se asoció con una mejora significativa de la supervivencia y reducciones en el riesgo de episodios cardiovasculares mayores.
Fuente de financiación. Ninguna.
Comentario
El uso de estatinas en pacientes sin enfermedad cardiovascular establecida pero con factores de riesgo es un tema controvertido, su uso en estas condiciones supone sólo el 0,32%1 de las muertes evitadas por modificación de factores de riesgo, frente al 65% que supone dejar de fumar. Además, la industria farmacéutica mantiene la realización de ensayos con cada nueva estatina en esta población, con un claro objetivo de ampliar mercado.
No es el primer metaanálisis que se realiza con este objetivo y sus datos coinciden con los de Mill et al2. Muestra unos resultados favorables con un número de pacientes que es necesario tratar elevados de 173 para mortalidad, 81 para evitar un episodio coronario grave y 244 para la compuesta de accidentes cerebrovasculares. Sin embargo, desconocemos la relevancia clínica real y la aplicabilidad. Los pacientes tienen diferentes características y distintos niveles de riesgo, se permitía incluir ensayos clínicos con hasta un 20% de participantes con historia previa de episodio cardiovascular grave, lo que podría suponer diferentes beneficios. Además, siendo una cuarta parte de los pacientes del estudio JUPITER, se echan en falta datos globales excluyéndolo.
España tiene cuatro veces menos tasas de cardiopatía isquémica en comparación con los países anglosajones, es la llamada "paradoja mediterránea". Ello, unido al problema de la adherencia que no supera el 50% al año de tratamiento, hace que la aplicabilidad de los resultados sea más que dudosa.
Arroja pocos datos en cuanto a efectos adversos. No hay diferencias respecto al cáncer, ni rabdomiólisis2, pero carecemos de información sobre otros eventos como mialgias, alteraciones hepáticas o renales. El estudio JUPITER3 encontró un riesgo aumentado de diabetes con un número necesario para perjudicar (NNH) de 165.
Por todo esto, y a pesar de unos modestos resultados positivos de eficacia, el presente metaanálisis sigue sin tener peso suficiente para modificar recomendaciones actuales4: "el uso de estatinas debe ir encuadrado en una estrategia, en adultos con alto riesgo cardiovascular, calculado mediante escalas adecuadas. Previo a ofrecer un tratamiento con estatinas, se considera recomendable modificar otros factores de riesgo: tabaco, alcohol, hipertensión y obesidad, entre otras".
Mensaje para la práctica clínica. El uso de estatinas en prevención primaria debe ir enmarcado dentro de una estrategia global tras la valoración de todos los factores de riesgo. El uso de tablas puede ayudar a identificar a los pacientes de riesgo más elevado.
Términos Mesh: HMG-CoA reductase inhibitor, cardiovascular disease, cerebrovascular disease, coronary heart disease.
Autores:
E. Hevia Álvareza, C. Barreda Velásquezb y R. Fernández Urrusunoa
aServicio Andaluz de Salud.
bServicio Madrileño de Salud
Bibliografía
1. Unal B, Critchley JA, Capewell S. Modelling the decline in coronary heart disease deaths in England and Wales, 1981-2000: comparing contributions from primary prevention and secondary prevention. BMJ. 2005;331:614. doi10.1136/58561.633345.8F
2. Mills EJ, Rachlis B, Wu P, Devereaux PJ, Arora P, Perri D. Primary prevention of cardiovascular mortality and events with statin treatments: a network meta-analysis involving more than 65,000 patients. J Am Coll Cardiol. 2008;52:1769-81.
3. Ridker P, Danielson E, Fonseca F, Genest J, Gotto AM, Kastelein JJ, et al. JUPITER Study Group. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein. N Engl J Med. 2008;359:2195-207.
4. Cooper A, Nherera L, Calvert N, O'Flynn N, Turnbull N, Robson J, et al. Clinical guidelines and evidence review for lipid modification: cardiovascular risk assessment and the primary and secondary prevention of cardiovascular disease. London: National Collaborating Centre for Primary Care and Royal College of General Practitioners; 2008.
Utilidad de la hemoglobina glucosilada como predictor de riesgo de diabetes y enfermedad cardiovascular
Selvin E, Steffes MW, Zhu H, Matsushita K, Wagenknecht L, Pankow J,, et al. Glicated hemoglobin, diabetes and cardiovascular risk in nondiabetic adults. N Engl J Med. 2010;362:800-11.
Pregunta de investigación. ¿Es superior la medida de hemoglobina glucosilada (HbA1c) a la de glucosa en ayunas como indicador de riego para desarrollar diabetes mellitus (DM) o enfermedad cardiovascular en pacientes asintomáticos?
Método
Diseño. Estudio de cohortes prospectivo poblacional. Seguimiento. Media de 14 años por paciente.
Ámbito. Comunitario.
Contexto. Entre 1987-1989 se realizó un primer seguimiento (estudio ARIC) de 15.792 adultos no diabéticos de mediana edad de 4 comunidades de EE.UU. Entre 1990-1992 a 14.348 de los pacientes anteriores que no habían desarrollado la patología se les extrajo sangre que se utilizó posteriormente en este estudio para medir la hemoglobina glucosilada (HbA1c).
Pacientes. Un total de 11.092 adultos de raza blanca o negra no diabéticos.
Criterios de inclusión. Pacientes de mediana edad sin diagnóstico ni tratamiento de enfermedad cardiovascular o diabetes incluidos en el estudio ARIC.
Criterios de exclusión. Haber desarrollado patología cardiovascular o diabética desde el primer periodo de seguimiento.
Variables resultado principal. Medida de HbA1c. Diagnóstico de DM, desarrollo de cardiopatía isquémica o accidente cerebrovascular isquémico (ACV) confirmados mediante el examen de la historia clínica del paciente- y muerte por cualquier causa.
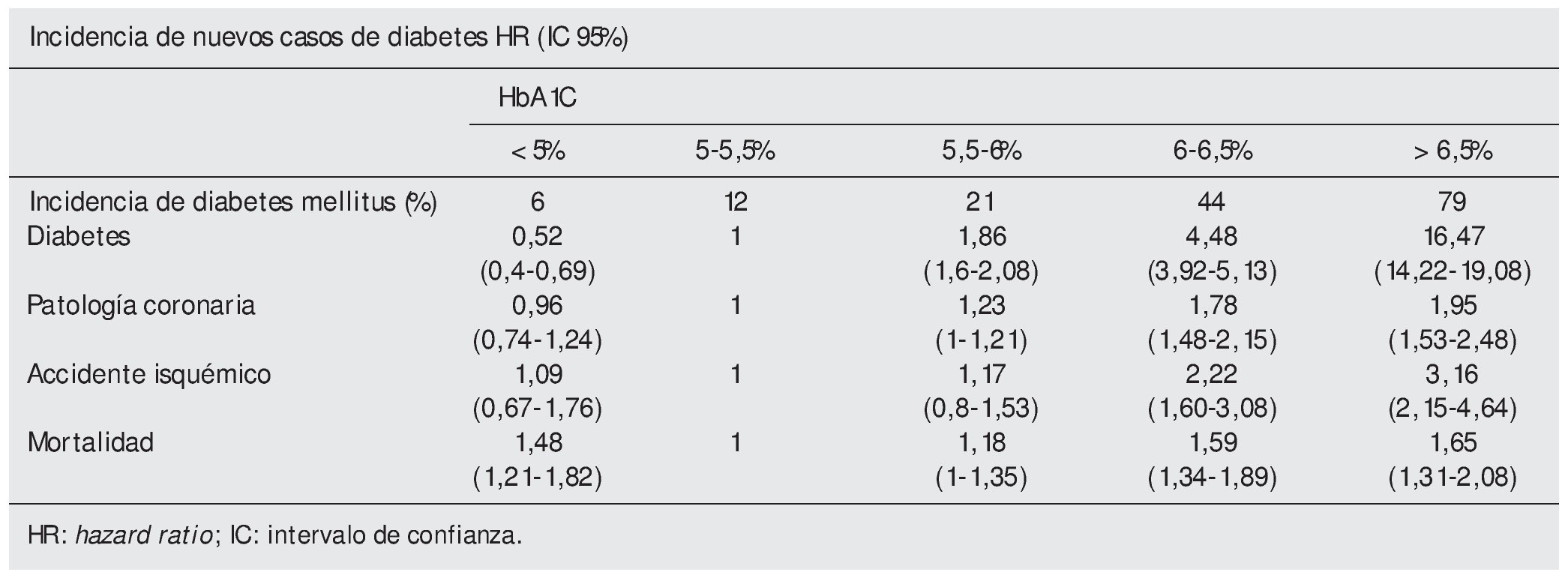
Resultados. Este estudio pone de manifiesto una alta correlación entre los niveles de glucemia y de HbA1c (r = 0,73), siendo estos mayores en mujeres, personas de raza negra, con peor perfil lipídico, con mayor índice de masa corporal (IMC) y no consumidores de alcohol.
Mayores niveles de HbA1c se asociaron con un mayor riesgo de cardiopatía isquémica de una forma más o menos lineal.
En los ACV y la mortalidad total, la asociación adoptaba para la forma de curva en J. Además, en este último caso, el grupo con HbA1c más baja tenía una mortalidad significativamente superior que el grupo de referencia.
Todos los resultados mostraron una relación estadísticamente significativa con la glucemia basal en el análisis crudo, pero que desaparecía en el análisis ajustado si en este se incluía la HbA1c, excepto para la probabilidad de ser diagnosticado de DM.
Conclusión de los autores. En este estudio la HbA1c se asoció con el riesgo de sufrir DM de forma similar a la glucemia en ayunas, y de forma más sólida en caso de enfermedad cardiovascular y muerte por cualquier causa. Estos resultados respaldan el uso de la HbA1c como test diagnóstico de la diabetes.
Fuente de financiación.National Institutes of Health.
Comentario
La HbA1c refleja los valores de glucemia que ha presentado el paciente en los últimos 2-3 meses1. Hace un año la American Diabetes Association (ADA) recomendó incluir como criterio diagnóstico de la DM la presencia de valores de HbA1c > 6,5%, mientras que valores entre 5,7-6,4% se considerarían marcadores de prediabetes e indicarían un mayor riesgo de sufrir una enfermedad cardiovascular. Esta decisión se basó en el hallazgo de una relación entre los valores de este parámetro y la prevalencia de retinopatía diabética en estudios transversales2.
Los resultados de este estudio suponen un respaldo al uso de la HbA1c como técnica diagnóstica en pacientes que no tienen una DM o enfermedad cardiovascular previa. Como ventajas frente a la glucemia en ayunas, la HbA1c proporciona en una sola medida más información a largo plazo, es una prueba fiable, reproducible, que varía escasamente en el tiempo y no se ve afectada por el estrés o la enfermedad del paciente. Además, dichos resultados son concordantes con lo que propugna la ADA, en el sentido de que las personas con una HbA1c > 6% deberían ser objeto de intervención para detectar posibles factores de riesgo cardiovascular y modificar su estilo de vida3.
Mensaje para la práctica clínica. El valor pronóstico de la HbA1c es superior al de la glucemia en ayunas para identificar a personas asintomáticas en riesgo de sufrir DM o una enfermedad cardiovascular. Valores de HbA1c > 6% aumentan el riesgo y nos indican qué pacientes se pueden beneficiar de intervenciones preventivas.
Cumple 19 de los 22 criterios STROBE.
Términos Mesh:diabetes mellitus, cardiovascular risk factors, hemoglobina, glycosylated/metabolism.
Autores:
M.V. Maestre Sánchez, A. García Bonilla y C. Fernández Oropesa
Servicio Andaluz de Salud
Bibliografía
1. Bash LD, Selvin E, Steffes M, Coresh J, Astor BC. Poor glycemic control in diabetes and the risk of incident chronic kidney disease even in the absence of albuminuria and retinopathy: Atherosclerosis Risk in Communities (ARIC) Study. Arch Intern Med. 168(22):2440-7.
2. Edelman D, Olsen MK, Dudley TK, Harris AC, Oddone EZ. Utility of hemoglobin A1c in predicting diabetes risk. J Gen Intern Med. 2004;19:1175-80.
3. American Diabetes Association Standars of medical care in diabetes-2009. Diabetes Care. 2009;32:1327-34.
Los beneficios cardiovasculares del tratamiento con estatinas contrarrestan el ligero incremento del riesgo de desarrollar diabetes
Sattar N, Preiss D, Murray HM, Welsh P, Buckley BM, de Craen AJ, et al. Statins and risk of incident diabetes: a collaborative meta-analysis of randomised statin trials. Lancet. 2010;375(9716):735-42.
Pregunta de investigación. ¿Existe relación entre el uso de estatinas y el desarrollo de diabetes mellitus?
Método
Diseño. Metaanálisis de ensayos controlados aleatorizados. Fuentes de datos. Medline, Embase, Registro Central de Ensayos Controlados Cochrane.
Selección y valoración de los artículos. Ensayos publicados en inglés entre 1994 y 2009, en los que se comparan estatinas con placebo o terapia estándar, con idéntico seguimiento en ambas ramas de tratamiento, y diseñados para establecer el efecto sobre variables cardiovasculares en pacientes estables (excluyendo trasplantados y sometidos a hemodiálisis). Se excluyen ensayos que comparan estatinas o dosis de una misma estatina, los realizados en pacientes diabéticos, los que estudian variables subrogadas, los que recluten menos de 1.000 pacientes o con media de seguimiento menor de un año.
Variables del resultado principal. Nuevos casos de diabetes.
Resultados. Trece ensayos clínicos reunieron los criterios establecidos (6 no publicados), reclutando 91.140 pacientes no diabéticos. La media de seguimiento fue de 4 años. La heterogeneidad entre los ensayos fue baja (I2 = 11,2%; intervalo de confianza [IC] 95% 0,0-50,2%).
Se identificó un incremento absoluto del riesgo de desarrollar diabetes del 0,4% en el grupo tratado con estatinas. Se desarrollaría un caso extra de diabetes por cada 255 (IC 95% 150-852) pacientes tratados con estatinas durante 4 años.
El análisis de meta-regresión muestra que el riesgo de desarrollar diabetes con estatinas es mayor en los ensayos con pacientes de mayor edad, pero ni el índice de masa cor poral basal ni los cambios en el colesterol LDL modifican el riesgo.
No se hallaron diferencias claras entre estatinas, en términos de riesgo de diabetes; tampoco entre moléculas hidrofílicas (pravastatina, rosuvastatina) y lipofílicas (atorvastatina, simvastatina, lovastatina).
Conclusión de los autores. La terapia con estatinas se asoció con un incremento del riesgo de desarrollar diabetes, pero este riesgo es bajo en términos absolutos y cuando se compara con la reducción de eventos coronarios. La práctica clínica en pacientes con riego cardiovascular moderado-alto o con enfermedad cardiovascular establecida no debería cambiar.
Fuente de financiación. Ninguna.
Comentario
Grandes ensayos controlados y aleatorizados han mostrado resultados contradictorios respecto al desarrollo de diabetes en pacientes tratados con estatinas; así, el estudio JUPITER1 encontró mayor número de individuos que desarrollan diabetes en el grupo tratado con rosuvastatina; sin embargo, el estudio WOSCOPS2 sugirió que la pravastatina reduce la frecuencia de la diabetes.
Este metaanálisis de datos publicados y no publicados establece que existe un leve incremento del riesgo de desarrollar diabetes (0,4%) en pacientes tratados con estatinas, comparado con los individuos asignados al grupo control, o lo que es lo mismo, se deben tratar 255 pacientes para producir un caso adicional de diabetes. El riesgo es mayor en pacientes con más edad y no se aprecian diferencias entre estatinas.
Esta asociación podría explicarse por ciertos factores de confusión tales como cambios en el estilo de vida —por ejemplo, pérdida de peso con la correspondiente reducción de la incidencia de diabetes— que pueden ser más comunes en individuos asignados al grupo placebo, o el aumento de la supervivencia en los tratados con estatina. Igualmente, se observó que los 2 estudios con menor incidencia de diabetes se referían a ensayos en prevención primaria y los 4 estudios con mayor incidencia incluían pacientes con alto riesgo de diabetes (edad 70-82 años, infarto de miocardio reciente, insuficiencia cardiaca).
No obstante, el riesgo hallado es pequeño en relación con la reducción de eventos cardiovasculares. Los autores estiman una reducción de 5,4 eventos cardiovasculares mayores (muerte por enfermedad coronaria o infarto de miocardio) por cada 255 pacientes tratados con estatinas durante 4 años, por lo que el balance beneficio-riesgo sería favorable hacia el uso de estatinas.
Por ello, el criterio clínico no debería cambiar para aquellos pacientes en quienes esté indicada la terapia con estatinas: enfermedad cardiovascular establecida (prevención secundaria) o riesgo cardiovascular intermedio-alto cuantificado mediante escalas validadas (prevención primaria)3.
Mensaje para la práctica clínica. El leve incremento del riesgo de desarrollar diabetes con el uso de estatinas es contrarrestado con su beneficio cardiovascular en individuos en quienes está indicado el tratamiento con estatinas: enfermedad cardiovascular establecida o riesgo cardiovascular intermedio-alto.
Cumple 26/27 criterios PRISMA y 15/18 criterios QUORUM.
Términos Mesh: hydroxymethylglutaryl-CoA reductase inhibitors, diabetes mellitus, cardiovascular diseases.
Autores:
B. García Robredoa, V. Arroyo Pinedab y C. Barreda Velázquezc
aServicio Andaluz de Salud.
bServicio de Salud de Castilla La Mancha.
cServicio Madrileño de Salud
Bibliografía
1. Ridker PM, Danielson E, Fonseca FA, Genest J, Gotto AM Jr, Kastelein JJ, et al. Rosuvastatin to prevent vascular events in men and women with elevated C-reactive protein. N Engl J Med. 2008;359(21):2195-207.
2. Freeman DJ, Norrie J, Sattar N, Neely RD, Cobbe SM, Ford I, et al. Pravastatin and the development of diabetes mellitus: evidence for a protective treatment effect in the West of Scotland Coronary Prevention Study. Circulation. 2001;103(3):357-62.
3. San Vicente Blanco R, Pérez Irazusta I, Ibarra Amarica J, Berraondo Zabalegui I, Uribe Oyarbide F, Urraca Garcia de Madinabeitia J, et al. Guía de Práctica Clínica sobre el manejo de los lípidos como factor de riesgo cardiovascular. Vitoria-Gasteiz: Osakidetza; 2008.
La reducción del colesterol con rosuvastatina no frena la progresión de la estenosis aórtica
Chan KL, Teo K, Dumesnil JG Ni A, Tam J; ASTRONOMER Investigators. Effect of lipid lowering with rosuvastatin on progression of aortic stenosis: results of the aortic stenosis progression observation: measuring effects of rosuvastatin (ASTRONOMER) trial. Circulation. 2010;121: 306-14.
Pregunta de investigación. ¿Cuál es el efecto de rosuvastatina 40 mg sobre la progresión de la estenosis aórtica (EA) en pacientes asintomáticos con EA leve a moderada?
Método
Diseño. Ensayo clínico multicéntrico, doble ciego, aleatorizado y controlado con placebo.
Aleatorización. Centralizada y generada por un programa informático de AstraZeneca; ratio 1:1.
Enmascaramiento. Doble ciego.
Seguimiento. Durante un mínimo de 3 años y un máximo de 5; cada 3 meses visita de seguimiento para valorar los efectos adversos y la adherencia al tratamiento; perfil lipídico cada 6 meses el primer año y anualmente después; ecocardiograma doppler anual.
Ámbito. Veintitrés centros canadienses.
Pacientes. Hombres y mujeres entre 18 y 82 años identificados de las unidades de ecocardiografía y cardiología de los centros participantes.
Criterios de inclusión. Pacientes asintomáticos con EA de leve a moderada (definida como velocidad valvular aórtica máxima entre 2,5 y 4 m/s).
Criterios de exclusión. Pacientes con indicación clínica de tratamiento con estatinas, pacientes de origen asiático.
Intervención. Rosuvastatina 40 mg al día.
Control. Placebo.
Variables del resultado principal. Gradiente transvalvular y área de la válvula aórtica. Variable secundaria compuesta de recambio valvular y muerte cardiaca.
Diseño del análisis. Análisis por intención de tratar; las pérdidas y sus causas estuvieron equilibradas en ambos grupos.
Resultados. Fueron aleatorizados 269 pacientes con una mediana de seguimiento de 3,5 años. Los niveles de colesterol LDL en el grupo placebo permanecen sin cambios y en el grupo de tratamiento con rosuvastatina disminuyen un 54% (de 3,18 mmol/l a 1,45 mmol/l p < 0,0001). Las curvas de supervivencia de la variable secundaria no muestran diferencias significativas entre los 2 grupos (p = 0,446). El tratamiento con rosuvastatina no se asoció con diferente progresión de la EA en ninguno de los subgrupos (edad, gravedad de la EA, morfología de la válvula). No existen diferencias en el perfil de efectos adversos entre los 2 grupos de tratamiento (p = 0,64). Un análisis por protocolo muestra resultados similares.
Conclusión de los autores. La reducción del colesterol con rosuvastatina 40 mg diaria no reduce la progresión de la EA en pacientes con EA leve a moderada; por tanto, no debería utilizarse con el único objeto de reducir la progresión de la estenosis.
Fuente de financiación. Instituto Canadiense de Investigación Sanitaria, con soporte adicional de AstraZeneca Canadá Inc.
Comentario
La EA es una disfunción valvular común cuya prevalencia aumenta con la edad. Cuando la gravedad es de leve a moderada es bien tolerada, pero si progresa a severa aumenta la morbimortalidad precisando generalmente recambio valvular. Por ello, cualquier estrategia que permita prevenir su progresión resulta interesante.
Estudios retrospectivos1 han mostrado que el desarrollo de la estenosis es un proceso similar a la ateroesclerosis y que existe asociación entre hipercolesterolemia y EA. Sin embargo, existen resultados contradictorios en cuanto a la asociación del uso de estatinas y el enlentecimiento de la progresión de la estenosis.
El estudio prospectivo pero no aleatorizado RAAVE2 comunicó una menor progresión de la enfermedad en los pacientes con niveles de colesterol LDL elevados y tratados con rosuvastatina. En el estudio prospectivo SALTIRE3, con pacientes con formas severas de EA, no se observaron cambios en la progresión relacionados con el tratamiento (atorvastatina). El estudio prospectivo SEAS estudió los efectos de la reducción de colesterol con la combinación de simvastatina/ezetimiba y no demostró reducir la tasa de progresión de EA.
Los resultados del presente estudio ASTRONOMER son congruentes con los obtenidos en SALTIRE y SEAS rosuvastatina a pesar de tener un efecto importante en la bajada del colesterol total y colesterol LDL no tiene repercusión en la progresión de la EA.
Las diferencias en estos resultados pueden deberse a que tanto en los estudios retrospectivos como en el estudio RAAVE, los participantes tenían hipercolesterolemia y en SALTIRE, SEAS y ASTRONOMER este tipo de pacientes estaban sistemáticamente excluidos.
La evidencia disponible permite afirmar que no existe asociación entre tratamiento con estatinas y reducción de la progresión de EA en pacientes con EA de leve a moderada sin hipercolesterolemia, si bien no se han utilizado variables finales fuertes relacionadas con el paciente, como mortalidad o eventos cardiovasculares mayores.
Mensaje para la práctica clínica. La disminución del colesterol no afecta a la progresión de la EA, por lo que no deberían utilizarse estatinas con el único propósito de reducir la progresión de la enfermedad, es decir, la EA por sí misma no debería ser una indicación de terapia con estatinas.
Cumple 22 de los 25 criterios CONSORT 2010. Términos Mesh:aortic valve stenosis, hydroxymethylglutaryl-CoA reductase inhibitors, rosuvastatin.
Autores:
B. García Robredoa, E. Candela Marroquínb y C. Barreda Velázquezc
aServicio Andaluz de Salud.
bServicio Extremeño de Salud.
cServicio Madrileño de Salud
Bibliografía
1. Miller JD, Weiss RM, Serrano KM, Brooks RM, Berry CJ, Zimmerman K et al. Lowering plasma cholesterol levels halts progression of aortic valve disease in mice. Circulation. 2009;119:2693-701.
2. Moura LM, Ramos SF, Zamorano JL, Barros IM, Azevedo LF, Rocha-Gonçalves F, et al. Rosuvastatin affecting aortic valve en-dothelium to slow the progression of aortic stenosis. J Am Coll Cardiol. 2007;49:554-61.
3. Cowell SJ, Newby DE, Prescott RJ, Bloomfield P, Reid J, Northridge DB, et al. A randomized trial of intensive lipid-lowering therapy in calcific aortic stenosis. N Engl J Med. 2005;352:2389-97.
4. Rossebø AB, Pedersen TR, Boman K, Brudi P, Chambers JB, Egstrup K, et al. Intensive lipid lowering with simvastatin and ezetimibe in aortic stenosis. N Engl J Med. 2008;359:1343-56.
Riesgo cardiovascular y mortalidad asociada a los antidiabéticos orales: un estudio observacional con limitaciones que no modifica las recomendaciones actuales
Tzoulaki I, Molokhia M, Curcin V, Little MP, Millett CJ, Ng A, et al. Risk of cardiovascular disease and all cause mortality among patients with type 2 diabetes prescribed oral antidiabetic drugs: retrospective cohort study using UK general practice research. BMJ. 2009;339:b4731 doi:10.1136/bmj.b4731 database.
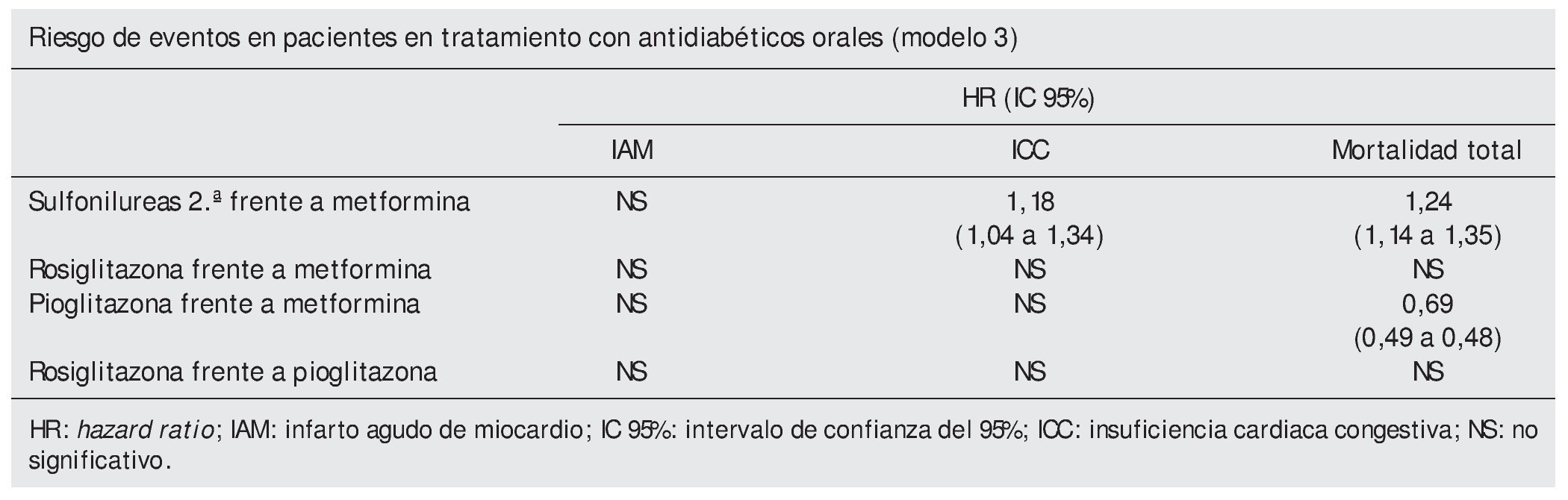
Pregunta de investigación. ¿Cuál es el riesgo de infarto agudo de miocardio (IAM), insuficiencia cardiaca congestiva (ICC) y de mortalidad por cualquier causa (MT) asociados a la prescripción de antidiabéticos orales (ADO)?
Método
Diseño. Estudio de cohortes retrospectivo.
Ámbito. Atención Primaria.
Contexto. Pacientes de medicina general en el Reino Unido entre 1990 y 2005.
Seguimiento. Media de 7,1 años por paciente. Participantes. Pacientes de 35-90 años, identificados como diabéticos, con un episodio de cuidados en el periodo de reclutamiento y registro de algún evento clínico o relacionado con diabetes. Se excluyeron los registros con fecha de fallecimiento duplicada. En el ajuste completo de covariables (modelo 3) se excluyeron 28.812 pacientes por pérdida de información.
Tamaño muestral. Sin determinar. Se incluyeron 91.521 diabéticos, con un total de 2.843.007 intervalos de tratamiento con ADO.
Variable resultado principal. Tasa de episodios nuevos de IAM, ICC y MT.
Intervalos personas/tiempo de tratamiento con ADO (periodo desde el inicio de un ADO hasta el inicio del siguiente ADO, inicio de otro medicamento, finalización o aparición del evento de interés). Se categorizaron en: rosiglitazona, pioglitazona (monoterapia y combinación), sulfonilureas 1.ª y 2.ª generación (monoterapia), metformina (monoterapia), otros ADO y combinaciones excluidas glitazonas e insulinas. Se excluyeron los periodos sin tratamiento o con insuli na y sus eventos.
Variable resultado secundaria. Fracturas (no cadera) como control positivo.
Se realizó una regresión estratificada por edad y año de prescripción, ajustando secuencialmente por sexo y duración de la diabetes (modelo 1), más complicaciones previas, edema agudo de pulmón (EAP); enfermedad cardiovasular (ECV) y tratamiento con otros medicamentos (modelo 2), más índice masa corporal (IMC), colesterol, presión sistólica, HbA1c, creatinina, albúmina y tabaquismo (modelo 3).
Fuente de datos. Base de datos de investigación de médicos generales del Reino Unido.
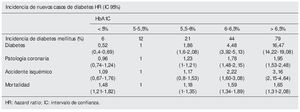
Resultados. Ver tabla.
Mediana de seguimiento por intervalo de tratamiento de 24 días. Metformina en monoterapia fue el fármaco más prescrito (74,5%) seguido de las sulfonilureas de 2.ª generación en monoterapia (63,5%). Durante el periodo de estudio se produjeron 3.588 nuevos IAM, 6.900 ICC, 18.549 muertes y 2.123 fracturas.
Conclusión de los autores. Los resultados sugieren un perfil de riesgo desfavorable de las sulfonilureas comparadas con metformina. Pioglitazona se asoció con una mortalidad por cualquier causa inferior a la de metformina y un mejor perfil de riesgo que rosiglitazona.
Fuente de financiación. Ninguna.
Comentario
El objetivo del tratamiento de la diabetes mellitus 2 (DM2) es disminuir las complicaciones micro y macrovasculares mediante el control de la glucemia y los factores de riesgo cardiovascular (RCV). Los beneficios y riesgos cardiovasculares de los ADO son controvertidos, fundamentalmente por la escasez de ensayos clínicos controlados que estudian dichos efectos1. Las glitazonas incrementan la incidencia de ICC y las fracturas óseas, existiendo un debate importante sobre el riesgo asociado de IAM y muerte cardiovascular2,3. También hay dudas sobre la seguridad cardiovascular de las sulfonilureas4.
Este estudio sugiere un mayor riesgo de ICC y MT con sulfonilureas, no confirma el mayor riesgo de IAM asociado a rosiglitazona, e incluso asocia pioglitazona con un menor riesgo de mortalidad por cualquier causa, comparados con metformina. Entre las glitazonas, pioglitazona se asocia con un menor riesgo de morir o sufrir una ICC que rosiglitazona.
Los resultados son interesantes, aunque algunos contradicen los publicados con anterioridad. No obstante, contiene limitaciones y factores de confusión, que aunque estudiados no pueden ser obviados y que comprometen su validez. A pesar de incluir un número elevado de diabéticos, algunas diferencias observadas podrían deberse a diferencias en las características basales de los pacientes y no a los diferentes tratamientos.
El análisis de covariables completo (modelo 3) disminuye el número de registros disponibles y eventos detectados, limitando el poder para detectar diferencias y aunque algunas estimaciones puntuales sugieren discrepancias, estas no tienen significación estadística, que sí se alcanza excluyendo del análisis (modelo 2) factores importantes para el RCV en pacientes diabéticos como HbA1c, IMC, colesterolemia y tabaquismo, limitando la validez de sus conclusiones.
Mensaje para la práctica clínica. Este estudio no proporciona evidencia para modificar las recomendaciones actuales: metformina como tratamiento inicial de la DM2 y elección preferente de sulfonilureas frente a glitazonas en el segundo escalón. En caso de considerar necesario el uso de una glitazona se recomienda seleccionar pioglitazona por su perfil de seguridad más favorable5.
Cumple 18 de los 22 criterios STROBE.
Términos Mesh:diabetes mellitus type 2, oral antidiabetes drugs, cardiovascular risk factors, retrospective studies.
Autores:
C. Suárez Alemán, C. Fernández Oropesa y E. Hevia Álvarez
Servicio Andaluz de Salud
Bibliografía
1. Bolen S, Feldman L, Vassy J, Wilson L, Yeh HC, Marinopoulos S, et al. Systematic review: comparative effectiveness and safety of oral medications for type 2 diabetes mellitus. Ann Intern Med. 2007;147:386-99.
2. Lincoff AM, Wolski K, Nicholls SJ, Nissen SE. Pioglitazone and risk of cardiovascular events in patients with type 2 diabetes mellitus: a meta-analysis of randomized trials. JAMA. 2007;298: 1180-8.
3. Home PD, Pocock SJ, Beck-Nielsen H, Curtis PS, Gomis R, Hanefeld M, et al. Rosiglitazone evaluated for cardiovascular outcomes in oral agent combination therapy for type 2 diabetes (RECORD): a multicentre, randomised, open-label trial. Lancet. 2009;373(9681):2125-35.
4. Bell DSH. Do sulfonylurea drugs increase the risk of cardiac events? Can Med Assoc J. 2006;174:185-6.
5. Grupo de Trabajo de la Guía de Práctica Clínica sobre diabetes tipo 2. Guía de Práctica Clínica sobre Diabetes tipo 2: Plan Nacional para el SNS del MSC. Agencia de Evaluación de Tecnologías Sanitarias del País Vasco 2008. Guías de Práctica Clínica en el SNS: OSTEBA nº 2006/8.