INTRODUCCIÓN
Desde el inicio de los programas de trasplante, la continua mejora en la selección de candidatos, técnica quirúrgica, regímenes de inmunodepresión, junto con la acumulación de experiencia de la totalidad de los profesionales implicados en el cuidado de estos enfermos, ha logrado un constante aumento de las tasas de supervivencia, que actualmente superan el 90% al año1. Sin embargo, las complicaciones neurológicas siguen constituyendo una causa significativa de mortalidad y morbilidad. De hecho, los estudios necrópsicos de pacientes trasplantados muestran lesiones cerebrales estructurales en la mayor parte de los casos2-4. Existe un número considerable de publicaciones que hacen referencia a este hecho5-13. Sin embargo, la estructuración de la información no es fácil, debido a que la mayoría de los estudios son retrospectivos, la definición de las complicaciones es diferente de unos a otros, la nomenclatura es en ocasiones equívoca (se mezclan presentaciones clínicas con lesiones estructurales) y, finalmente, en unos las complicaciones neurológicas y psiquiátricas se analizan conjuntamente, mientras que en otros se hacen por separado. En cualquier caso, los receptores de trasplante hepático tienen una incidencia de complicaciones muy superior a los receptores de trasplantes cardíaco, renal o pulmonar. Esto es debido a la peculiar situación del paciente receptor de trasplante hepático.
En el caso del trasplante hepático electivo por enfermedad crónica avanzada, generalmente una cirrosis, muchos pacientes presentan alteraciones funcionales cerebrales en forma de encefalopatía hepática crónica, clínica o subclínica, o episodios repetidos de encefalopatía aguda. En los casos avanzados puede existir incluso cierto grado de edema cerebral. Por otra parte, presentan con frecuencia alteraciones hidroelectrolíticas, fundamentalmente hiponatremia, que afectan a la función cerebral.
En el caso de trasplante urgente por insuficiencia hepática aguda grave, la alteración funcional cerebral es obligada (encefalopatía hepática) y en muchos casos existe edema cerebral considerable. De hecho, el edema cerebral es la causa más frecuente de muerte en esta situación.
Durante el trasplante, estos pacientes, además de la anestesia, pueden sufrir alteraciones hemodinámicas, hemorragias, sobrecarga de volumen, cambios hidroelectrolíticos bruscos y, en ocasiones, disfunción pulmonar o renal. En el período postrasplante inmediato, sobre la función cerebral pueden influir la función del injerto, trastornos hidroelectrolíticos, alteraciones hemodinámicas, complicaciones sistémicas y los fármacos inmunodepresores tanto por su potencial directo neurotóxico como por su efecto inmunodepresor. Todos estos hechos hacen que las complicaciones neurológicas afecten como media a un 30% de los pacientes, porcentaje que en la mayor parte de las series se sitúa entre el 27 y el 54%5-13. De dichas complicaciones, la mayor parte afectan al sistema nervioso central, aunque también se observan lesiones del sistema nervioso periférico.
PRESENTACIÓN CLÍNICA Y LESIONES ESTRUCTURALES
Hay que diferenciar entre la presentación clínica y la lesión subyacente que la produce. La presentación clínica de las complicaciones neurológicas se especifican en la tabla I. Las lesiones estructurales subyacentes fundamentales que se han descrito en los estudios necrópsicos se recogen en la tabla II2-4. De estas lesiones estructurales en estudios necrópsicos aproximadamente el 40% son vasculocerebrales. Cabe destacar que la aspergilosis constituye hasta el 10% en algunos estudios2.
CRONOLOGÍA
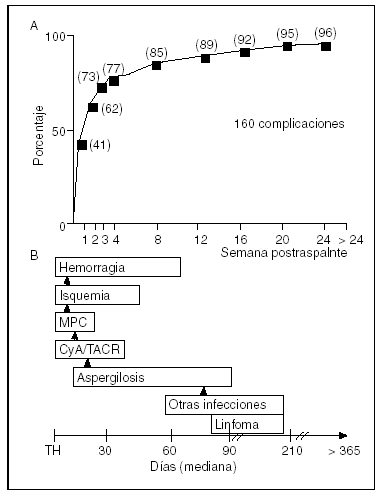
Por el entorno perioperatorio previamente descrito, la aparición de las complicaciones neurológicas es muy temprana. Prácticamente el 90% de las lesiones aparecen en los primeros 3 meses y casi el 80% en el primer mes. Este patrón global es aplicable a cualquiera de las complicaciones, de modo que a las 2 semanas han aparecido el 70% de las alteraciones del nivel de concciencia, el 50% de las convulsiones, el 60% de los episodios de toxicidad farmacológica, el 50% de las infecciones del sistema nervioso central, el 43% de las hemorragias y el 100% de los episodios de mielinólisis10. En las figuras 1A y B se muestran la curva de aparición de las complicaciones neurológicas y la cronología de las complicaciones más frecuentes.
Fig. 1. Aparición de complicaciones neurológicas tras el trasplante hepático (A)10 y cronología de las principales complicaciones neurológicas tras el trasplante hepático (B). TH: trasplante hepático; MPC: mielinólisis pontina central; CyA: ciclosporina; TACR: tacrolimus.
ASPECTOS CLÍNICOS Y PATOLÓGICOS
A continuación se comentan algunos de los aspectos clínicos o patológicos de mayor interés.
Alteración del nivel de consciencia
Es una de las presentaciones clínicas más comunes y puede ser debida a múltiples causas. Entre ellas, las fundamentales son: edema cerebral, encefalopatía anóxica difusa, hemorragia o isquemia cerebrales, infecciones del sistema nervioso central (meningitis, meningoencefalitis, abscesos), crisis comiciales y estado postictal, disfunción del injerto hepático (por encefalopatía metabólica y/o déficit de aclaramiento de fármacos), estados de hiperosmolaridad, toxicidad por ciclosporina o tacrolimus, mielinólisis pontina central, trastornos hidroelectrolíticos o acidosis intensa. Hay casos en que no se consigue averiguar la causa (véase más adelante)8.
Convulsiones
Las causas más comunes de las convulsiones son las alteraciones hidroelectrolíticas. Destacan la hiponatremia, hipocalcemia, hipomagnesemia, encefalopatía hipóxica difusa, infecciones del sistema nervioso central, accidentes hemorrágicos o isquémicos, efecto tóxico de la ciclosporina o el tacrolimus, otros fármacos con potencial convulsivo, la mielinólisis pontina o, en algunos casos, la epilepsia preexistente8,14,15.
Se comentarán a continuación con más detalle algunos aspectos de la encefalopatía anóxica, los accidentes cerebrovasculares hemorrágicos, la mielinólisis pontina y los efectos neurotóxicos de los inmunodepresores.
Complicaciones cerebrovasculares
Las alteraciones cerebrovasculares pueden dar lugar a encefalopatía anóxica, hemorragia o trombosis. De ellas, las 2 primeras son las más frecuentes16-18.
La encefalopatía anóxica suele ocurrir en el período intraoperatorio o postoperatorio temprano debido a hipotensión arterial de cualquier etiología. Las más comunes son la hemorragia y la sepsis. La disminución de la perfusión cerebral produce la lesión del sistema nervioso central que, dependiendo de su intensidad, puede dar lugar a recuperación completa, daño focal leve, que dejará como secuela déficit focales, o una extensa necrosis laminar cortical, que cursa clínicamente con convulsiones y alteración del nivel de consciencia, y que tiene una alta mortalidad o graves secuelas en los supervivientes.
La causa más común de hemorragia cerebral intraparenquimatosa en la población general es la hipertensión arterial de larga evolución. Los pacientes hipertensos desarrollan con los años pequeños aneurismas en las arteriolas cerebrales (aneurismas de Charcot) que finalmente acaban rompiéndose y dando lugar a la hemorragia intraparenquimatosa.
Los pacientes cirróticos en general suelen ser hipotensos y, si existía hipertensión previa, acostumbra normalizarse conforme avanza la enfermedad hepática. Por una serie de razones, en general presentan menor daño aterosclerótico que la población general. En el período postoperatorio inmediato al trasplante hepático el factor que fundamentalmente conduce a la hemorragia cerebral es la coagulopatía, cuya asociación con la hemorragia está demostrada estadísticamente. Se han comunicado casos aislados de vasculitis como origen de hemorragia y es dudoso el papel de la hipertensión arterial, aunque podría actuar como factor coadyuvante en el inicio de la hemorragia en pacientes con coagulopatía.
Una causa particular de hemorragia cerebral en estos enfermos es la aspergilosis cerebral. La infección por Aspergillus, cuya puerta de entrada es respiratoria, puede diseminarse a todo el organismo por vía hematógena. La complicación más grave y mortal en todos los casos es la colonización de los vasos cerebrales con posterior rotura, lo que da lugar a hemorragias cerebrales múltiples. Debido a la inmunodepresión, la población trasplantada es especialmente susceptible a este agente infeccioso19,20.
Mielinólisis pontina central
La mielinólisis pontina central21,22 consiste en una desmielinización de la sustancia blanca en la protuberancia, aunque al menos en el 50% de los casos existe también afectación de la sustancia blanca del cerebelo, ganglios basales, tálamo y cápsulas interna y externa. Esta alteración se da preferentemente en las zonas de frontera entre las sustancias blanca y gris y cursa clínicamente con síndrome de enclaustramiento, alteración del nivel de consciencia, convulsiones, tetraplejía, parálisis seudobulbar o cualquier combinación de las anteriores. Su pronóstico es fatal y la recuperación, excepcional.
Se ha postulado que la hiperosmolaridad, el alcoholismo y la enfermedad hepática actuarían como predisponentes. El mecanismo más común en los pacientes en el período inmediato al trasplante hepático es la brusca corrección de la hiponatremia preexistente, con aumentos entre 15 y 30 mEq de sodio por litro en un período corto de tiempo. Este brusco cambio de la osmolaridad produciría edema cerebral, aumento de volumen de la sustancia gris (células) y compresión de la sustancia blanca adyacente (axones), lo que originaría la mielinólisis.
Neurotoxicidad por inmunodepresores
Múltiples estudios avalan la neurotoxicidad de los inhibidores de la calcineurina ciclosporina y tacrolimus, que son los 2 inmunodepresores fundamentales para evitar el rechazo en los pacientes sometidos a trasplante hepático. Los glucocortidoides pueden producir alteraciones de la conducta o incluso cuadros psicóticos a dosis altas, y el micofenolato mofetil, la azatioprina y la rapamicina no son neurotóxicos8,23.
El perfil neurotóxico de la ciclosporina y el tacrolimus es similar. En los estudios comparativos iniciales el tacrolimus producía una mayor frecuencia e intensidad de complicaciones, que se igualaron a las producidas por la ciclosporina una vez alcanzadas las dosis de tacrolimus que actualmente se usan de manera habitual. El estudio más extenso publicado que compara la neurotoxicidad de estos 2 fármacos en más de 500 pacientes describe los siguientes efectos neurológicos: somnolencia, encefalopatía, convulsiones, afasia, disartria, psicosis, confusión-delirio, reacciones paranoides, insomnio, depresión, cefalea, temblor, ceguera cortical, neuropatía y una miscelánea de otras complicaciones8,23.
En el primer mes tras el trasplante, el insomnio (un 26 y un 18% en los grupos tratados con tacrolimus y ciclosporina, respectivamente) y el temblor (un 16 y un 10%, respectivamente) fueron las complicaciones más frecuentes entre las menos graves. Presentaron convulsiones el 4,1 y el 2,6% de los pacientes tratados con tacrolimus y ciclosporina, respectivamente, cuadros psicóticos el 4,9 y el 4,0%, y somnolencia o confusión y delirio el 12,4 y el 6,6%, respectivamente9.
La toxicidad de estos fármacos parece residir fundamentalmente en el mismo mecanismo por el cual inducen inmunodepresión, que es la inhibición de la calcineurina celular. Se ha demostrado que estos fármacos son tóxicos para las células de la neuroglia y específicamente producen apoptosis de los oligodendrocitos, que son las células más ricas en calcineurina del sistema nervioso central. Esta proteína constituye aproximadamente el 1% de la proteína cerebral total. Además, por este mismo mecanismo pueden modificar la neurotransmisión. Se ha demostrado que la ciclosporina y el tacrolimus pueden modular la actividad de receptores de aminoácidos excitadores, como el ácido N-metil-D aspártico, e inhibitorios, como el ácido gammaaminobutírico (GABA). La calcineurina puede modular también la neutrotransmisión glutamatérgica a través de sitios de acción tanto pre como postsinápticos. Finalmente, estudios con neuronas aisladas de rata han demostrado que los complejos ciclosporina-ciclofilina interfieren con las respuestas mediadas por GABA, lo que indicaría que la calcineurina puede regular la desensibilización de los receptores GABA23.
Además de las acciones ligadas a su efecto principal, es posible la participación de los efectos vasculares (vasoconstricción) de la ciclosporina o del tacrolimus o la participación de vasculitis en las complicaciones del sistema nervioso central producidas por estos fármacos24-26.
Se han identificado una serie de factores que predisponen o agravan la neurotoxicidad de estos fármacos: la disfunción del injerto hepático probablemente por disminución de su metabolización, la coexistencia de hipertensión arterial, de hipocolesterolemia, la coadministración de metilprednisolona a dosis altas o la administración intravenosa tanto de ciclosporina como de tacrolimus, sus concentraciones sanguíneas elevadas o la coadministración de fármacos inhibidores de su metabolismo23. La lesión de la sustancia blanca que producen estos fármacos y que se manifiesta como déficit focales frecuentemente aditivos en horas o días de duración es reversible, aunque en algunos casos pueden quedar secuelas23.
MORTALIDAD
La aparición de complicaciones neurológicas se asocia invariablemente a un aumento de la mortalidad postrasplante.
Pujol et al13, en un estudio prospectivo que incluyó a 84 pacientes, observaron una mortalidad del 17,2% en los pacientes sin complicaciones neurológicas, frente a un 55% en los pacientes que sí las presentaban (p < 0,002). Dichos porcentajes se refieren sólo a complicaciones que afectaron al sistema nervioso central. Otras 2 series muestran hallazgos similares. Lewis y Howdle11, en una serie de 627 pacientes, observaron una mortalidad temprana en el 12% de los pacientes con complicaciones neurológicas, mientras que ésta se reducía al 5% en aquellos que no las había presentando (p < 0,009). Guarino et al12 observaron en 197 pacientes cifras del 46 y del 12,5%, respectivamente.
Estos hechos se repiten cuando se analiza la mortalidad tras retrasplante hepático. En un estudio que evaluó a 149 pacientes sometidos a retrasplante hepático, López et al27 observaron que las alteraciones del nivel de consciencia se habían presentado en el 25% de los supervivientes y en el 45% de los fallecidos (p < 0,05), convulsiones en el 8 y el 19% de estos 2 grupos (p < 0,01) y déficit motores focales en el 3 y el 11%, respectivamente (p < 0,05).
FACTORES DE RIESGO
En el estudio de Pujol et al13 al que antes hemos hecho referencia se identificaron una serie de variables asociadas a la aparición de complicaciones neurológicas intrahospitalarias. En el estudio univariado los pacientes que presentaron complicaciones que afectaron al sistema nervioso central eran, en el período preoperatorio, significativamente diferentes del grupo que no las presentó en los siguientes aspecto: etiología de la enfermedad hepática por la que se indicó el trasplante (ninguna colestásica en los que tuvieron complicaciones), superior consumo de alcohol, mayor prevalencia de encefalopatía hepática, exploración neurológica anormal en el período pretrasplante, mayor alargamiento del tiempo de protrombina y mayor frecuencia de hiperintensidad del globo pálido en el estudio de resonancia magnéticia nuclear. Durante el período intraoperatorio los pacientes con complicaciones presentaron mayor pérdida hemática, mayor necesidad de transfusión plasmática y mayor aumento de sodio en plasma por hora. En el estudio multivariado, a la aparición de complicaciones únicamente se asociaron de forma independiente los siguientes factores: exploración neurológica anormal en el período inmediatamente previo al trasplante, que significó un riesgo relativo del 4,72% (p = 0,007), y la etiología no colestática de la cirrosis (p < 0,01).
En estudio de Lewis y Howdle11 se evaluó el riesgo de complicaciones neurológicas según la etiología de la cirrosis por la cual se indicó el trasplante. Este estudio corrobora sólo parcialmente los resultados del de Pujol et al13 antes citado, dado que el 43% de los pacientes con cirrosis alcohólica presentó complicaciones neurológicas pero, en contra de lo observado en el estudio anterior, los paciente con cirrosis biliar primaria presentaron esta complicación en un 41%. En este mismo estudio se demostró que la incidencia de complicaciones en pacientes tratados con ciclosporina (25%) y tacrolimus (24%) era la misma.
El retrasplante también constituye un factor de riesgo para presentar complicaciones neurológicas. En un estudio sobre 149 pacientes retrasplantados, las alteraciones del nivel del consciencia se presentaron en un 25% de los pacientes en el primer trasplante y en un 54% en el segundo (p < 001), las convulsiones en un 9 y un 22%, respectivamente (p < 0,001), y los déficit motores focales en un 0,7 y un 14% (p < 0,0001)27.
En un estudio reciente28 se han identificado como factores que predisponen a la alteración del nivel de consciencia de causa no identificada, es decir, sin lesiones estructurales en la tomografía axial computarizada o resonancia magnética nuclear, los siguientes: alteraciones metabólicas evidentes e insuficiencia grave de otros órganos, ventilación mecánica antes del trasplante, cirrosis etílica o metabólica, una puntuación de MELD superior a 15 y la realización de un trasplante no electivo.
Además de la mortalidad, el hecho de presentar complicaciones neurológicas aumenta significativamente la duración del ingreso postrasplante, la necesidad de traslado a un centro de apoyo tras el trasplante, la presencia de secuelas significativas o una mala evolución global11.
DIAGNÓSTICO
El diagnóstico de estos pacientes es difícil debido a la existencia de múltiples factores etiológicos con manifestaciones clínicas comunes, la posible coexistencia de varias lesiones y la dificultad de realizar exploraciones complementarias, dado que en general se encuentran ingresados en una unidad de cuidados intensivos.
Son esenciales la historia y la exploración física, el estudio evolutivo de los cambios analíticos o de las complicaciones sistémicas inmediatas, el análisis de laboratorio, con bioquímica completa y concentraciones de inmunodepresores, la gasometría, los cultivos y serologías si así lo requiere la situación y el estudio del líquido cefalorraquídeo. El electroencefalograma es útil en casos de alteración del nivel de consciencia o crisis comiciales. En general, si la causa no es clínicamente evidente, es imprescindible realizar una exploración de imagen (tomografía computarizada o resonancia magnética) incluyendo estudio vascular.
Para las alteraciones del sistema nervioso periférico está indicado el estudio electrofisiológico.
Estos pacientes deben manejarse de modo multidisciplinario.
PREVENCIÓN
A la vista de que la frecuencia de complicaciones neurológicas no ha disminuido de modo significativo a pesar de la mejora global de los resultados del trasplante y de la gran experiencia de los equipos, es evidente que la prevención es difícil. Muchas de estas complicaciones neurológicas ocurren a consecuencia de complicaciones sistémicas. La adecuada selección de los candidatos a trasplante, un estricto control de los pacientes antes del trasplante para minimizar los efectos de la encefalopatía o de las alteraciones metabólicas, la identificación de factores de riesgo, un manejo adecuado del medio interno, el control hemodinámico y el uso adecuado de los fármacos son las bases para evitar estas complicaciones.