La colangiopancreatografía retrógrada endoscópica (CPRE) es la técnica de elección para el tratamiento de la patología biliopancreática. Sin embargo, las imágenes fluoroscópicas no siempre permiten un diagnóstico adecuado. Por otra parte, algunos cálculos de gran tamaño no se pueden extraer con los métodos habituales. En estas situaciones, la colangioscopia ha mostrado ser una herramienta fundamental para el diagnóstico de las estenosis biliares y el tratamiento de los cálculos de gran tamaño. Además, su papel en la patología pancreática está en creciente aumento. El desarrollo de un colangioscopio de un único operador y desechable ha permitido expandir la técnica entre buena parte de los hospitales que realizan CPRE. Por este motivo, la Sociedad Española de Endoscopia Digestiva ha desarrollado este documento de consenso sobre la utilización del colangioscopio Spyglass-DS. El documento ha sido elaborado por un grupo de endoscopistas expertos en colangioscopia, revisando la evidencia científica de las principales indicaciones actuales de la colangiopancreatoscopia.
Endoscopic retrograde cholangiopancreatography (ERCP) is the technique of choice for the treatment of biliopancreatic pathology. However, fluoroscopic imaging does not always allow an adequate diagnosis. On the other hand, some large stones cannot be removed by the usual methods. In these situations, cholangioscopy has proven to be an essential tool for the diagnosis of biliary strictures and the treatment of large stones. Its role in pancreatic pathology is also increasing. The development of a single-operator, disposable cholangioscope has made it possible to expand the technique to a large number of hospitals that perform ERCP. For this reason, the Spanish Society of Digestive Endoscopy has developed this consensus document on the use of the Spyglass-DS cholangioscope. The document has been prepared by a group of endoscopists with expertise in cholangioscopy, reviewing the scientific evidence on the main current indications for cholangiopancreatoscopy.
La colangiopancreatografía retrógrada endoscópica (CPRE) es una herramienta imprescindible para el tratamiento de las enfermedades biliopancreáticas. Sin embargo, una de sus principales limitaciones es la definición subóptima de las imágenes fluoroscópicas en el diagnóstico de la patología del conducto biliopancreático.
La colangiopancreatoscopia no solamente permite la evaluación macroscópica directa del interior de la vía biliar y del páncreas, sino que también nos permite obtener biopsias dirigidas de las lesiones o realizar un tratamiento dirigido como la litotricia en los cálculos difíciles.
Con la introducción del sistema de colangiopancreatoscopia de un solo uso SpyGlass (Boston Scientific, Natick, MA, EE.UU.) en 2007, la técnica ha adquirido interés entre los profesionales que realizan CPRE, consiguiendo una notable difusión debido a que, con un único explorador, nos permite acceder de forma sencilla a la vía biliopancreática, es un dispositivo desechable, con buena maniobrabilidad, con canal accesorio independiente para irrigación y debido a su calibre permite la exploración de la vía biliar aun si no está dilatada. Otros sistemas de colangioscopia, como son los colangioscopios madre-hijo, han tenido menor aceptación, por su fragilidad y el coste de las reparaciones y por el hecho de precisar de 2 operadores para realizar la exploración. Así pues, estos sistemas solo están disponibles en unos pocos centros de referencia a nivel mundial. Por último, la colangioscopia a través de la boca mediante el uso de endoscopios ultrafinos, aunque presenta una mejor calidad de imagen, tiene una maniobrabilidad limitada, especialmente en vías biliares intrahepáticas y de calibre fino.
La segunda generación de SpyGlass, el SpyGlass DS (SG-DS), tiene un incremento en la calidad de imagen significativo, además de que mejora considerablemente la maniobrabilidad y facilidad de uso con respecto al Spyglass óptico. Este sistema incorporaba una fibra óptica reutilizable, con una calidad de imagen deficiente. El sistema actual DS incorpora un chip digital que mejora la imagen y facilita su uso, al ser todo el sistema desechable. La nueva versión DS-II mejora aún más la imagen, la profundidad de campo y la iluminación dentro de la vía biliar, evitando la aparición de reflejos y áreas de sombras.
El presente documento de consenso hace referencia a la utilización del SpyGlass DS (Boston Scientific corp.), el único aprobado en España para la colangioscopia actualmente, siendo este el sistema de colangioscopia más utilizado a nivel mundial.
Este artículo complementa al artículo de Dolz Abadía et al.1, publicado previamente por este mismo equipo.
Nuestro objetivo es definir las indicaciones, determinar las posibilidades y determinar las cuestiones que plantea al endoscopista la aplicación de esta tecnología.
MétodoEl equipo de trabajo se ha formado por 13 endoscopistas de todo el territorio nacional que desarrollan 30 o más procedimientos con SG-DS en su centro de trabajo al año.
Dividimos la temática en 7 bloques que se corresponden con las principales indicaciones de SG-DS:
- -
Estenosis biliar indeterminada.
- -
Tratamiento del cálculo difícil.
- -
Avance de guía a través de estenosis difíciles.
- -
Diagnóstico de la neoplasia mucinosa papilar intraductal de páncreas.
- -
Evaluación de dilatación/estenosis del conducto pancreático.
- -
Litiasis intraductal pancreática.
- -
Otras indicaciones.
Las recomendaciones finales se han establecido aplicando el método Delphi, incluyendo en el documento las recomendaciones que alcanzaron el grado de acuerdo (GA) necesario. Las recomendaciones que no alcanzaron el GA adecuado fueron reformuladas y sometidas a una nueva evaluación (aparecen indicadas con *). En caso de no llegar a alcanzar este acuerdo, fueron desestimadas.
En las recomendaciones elaboradas por el grupo de expertos se presenta el nivel de evidencia (NE), el grado de recomendación (GR), según el Center for Evidence Based Medicine de Oxford2, y el GA entre los expertos.
Recomendaciones y propuestasBloque 1: Estenosis biliar indeterminada (EBI)1. ¿Cuál es el papel de SG-DS en la evaluación de la EBI?Se recomienda la utilización de colangioscopia mediante SG-DS en la evaluación de la estenosis biliar indeterminada (EBI) tras citología y/o biopsia no concluyente.
(NE Fuerte, GR D, GA 91%)
Comentario: En las EBI, la citología por cepillado tiene una sensibilidad muy baja (45%), al igual que la biopsia intraductal a ciegas (48,1%)3. Cuando estos pacientes son intervenidos en base a la sospecha de neoplasia, un 15-24% tienen patología benigna4.
2. ¿Cuál es el éxito técnico esperable en la evaluación con SG-DS de una EBI?El éxito técnico es superior al 98%, siendo este dependiente del éxito técnico de la CPRE. Esta tasa de éxito técnico puede ser menor en aquellos casos en los que la EBI sea distal o afectar a conductos intrahepáticos.
(NE Fuerte, GR D, GA 100%)
Comentario: El sistema SG-DS tiene un elevado éxito técnico en este contexto, los escasos fallos técnicos se relacionan sobre todo con lesiones de localización muy distal, en los que es difícil la exploración con SG-DS.
3. ¿En qué momento del proceso diagnóstico se debe utilizar SG-DS?Se recomienda la utilización de SG-DS en los casos de EBI en las que la información que aporte la inspección visual, con o sin anatomía patológica, comporte un cambio en el manejo del paciente.
(NE Fuerte, GR D, GA 91%)
4. ¿Es suficiente el diagnóstico visual mediante SG-DS en la EBI?El rendimiento diagnóstico de la valoración visual en la caracterización de las estenosis indeterminadas es elevado. La presencia de vasos dilatados y tortuosos es altamente sugestiva para el diagnóstico de malignidad. A pesar de la elevada eficacia de la evaluación visual, la toma de biopsias es obligada, cuando es técnicamente factible, por su elevado valor predictivo positivo (VPP).
(NE Fuerte, GR D, GA 100%)*
Comentario: SG-DS tiene una sensibilidad para el diagnóstico visual del 95,5-96,6%, con una especificidad del 93,3-94,5% y un valor predictivo negativo (VPN) del 96,3-97,7%. Sin embargo, la sensibilidad del diagnóstico histológico es menor (57,7-86,2%)3,5.
5. ¿Cuál es la rentabilidad diagnóstica de la biopsia guiada por SG-DS en la EBI?Actualmente el rendimiento diagnóstico de la biopsia guiada por SG-DS es menor que la valoración visual por su limitada sensibilidad. Se recomienda un mínimo de 4 biopsias para aumentar el rendimiento.
(NE Fuerte, GR D, GA 100%)*
6. ¿Cuáles son los criterios por imagen de malignidad?El criterio predictivo de malignidad más potente es la presencia de vasos dilatados y tortuosos, con un VPP que llega a ser del 100% en algunos estudios.
(NE Fuerte, GR D, GA 100%)
Comentario: Actualmente se sabe que la presencia de vasos anómalos o arañas vasculares en la estenosis, junto con proyecciones papilares vellosas, es un criterio suficiente para definir la existencia de malignidad, con una especificidad y VPP del 100%. La presencia de vasos anómalos muestra una sensibilidad del 94% y una especificidad del 63%, VPP del 75% y VPN del 90% para el diagnóstico de estenosis maligna6.
Para el diagnóstico de las estenosis biliares se han propuesto la clasificación de Robles-Medranda et al.7 y posteriormente se han definido los criterios Mendoza8. La precisión diagnóstica de esta clasificación es del 77% (64-88%).
7. ¿Cuál es la utilidad del SG-DS en el diagnóstico de extensión endoluminal del colangiocarcinoma extrahepático?Se sugiere la utilización de colangioscopia mediante SG-DS en el estudio de extensión del colangiocarcinoma extrahepático en aquellos pacientes candidatos a cirugía, en los que el estudio mediante métodos de imagen no permita definir la extensión endoluminal de la lesión.
(NE Fuerte, GR D, GA 100%)*
Comentario: En los casos que la información comporte un impacto en el manejo clínico del paciente. Nota: en estenosis del tramo intrapancreático distal, el estudio por SG-DS puede estar comprometido debido al grado de estenosis y proximidad con la papila.
8. ¿Cuál es el papel del SG-DS en la evaluación de los pacientes con colangitis esclerosante primaria (CEP)?Se recomienda la utilización del SG-DS como método de elección para el diagnóstico de colangiocarcinoma en pacientes con CEP, siempre y cuando el hallazgo en métodos de imagen (TC/RNM) no sea concluyente.
(NE Fuerte, GR D, GA 82%)
Spyglass es eficaz y seguro en el manejo endoscópico de los pacientes con CEP. En un estudio reciente, detectó la presencia de colangiocarcinoma en el 18% de los pacientes con estenosis dominante9.
9. ¿Cuál es la utilidad del SG-DS en la evaluación del tratamiento con radiofrecuencia de las lesiones biliares?No hay datos para recomendar la utilización de SG-DS en la evaluación del tratamiento con radiofrecuencia de las lesiones biliares.
(NE Bajo, GR D, GA 91%)
10. ¿Tiene alguna utilidad el SG-DS en el estudio de extensión intraductal de las lesiones ampulares?No hay datos para recomendar la utilización de SG-DS en la evaluación de la extensión intraductal de las lesiones ampulares.
(NE Bajo, GR D, GA 91%)
11. ¿Cuál es el papel en la evaluación de otros hallazgos de la colangiografía, como defectos de llenado de contraste radiológico de naturaleza incierta?Se sugiere la utilización de la colangioscopia con SG-DS como un método eficaz para evaluar defectos de llenado de naturaleza incierta en la colangiografía.
(NE Fuerte, GR D, GA 100%)*
Bloque 2: Tratamiento del cálculo difícil (CD)Las características clásicas que definen un cálculo difícil (CD) son: tamaño mayor de 15mm, más de 3 cálculos simultáneos mayores de 10mm, desproporción entre el tamaño del cálculo y el colédoco distal, morfología facetada y localización supraestenótica, en el conducto cístico o intrahepática10 (tabla 1). También podríamos hablar de CD cuando no se consigue la extracción tras la aplicación de las técnicas convencionales (esfinterotomía, esfinteroplastia, cesta de extracción y/o litotriptor mecánico)11.
Cálculos difíciles en los conductos biliares
| Categoría | Condiciones | Razones |
|---|---|---|
| Características de la litiasis | Litiasis grande (>15mm) | Necesidad de litotricia y dificultad para capturar el cálculo con una canasta |
| Múltiples litiasiss (>3 litiasis, talla>10mm) | ||
| Litiasis dura | ||
| Litiasis con forma extraña | ||
| Localización de la litiasis | Cálculo del conducto intrahepático | Difícil acceso |
| Litiasis por encima de una estenosis | ||
| Cálculo impactado en el conducto biliar/conducto cístico | ||
| Síndome Mirizzi | ||
| Situación anatómica | Anatomía alterada | Dificultad en el acceso biliar y limitación del endoscopio/accesorio |
| Anatomía de bypass gástrico de Billroth II/Roux-en-Y | ||
| Divertículo periampular | ||
| Factores del paciente | Vejez/mal estado general | Riesgo de acontecimientos adversos |
| Signos vitales inestables | ||
| Tendencia a sangrar | ||
| Respuesta paradójica |
Fuente: Oh y Dong10.
a) Se recomienda el uso de litotricia asistida mediante colangioscopia con SG-DS como un tratamiento eficaz y seguro en el tratamiento de los CD.
(NE Moderado, GR D, GA 100%)
Comentario: Entre el 10-15% de los cálculos biliares12,13 no pueden extraerse por los medios habituales y es preciso recurrir a técnicas especiales como la litotricia mecánica (LM), la dilatación con balón de gran diámetro (DBGD) o la colocación de stents, con reintento de extracción de las litiasis en posteriores CPRE.
Una revisión sistemática sugiere que la litotricia con láser (LL) es más efectiva en cuanto al aclaramiento y fragmentación de los cálculos que la litotricia externa con ondas de choque (LEX) y también se asocia a menor número de efectos adversos14.
Varios estudios comparan litotricia con SG-DS con la LM y/o DBGD14–16. De estos estudios se desprende que, tanto la litotricia electrohidráulica (LEH) como la LL mediante SG-DS, son un tratamiento eficaz para el manejo del CD, si bien parece recomendable reservar su utilización tras el fracaso de métodos convencionales. No obstante, cálculos de gran tamaño (>15mm), impactados, localizados en cístico, proximales a estenosis o con colédoco en embudo, donde la esfinteroplastia puede tener complicaciones significativas17, la litotricia mediante SG-DS puede ser el tratamiento inicial de elección. En estos casos, la colocación de una prótesis biliar para descomprimir la vía biliar puede ser una opción si se realiza la colangioscopia de forma diferida18.
b) ¿Es factible la realización de SG-DS transluminal para el tratamiento de CD?
La litotricia de CD con SG-DS es factible mediante la creación previa de un acceso transluminal guiado por USE, siempre que el acceso transpapilar no sea posible.
(NE Fuerte, GR D, GA 100%)*
Comentario: La aplicación de litotricia con SG-DS a través de un acceso biliar guiado por USE se ha descrito en el caso de CD que no puedan pasar a través de la papila dilatada. Solo se ha publicado un estudio piloto de litotricia con SG-DS a través de acceso transluminal endosonográfico que demuestra que es factible realizar litotricia de CD en 8 casos19.
c) ¿Tiene alguna ventaja la litotricia con SG-DS con respecto a otras técnicas de colangioscopia?
La litotricia con SG-DS se utiliza con mayor facilidad que la colangioscopia directa con endoscopios ultrafinos y que la colangioscopia clásica «madre-hijo».
(NE Bajo, GR D, GA 91%)
Comentario: El acceso a la vía biliar para litotricia en CD15,16 mediante colangioscopia se ha realizado con tres métodos diferentes: de forma directa a través de endoscopio ultrafino, con el sistema «madre-hijo» (colangioscopio ultrafino que pasa a través de un duodenoscopio de canal ancho) y, más recientemente, con el sistema SG-DS. La diferencia entre los tres sistemas puede verse en la tabla 2.
Tres tipos de sistema de colangioscopia
| «Madre-hijo» colangioscopia de doble operador | Operador simple de colangioscopia (SpyGlass DS System) | Colangioscopia peroral directa (endoscopio ultradelgado) | |
|---|---|---|---|
| Endoscopista | 2 | 1 | 1 |
| Sistema de endoscopio adicional | Sí | Sí | No |
| Diámetro del alcance, mm | 3,3-3,5 | 3,6 | 5-6 |
| Canal de accesorios, mm | 1,2 | 1,2 | 2 |
| Canal de riego | No | Sí | No |
| Costo | Alto | Alto | Bajo |
| Calidad de la imagen | Alto | Intermedia | Alto |
Fuente: Oh y Dong10.
La posición actual de la litotricia con SG-DS en el algoritmo de tratamiento del CD se situaría en los casos en que las técnicas convencionales han fallado. El grupo de expertos recomienda la incorporación de LL/LEH con SG-DS de forma precoz en el manejo del CD.
(NE Bajo, GR D, GA 82%)
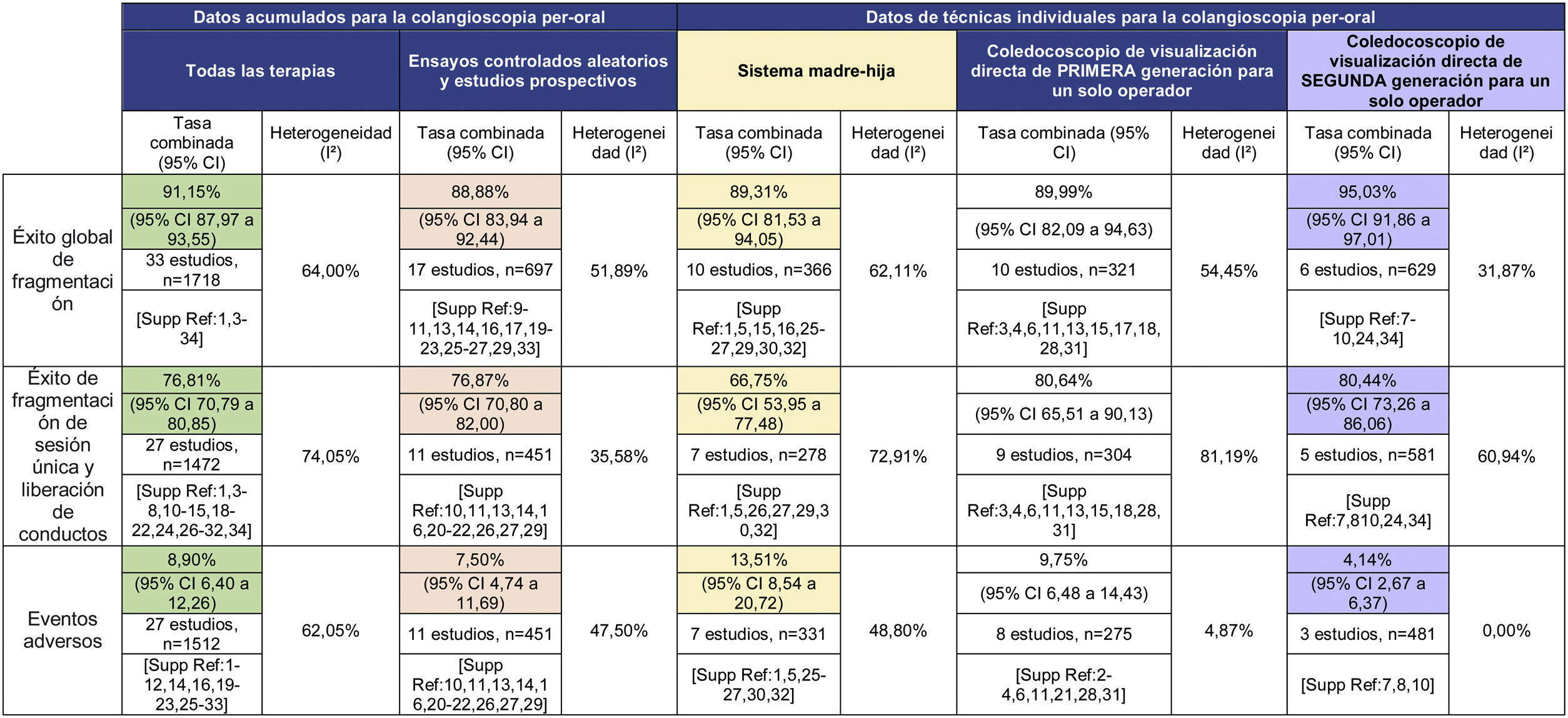
Comentario: La indicación de litotricia con SG-DS para el manejo del CD puede inferirse de los diferentes estudios que se resumen en el reciente metaanálisis16 (tabla 3).
En los últimos años la DBGD ha sustituido a la LM con reducciones significativas en la tasa total de efectos adversos22–27. La seguridad de estas técnicas se relaciona con el tamaño del cálculo y con la anatomía de la vía biliar28.
La LEX en el CD reporta una capacidad de aclaramiento de la vía biliar del 78-90%27,28, mientras que con la litotricia (LEH/LL) por colangioscopia lo consigue en el 75-100%16. En ambos casos, con frecuencia se requiere más de una sesión para conseguir un aclaramiento completo de la vía biliar29,30.
En pacientes con CD, en los que las técnicas clásicas de LM y DBGD tienen una tasa de aclaramiento menor y un mayor número de complicaciones, la litotricia (LEH/LL) a través de SG-DS podría sustituir como indicación de primera elección31.
3. ¿Cuál es la utilidad del SG-DS en la detección de cálculos residuales?SG-DS es capaz de detectar cálculos residuales en un 34%, la mayoría inferiores a 7mm, más frecuentemente cuando se ha hecho litotricia previamente32,33.
(NE Bajo, GR D, GA 91%)
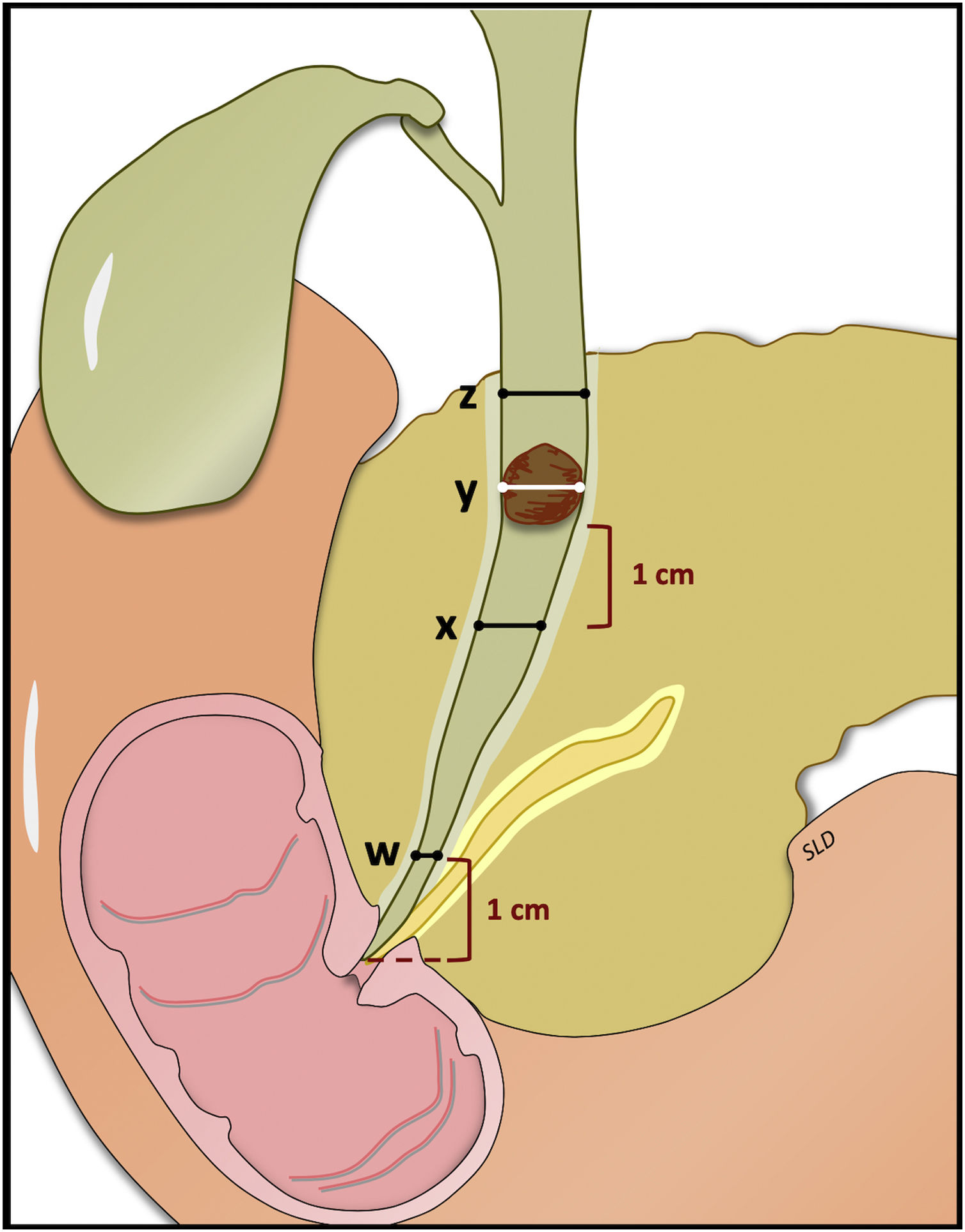
4. ¿Cuál es el esquema de tratamiento recomendado para el manejo del CD?Se recomienda ver la figura 1 y el algoritmo que se muestra en la figura 2.
Imagen cortesía del Dr. López Durán.
z=diámetro más ancho del conducto biliar extrahepático; y=diámetro transversal del cálculo; x=diámetro del conducto biliar extrahepático 1cm bajo el cálculo; w=diámetro del colédoco 1cm sobre orificio papilar. Colédoco en embudo: w<z. Litiasis impactada: y>x.
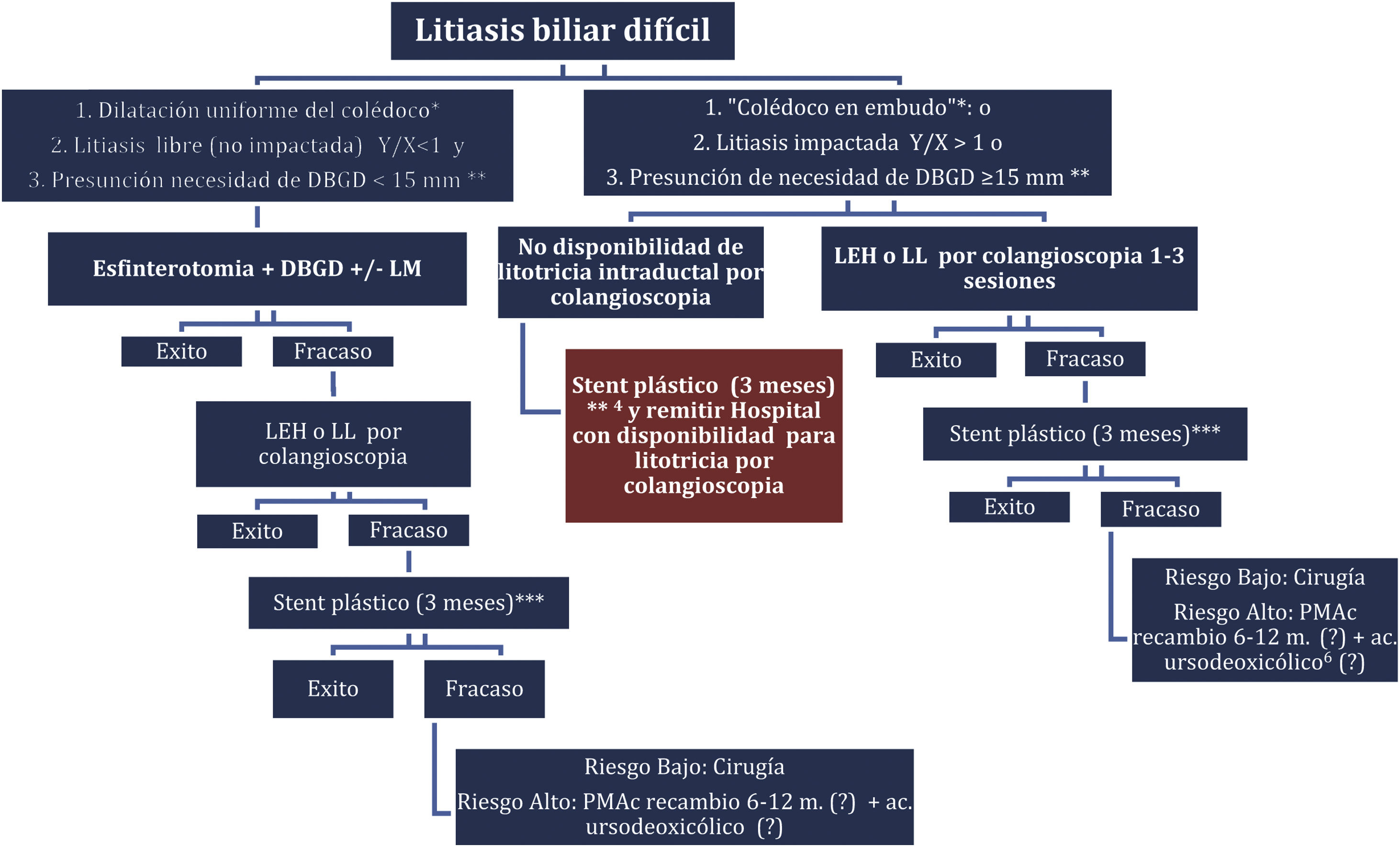
Algoritmo.
DBGD: dilatación con balón de gran diámetro; LEH: litotricia electrohidráulica; LL: litotricia con láser; LM: litotricia mecánica; PMAc: prótesis metálica autoexpandible cubierta.
* Dilatación uniforme del colédoco: relación diámetro colédoco (1cm sobre papila) (w)/diámetro colédoco proximal más ancho (z) 1≥0,5; «Colédoco en embudo»: Relación colédoco (1cm sobre papila) (w)/diámetro colédoco proximal más ancho (z) 1<0,5. ** La extracción será posible con balón (DBGD)<15mm. *** Se recomienda dos stents doble pigtail de 7 F en paralelo.
Dependiendo de a) las características anatómicas del colédoco, b) la presencia de litiasis biliar libre o impactada y c) la presunción del diámetro del balón de dilatación a emplear, se recomienda DBGD o la realización de litotricia con SG-DS en la primera sesión. En caso de no obtener el aclaramiento del colédoco con la DBGD, se recomienda realizar litotricia con SG-DS. Si no se consigue el aclaramiento de la litiasis o bien no se dispone de SG-DS, se aconseja la inserción de stent de plástico durante 3 meses34 y nuevo intento de litotricia, o bien cirugía en casos de riesgo bajo. Cuando fracasan todas las opciones en pacientes de riesgo alto se aconseja prótesis metálica autoexpandible cubierta (PMAc) con recambios cada 6-12 meses y la posibilidad de añadir tratamiento continuado con ácido ursodesoxicólico.
5. ¿Cuál es el método de litotricia recomendado?a) La litotricia intraductal mediante cualquiera de las dos técnicas disponibles (LL y LEH) es un tratamiento muy eficaz para el manejo de las litiasis complejas.
(NE Fuerte, GR D, GA 100%)
Comentario: Aunque la mayor parte de los estudios no muestran una superioridad clara entre la LL y LEH35, en una revisión sistemática, la LL consigue un mayor aclaramiento de las litiasis que la LEH y LM (95,1%, 88,4% y 84,5%, respectivamente; p<0,001)12.
Probablemente, las sondas láser deben seleccionarse solo en casos de cálculos muy grandes, múltiples o duros, para superar la limitación de la vida útil de la sonda LEH36.
b) La LL y LEH han demostrado ser eficaces en la extracción de CD en primera elección y como técnica de rescate de otros métodos (LM y que la combinación de DBGD/LM)14,37.
(NE Fuerte, GR D, GA 100%)*
Comentario: Para la LM, cuando la litiasis es>25mm, está impactada o localizada en la confluencia de los hepáticos principales, la tasa de éxito no supera el 68%38.
c) Actualmente no existe suficiente evidencia científica para determinar cuál es el mejor método de litotricia intraductal, siendo necesaria la realización de estudios especialmente diseñados para comparar la LL con la LEH.
(NE Bajo, GR D, GA 100%)
6. ¿Cuál es el impacto económico del uso de SG-DS en el manejo del paciente con CD?La litotricia intraductal con SG-DS puede ser coste-efectiva empleada precozmente39 y cuando se prevé que otros métodos pueden fracasar, evitando la repetición de nuevas sesiones de CPRE y rescate quirúrgico.
(NE Fuerte, GR D, GA 100%)*
Comentario: La litotricia intraductal supondría una reducción del 27% en el número de procedimientos y en último término, una reducción del coste económico del 11%39.
El único estudio en el que se incluye un estudio de costes no encontró diferencias económicas significativas entre el método de DBGD y la LL intraductal, aunque presentó mayor tasa de limpieza de la vía biliar (72,7% vs. 93,9%; p=0,021)40.
Bloque 3: Avance selectivo de guía a través de estenosis difíciles1. ¿Cuál es la utilidad del SG-DS en el avance de guía a través de estenosis biliares difíciles?Se sugiere el uso de SG-DS como método para el paso de guías a través de estenosis biliares difíciles, canulación selectiva de un conducto hepático o del cístico, cuando fracasan los métodos convencionales.
(NE Bajo, GR D, GA 91%)
SG-DS facilita la progresión de la guía en las estenosis biliares del paciente trasplantado hepático cuando fracasan los métodos convencionales.
(NE Bajo, GR D, GA 82%)
Comentario: Un estudio41, bajo visión directa con SG-DS, consigue el paso de la guía a través de la estenosis en el 70% de los casos: en el 88,2% de estenosis benignas y en el 46,2% de estenosis malignas, p=0,02. En otro estudio con pacientes trasplantados, los autores consiguen el paso de la guía mediante SG-DS en los todos los casos, con un ahorro estimado en este tipo de pacientes de entre 6.240 y 66.540$42. El resto de estudios43–47, en pacientes con trasplante, en general muestran que la eficacia parece mayor en estenosis benignas.
La canulación del cístico con SG-DS resulta útil en pacientes con colecistitis aguda para drenaje transcístico48.
Bloque 4: Diagnóstico de la neoplasia mucinosa papilar intraductal (NMPI) del páncreas1. ¿Cuál es el papel del SG-DS en el diagnóstico de las NMPI de conducto principal?La realización de pancreatoscopia con SG-DS es de utilidad en el diagnóstico de NMPI de conducto pancreático principal en pacientes con dilatación del conducto en los que el diagnóstico no haya podido ser confirmado mediante métodos de imagen habituales (TAC, RNM, USE).
(NE Moderado, GR D, GA 91%)
Comentario: Dos estudios49,50 muestran que el éxito técnico es superior al 90%, pero la sensibilidad para el diagnóstico de NMPI es muy dispar. La especificidad es del 100% para el diagnóstico de malignidad. La pancreatoscopia conlleva un cambio en la decisión terapéutica en 3 de cada 4 casos49.
2. ¿Qué papel tiene el SG-DS en el diagnóstico de extensión preoperatorio de los NMPI de conducto principal?La realización de pancreatoscopia preoperatoria puede ser de ayuda para definir la extensión del NMPI y la presencia de lesiones sincrónicas en el conducto pancreático.
(NE Bajo, GR D, GA 91%)
Comentario: La sensibilidad de SG-DS para definir el margen de resección es del 85,7%51, pero la eficacia de la toma de biopsias proximales y distales a la lesión (mapeo) para la evaluación histológica de la extensión del NMPI no ha sido investigada.
3. ¿Qué hallazgos son indicativos de malignidad?La presencia de vasos en las estructuras papilares del NMPI, así como la presencia de nódulo, estenosis infiltrativa y de márgenes irregulares se asocian a carcinoma in situ o invasivo.
(NE Bajo, GR D, GA 91%)
Comentario: La presencia de vasos se asocia a carcinoma in situ o invasivo en el 89% de los casos, mientras que el tipo velloso o vegetativo lo hacen en el 91-92% de los casos52.
4. ¿Tiene alguna utilidad en la evaluación de los pacientes con NMPI de rama secundaria?La pancreatoscopia con SG-DS tiene utilidad en pacientes con NMPI de rama lateral cuando se sospecha afectación de conducto principal (NMPI mixto) para confirmar o excluir la afectación del mismo, con el fin de establecer el mejor abordaje terapéutico.
(NE Fuerte, GR D, GA 100%)*
Comentario: La utilidad de la pancreatoscopia con SG-DS en pacientes con NMPI de rama secundaria49 muestra una sensibilidad del 78%.
Bloque 5: Evaluación de dilatación/estenosis del conducto pancreático1. ¿Cuál es el papel del SG-DS en la evaluación de pacientes con dilatación del conducto pancreático?Se sugiere la utilización de pancreatoscopia mediante SG-DS en la evaluación de los pacientes con dilatación significativa del conducto pancreático de causa no diagnosticada por las técnicas de imagen habituales.
(NE Fuerte, GR D, GA 100%)*
2. ¿Qué papel tiene en la evaluación de estenosis indeterminadas del conducto pancreático?Es factible la utilización de pancreatoscopia mediante SG-DS y toma de biopsias en la evaluación de estenosis o anomalías indeterminadas del conducto pancreático en ausencia de diagnóstico por otras técnicas de imagen, siempre que el diámetro del conducto pancreático distal a la lesión permita el paso de SG-DS. Pero no se debe obviar el riesgo de pancreatitis aguda postexploración, por lo que es preciso tenerlo muy presente en el balance del riesgo/beneficio.
(NE Fuerte, GR D, GA 100%)*
Bloque 6: Litiasis intraductal pancreática1. ¿Cuál es la indicación de realizar litotricia mediante SG-DS en pacientes con pancreatitis crónica y litiasis intraductal?La indicación sería la presencia de litiasis intraductal que no puede extraerse mediante técnica convencional (preferentemente balón), generalmente litiasis mayores de 5mm.
(NE Bajo, GR D, GA 100%)
Comentario: La localización no es una limitación, si bien es preferible por su menor dificultad si se sitúa en cabeza o cuerpo distal. Los cálculos próximos a papila pueden presentar mayor dificultad para la realización de litotricia mediante SG-DS.
2. ¿Qué método de litotricia es mejor para la litotricia intraductal pancreática?a) Se sugiere que la LL o LEH aplicada a través de pancreatoscopia con SG-DS es factible, con efectos probablemente superiores a la extracción estándar con balón y comparable a la LEX.
(NE Bajo, GR D, GA 100%)
b) No se observan diferencias entre el uso de LL o LEH53.
(NE Bajo, GR D, GA 91%)
3. ¿Cuál es el papel de la litotricia mediante SG-DS vs. litotricia extracorpórea en el tratamiento de la pancreatitis crónica?Se sugiere que la LL o LEH a través de pancreatoscopia con SG-DS puede sustituir en centros en los que la LEX no está disponible o no es fácilmente accesible, con un nivel de eficacia y perfil de seguridad similar.
(NE Bajo, GR D, GA 100%)
Comentario: En dos recientes metaanálisis53,54, observamos una eficacia y seguridad similar entre la LEX y la litotricia intraductal mediante pancreatoscopia, por ello y mientras no exista una evidencia mayor, ambas técnicas pueden recomendarse por igual y su utilización estará más en función de la disponibilidad y experiencia con cada una de ellas.
Bloque 7: Otras indicaciones para SG-DS1. ¿Tiene alguna utilidad el SG-DS en la evaluación del paciente con hemobilia?No se recomienda el uso de SG-DS en la evaluación de pacientes con hemobilia, especialmente en los casos de hemobilia significativa donde puede retrasar el tratamiento55.
(NE Bajo, GR D, GA 100%)
2. ¿Qué papel tiene el SG-DS en el manejo de los cuerpos extraños alojados en la vía biliar y pancreática?Se sugiere que el SG-DS puede ser de utilidad en la extracción de cuerpos extraños biliares cuando fracasan los métodos convencionales.
(NE Bajo, GR D, GA 91%)
Comentario: Únicamente existen casos clínicos publicados en los que se describe la utilidad de SG-DS en la extracción de cuerpos extraños alojados en la vía biliar56–61. La mayoría de los casos utilizan la pinza de biopsia (Spybite) para la extracción. Recientemente se ha comercializado un asa (Spysnare) y una cesta (Spybasket) que pueden ser de mayor utilidad para la extracción de cuerpos extraños.
3. ¿Puede sustituir el SG-DS a la fluoroscopia para la realización de CPRE en algunas situaciones?Se sugiere el uso de SG-DS como método alternativo a la fluoroscopia en aquellas situaciones en las que no se puede utilizar o está contraindicada para el tratamiento de los cálculos biliares no complicados.
(NE Moderado, GR D, GA 91%)
Comentario: Confirman la posibilidad de realizar fragmentación de coledocolitiasis no complicada y limpieza de la vía biliar sin necesidad de utilizar fluoroscopia o reduciendo mucho el uso de esta62–64.
FinanciaciónPara la discusión del Documento de consenso, Boston Scientific España ha financiado las reuniones físicas y ha facilitado las reuniones on-line de los autores firmantes.
Conflicto de interesesJR Aparicio Tormo Ramón es consultor de Boston Scientific. J Vila Costas es consultor de Boston Scientific y ha participado como ponente en cursos y actividades docentes patrocinados por Cook Endoscopy, Pentax, Olympus, Cassen y Norgine. J Gornals Soler es consultor de Boston Scientific. E Domínguez-Muñoz ha recibido honorarios como conferenciante y reuniones de asesoría para Boston Scientific. F González Huix ha sido conferenciante o participante en Advisory Boards para Olympus, Ambu e Izasa hasta 2021 y se mantiene en la actualidad como Advisory Boards para Boston Scientific. V Pons Beltrán es consultor de Boston Scientific. El resto de autores declara no tener conflicto de intereses.