La hemorragia digestiva baja (HDB) masiva es una complicación infrecuente en la enfermedad inflamatoria intestinal que aparece en menos del 5% de los pacientes con enfermedad de Crohn (EC)1–3. La HDB masiva es aquella que se produce en el intestino distal al ángulo de Treitz, se acompaña de inestabilidad hemodinámica y requiere transfusión de al menos 2 concentrados de hematíes en 24 h4. Para el diagnóstico urgente de esta patología se utiliza la angiotomografía computarizada (angio-TC), que permite detectar el punto de sangrado activo, localizando el área de extravasación de contraste.
Clásicamente, el tratamiento de la HDB masiva en la EC ha sido quirúrgico5. Existen estudios en los que, en un primer episodio de sangrado en EC, hasta a un 60-90% de los pacientes se les realizaron cirugías resectivas amplias y colectomías subtotales1, con una importante morbimortalidad perioperatoria y con la posibilidad de producir un síndrome de intestino corto a aquellos pacientes que hayan requerido múltiples cirugías resectivas a lo largo de su vida. Las técnicas endovasculares, en especial la embolización supraselectiva, se han empleado ampliamente en el tratamiento de la HDB secundaria a enfermedad diverticular y angiodisplasia; sin embargo, en el contexto de la EC han sido raramente descritas5.
A continuación se presentan 2 casos clínicos de pacientes que empezaron con un cuadro diarreico y HDB masiva, siendo tratados mediante embolización supraselectiva de la arteria responsable, con buen control del sangrado.
Caso 1Varón de 74 años, hábito tabáquico activo y antecedentes médicos de diabetes mellitus tipo 2, enfermedad coronaria en tratamiento activo con antiagregantes plaquetarios y episodio en 1990 de fístulas perianales que requirieron tratamiento quirúrgico, tras el cual el paciente presentó incontinencia fecal, por lo que recibió nueva cirugía en la que se realizó colostomía permanente (Hartmann).
Acudió al servicio de urgencias de nuestro hospital por cuadro de 3 días de evolución de hematoquecia que se había precedido un mes antes de aumento en el volumen y en el número de deposiciones y disminución de consistencia de las mismas, que le obligaba a cambiarse la bolsa de colostomía con mayor frecuencia de lo habitual. El cuadro se acompañaba de pérdida de 5 kg de peso en 2 meses, astenia intensa e hiporexia. La exploración física fue normal a excepción de leve palidez mucocutánea y heces hematoquécicas en la bolsa de colostomía. En la analítica destacaba anemia de 10,9g/dl −previa de 16g/dl−, trombocitosis, leucocitosis con neutrofilia y proteína c reactiva (PCR) de 23mg/dl.
Durante su ingreso se completó el estudio mediante muestras de heces (cultivos, detección parásitos y toxina de Clostridium difficile negativos), ecografía abdominal (esteatosis hepática grado ii, colelitiasis y vesícula escleroatrófica) y colonoscopia (colitis infecciosa vs EC con afectación parcheada desde el orificio de colostomía hasta colon ascendente proximal) (fig. 1A). La anatomía patológica fue compatible con EC, con lo que se inició tratamiento intravenoso con metilprednisolona (0,8mg/kg/día).
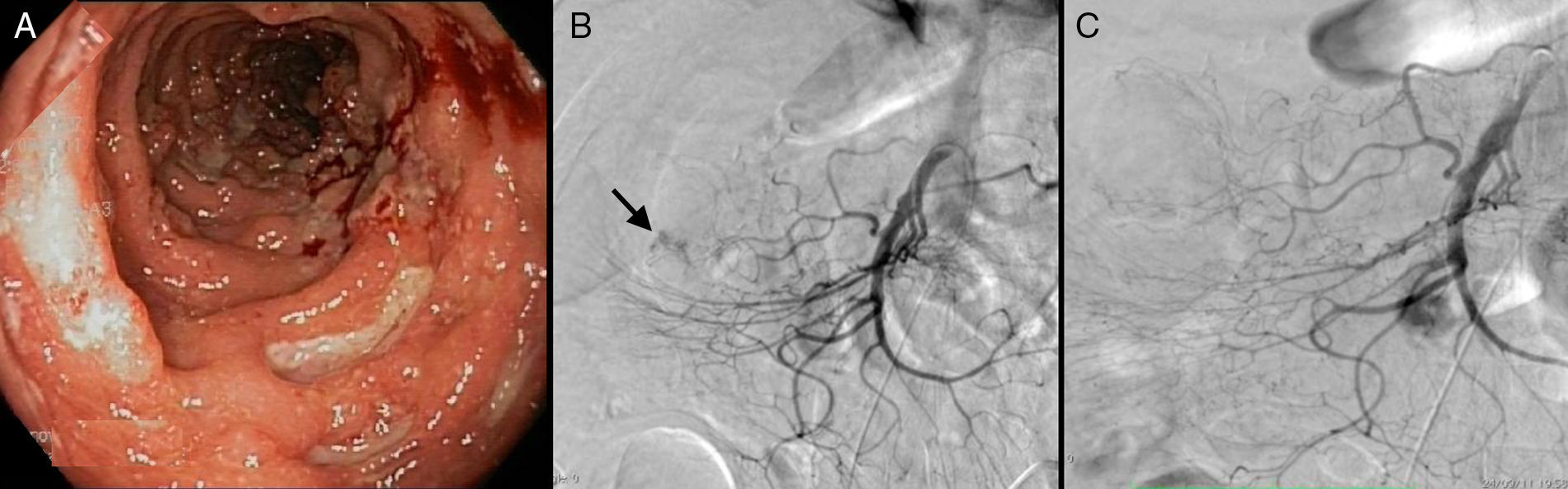
A) Imagen del colon ascendente en la que se aprecia la mucosa inflamada con seudopólipos y úlceras geográficas irregulares y profundas cubiertas de fibrina. En B) se localiza el área de extravasación de contraste (flecha), mediante arteriografía selectiva de la rama cólica media dependiente de la arteria mesentérica superior. Se ilustra el procedimiento de embolización, comprobándose la ausencia de sangrado activo en dicha zona en la imagen de control postembolización (C).
Una semana después presentó HDB masiva con inestabilidad hemodinámica y necesidad de transfusión de 3 concentrados de hematíes debido a anemización de 3g/dl en menos de 24 h. Se realizó angio-TC y arteriografía detectando el sangrado activo a nivel del ángulo hepático del colon, correspondiente a la arteria cólica media y controlándose el mismo mediante embolización selectiva con partículas de alcohol polivinílico (PVA) de entre 300 y 500 μ y con esponja de gelatina reabsorbible (Espongostan®) (fig. 1B y C). Al paciente le fue dada el alta, añadiéndose tratamiento para la EC con mesalazina y azatioprina, además de pauta descendente corticoidea, sin presentar recurrencia del sangrado en el seguimiento a los 3 meses. Posteriormente, el paciente presentó perforaciones por úlceras gástricas, y finalmente falleció por complicaciones sépticas derivadas de la cirugía.
Caso 2Mujer de 52 años, con antecedente de aneurisma cerebral gigante que 2 meses antes había sido tratado mediante la colocación de un stent endovascular y que, por su enfermedad vascular, mantenía tratamiento con antiagregantes plaquetarios, pantoprazol, naproxeno y dexametasona (16mg/día, en pauta descendente). Reingresó posteriormente para monitorización en la unidad de cuidados intensivos por cefalea frontooccipital izquierda resistente a analgesia, sin focalidad neurológica y sin nuevos hallazgos patológicos en los estudios que se realizaron durante el ingreso. Durante este episodio había presentado además anemia normocítica normocrómica (9,7g/dl) considerada de origen multifactorial y diarrea líquida (sin productos patológicos), acompañada de dolor abdominal, leucocitosis y evidenciándose en la TC abdominal una leve inflamación de recto y sigma. Se había considerado que el cuadro de diarrea podía estar provocado por una infección por Clostridium difficile en relación con la antibioticoterapia recibida previamente por cuadro de pielonefritis aguda por Escherichia coli. No llegó a obtenerse confirmación microbiológica de dicha colonización, pero se inició tratamiento empírico con metronidazol, con buena respuesta clínica y analítica inicial, por lo que le fue dada el alta.
A la semana reingresó por dolor en hemiabdomen izquierdo y hematoquecia. Se realizó una colonoscopia, en la que se apreciaron hallazgos indicativos de EC cólica con actividad moderada: úlcera de unos 10mm de aspecto inflamatorio en el colon ascendente, mucosa con aspecto de úlceras previas cicatrizadas en colon transverso y con coágulo adherido sobre un vaso visible a 40cm del margen anal (ángulo esplénico del colon) que se desprendió tras la inyección de adrenalina, mostrando un sangrado babeante (fig. 2A) sobre el que se colocó un hemoclip con buena hemostasia.
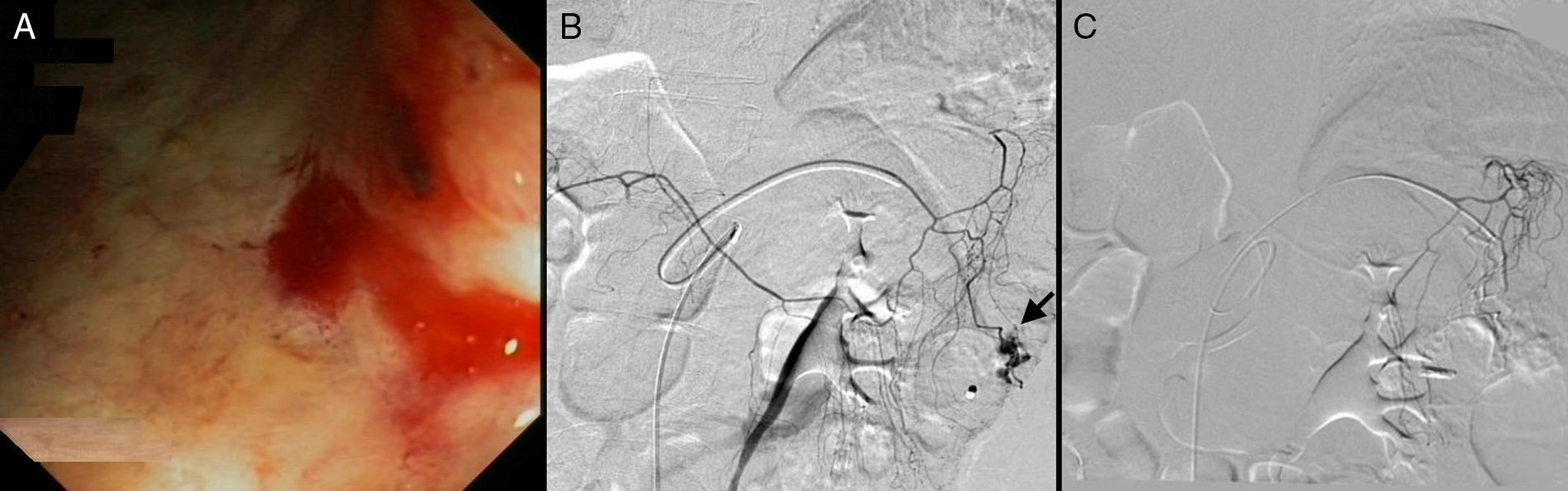
A) Imagen de la colonoscopia en la que se observa sangrado babeante a través de un vaso visible a 40cm de margen anal (ángulo esplénico del colon). En B) se ilustra el procedimiento de embolización mediante arteriografía supraselectiva de la rama cólica media dependiente de la arteria mesentérica superior. Se observa un sangrado activo en el área descrita (flecha), comprobándose la ausencia de extravasación de contraste en dicha zona en la imagen de control postembolización (C).
Durante el ingreso presentó un nuevo episodio de dolor en hemiabdomen izquierdo sin signos de irritación peritoneal acompañado de HDB con inestabilidad hemodinámica que respondió a la administración de volumen, llegando a precisar la transfusión de un total de 13 concentrados de hematíes y una bolsa de plasma a lo largo de todo el ingreso. Se realizó angio-TC abdominal, identificándose extravasación de contraste en fase tardía en el ángulo esplénico del colon, donde también se apreciaba el clip de hemostasia, con un sangrado en sábana en dicha zona. Se realizó arteriografía supraselectiva de la rama sangrante que dependía de la arteria cólica media y embolización con partículas de PVA de entre 300 y 500 μ, con buen resultado radiológico y confirmándose el control de la hemorragia en angiografía posterior (fig. 2B y C). Tras el control del sangrado se inició tratamiento corticoideo con metilprednisolona (0,8mg/kg/día), habiéndolo pospuesto hasta ese momento porque clínica y endoscópicamente el cuadro era indistinguible entre una enfermedad inflamatoria intestinal y un cuadro isquémico o infeccioso, por lo que había estado únicamente con tratamiento antibiótico hasta entonces. Actualmente no ha presentado resangrado ni complicaciones del procedimiento en los 21 meses siguientes, a pesar de que la paciente continuó con tratamiento antiagregante.
DiscusiónSe presentan 2 casos de HDB masiva en los pacientes con EC. De acuerdo con la clasificación de Montreal, tuvieron un patrón inflamatorio (B1), fueron diagnosticados después de los 40 años (A3) y de localización cólica (L2) e ileocólica (L3). En el momento de la HDB nuestros pacientes tenían un brote moderado y una PCR>10mg/dl, a diferencia de los estudios previos, en los cuales una mayoría de los pacientes tienen una EC quiescente2,4.
La prevalencia de HBD en pacientes con EC, según las series clásicas realizadas en pacientes occidentales, se encuentra entre 0,9 y 2,5%1; sin embargo, en estudios más recientes, como el de Kim et al.2 en pacientes orientales, llega a ser hasta de un 4%. La HDB puede ser la manifestación inicial de la EC entre un 15 y un 23% de los casos1,6. Después del diagnóstico de la EC, la probabilidad de presentar una HDB aumenta según el tiempo de evolución, con una probabilidad acumulada del 1,7% después de un año, el 6,5% a los 10 años y el 10% a los 20 años del diagnóstico2.
La colonoscopia es la primera técnica empleada habitualmente para el estudio de la HDB. Sin embargo, tiene la limitación de no poder identificar el origen del sangrado cuando este es masivo, debido a la gran cantidad de sangre presente en el colon, o cuando se localiza en intestino delgado2. Algunos autores recomiendan la combinación de métodos endoscópicos con la angiografía para localizar el sitio de sangrado, con una elevada tasa de éxito7,8.
El tratamiento estándar de la HDB masiva sigue siendo la cirugía urgente hasta en un 60% de los pacientes en el primer episodio de sangrado, con la consiguiente elevada morbimortalidad perioperatoria4,8. Además, un importante número de pacientes con enfermedad inflamatoria intestinal requerirán una o más cirugías resectivas a lo largo de su vida, debido a que las recidivas de la enfermedad son frecuentes5. El síndrome de intestino corto es una complicación frecuente en los pacientes que han requerido múltiples resecciones intestinales, por lo que el objetivo en la EC es diferir o evitar las cirugías en la medida de lo posible.
Los métodos de embolización endovascular son una alternativa de tratamiento de la HDB masiva5. Las potenciales complicaciones de estos tratamientos son la isquemia y el infarto intestinal. Sin embargo, en los últimos 10 años, con los avances en la tecnología y el perfeccionamiento de las técnicas de intervención, la selectividad del procedimiento se ha incrementado notablemente. Existen actualmente microcatéteres coaxiales y nuevos agentes embolizantes, tales como microplatino y partículas de PVA, que hacen posible la embolización arterial más allá de los vasa recta, lo que reduce considerablemente el riesgo de isquemia. Recientemente, se han publicado estudios prometedores que describen la embolización transcatéter en HBD masiva con una tasa de éxito del 81-93% y una tasa de mortalidad del 0-7%. En nuestros 2 pacientes se logró el control de la hemorragia de forma efectiva, empleando técnicas de embolización endovascular selectiva y supraselectiva transcatéter, sin recurrencia del sangrado durante el seguimiento.
ConclusiónLa arteriografía y las nuevas técnicas de embolización arterial selectiva y supraselectiva pueden ser una buena opción diagnóstica y terapéutica para el control de la HDB masiva en pacientes con EC, como alternativa al tratamiento quirúrgico.