INTRODUCCIÓN
La infección por Mycobacterium tuberculosis ha sufrido un notable aumento en su incidencia en las últimas décadas. La existencia de factores predisponentes que condicionan una depresión del sistema inmunitario ha conformado una serie de grupos de riesgo poblacionales en los que la posibilidad de infección resulta más frecuente. La depresión de defensas del huésped en este tipo de pacientes permite la diseminación de la micobacteria a través del torrente sanguíneo o del sistema linfático a todo el organismo, lo que favorece la aparición de formas extrapulmonares y, por tanto, se diferencia del patrón clínico de tuberculosis (TBC) clásico hasta la fecha. En esta nota clínica presentamos un caso en el que se pone de manifiesto lo mencionado anteriormente.
OBSERVACIÓN CLÍNICA
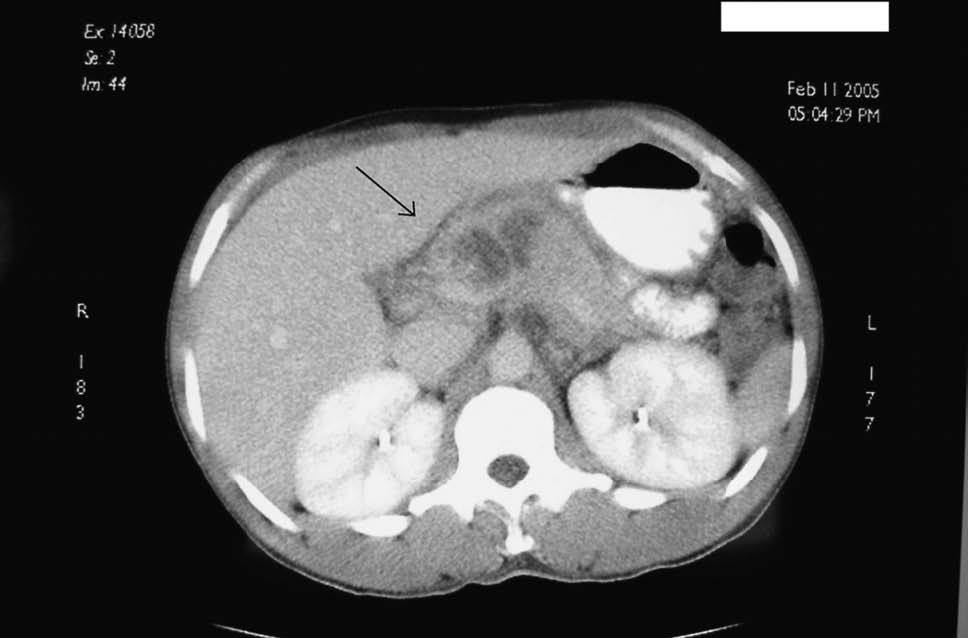
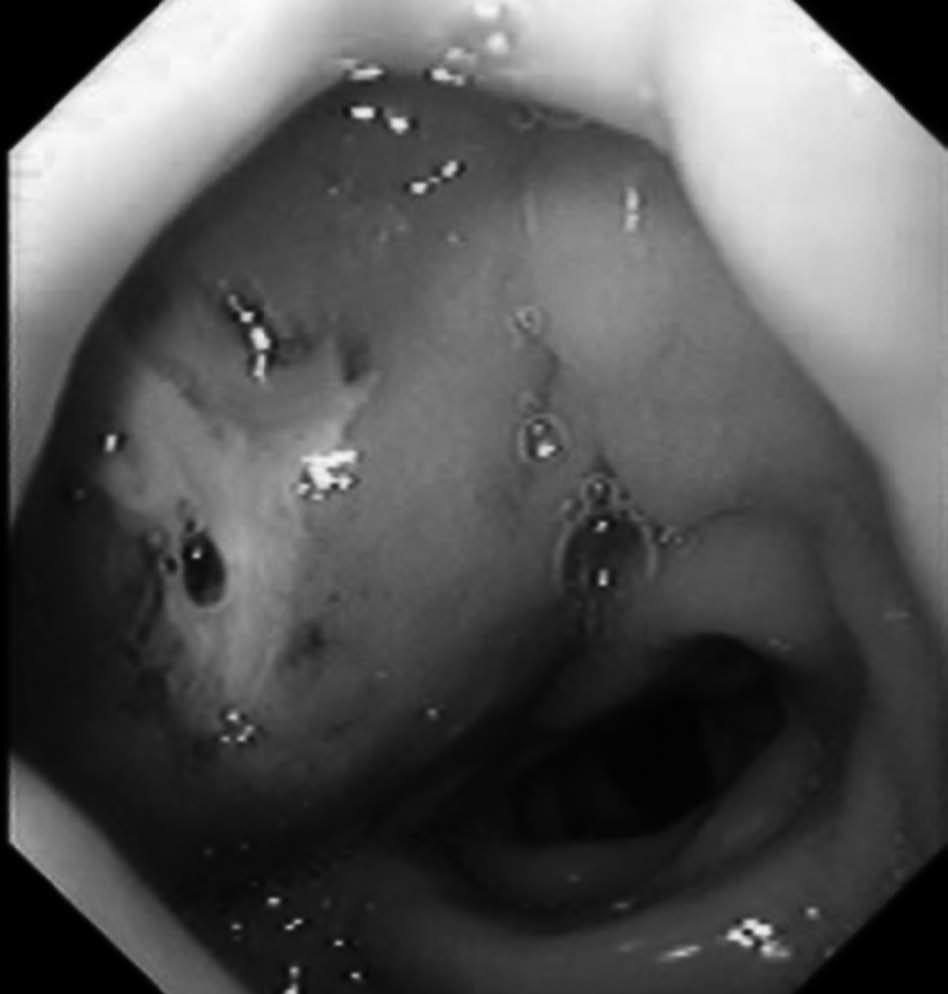
Paciente subsahariano de raza negra, de 33 años de edad, sin antecedentes conocidos de enfermedad, que acude a nuestro centro por presentar un cuadro de epigastralgia no irradiada, acompañada de fiebre de alto grado y síndrome diarreico sin signos inflamatorios. En la exploración física, tras una palpación profunda, se detecta la presencia de una masa de consistencia pétrea en el epigastrio; sin otros datos anormales en los diferentes órganos explorados. Se realizó una analítica ordinaria cuyos datos más relevantes fueron los siguientes: hemoglobina 15 g/dl; hematocrito 43%; 13.000 leucocitos (95% polimorfonucleares); amilasa y lipasa normales; coagulación normal; velocidad de sedimentación globular 87 mm/h; proteína C reactiva 15 mg/l. Se obtienen muestras séricas y de heces para el análisis microbiológico y el cultivo. Se realiza una ecografía y una tomografía computarizada (TC) abdominal con contraste oral e intravenoso (fig. 1), que confirman la presencia de una masa heterogénea sin imágenes quísticas en la cabeza pancreática; no se observa dilatación del colédoco y, además, se descarta la presencia de gas y/o líquido libre. El paciente presenta un gran deterioro de su estado general al cabo de 48 h, por lo que se procede a repetir las técnicas de imagen, que no son informadas en sentido diferente al previo. Los cultivos realizados al ingreso son negativos. Se decide la realización de una punción aspiración con aguja fina (PAAF) de la lesión, que revela la presencia en el aspirado de polimorfonucleares, sin apreciar células de aspecto neoplásico. Se obtienen nuevas muestras séricas y de heces para el análisis y se inicia un tratamiento antibiótico empírico por vía intravenosa. En el coprocultivo se informa de la presencia de abundantes formas compatibles con bacilos alcohol-resistentes (BAAR). Se decide la realización de una gastroscopia que informa de la presencia de un área mucosa indurada en la segunda porción duodenal, la cual, tras una movilización con pinza de biopsia, revela la presencia de un orificio fistuloso (fig. 2) por el que drena un contenido líquido de aspecto purulento. Se realiza una citología del líquido mediante cepillado y una aspiración mediante lavados con suero. El análisis del material revela la presencia de abundantes polimorfonucleares, así como positividad en la tinción de Ziehl-Nielsen (Z-N). Se realiza un Mantoux, que resulta negativo, y se solicita una batería serológica completa (virus de la hepatitis A, B y C, virus de la inmunodeficiencia humana [VIH], virus de Epstein-Barr, y citomegalovirus), en la que se detectó únicamente positividad para el VIH con una carga viral de 175.000 copias/ml y CD4 75/ml. Una vez definido el diagnóstico de TBC pancreática con fistulización a duodeno en un paciente inmunocomprometido, se inicia tratamiento tuberculoestático con terapia cuádruple (isoniazida, rifampicina, pirazinamida y etambutol) durante 12 meses; al cabo de este período se realiza un control evolutivo mediante endoscopia y TC, y se constató la total desaparición de las imágenes descritas anteriormente. Tras 48 semanas de tratamiento con tenofovir + emtricitabina (Trubada) y efavirenz en dosis de 600 mg, el paciente presenta una carga viral positiva, VIH-1 < 40 copias/ml y CD4 352/ml, así como una ganancia de peso de 15 kg. En el estudio de resistencias se puso de manifiesto una sensibilidad de la micobacteria al tratamiento tuberculostático.
Fig. 1. Imagen de tomografía computarizada de una lesión pancreática (flecha).
Fig. 2. Imagen endoscópica de un orificio fistuloso en el duoden
DISCUSIÓN
El VIH y M. tuberculosis son 2 patógenos intracelulares con una gran interacción, tanto desde una perspectiva epidemiológica como desde el punto de vista clínico y celular. La TBC es la enfermedad que con mayor frecuencia se asocia al sida en nuestro país; según los datos acumulados del Plan Nacional del Sida, en el 40% de los casos la TBC es la enfermedad definitoria inicial. En la década de los noventa la incidencia media anual de TBC en España fue de casi 40 casos por 100.000 habitantes, cifra muy superior a la tasa media de la Unión Europea1.
La tuberculosis abdominal constituye, aun así, una localización poco frecuente en nuestro medio en la actualidad, si bien en los últimos años se ha constatado un aumento en su incidencia debido en parte al incremento de enfermedades que cursan con depresión del sistema inmunitario y al aumento de los flujos migratorios provenientes de áreas menos desarrolladas2. Los órganos más frecuentemente afectados en esta localización son el hígado, el bazo, el intestino, el peritoneo y los nódulos linfáticos3. La afectación pancreática asociada a la TBC abdominal es muy baja: se han indicado frecuencias en series de necropsias del 0-4,7%4. El diagnóstico de infección pancreática por TBC resulta complejo. Se han descrito diferentes modos de presentación en esta área, como abscesos pancreáticos, pancreatitis aguda o crónica, hemorragia digestiva, ictericia obstructiva o masa pancreática, que simula un proceso neoplásico5,6. La clínica resulta en estos casos altamente inespecífica, y el dolor abdominal es el dato más frecuente7 en la afectación pancreática, por lo que se debe considerar un diagnóstico diferencial con enfermedades más frecuentes que afectan a este órgano, como los procesos inflamatorios (pancreatitis) y/o neoplásicos. Los hallazgos radiológicos también son muy inespecíficos. Las imágenes obtenidas mediante ultrasonidos, TC o resonancia magnética resultan, en numerosas ocasiones, indistinguibles de las observadas en otras enfermedades. En los últimos años, con el advenimiento de la ecoendoscopia, el algoritmo diagnóstico de las masas pancreáticas ha sufrido un drástico cambio, con la posibilidad de realizar punción y drenajes8. La existencia de lesiones en otros órganos, la presencia de adenopatías o el engrosamiento mural en el íleon puede ayudar en el diagnóstico, pero en la actualidad no hay ningún patrón iconográfico patognomónico definitorio de la infección. La afectación pancreática, además, se presenta en numerosas ocasiones de manera aislada, sin acompañarse de alteraciones en otro órgano; en este sentido, se ha descrito una serie de pacientes afectados de TBC pancreática, en quienes sólo se detectó un foco primario pulmonar en el 19%9, lo cual contribuye a un bajo índice primario de sospecha de la enfermedad. La obtención de material o tejido de la lesión mediante PAAF se revela como una herramienta diagnóstica de gran importancia, ya que se pueden observar micobacterias mediante Z-N y aislarlas en cultivo10. Aun así, se han registrado un alto número de falsos negativos mediante esta técnica. El bajo nivel de sospecha de la enfermedad, motivado por la presentación clínica irrelevante, así como la falta de especificidad de los datos obtenidos mediante los medios diagnósticos convencionales, explican el hecho de que un significativo grupo de pacientes se diagnostique mediante una laparotomía exploradora realizada en primera instancia con otra sospecha diagnóstica. En un considerable número de pacientes el diagnóstico final se realiza mediante el análisis histológico de la pieza resecada11,12. La publicación de numerosos casos en la literatura médica revela que el diagnóstico a posteriori condiciona un gran índice de morbilidad asociado a la cirugía realizada en ellos13-15. La realización de biopsias intraoperatorias en búsqueda de signos de infección por micobacterias resulta fundamental para evitar las resecciones innecesarias; aun así, el índice de falsos negativos en la tinción de Z-N resulta elevado y los cultivos específicos suelen ser muy lentos en su positividad. Además, hay otras formas bacilares, como M. avium intracelulare, cuya frecuencia va en aumento en la población general sin factores predisponentes, que pueden inducir a establecer un diagnóstico erróneo. La mayor parte de las series publicadas incluye pacientes que provienen de países en vías de desarrollo, en los que las tasas de incidencia de TBC están notablemente elevadas. El estado inmune del paciente constituye, si este es deficiente, un factor predisponente para el desarrollo de TBC; la existencia de formas extrapulmonares es especialmente elevada en este grupo de población. El rebrote de la incidencia de la infección por TBC es consecuencia de los factores previamente comentados. Este hecho explica, a su vez, por qué el índice de sospecha ha aumentado en nuestro días, pero, a pesar de ello, todavía hoy constituye un reto para el diagnóstico. En el caso presentado llama la atención la detección BAAR en heces; en las series publicadas la tasa de positividad comunicada en este tipo de extensiones resulta extremadamente baja10,13. La fistulización a duodeno de la masa pancreática permitió, en primer lugar, el aislamiento de BAAR en la extensión de heces y el posterior diagnóstico de la infección. No se han descrito hasta la fecha casos similares en los que se detecta una fistulización mediante endoscopia.
La patogenia de la TBC pancreática aún no se ha esclarecido completamente. Se han postulado a este efecto varias teorías que intentan explicar este hecho, entre otras: diseminación hematógena de un foco oculto, respuesta tóxico-alérgica del páncreas en respuesta a la TBC sistémica, afectación pancreática por diseminación miliar o afectación directa por extensión desde los nódulos linfáticos3,14.
La respuesta a la terapia tuberculostática específica en los pacientes afectados de TBC pancreática presenta tasas de respuesta similares a las observadas en otras formas de TBC. El principal problema de este tipo de infección reside en un retardo en el diagnóstico, que puede ocasionar una diseminación de la infección con el consiguiente fracaso terapéutico y un aumento del índice de morbimortalidad en estos pacientes15,16. El número de fármacos tuberculostáticos, así como la duración del tratamiento, depende en gran medida de los valores locales de resistencia a los tuberculostáticos; se considera que unos valores por debajo del 4% permitirían el uso de terapias combinadas triples, mientras que unas tasas de resistencia superiores a este valor obligaría a realizar una terapia cuádruple, asociando etambutol o estreptomicina17, como en el presente caso clínico. En general, en España las tasas de resistencia se sitúan por debajo de este nivel si bien en el África subsahariana se registran altas tasas de resistencia. El paciente residía en España desde hacía 3 años, por lo que se podría considerar como una infección adquirida, pero el hecho de que la forma de presentación fuera extrapulmonar planteó el diagnóstico de reactivación de una infección latente y obligó a iniciar un tratamiento con terapia cuádruple hasta que el estudio de disponibilidades estuviera disponible. Dada la elevada frecuencia de coinfección VIH/TBC, en los pacientes infectados por el VIH se considera indicado establecer un tratamiento antituberculoso, no solamente cuando se ha confirmado por baciloscopia o cultivo el diagnóstico de TBC, sino que debe iniciarse de forma empírica cuando en cualquier muestra se identifique la presencia de BAAR, o en ciertos contextos clínicos sugestivos como, por ejemplo, ante un síndrome febril prolongado en el que se hayan descartado otras causas. El tratamiento de la TBC en los pacientes infectados por el VIH presenta una singular complicación, derivada de las interacciones farmacológicas entre la rifampicina y 2 familias de antirretrovirales: los inhibidores de la proteasa y los inhibidores de la transcriptasa inversa no análogos de nucleósidos, lo que obliga a un ajuste de dosis y a considerar, como en este caso, el uso de antirretrovirales que no presenten interacciones con el fármaco tuberculostático18.
A pesar del importante avance en las técnicas diagnósticas, tanto la experiencia como la sospecha clínica todavía son dos pilares fundamentales sobre los que se asienta el reconocimiento de esta enfermedad, potencialmente fatal pero curable con un diagnóstico temprano. Este caso clínico resalta la necesidad de incluir en el diagnóstico diferencial de masas pancreáticas la posibilidad de infección por TBC, sobre todo en pacientes pertenecientes a grupos de alto riesgo. El papel de las técnicas de imagen, como la ecoendoscopia con punción, resulta de especial interés en el diagnóstico en este tipo de lesiones.