Casos Clínicos en Gastroenterología y Hepatología
Más datosLa tuberculosis (TBC) es la infección más prevalente ya que afecta a un tercio de la población mundial. Así, en 2019 se diagnosticaron 9.960.000 casos en todo el mundo, con una incidencia de 130 casos por 100.000 habitantes por año1. Por otro lado, la TBC gastrointestinal, que representa la 6.ª causa de afectación extrapulmonar, puede simular otras enfermedades, como la enfermedad de Crohn2.
Se presenta el caso de un varón de 23 años, natural del norte de África, con síndrome de Down, que consultó por dolor abdominal y fiebre en diciembre de 2019. Con el diagnóstico de plastrón inflamatorio apendicular, fue tratado con antibiótico (4g/0,5g de piperacilina-tazobactam por vía intravenosa cada 8 h durante 14 días). Se completó el estudio con la prueba de la tuberculina (PT), el ensayo de liberación de interferón-γ (IGRA) y una radiografía de tórax para descartar TBC, que resultaron negativas. En la rectocolonoscopia, el orificio apendicular y la válvula ileocecal estaban deformados, eritematosos y edematosos, con erosiones y úlceras. El orificio valvular no se consiguió atravesar para ileoscopia por la inflamación y la gran friabilidad al mínimo roce, por lo que únicamente se tomaron biopsias a nivel cecal y de la válvula ileocecal. Las biopsias fueron sugestivas de enfermedad de Crohn (abundante tejido de granulación, afectación parcheada y discontinua de la mucosa, distorsión arquitectural, criptitis, abscesos crípticos y ulceración). En la enterorresonancia magnética destacaba un engrosamiento inflamatorio crónico ileal con fístulas enteroentéricas. El diagnóstico final fue enfermedad de Crohn fistulizante A2L3B3. Se comenzó el tratamiento con prednisona oral (40mg inicialmente, con pauta descendente semanal), azatioprina oral (150mg cada 24 h) y 220 mg de infliximab intravenoso (perfusión inicial, a la 2.ª y 6.ª semanas, y posteriormente cada 8 semanas).
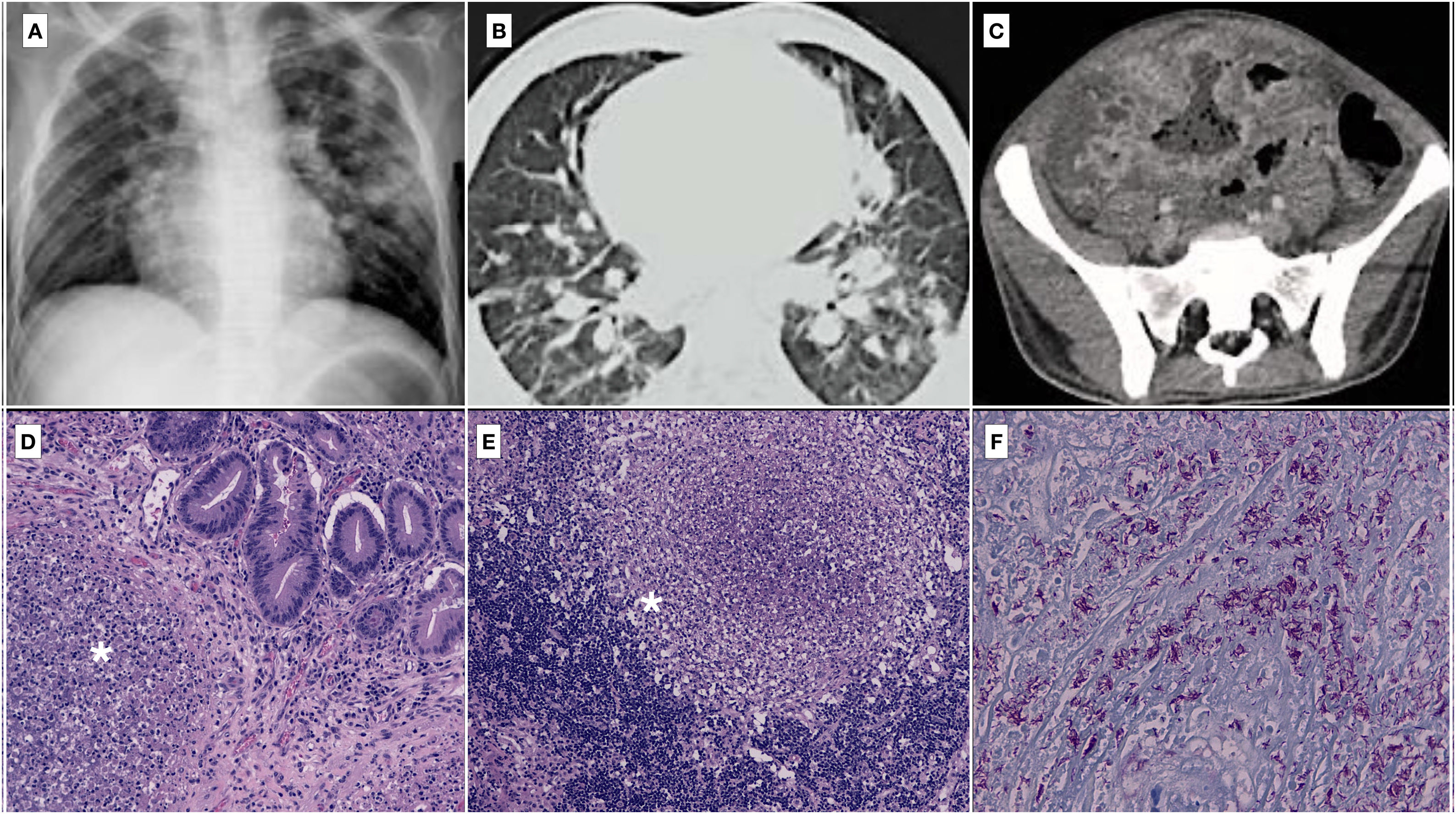
En abril de 2020, 4 meses después, el paciente consultó por diarrea, dolor abdominal y fiebre vespertina. El tratamiento que estaba tomando era azatioprina oral (150mg cada 24 h) e infliximab intravenoso (220mg cada 8 semanas), ya que había finalizado la pauta descendente de corticoides. En la exploración física destacaban: temperatura de 39°C, presión arterial 75/30mmHg, frecuencia cardiaca 80 lpm, saturación de oxígeno del 88% y un abdomen blando y depresible, doloroso en fosa ilíaca derecha, sin signos de irritación peritoneal. En la analítica presentaba: proteína C reactiva 16,26mg/dl (N: 0-0,5mg/dl); procalcitonina 20,53 ng/ml (N: 0,02-0,5 ng/ml); leucocitos 1.910 (N: 4.200-10.500); neutrófilos 82,93% (N: 42-77%); ferritina 12.574 ng/ml (N: 20-250 ng/ml); interleucina-6 (IL6) 314,1 pg/ml (N: 0-7 pg/ml) y dímero D 5.705 ng/ml (N: 0-500 ng/ml). La radiografía de tórax (fig. 1A) fue compatible con COVID-19 y la tomografía computarizada (TC) con proceso infeccioso pulmonar y absceso intraabdominal (fig. 1 B y C). Se solicitaron una reacción en cadena de la polimerasa (PCR) para coronavirus 2019 (COVID-19) y una tinción de Ziehl-Neelsen en esputo.
A) Radiografía de tórax posteroanterior: opacidades múltiples periféricas en ambos lóbulos sugerentes de infección por SARS-CoV-2. B) Tomografía computarizada torácica: condensación alveolar parcheada, de morfología nodular a nivel central y periférico, compatible con proceso infeccioso. C) Tomografía computarizada abdominal (corte axial): asas de intestino delgado de pared engrosada con absceso interasas en el promontorio. D) Granuloma necrosante con inflamación aguda añadida (asterisco) en relación con la mucosa-submucosa cecal (tinción hematoxilina-eosina, 100×). E) Granuloma necrosante con fenómenos de abscesificación en tejido linfoide ganglionar (asterisco) tinción hematoxilina-eosina, 100×). F) Abundantes BAAR en áreas de necrosis granulomatosa (Ziehl-Neelsen, 400×).
Sin esperar al resultado de las últimas pruebas por empeoramiento clínico del paciente, se indicó cirugía urgente. Se intervino mediante una laparotomía media y se halló líquido libre intraabdominal seroso, un plastrón inflamatorio ileocecal y adenopatías mesentéricas de gran tamaño. Se realizó una resección ileocecal en bloque y anastomosis ileocólica. La PCR fue negativa para COVID-19 y la tinción de Ziehl-Neelsen positiva para bacilos ácido-alcohol resistentes, por lo que se suspendió el tratamiento pautado para la enfermedad de Crohn. En el estudio histopatológico (figs. 1 D-F) se confirmó el diagnóstico de TBC intestinal; se comenzó el tratamiento con 150mg de rifampicina, 75mg de isoniazida, 400mg de pirazinamida y 275mg de etambutol hidrocloruro (Rimstar®), 3 comprimidos cada 24 h durante 2 meses y, posteriormente, con 300mg de rifampicina y 150mg de isoniazida (Rifinah®) 2 comprimidos cada 24 h durante 4 meses. Tras 4 meses de seguimiento, el paciente presentó una evolución satisfactoria con baciloscopia negativa; en la TC torácica se evidenció una disminución del número y tamaño de las áreas de condensación alveolar, así como disminución de las adenopatías mediastínicas, y en la TC abdominal las asas intestinales presentaban paredes de grosor normal, sin evidenciar fístulas, gas ectópico ni colecciones.
En cuanto al origen y desarrollo de la TBC en este caso, se plantean 2hipótesis. La primera es que se tratara de una enfermedad de Crohn de base, que durante el tratamiento inmunosupresor hubiera producido una TBC activa, pulmonar y extrapulmonar (intestinal), a pesar del cribado negativo de una TBC latente basal con PT, IGRA y radiografía de tórax. La segunda es que se tratara de una TBC intestinal de base que, tras un tratamiento inmunosupresor para la sospecha de enfermedad de Crohn se hubiera diseminado, con afectación pulmonar también. El origen del paciente, al ser de un área de alta incidencia de TBC, podría apoyar la segunda hipótesis diagnóstica.
La TBC intestinal suele tener un comienzo más agudo que la enfermedad de Crohn, con predominio de la astenia y la fiebre elevada con sudoración vespertina3, que puede ocurrir en ausencia de afectación pulmonar4. La PT puede tener falsos negativos, como en el caso presentado, debidos, entre otros, a situaciones de inmunodepresión, como la TBC grave5. En la TC, el engrosamiento (>6mm) simétrico de la pared intestinal con afectación transmural, los cambios inflamatorios en la grasa pericólica y mesentérica, y las fístulas y abscesos orientarían a enfermedad de Crohn. En la endoscopia, la afectación de menos de 4segmentos de colon con úlceras transversales y cicatrices, la válvula ileocecal incompetente, las estenosis únicas y cortas, y los divertículos por tracción serían característicos de la TBC, mientras que en la enfermedad de Crohn existen más frecuentemente ulceraciones aftoides longitudinales, que afectan la mucosa de manera discontinua y producen estenosis de la válvula ileocecal. En el estudio histopatológico, los grandes granulomas confluentes, la necrosis caseosa, la inflamación submucosa desproporcionada y las ulceraciones lineales con conglomerados epitelioides de histiocitos son más frecuentes en la TBC3.
Recientemente se han publicado las recomendaciones del Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa sobre el cribado y tratamiento de la infección tuberculosa en pacientes con enfermedad inflamatoria intestinal6. En el caso presentado, se realizaron la PT y el IGRA para descartar TBC en el diagnóstico diferencial del plastrón apendicular. Al resultar estas pruebas negativas, se inició el tratamiento inmunosupresor de la enfermedad de Crohn. En el cribado de la TBC en pacientes con enfermedad de Crohn se recomienda la PT, o en su defecto el IGRA, aunque este último pueda ser menos sensible para detectar casos antiguos. Aunque la radiografía de tórax solamente está recomendada en los casos de cribado positivo o, ante un contacto reciente con alguien con TBC, en el caso que se presenta también se realizó para descartar una infección activa a nivel pulmonar.
En ausencia de sintomatología respiratoria de la COVID-19, son característicos el aumento de proteína C reactiva con procalcitonina normal y linfopenia (<1.100 cél/μl). Los casos graves pueden presentar niveles elevados de ferritina, dímero D e IL67. En la radiografía de tórax se observan zonas asimétricas de opacidad alveolar o intersticial, parcheadas o difusas, siendo la neumonía bilateral el patrón más habitual, mientras que en la TC se evidencian múltiples opacidades en vidrio deslustrado con consolidaciones en la periferia pulmonar, a nivel subpleural y de márgenes mal definidos8. Estos hallazgos podrían confundirse con los infiltrados parenquimatosos de la TBC pulmonar primaria5. En el caso presentado, el contexto epidemiológico actual por la COVID-19, la negatividad previa de la PT y el IGRA, la fiebre, la saturación de oxígeno al 88% y la concordancia de los valores analíticos con los descritos en la literatura para infección por SARS-CoV-2 plantearon que los hallazgos radiológicos pudieran ser más compatibles con COVID-19 que con TBC.
En conclusión, la TBC puede simular varias enfermedades en un mismo paciente, como la enfermedad de Crohn y la COVID-19, por lo que debe considerarse en el diagnóstico diferencial para pautar un tratamiento adecuado.
Conflicto de interesesDeclaramos que no existen aspectos de financiación ni de cualquier otro tipo que puedan llevar a un conflicto de intereses.