Los fármacos biológicos dirigidos contra moléculas implicadas en la respuesta inmune, se han establecido como la base del tratamiento de muchos pacientes con enfermedades de base autoinflamatoria como la enfermedad inflamatoria intestinal (EII).
Los fármacos que bloquean el factor de necrosis tumoral alfa (anti-TNF-α) son los biológicos más utilizados en el tratamiento de la EII. Se ha descrito ampliamente la manifestación paradójica de inducción o empeoramiento de la psoriasis como efecto adverso de los fármacos anti-TNF-α. En cambio, es menor el número de casos publicados de la situación inversa, el debut de una EII como efecto adverso del tratamiento biológico utilizado para otras patologías.
El secukinumab es un anticuerpo monoclonal anti-interleukina-17A empleado en el tratamiento de la psoriasis, artritis psoriásica y espondilitis anquilosante. En estudios previos se ha observado que carece de eficacia en el tratamiento de la Enfermedad de Crohn (EC)1, sin existir estudios con la colitis ulcerosa (CU). El riesgo de exacerbar una EII subyacente en pacientes en tratamiento con dicho fármaco es controvertido.
Presentamos el caso de un hombre de 52 años de edad diagnosticado de psoriasis, sin otros antecedentes de interés, en tratamiento con secukinumab durante dos semanas.
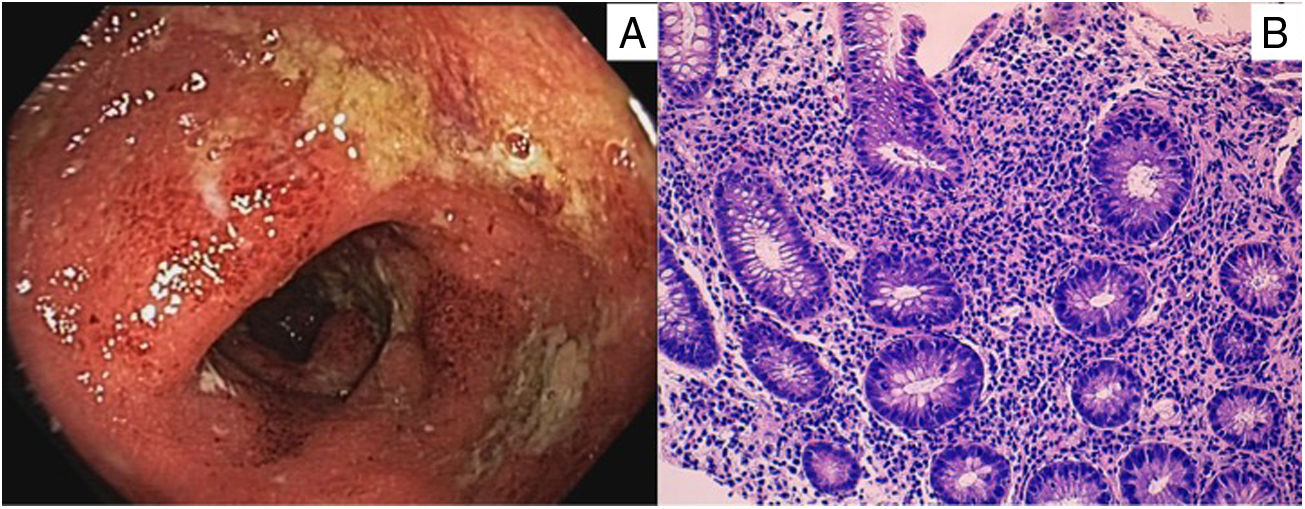
Ingresó en la unidad de Gastroenterología por diarrea de cinco días de evolución, con unas 20-30 deposiciones diarias. Asociaba dolor abdominal de tipo cólico. Los últimos días las deposiciones se acompañaban de sangre, con fiebre de hasta 38,5°C y quebrantamiento del estado general. Analíticamente presentaba elevación de reactantes de fase aguda, con PCR de 194,6 mg/L (normal < 5 mg/L). El coprocultivo y la toxina de C. difficile fueron negativos. Se realizó rectoscopia a los tres días del ingreso, evidenciando una mucosa edematosa y eritematosa, con pérdida del patrón vascular y exudado purulento, así como varias úlceras en sigma, superficiales y con fibrina (fig. 1A). Se realizó toma de biopsias, que mostró un aumento difuso del infiltrado inflamatorio mononuclear de la lámina propia de la mucosa rectal, con criptitis y microabscesos y distorsión arquitectural de las criptas, respetando la muscularis mucosae, hallazgos histopatológicos compatibles con EII tipo CU en actividad moderada (fig. 1B).
A) Mucosa de sigma edematosa y eritematosa, con pérdida del patrón vascular, exudado purulento y úlceras superficiales cubiertas de fibrina.
B) Aumento difuso del infiltrado inflamatorio mononuclear de la lámina propia de la mucosa rectal, con criptitis, microabscesos y distorsión arquitectural de las criptas, respetando la muscularis mucosae.
Se inició tratamiento con corticoides sistémicos, prednisona a dosis de 60 mg en pauta descendente, así como mesalazina tópica (1 supositorio de 500 mg cada 12 horas) y oral (3.200 mg/24 horas), con remisión progresiva de la sintomatología y desaparición de las lesiones en la colonoscopia de control a los tres meses. El paciente siguió tratamiento de mantenimiento con 5-ASA, retirándose tras iniciar tratamiento con adalimumab por parte de su dermatólogo a los cuatro meses del diagnóstico para tratamiento de la psoriasis. Tras 24 meses de seguimiento se encuentra en remisión de la enfermedad cutánea y digestiva.
La IL-17 es una citocina proinflamatoria producida por las células T helper 17 (Th17), que ha sido relacionada con diversas enfermedades inflamatorias crónicas. Se ha comprobado que el intestino de los pacientes con EII contiene una elevada infiltración de linfocitos Th17, los cuales producen grandes cantidades de IL-17A, cuyo papel en la patogénesis de la enfermedad es controvertido: mientras que se ha relacionado con la inflamación intestinal en algunos estudios, en otros se le ha asignado un papel protector, mostrando que la inhibición de la misma ha conducido a una exacerbación de la EII2.
En 2012 se publicó un estudio que investigaba la utilidad del secukinumab sobre la enfermedad de Crohn, mostrando efectos escasos y un aumento de las reacciones adversas en comparación con el placebo1. Sin embargo, escasos estudios han descrito la aparición o exacerbación de la enfermedad de Crohn en pacientes en tratamiento con secukinumab, siendo aún menor el número de estudios que describen la CU como efecto secundario3. En una revisión publicada en 2019, que incluye 21 ensayos clínicos con pacientes tratados con secukinumab para espondilitis anquilosante, psoriasis y artritis psoriásica, se observó la aparición de nuevos casos de EII de forma infrecuente (< 1%), aunque con un 22% de exacerbaciones en pacientes con historia previa de EII4.
Recientemente se ha publicado un caso de colitis ulcerosa inducida por secukinumab5, aunque en este el paciente presentaba síntomas intestinales previos compatibles con EII, al contrario que el nuestro, que no mostraba sintomatología digestiva hasta el momento del inicio del fármaco. Cabe destacar que publicaciones recientes han descrito el empeoramiento y la aparición de EII de novo tras el tratamiento con otros fármacos inhibidores de la IL-17A, como ixikizumab6 y brodalumab2.
En resumen, presentamos el debut de una CU como probable efecto adverso de un inhibidor de la IL-17A, lo que apoya la hipótesis del efecto protector de esta interleucina en el intestino. Recomendamos realizar una monitorización intensiva de síntomas gastrointestinales en pacientes en tratamiento con este fármaco para evitar un retraso en el diagnóstico y tratamiento de una posible EII.
FinanciaciónEste trabajo no ha recibido ningún tipo de financiación.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.