La pandemia por COVID-19ha conllevado la suspensión de la actividad programada en la mayoría de las Unidades de Endoscopia de nuestro medio. El objetivo del presente documento es facilitar el reinicio de la actividad endoscópica electiva de forma eficiente y segura.
Material y métodosSe formuló una serie de preguntas consideradas de relevancia clínica y logística. Para la elaboración de las respuestas, se realizó una búsqueda bibliográfica estructurada en las principales bases de datos y se revisaron las recomendaciones de las principales instituciones de Salud Pública y de endoscopia digestiva. Las recomendaciones finales se consensuaron por vía telemática.
ResultadosSe han elaborado un total de 33 recomendaciones. Los principales aspectos que se discuten son: 1) la reevaluación y priorización de la indicación; 2) la restructuración de espacios, agendas y del personal sanitario; 3) el cribado de la infección, y 4) las medidas de higiene y los equipos de protección individual.
ConclusiónLa AEG y la SEED recomiendan reiniciar la actividad endoscópica de forma escalonada, segura, adaptada a los recursos locales y a la situación epidemiológica de la infección por SARS-CoV-2.
The COVID-19 pandemic has led to the suspension of programmed activity in most of the Endoscopy Units in our environment. The aim of this document is to facilitate the resumption of elective endoscopic activity in an efficient and safe manner.
Material and methodsA series of questions considered to be of clinical and logistical relevance were formulated. In order to elaborate the answers, a structured bibliographic search was carried out in the main databases and the recommendations of the main Public Health and Digestive Endoscopy institutions were reviewed. The final recommendations were agreed upon through telematic means.
ResultsA total of 33 recommendations were made. The main aspects discussed are: 1) Reassessment and prioritization of the indication, 2) Restructuring of spaces, schedules and health personnel, 3) Screening for infection, 4) Hygiene measures and personal protective equipment.
ConclusionThe AEG and SEED recommend restarting endoscopic activity in a phased, safe manner, adapted to local resources and the epidemiological situation of SARS-CoV-2 infection.
La Organización Mundial de la Salud (OMS) declaró la situación de pandemia por coronavirus SARS-CoV-2 el 11 de marzo del 2020. A mediados del mes de abril, el número de casos confirmados a nivel mundial superaba los 2 millones, afectaba a más de 200 países y había causado más de 139.000 muertes1. En nuestro país, en esa misma fecha, se notificaron un total de 188.068 casos confirmados y 19.478 fallecidos2.
Durante varias semanas la inmensa mayoría de las Unidades de Endoscopia (UE) del país decidieron suspender su actividad programada para reducir el riesgo de contraer la infección por SARS-CoV-2 y contribuir a reducir su propagación. Ante la posibilidad de inducir un daño en los pacientes y teniendo en mente la máxima primum non nocere, únicamente se llevaron a cabo procedimientos urgentes o aquellos cuya demora podía suponer un empeoramiento clínico sustancial. Por ese motivo, un importante número de pacientes no pudieron someterse a las exploraciones que tenían programadas.
Dada la situación excepcional, motivada por la pandemia, la Asociación Española de Gastroenterología (AEG) y la Sociedad Española de Endoscopia Digestiva (SEED) comisionaron la elaboración del presente documento sobre el reinicio de la actividad endoscópica. En este documento se proporcionan recomendaciones basadas en la evidencia para la reprogramación de los procedimientos suspendidos en los centros en los que los pacientes se encontraban citados inicialmente. Se requiere, por tanto, un compromiso tanto de los médicos especialistas de Aparato Digestivo como de los gestores de las mencionadas instituciones para resolver en los centros afectados la situación que ha generado la pandemia.
El ámbito de aplicación previsto es el de aquellas UE que se hayan podido ver afectadas por la epidemia y el tiempo establecido, el período que transcurra hasta la normalización de la actividad endoscópica en los términos en que se realizaba antes de la pandemia.
El presente consenso de expertos persigue facilitar la labor de los responsables y del resto de profesionales de las UE en el marco geográfico de nuestro país. Se pretende apoyar la toma de decisiones en un contexto nuevo y especialmente complejo, que permita la reprogramación de los procedimientos anulados durante la fase más aguda de la pandemia, y su realización de forma segura.
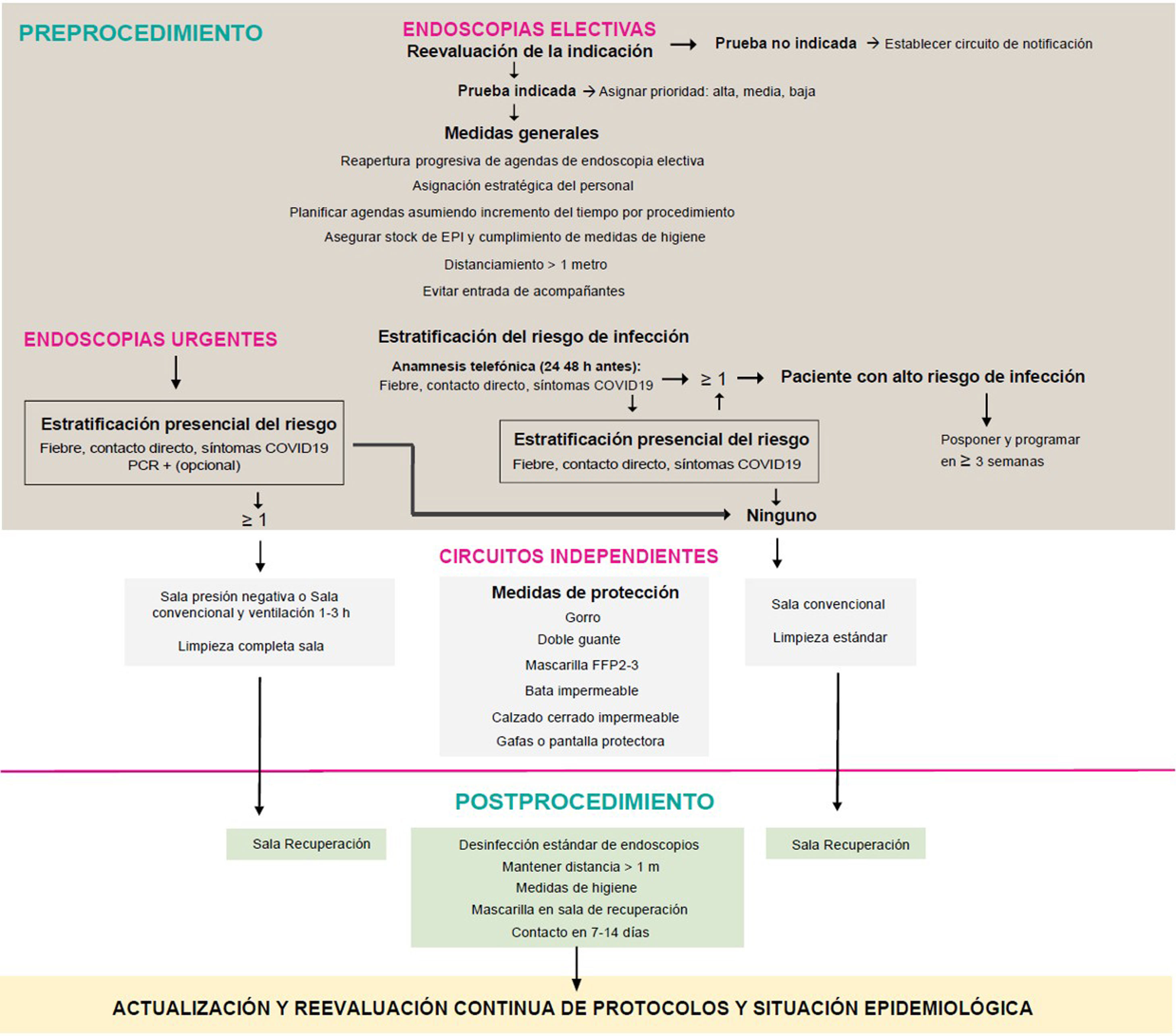
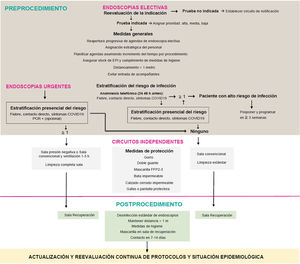
Material y métodosEn primer lugar, el conjunto de autores formuló una serie de preguntas consideradas de relevancia clínica y logística para el reinicio de la actividad endoscópica. Seguidamente, se realizó una búsqueda bibliográfica en Embase, Pubmed y la Cochrane Database of Systematic Reviews con palabras clave siguiendo la estrategia detallada en el anexo, tabla suplementaria 1, sin restricción de idioma, fecha o diseño. Asimismo, se consultaron artículos citados en la bibliografía de los trabajos revisados y aquellos considerados de interés durante la elaboración de las respuestas mediante búsquedas no sistematizadas. Se revisaron las recomendaciones vigentes por parte de instituciones nacionales, internacionales y de las principales sociedades científicas de Gastroenterología y Endoscopia Digestiva con fecha 17 de abril del 2020 (anexo, tabla suplementaria 1). Las recomendaciones finales se consensuaron entre todos los autores por vía telemática y se resumen en la tabla 1. La propuesta de actuación del presente documento se presenta en la figura 1.
Sumario de recomendaciones
| La AEG y la SEED recomiendan |
|---|
| Preprocedimiento |
| Reiniciar la actividad endoscópica de forma escalonada, adaptada a los recursos locales y a la situación epidemiológica de la infección por SARS-CoV-2 |
| Reevaluar la indicación de la endoscopia y priorizar aquellas donde el beneficio esperado sea mayor |
| Priorizar los procedimientos endoscópicos basándose en la probabilidad de encontrar lesiones clínicamente relevantes |
| Monitorizar los resultados del plan de priorización |
| Establecer un registro de las solicitudes evaluadas en la lista de espera de procedimientos endoscópicos, su nivel de prioridad y los motivos de anulación, cuando corresponda |
| Registrar en la historia clínica el motivo de suspensión de un procedimiento programado cuando este se anule por considerarse inadecuado |
| Asegurar la transmisión de la comunicación entre los agentes implicados en el proceso: especialistas evaluadores facultativos peticionarios y pacientes |
| Cribar la infección por SARS-CoV-2 mediante anamnesis dirigida en todos los pacientes |
| Actualmente, no existe evidencia científica de calidad que avale el cribado de la infección por SARS-CoV-2 mediante PCR o detección de anticuerpos previo a la realización de procedimientos endoscópicos. Por el momento, su rendimiento diagnóstico en contextos diferentes del de los pacientes sintomáticos es poco conocido y conlleva considerables dificultades de interpretación |
| Demorar los casos electivos sospechosos de COVID-19. El resto se llevará a cabo como si todos los pacientes estuvieran potencialmente infectados, mientras el área sea de alto riesgo |
| Establecer reuniones de todo el equipo de trabajo de la Unidad de Endoscopia para dar a conocer los protocolos de actuación y asegurar su cumplimiento |
| El empleo de mascarilla quirúrgica, así como el distanciamiento físico aconsejado por la OMS, durante las reuniones del equipo de trabajo |
| No permitir el paso de los acompañantes del paciente al interior de la Unidad de Endoscopia salvo en casos seleccionados |
| Que los pacientes mantengan una distancia interpersonal mínima de 1-2 m durante su paso por las dependencias de la Unidad de Endoscopia |
| Facilitar mascarillas de protección, ropa hospitalaria y una adecuada higiene de manos en los pacientes |
| Reajustar el tiempo asignado a cada endoscopia y el volumen de procedimientos, debido a la necesidad de implementar medidas de seguridad e higiene adicionales |
| Procedimiento |
| Establecer un circuito de pacientes independiente para los pacientes con alta sospecha o infección confirmada por SARS-CoV-2 |
| Fomentar la aplicación de medidas básicas de higiene para la prevención de la infección en todo el personal |
| La utilización de EPI en todo el personal sanitario involucrado en la realización de un procedimiento endoscópico |
| No realizar un procedimiento endoscópico si no se dispone de los equipos de protección necesarios para garantizar la seguridad de la endoscopia |
| No utilizar de forma sistemática barreras adicionales sobre el área nasobucal del paciente. La utilidad y la eficiencia de estas medidas, así como la aplicación de otras barreras sobre las válvulas del endoscopio, deben evaluarse en el seno de protocolos de investigación |
| Suplementar la oxigenoterapia con mascarillas con filtro de exhalado en pacientes con alta sospecha o infección confirmada por SARS-CoV-2 que se realicen una colonoscopia. Si no se dispone de estos dispositivos, recomendamos colocar una mascarilla quirúrgica por encima de las gafas nasales o mascarilla tipo Venturi |
| Los procedimientos en pacientes con alta sospecha o infección confirmada por SARS-CoV-2 serán realizados por personal experimentado estratégicamente asignado |
| Promover la participación de los residentes de Aparato Digestivo en los procedimientos endoscópicos en pacientes con bajo riesgo de infección por SARS- CoV-2, siempre y cuando se disponga de los recursos necesarios que garanticen la seguridad del procedimiento |
| Evitar la toma de muestras biológicas durante la endoscopia cuando el impacto clínico del resultado sea previsiblemente marginal |
| Realizar el procesamiento de muestras biológicas siguiendo los protocolos estandarizados de bioseguridad para sustancias con alta capacidad infectiva |
| Posprocedimiento |
| Realizar la desinfección y reprocesamiento de los endoscopios siguiendo los protocolos habituales |
| No reutilizar los dispositivos de un solo uso |
| Asignar personal de limpieza dedicado exclusivamente a la Unidad de Endoscopia |
| Aplicar protocolos para la limpieza y desinfección de las salas de endoscopia y de los materiales que hayan contactado con el paciente o con sus secreciones |
| Gestionar los residuos siguiendo los protocolos locales de cada centro para material con alta capacidad infectiva categoría B (UN3291) |
| Mantener la distancia interpersonal de 1-2 m, las medidas de higiene básicas y el flujo independiente de pacientes en las salas de recuperación |
| Considerar la implantación de programas de seguimiento de los pacientes entre los 7-15 días después del procedimiento para valorar la aparición de síntomas compatibles con infección por SARS-CoV-2 |
PCR: detección de RNA viral por reacción en cadena de polimerasa.
La AEG y la SEED recomiendan que el reinicio de la actividad endoscópica se realice de forma escalonada, adaptada a los recursos locales y a la situación epidemiológica de la infección por SARS-CoV-2.
Aunque no es el único factor para evaluar el potencial de propagación de una enfermedad infecciosa, el número reproductivo básico (R0) define la media de infecciones secundarias producida por un caso en la población. Cuando R0 es <1, cada caso no llega a inducir una infección adicional, de manera que la población quedaría protegida. Las primeras estimaciones de R0 realizadas por la OMS, la situaban entre 1,4 y 2,5; recientemente, se han publicado valores ligeramente superiores (media de 3,28)3.
El valor de R0 a fecha de 16 de abril del 2020 en nuestro país es de 0,914. Al inicio de esta, fue superior a 7. El actual dato implica que la enfermedad deja de propagarse en la población. Sin embargo, este indicador es cambiante y depende de las medidas de control de la infección aplicadas.
La infección por SARS-CoV-2 presenta varios desafíos: no se dispone de vacunas ni de tratamientos eficaces y se desconoce la prevalencia en nuestra población y la duración de la inmunidad. Por tanto, no es posible prever si permanecerá como patógeno circulante o acabará desapareciendo. Además, modelos matemáticos recientes sugieren que algún tipo de distanciamiento social puede ser preciso hasta 20225. Por todo ello, predecir cuándo se podrá reanudar la actividad programada es complejo. Si establecemos el paralelismo con China, solo tras más de 3 meses después de la aparición de los primeros casos, el número de casos incidentes parece estabilizarse en cifras de 2dígitos. Según el reciente consenso Asia-Pacífico, la actividad endoscópica a plena capacidad debería plantearse cuando no se detectan casos incidentes durante al menos 2 semanas y los recursos de material de protección sean los óptimos6. Mientras se redactaba este documento se producían retrasos en la llegada del material y recepción de equipos de escasa o nula calidad7 en nuestro país. Algunos expertos estiman que la actividad asistencial, con las salas a su completa capacidad, puede llegar a suspenderse al menos durante 2-3 meses. Sin embargo, las nuevas solicitudes y la incidencia de enfermedades digestivas no se modificarán8. Aunque no se realice una mención expresa a la endoscopia digestiva, la Sociedad Española de Medicina Preventiva, Salud Pública e Higiene se posiciona expresamente por no establecer etapas en la fase de transición de la pandemia, sino por una respuesta adaptativa escalonada9. Por este motivo, la solución más razonable es llegar a un consenso para decidir qué exploraciones realizar con mayor inmediatez y cuáles posponer. Esta decisión debe individualizarse en función de la situación epidemiológica local y, si es posible, consensuarse con el Servicio de Medicina Preventiva.
¿Es preciso realizar una reevaluación de la indicación de la endoscopia previo al inicio de la reprogramación de actividad tras superar el pico de pandemia por SARS-CoV-2?Se recomienda reevaluar la indicación de la endoscopia y priorizar aquellas donde el beneficio esperado sea mayor.
Las UE de acceso abierto sufren, desde hace un largo período, una sobrecarga asistencial que se ha incrementado con la llegada de los programas de cribado de cáncer colorrectal (CCR). Evaluar la correcta indicación es una de las posibilidades que permiten reducir la mencionada sobrecarga. El objetivo de las guías que evalúan la adecuación de las peticiones endoscópicas como la europea European Panel on the Appropriateness of Gastrointestinal Endoscopy (EPAGE) es asistir a los profesionales en la toma de decisiones incrementando la probabilidad de detectar lesiones relevantes10.
El porcentaje de inadecuación se sitúa aproximadamente en un 30%11. Esto implica que, con la revisión de la inadecuación de 3 salas de endoscopias, se puede liberar una agenda completa para programar procedimientos adecuadamente solicitados. El potencial ahorro y la reducción del tiempo de espera son beneficios evidentes. La situación de parada de la actividad programada durante el pico de la pandemia hace necesario retomar estas herramientas.
¿Qué criterios se recomienda emplear para priorizar los procedimientos endoscópicos en nuestro medio?Se recomienda priorizar los procedimientos endoscópicos basándose en la probabilidad de encontrar lesiones clínicamente relevantes en función de la sintomatología y las pruebas complementarias, fundamentalmente un TSOH positivo en las colonoscopias y la presencia de anemia en las gastroscopias.
Entre las peticiones de procedimientos pendientes de reprogramación encontramos diferentes situaciones, aplicables a las peticiones más frecuentes, gastroscopia y colonoscopia: 1) exploraciones terapéuticas; 2) colonoscopia en el contexto de cribado de CCR tras test de sangre oculta en heces inmunológico (TSOH-i) positivo; 3) endoscopia por sintomatología de nueva aparición, y 4) seguimiento o vigilancia de enfermedades ya conocidas previamente.
ColonoscopiaTanto para este procedimiento como para la gastroscopia, las exploraciones terapéuticas constituyen los casos que se recomienda resolver con mayor celeridad para evitar, en lo posible, una pérdida de oportunidad.
En lo concerniente a la prioridad asignada al cribado poblacional, el estudio QUALISCOPIA demostró un mayor porcentaje de detección de adenomas (TDA) global (46,4% vs. 28,1%) y de adenomas avanzados (TDAA) (26,3% vs. 10,5%) en esta población cuando se ha comparado con esas proporciones en sujetos sintomáticos12. El porcentaje de casos con CCR, sin embargo, fue similar (5,1% vs. 4,5%). Algunos autores han recomendado emplear la cuantificación de hemoglobina fecal para asignar diferentes niveles de prioridad13. Sin embargo, un estudio reciente ha demostrado que no existen diferencias significativas en el número de CCR detectados ni en el de estadios avanzados cuando se comparan tiempos de espera inferiores a 30 días frente a aquellos de hasta 9 meses14. Otros estudios que han evaluado el tiempo en lista de espera de pacientes con CCR tampoco han observado diferencias en la proporción de casos más avanzados cuando se comparó la demora superior o inferior a 2 meses15.
En la tercera situación, cuando se trata de exploraciones solicitadas por síntomas de nueva aparición, parece razonable asignar un sistema de priorización en función de las indicaciones, datos clínicos disponibles y riesgo potencial de diagnosticar enfermedades relevantes. En los casos en los que, además de síntomas, se disponga de un TSOH-i positivo, parece razonable priorizar estos casos puesto que la clínica, de manera aislada, no predice adecuadamente la presencia de CCR. De hecho, con base en el estudio COLONPREDICT, los valores de hemoglobina fecal de manera aislada o combinados con modelos predictivos, demostraron mayor precisión que los síntomas para detectar CCR16. La combinación del TSOH-i y calprotectina fecal no han demostrado incrementar la precisión diagnóstica para detectar CCR17.
Por último, en lo que se refiere a pacientes ya incluidos en programas de vigilancia, parece razonable permitir mayor flexibilidad. Al menos, en lo que se refiere a la colonoscopia, el estudio de Mangas-Sanjuan et al. observó un riesgo de cáncer en indicaciones por seguimiento de pólipos del 0,8%, muy inferior al de los pacientes sintomáticos o con TSOH positivo, con un TDAA solo discretamente superior que el de los pacientes remitidos por síntomas12.
Desafortunadamente, en este contexto de exploraciones solicitadas por síntomas de nueva aparición, la evidencia científica sobre los tiempos en lista de espera que se consideran admisibles es escasa y los intervalos sugeridos son, frecuentemente, fruto de consensos de expertos18.
GastroscopiaEn un estudio italiano, las peticiones inadecuadas se cifraron en un 27%, pero alcanzaron el 50% cuando se trataba de pacientes con gastroscopia previa. La ausencia de lesiones relevantes alcanzó el 82,5%. Los factores que se correlacionaron con una mayor proporción de lesiones clínicamente relevantes (cáncer, enfermedad péptica, varices esofágicas, enfermedad celíaca, esófago de Barrett o displasia sobre gastritis atrófica) fueron la solicitud preferente, el adecuado seguimiento de las guías y el acuerdo en el nivel de prioridad entre atención primaria y especializada19.
Por otra parte, los circuitos de derivación como el propuesto por las guías del National Institute for Health and Care Excellence para pacientes con dispepsia o reflujo gastroesofágico, mayores de 55 años y refractarios al tratamiento no han demostrado que se detecten más lesiones malignas en ese grupo de pacientes20. Sin embargo, algunas indicaciones demostraron un valor predictivo positivo superior para el diagnóstico de cáncer. En orden de mayor a menor relevancia: disfagia, pérdida de peso con o sin anemia, dispepsia con anemia o pérdida de peso como signos de alarma, la presencia aislada de anemia y, por último, la dispepsia de manera aislada21.
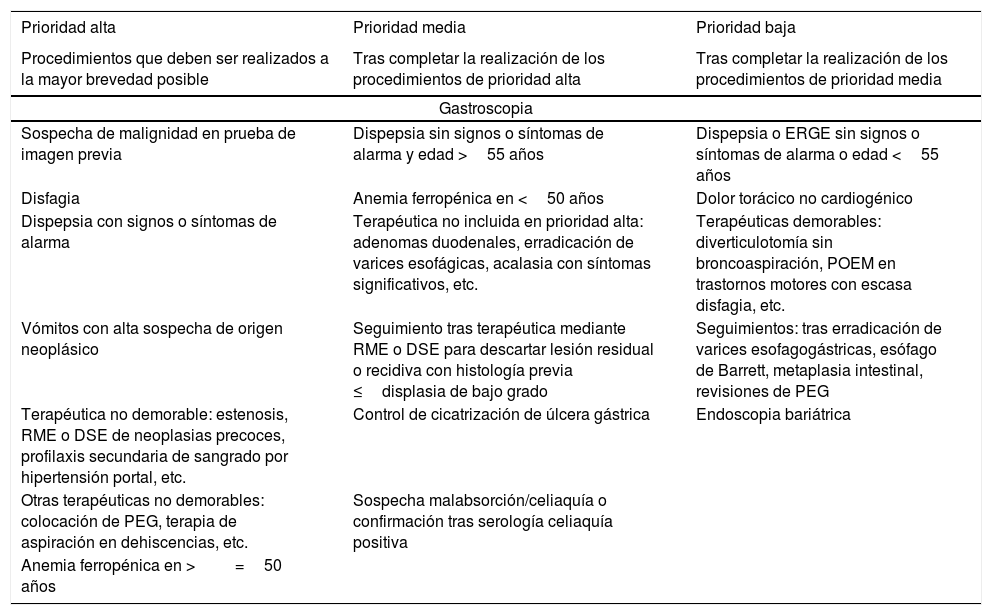
El presente documento incluye una tabla de prioridades (tabla 2 y de forma más detallada en el anexo, tabla suplementaria 2) estratificada por aquellos procedimientos más frecuentes. Para cada uno de estos procedimientos se ha definido una serie de motivos de petición que no pretende ser exhaustiva, sino únicamente servir de orientación para los responsables de las UE. Las recomendaciones descritas permiten su adaptación en función de la disponibilidad y situación local.
Tabla resumen de grupos de priorización en función de la indicación
| Prioridad alta | Prioridad media | Prioridad baja |
|---|---|---|
| Procedimientos que deben ser realizados a la mayor brevedad posible | Tras completar la realización de los procedimientos de prioridad alta | Tras completar la realización de los procedimientos de prioridad media |
| Gastroscopia | ||
| Sospecha de malignidad en prueba de imagen previa | Dispepsia sin signos o síntomas de alarma y edad >55 años | Dispepsia o ERGE sin signos o síntomas de alarma o edad <55 años |
| Disfagia | Anemia ferropénica en <50 años | Dolor torácico no cardiogénico |
| Dispepsia con signos o síntomas de alarma | Terapéutica no incluida en prioridad alta: adenomas duodenales, erradicación de varices esofágicas, acalasia con síntomas significativos, etc. | Terapéuticas demorables: diverticulotomía sin broncoaspiración, POEM en trastornos motores con escasa disfagia, etc. |
| Vómitos con alta sospecha de origen neoplásico | Seguimiento tras terapéutica mediante RME o DSE para descartar lesión residual o recidiva con histología previa ≤displasia de bajo grado | Seguimientos: tras erradicación de varices esofagogástricas, esófago de Barrett, metaplasia intestinal, revisiones de PEG |
| Terapéutica no demorable: estenosis, RME o DSE de neoplasias precoces, profilaxis secundaria de sangrado por hipertensión portal, etc. | Control de cicatrización de úlcera gástrica | Endoscopia bariátrica |
| Otras terapéuticas no demorables: colocación de PEG, terapia de aspiración en dehiscencias, etc. | Sospecha malabsorción/celiaquía o confirmación tras serología celiaquía positiva | |
| Anemia ferropénica en >=50 años | ||
| Colonoscopia | ||
| Sospecha de CCR por prueba de imagen o exploración física | Ferropenia sin anemia con gastroscopia sin lesiones | |
| TSOH-i positivoa | Rectorragia/hematoquecia (sin EII) en≥50 años, no urgente, con colonoscopia previa <5 años | Anemia ferropénica con colonoscopia previa (últimos 5 años) |
| Terapéutica no demorable: por ejemplo, dilatación de estenosis, resección de lesiones sugestivas de neoplasia avanzadab, etc. | Anemia ferropénica en <50 años sin factores de riesgo de CCRc | Seguimientos: pospolipectomía, CCR familiar, síndromes hereditarios, tras cirugía por CCR, etc. |
| Anemia ferropénica en>=50 años o con factores de riesgo de CCRc sin colonoscopia previa (últimos 5 años) | Estreñimiento crónico/distensión abdominal/dolor abdominal en> 50 años | Rectorragia/hematoquecia con colonoscopia previa <5 años |
| Rectorragia/hematoquecia (sin EII) en≥50 años, no urgente, sin colonoscopia previa | Sospecha de CCR por criterios clínicos (Guía NICE 2015 actualizada en 2017d) sin TSOH-i realizado | Cribado de displasia en paciente con EII |
| Evaluación de extensión, de actividad o deterioro clínico en EII (excluido cribado de displasia) | Estudio tras episodio de diverticulitis aguda complicada o con diagnóstico incierto | Estreñimiento crónico/distensión abdominal/dolor abdominal no incluido en prioridad media |
| Melenas con gastroscopia sin lesiones | Resección compleja (RME o UEMR) de lesiones con baja probabilidad de neoplasia avanzada | Diarrea crónica no indicativa de EII |
| Alta sospecha clínica de EII | Evaluación tras resección fragmentada (descartar recidivas) | |
| Cambio del ritmo intestinal de reciente comienzo en <50 años | ||
| CPRE | ||
| Coledocolitiasis sintomática sin colangitis | Ampulectomía | Sospecha de disfunción del esfínter de Oddi |
| Fugas y estenosis biliopancreáticas | Coledocolitiasis asintomática sin colangitis | Recambio o retirada programada de prótesis biliar |
| Colangioscopia intraductal por enfermedad benigna | Terapéuticas pancreáticas | |
| Estudio de pancreatitis recurrente | ||
| Litotricia en paciente con vía biliar ya drenada | ||
| USE | ||
| Estadificación neoplasias esofago-gástricas y bilio-pancreáticas | Sospecha de tumor neuroendocrino pancreático | Estudio+/– PAAF de lesiones subepiteliales |
| Drenaje de colecciones pancreáticas y vesícula biliar | PAAF de probable recidiva neoplásica | Estudio pancreatitis recidivante idiopática |
| PAAF de lesiones focales sólidas de páncreas | Sospecha de coledocolitiasis | Estudio probable pancreatitis crónica |
| PAAF de adenopatías y otras lesiones en contexto de neoplasia | Estudio+/– PAAF de lesiones quísticas pancreáticas con signos de riesgo | Diagnóstico y seguimiento de NMPI/lesiones pancreáticas quísticas sin signos de riesgo |
| Derivaciones biliares o gastroentéricas paliativas | Cribado de neoplasia de páncreas en población de riesgo | |
| PAAF de glándula suprarrenal patológica | Estudio de dilatación biliar o pancreática incidentales | |
| Cápsula endoscópica | ||
| Anemia con origen en ID con repercusión clínica/analítica/hemodinámica | Anemia con origen en ID sin repercusión clínica/analítica/hemodinámica | Seguimiento de síndromes hereditarios de neoplasias gastrointestinales con afectación de ID |
| Sospecha de neoplasia en ID | Sospecha de EII y síntomas moderado-graves | Paciente con EII: estudio de extensión |
| Paciente con EII sintomático y no respuesta a tratamiento médico habitual | ||
| Enteroscopia | ||
| Lesión indicativa de malignidad en el ID en prueba de imagen previa | Lesión no indicativa de MG en pruebas de imagen previas | Lesiones causantes de HDOO sin repercusión clínica/analítica/hemodinámica |
| Lesiones causantes de HDOO con repercusión clínica/analítica/hemodinámica | ||
| Terapéutica en estenosis ID | ||
Esta tabla de priorizaciones es orientativa y no sustituye al buen juicio del clínico. No se incluyen procedimientos urgentes o muy preferentes que se habrán realizado durante la fase de pandemia.
CCR: cáncer colorrectal; CPRE: colangiopancreatografía retrógrada endoscópica; DSE: disección submucosa endoscópica; EII: enfermedad inflamatoria intestinal; ERGE: enfermedad por reflujo gastroesofágico; HDOO: hemorragia digestiva de origen oculto; ID: intestino delgado; NMPI: neoplasia mucinosa papilar intraductal; PAAF: punción por aspiración con aguja fina; PEG: gastrostomía percutánea; POEM: miotomía peroral endoscópica; RME: resección mucosa endoscópica; TSOH-i: test de sangre oculta en heces inmunológico; UEMR: resección mucosa endoscópica underwater; USE: ultrasonografía endoscópica.
Lesión avanzada: adenoma≥10mm, componente velloso o displasia de alto grado. Lesión serrada≥10mm o con displasia.
Se establecen 3estratos de priorización: 1) alta: procedimientos que se reprogramarán en primer lugar; 2) media: exploraciones que se deberán realizar a continuación de las anteriores, y 3) baja: técnicas endoscópicas que se reprogramarán a continuación de las previas. Asimismo, se ha considerado un estado adicional que se asigna a procedimientos de prioridad baja o de vigilancia, en el que la técnica se considera susceptible de una demora adicional, de entre 6 y 12 meses. Por otra parte, se han incluido algunas situaciones en las que se considera que el procedimiento puede suspenderse, en función de los datos consignados en el motivo de petición, o en los que el facultativo peticionario debería reevaluar la necesidad de estos (anexo, tabla suplementaria 2). Se recomienda tener en cuenta no solo los motivos de petición, sino otras circunstancias. El acceso a la historia clínica y una valoración más precisa de la solicitud, el tiempo en lista de espera, la demora aceptable según los diferentes tipos de prioridad o factores psicosociales que afecten a determinados pacientes serían algunas de ellas.
Se ha preferido no establecer intervalos de tiempo definidos por las siguientes razones: 1) la evolución de la pandemia es difícilmente previsible; 2) se desconoce en qué marco temporal las UE podrán retomar su actividad programada habitual; 3) la escasa y heterogénea evidencia disponible en lo que a tiempos de espera se refiere, y 4) las diferentes situaciones locales de cada unidad.
Se recomienda monitorizar los resultados del plan de priorización.
Finalmente, se recomienda que siempre que sea factible, y en función de los recursos de la institución, se recopilen indicadores cuantificables que permitan evaluar los resultados y el impacto de la estrategia expuesta en el presente documento, a fin de evaluar la consecución de los objetivos propuestos. Estos indicadores deben reevaluarse con frecuencia a fin de minimizar los riesgos para los pacientes en lista de espera y, en caso de ser preciso, modificar el plan de asignación de prioridades.
¿Se deben articular circuitos específicos de gestión para establecer los diferentes niveles de prioridad?Se recomienda establecer un registro de las solicitudes evaluadas en la lista de espera de procedimientos endoscópicos, su nivel de prioridad y los motivos de anulación, cuando corresponda.
La evidencia disponible acerca de sistemas específicos de gestión en lo que concierne a la priorización de la actividad endoscópica es escasa. La formación de equipos de trabajo entre los médicos de familia, especialistas de Aparato Digestivo y el jefe de Servicio de la especialidad mostró inicialmente, en un estudio italiano, una reducida concordancia en la asignación de los niveles de prioridad22 cuando se crean los denominados grupos homogéneos de demora (GHD), pero mejora con el paso del tiempo19. Estos GHD asignan a cada petición una categoría de priorización y un tiempo máximo de espera por categoría, independientemente de si se trata de gastroscopias o colonoscopias.
En los centros en los que ya se disponga de sistemas de discusión de la adecuación de procedimientos similar al mencionado y cuyo funcionamiento sea el adecuado, parece razonable mantenerlos. Cuando este no sea el caso, se recomienda establecer un registro de las solicitudes evaluadas pendientes de reprogramación en el que se refleje el motivo de solicitud, el nivel de prioridad asignado, así como el motivo de anulación del procedimiento en su caso6.
Se recomienda registrar en la historia clínica el motivo de suspensión de un procedimiento programado cuando este se anule por considerarse inadecuado.
En cuanto a las solicitudes consideradas inadecuadas, cuya reprogramación se considerará no indicada, se recomienda reflejar en la historia clínica del paciente la causa de anulación, así como un comentario descriptivo que justifique dicha decisión en función de las guías de práctica clínica (GPC) o los documentos de posicionamiento. Sería recomendable, adicionalmente, sugerir pautas de actuación alternativas basadas en GPC.
¿Se deben establecer circuitos de comunicación entre los proveedores de servicios de salud para informar acerca de modificaciones en la programación de los procedimientos pendientes de realización?Se recomienda asegurar una adecuada transmisión de la comunicación entre los diferentes agentes implicados en el proceso: especialistas evaluadores, facultativos peticionarios y pacientes.
Como en el caso anterior, en los centros donde ya existan los equipos de trabajo multidisciplinares mencionados, el circuito de comunicación y el ciclo de mejora continua estarán establecidos y continuarán siendo la herramienta de comunicación fundamental.
Cuando esta herramienta no esté disponible, se recomienda que cada centro decida localmente la manera más adecuada de establecer la comunicación entre los usuarios del sistema sanitario, los médicos peticionarios y los especialistas evaluadores de la adecuación y priorización. Se recomienda, al menos, informar de los procedimientos anulados. Esta comunicación debe transmitirse tanto al médico peticionario como al propio paciente.
¿Se debe realizar un cribado de la infección por SARS-CoV-2 en todos los pacientes antes de un procedimiento endoscópico?Se recomienda el cribado de infección por SARS-CoV-2 en todos los pacientes mediante una anamnesis dirigida a detectar síntomas o signos de COVID-19.
La prevención y el control de la infección permite asegurar la seguridad del personal sanitario y de los pacientes. Existen múltiples publicaciones que apoyan el cribado para detectar infección por SARS-CoV-2, aunque no exista consenso en cuál es la mejor estrategia6,23–26. No se dispone de estudios comparativos que permitan establecer cuál es la medida más coste-efectiva para el cribado.
Se recomienda interrogar por síntomas respiratorios, presencia de fiebre, riesgo ocupacional o contactos recientes con pacientes diagnosticados de COVID-19, tomar la temperatura y valorar la inclusión de cuestiones dirigidas a detectar manifestaciones gastrointestinales, anosmia y ageusia6,23,24. Se ha recomendado realizar esta anamnesis dirigida, si es posible, el día previo al procedimiento y antes de la entrada del paciente a la UE25,27. No existen estudios que evalúen la validez diagnóstica de este cribado mediante anamnesis y síntomas, pero el coste de dicha estrategia es mínimo. Podría argumentarse que las manifestaciones gastrointestinales de la COVID-19 pueden solaparse con la indicación de la prueba. Según un metaanálisis reciente, las manifestaciones digestivas más frecuentes son la anorexia (26,8%), la diarrea (12,5%), las náuseas o los vómitos (10,2%) y el dolor abdominal (9,2%), siendo más frecuentes en pacientes con enfermedad grave28. En una serie occidental reciente, donde se detalla la cronicidad de la sintomatología, ninguno de los pacientes desarrolló síntomas gastrointestinales de forma aislada o como forma de presentación de la COVID-1929. Por lo tanto, ante la presencia de síntomas gastrointestinales en la anamnesis de cribado, se debe prestar atención a su temporalidad (aguda en el COVID-19 vs. crónica en la mayoría de los procedimientos programados) y a la presencia de sintomatología concomitante, para así individualizar la decisión.
Existen diferentes pruebas de laboratorio para diagnosticar la infección por SARS-CoV-2: PCR, test de antígeno rápido y estudios serológicos27. Las pruebas de antígeno rápido poseen la ventaja de la inmediatez, pero su sensibilidad es insuficiente30.
En China, además de este triaje, se solicita analítica y una TAC torácica, puesto que los hallazgos radiológicos pueden preceder a la positivización de la PCR26. Esta estrategia, sin embargo, es difícilmente generalizable en países occidentales. Además, el día del procedimiento se realiza una PCR rápida si el procedimiento es urgente (3 h de demora). En los procedimientos electivos, 3días antes del procedimiento se realiza una PCR. Si esta resulta negativa, se realiza la endoscopia. En los sujetos con resultado positivo, se pospone el procedimiento31,32.
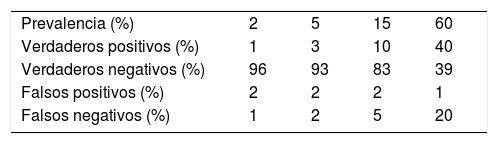
En cualquier caso, para que estos resultados sean precisos, además de exigir sensibilidad suficiente a las pruebas diagnósticas, se debe conocer la prevalencia de la enfermedad en la población local. Solo con este dato, además de los parámetros de validez del test, es factible obtener la probabilidad posprueba de que un paciente concreto sea portador de la enfermedad31. Estos cálculos se pueden realizar de manera intuitiva mediante herramientas online gratuitas (https://calculator.testingwisely.com/playground). En la tabla 3 se presenta la variación en la identificación de casos, manteniendo la sensibilidad y la especificidad de la prueba mientras que se varía únicamente la prevalencia del 2 al 60%.
Exactitud de una prueba diagnóstica en función de la prevalencia
| Prevalencia (%) | 2 | 5 | 15 | 60 |
| Verdaderos positivos (%) | 1 | 3 | 10 | 40 |
| Verdaderos negativos (%) | 96 | 93 | 83 | 39 |
| Falsos positivos (%) | 2 | 2 | 2 | 1 |
| Falsos negativos (%) | 1 | 2 | 5 | 20 |
Ejemplos teniendo en cuenta una sensibilidad del 67% y una especificidad del 98% (razón de verosimilitud positiva=33; razón de verosimilitud negativa=0,34) correspondientes a los descritos para PCR en detección de COVID-19 en los primeros días de aparición de los síntomas.
Actualmente, no existe evidencia científica de calidad que avale el cribado de la infección por SARS-CoV-2 mediante PCR o detección de anticuerpos previo a la realización de procedimientos endoscópicos. Por el momento, su rendimiento diagnóstico en contextos diferentes del de los pacientes sintomáticos es poco conocido y conlleva considerables dificultades de interpretación.
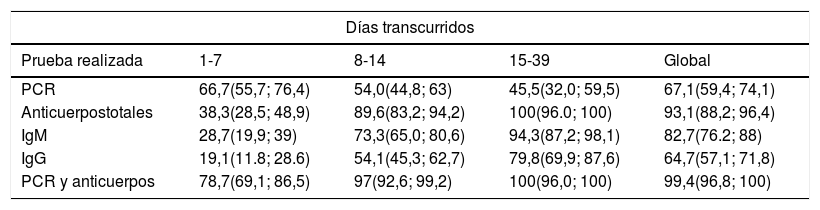
Asimismo, es preciso conocer que la sensibilidad varía en función del período de la infección, según se muestra en la tabla 433. La situación que maximiza la probabilidad de una correcta clasificación de los casos, asumiendo una adecuada disponibilidad de recursos, es la combinación de PCR y de niveles de anticuerpos durante la fase sintomática de la infección o cuando se encuentra en fase de resolución. Sin embargo, incluso con ambas en combinación, la sensibilidad continúa siendo inferior al 80% durante la primera semana de la infección o en sujetos con sintomatología incipiente. De hecho, aunque a partir de la tercera y cuarta semanas los niveles de anticuerpos poseen alta sensibilidad para detectar contagio previo, la PCR presenta baja sensibilidad para confirmar infección activa. Además, los datos que existen sobre su precisión diagnóstica en la fase presintomática o en individuos en los que la infección cursa de manera asintomática son escasos. Una aproximación a la interpretación de los resultados de estos test se presenta en la tabla 534. Se debe considerar, además del riesgo que supone un falso negativo para el personal sanitario y el resto de los pacientes, los inconvenientes asociados a los falsos positivos. Las implicaciones para estos últimos pueden ser leves (aislamiento durante al menos 14 días para el sujeto y sus contactos, así como ausencias laborales por incapacidad temporal) o de índole más importante (aumento de la probabilidad de contagio al pasar por circuitos destinados a pacientes con COVID-19 o incremento de la demora diagnóstico-terapéutica en varias semanas adicionales). La esperable y deseable reducción de la prevalencia de la infección en la población llevará asociada una disminución del valor predictivo positivo de las pruebas y, por tanto, un incremento de los falsos positivos al emplearlas como técnicas de cribado universal.
Sensibilidad (%) e intervalo de confianza del 95% de las pruebas de detección para infección por SARS-CoV-2 estratificada por los días transcurridos desde la aparición de sintomatología
| Días transcurridos | ||||
|---|---|---|---|---|
| Prueba realizada | 1-7 | 8-14 | 15-39 | Global |
| PCR | 66,7(55,7; 76,4) | 54,0(44,8; 63) | 45,5(32,0; 59,5) | 67,1(59,4; 74,1) |
| Anticuerpostotales | 38,3(28,5; 48,9) | 89,6(83,2; 94,2) | 100(96.0; 100) | 93,1(88,2; 96,4) |
| IgM | 28,7(19,9; 39) | 73,3(65,0; 80,6) | 94,3(87,2; 98,1) | 82,7(76.2; 88) |
| IgG | 19,1(11.8; 28.6) | 54,1(45,3; 62,7) | 79,8(69,9; 87,6) | 64,7(57,1; 71,8) |
| PCR y anticuerpos | 78,7(69,1; 86,5) | 97(92,6; 99,2) | 100(96,0; 100) | 99,4(96,8; 100) |
PCR: detección de RNA viral por reacción en cadena de polimerasa.
Modificado de Zhao et al.33.
Interpretación simplificada de las pruebas diagnósticas de infección por SARS-CoV-2
| PCR | IgM | IgG | Diagnóstico |
|---|---|---|---|
| – | – | – | Negativo o fase presintomática con falso negativo de la PCR |
| + | – | – | Fase inicial de infección. Período ventana |
| + | + | – | Fase temprana de infección |
| + | + | + | Fase activa de infección |
| + | – | + | Fase avanzada de infección o reactivación |
| – | + | – | Estadio temprano. Probable falso negativo de la PCR |
| – | + | + | Enfermedad en evolución. Probable fase de recuperación |
| – | – | + | Fase de resolución de infección. A descartar reactivación con falso negativo de la PCR |
PCR: Detección de RNA viral por reacción en cadena de polimerasa.
Para mayor detalle, se recomienda consultar el documento oficial del Ministerio de Sanidad en colaboración con la Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica35.
Se recomienda demorar los casos electivos sospechosos de COVID-19. El resto se llevará a cabo como si todos los pacientes estuvieran potencialmente infectados mientras la situación epidemiológica en esa zona geográfica sea de alto riesgo de transmisión de la infección.
Por otra parte, disponer de PCR y serología no permite discriminar por completo si un individuo puede transmitir o no la enfermedad. Esto se debe a que se han descrito casos que han superado el proceso agudo y, posteriormente, han presentado positividad de la PCR, bien por reactivación o bien por presencia de restos del ARN viral. En estos casos, la PCR se positivizó en un rango de entre 4 a 17 días tras la negativización previa36. Tampoco existen datos acerca de si un individuo que ha superado la enfermedad se puede reinfectar y pasar a un estado de portador asintomático. Asimismo, aún se desconoce si los anticuerpos son o no protectores y, si lo son, durante cuánto tiempo. Ante esta compleja situación no es factible, en función incluso de pruebas combinadas (PCR y serología), decidir si se emplean o no medidas adicionales de protección. Adicionalmente, es probable que no se disponga del recurso de estas pruebas imperfectas y no existen, por el momento, datos clínicos de coste-efectividad de estas medidas. Por todo ello, parece razonable el empleo de equipos de protección individual (EPI) para todos los procedimientos mientras la prevalencia de la enfermedad en la población sea elevada y cribar con la anamnesis y la toma de temperatura. En los pacientes con sospecha, se demorará el procedimiento. Se prevé que, con el descenso de la incidencia de la infección en la población, se reduzca el número de falsos negativos de los test pero se incremente el de falsos positivos. Finalmente, estos supuestos pueden modificarse con el transcurso del tiempo: reducciones sustanciales en la prevalencia de la infección, la aparición de nuevos test con mayor sensibilidad y una precisión diagnóstica más independiente de la fase en que se encuentre la enfermedad pueden reducir drásticamente los falsos negativos37.
¿Es recomendable establecer reuniones diarias del personal de la UE donde se discuta específicamente el método de trabajo?Se recomienda establecer reuniones de todo el equipo de la UE al inicio de cada jornada para dar a conocer los protocolos de actuación y asegurar su cumplimiento.
La capacidad de toma de decisiones, la comunicación entre los estamentos del personal sanitario y con el paciente, la previsión de situaciones complejas, así como la capacidad de liderazgo son claves para formar equipos exitosos36. En la situación actual de alto riesgo de transmisión de la infección por SARS-CoV-2 en el entorno hospitalario, es crítico revisar los protocolos de la UE en relación con la circulación de los pacientes y acompañantes, las estrategias de cribado de COVID-19, la disponibilidad de EPI y las medidas de desinfección de las salas y equipos de endoscopia. Cada miembro del equipo debe conocer el flujo de trabajo y se deben definir claramente las responsabilidades.
Se recomienda el uso de mascarilla quirúrgica, así como el distanciamiento físico aconsejado por la OMS durante las reuniones del equipo de trabajo.
Dado que las pautas de actuación se encuentran en constante evolución, parece razonable que se establezcan reuniones con periodicidad diaria25. Es recomendable que los representantes de cada uno de los grupos de trabajo se reúnan en una zona amplia, adecuadamente ventilada y siguiendo las recomendaciones de distanciamiento físico y uso de mascarillas quirúrgicas establecidas27,38.
¿Debe limitarse la entrada de acompañantes a la UE?Se recomienda que los acompañantes del paciente no accedan al interior de la UE salvo en casos seleccionados. En caso de que su acceso sea imprescindible, deben someterse al cribado de SARS-CoV-2.
Según las recomendaciones de la European Society of Gastrointestinal Endoscopy (ESGE), los familiares o cuidadores no deberían acceder al interior de la UE27. Si esto se precisara, de manera excepcional, se recomienda evaluar su riesgo de la misma manera que se realiza el cribado de SARS-CoV-2 en los pacientes30. Estas mismas recomendaciones se contemplan en otras publicaciones6,24,38.
¿Se debe recomendar alguna medida de protección para los pacientes que acceden a la unidad de endoscopia?Se recomienda que los pacientes mantengan una distancia interpersonal mínima de 1-2 m durante su paso por la UE.
Se recomienda facilitar a los pacientes mascarillas quirúrgicas, ropa hospitalaria y una adecuada higiene de manos.
La medida general recomendada por la OMS en lo concerniente al distanciamiento físico es aplicable en el entorno de las UE. La distancia mínima recomendada debe ser de 1 m27,38. Se proveerá a los pacientes, para su entrada a la UE, de mascarilla quirúrgica y, si existe disponibilidad logística, ropa hospitalaria24,39. Asimismo, se recomienda tomar las medidas necesarias para facilitar la higiene de manos (agua corriente y jabón o solución hidroalcohólica) al menos antes de entrar a la UE y a la salida. Estas medidas se mantendrán o retirarán paulatinamente en función de la situación epidemiológica.
¿Es necesario modificar el tiempo habitual recomendado a cada procedimiento endoscópico?Se recomienda reajustar el tiempo asignado a cada endoscopia y el volumen de procedimientos debido a la necesidad de implantación de medidas de seguridad e higiene adicionales.
Es previsible que la circulación de pacientes en la UE se ralentice debido al cribado de la infección por SARS-CoV-2 y las medidas de higiene. Por lo que respecta al personal sanitario, la necesidad de colocarse y retirarse el EPI podría reducir discretamente el tiempo disponible que dedicar a las exploraciones. Asimismo, cada UE debería acordar con los servicios de limpieza los momentos en los que se realizará la desinfección de las salas. En la situación ideal de limpieza entre cada procedimiento, esto añadirá una demora adicional.
Además, mientras no se logre la contención de la pandemia, es prioritario reducir la exposición de la población al medio hospitalario. Esto implica reducir la concentración de personas en las salas de espera para lograr el adecuado distanciamiento físico. La forma más razonable de lograrlo es la reducción de la actividad endoscópica electiva en cada una de las salas de exploración24. La planificación en turnos de mañana y tarde, si existe disponibilidad, es aconsejable para espaciar los procedimientos y mantener la actividad endoscópica.
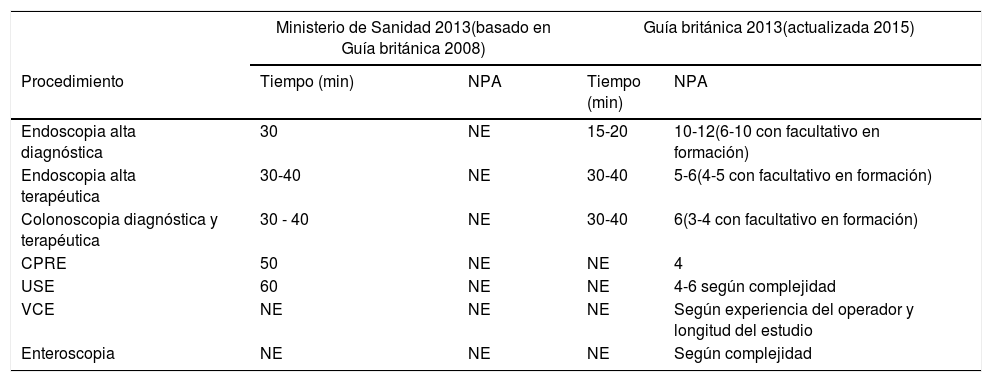
Actualmente, el Ministerio de Sanidad tiene publicados unos tiempos asignados a procedimientos endoscópicos basados en la GPC británica del año 2008 y únicamente reflejan el tiempo a dedicar para cada procedimiento, pero no el volumen total de ellos por jornada laboral. Tampoco tiene en cuenta los tiempos para procedimientos de especial complejidad como la resección mucosa de lesiones extensas, la disección endoscópica o la enteroscopia. En la tabla 6 se presentan las recomendaciones actuales en España y la última edición de la GPC británica.
Comparación de las Recomendaciones de tiempo y número de procedimientos a asignar por agenda de endoscopias entre los Estándares del Ministerio de Sanidad y la Guía del Royal College of Physicians
| Ministerio de Sanidad 2013(basado en Guía británica 2008) | Guía británica 2013(actualizada 2015) | |||
|---|---|---|---|---|
| Procedimiento | Tiempo (min) | NPA | Tiempo (min) | NPA |
| Endoscopia alta diagnóstica | 30 | NE | 15-20 | 10-12(6-10 con facultativo en formación) |
| Endoscopia alta terapéutica | 30-40 | NE | 30-40 | 5-6(4-5 con facultativo en formación) |
| Colonoscopia diagnóstica y terapéutica | 30 - 40 | NE | 30-40 | 6(3-4 con facultativo en formación) |
| CPRE | 50 | NE | NE | 4 |
| USE | 60 | NE | NE | 4-6 según complejidad |
| VCE | NE | NE | NE | Según experiencia del operador y longitud del estudio |
| Enteroscopia | NE | NE | NE | Según complejidad |
CPRE: colangiopancreatografía retrógrada endoscópica; NE: no especificado; NPA: número de procedimientos por agenda; USE: ecoendoscopia; VCE: videocápsula endoscópica.
* Incluye todo el proceso: sedación, procedimiento e informe.
Fuente: Guía del Royal College of Physicians40.
En definitiva, si bien el tiempo dedicado al propio procedimiento podría no variar sustancialmente, es previsible que los tiempos periprocedimiento se prolonguen significativamente. El porcentaje de ocupación de los gabinetes de endoscopia dependerá de la fase de descenso de la incidencia de infectados y de la disponibilidad de recursos físicos y materiales, incluyendo la capacidad de las salas de espera para poder garantizar la distancia mínima interpersonal de un metro.
Procedimiento¿Es necesario establecer un circuito independiente para los pacientes con alta sospecha o infección confirmada por SARS-CoV-2?Se recomienda establecer un circuito de pacientes independiente para los pacientes con alta sospecha o infección confirmada por SARS-CoV-2.
El virus SARS-CoV-2 puede permanecer en superficies durante más de 3 días y suspendido en aerosoles durante 3 h o más41. Teniendo en cuenta su mecanismo de transmisión, recomendamos que se establezca un circuito separado físicamente para los pacientes con alta sospecha o infección confirmada6,23,27,42,43. La independencia de ambos circuitos debe mantenerse antes, durante y después de la endoscopia. Este circuito debe incluir un lavabo y un inodoro para el paciente, dado que la corriente de aspiración que se produce durante la evacuación de residuos fecales genera aerosoles que podrían tener capacidad infectiva44.
Es aconsejable que las endoscopias en pacientes con alta sospecha o infección confirmada que no se puedan demorar se realicen en salas con presión negativa, y espaciar los procedimientos al menos 30 min6,45. Si la UE no está equipada con una sala de este tipo, como ocurre frecuentemente en nuestro medio, recomendamos realizar el procedimiento en una sala con presión negativa localizada fuera de la unidad. En caso de no disponer de una sala de presión negativa en el centro, se recomienda habilitar una sala con ventilación abierta y entornos separados para este grupo de pacientes y promover la instalación de un sistema de presión negativa. Por último, recomendamos programar estos procedimientos al final de cada turno si la condición clínica del paciente lo permite.
¿Qué medidas de higiene y protección deben implementarse para el personal sanitario? ¿Si no se dispone de equipos de protección personal, se debe realizar la endoscopia? ¿Es recomendable descontaminar y reutilizar las mascarillas FFP2-3/N95?Se recomienda fomentar la aplicación de medidas básicas de higiene para la prevención de la infección en todo el personal.
La higiene de manos es una medida fundamental que ha demostrado su efectividad en numerosos ensayos clínicos y metaanálisis46,47. La implementación de programas que garanticen una correcta higiene de manos mejora su efectividad y debe asegurarse en todas las UE48. El cambio de uniforme al final de cada jornada y la ducha antes de abandonar el centro hospitalario son medidas de higiene básica recomendadas por el Centro Europeo para la Prevención y Control de Enfermedades (European Center for Disease Prevention and Control [ECDC])49.
Se recomienda la utilización de EPI en todo el personal sanitario involucrado en la realización de un procedimiento endoscópico.
No se ha encontrado ningún estudio que compare diferentes EPI en la epidemia por SARS-CoV-2. El Ministerio de Sanidad indica que el EPI deberá estar certificado con base en el Reglamento (UE) 2016/425, lo cual queda evidenciado por el marcado CE de conformidad50.
La ESGE y la guía Asia-Pacífico sugieren que el EPI puede decidirse en función del riesgo de infección del paciente, siendo la principal diferencia el tipo de mascarilla (quirúrgica en bajo riesgo o FFP2-3 en alto riesgo) y de bata (protección mínima o moderada). Recomendamos que todos los procedimientos se realicen con el equipo detallado en la tabla 7, independientemente del riesgo a priori de infección del paciente. La decisión de no estratificar el EPI se debe a múltiples razones: 1) el nivel de la epidemia en nuestro país; 2) la posibilidad de generación de aerosoles; 3) la ausencia de estrategias de cribado de la infección validadas, y 4) garantizar la máxima seguridad del personal sanitario. Se recomienda habilitar una zona limpia para la colocación del EPI, separada físicamente de la sala de endoscopia. Nuestras recomendaciones sobre EPI se basan en las directrices de la OMS, el ECDC, el Gobierno de España y de otras sociedades científicas6,27,45,49,50,53,54.
Equipos de protección individual recomendados en la Unidad de Endoscopia
| Lugar | Equipo de protección individual |
|---|---|
| Sala de endoscopia | Mascarilla FFP2-FFP3/N95-N99/PAPRaGorro desechableBata resistente a penetración de microorganismos de manga larga desechableDoble guanteProtector ocular hermético o pantalla protectora facialProtector de zapatos desechable o calzado cerrado impermeable fácilmente lavable |
| Sala de limpiezaSala de procesamiento de biopsias | Mascarilla quirúrgica/FFP2/N95bBata resistente a penetración de microorganismos de manga larga desechableGuantesProtector ocular o pantalla protectora facialProtector de zapatos desechable o calzado cerrado impermeable fácilmente lavable |
| Zona de recepción o triaje | Mascarilla quirúrgicaDistancia de 1-2 mGuantes (opcional)Barrera física o pantalla protectora |
| Área administrativa | Mascarilla quirúrgica (opcional)Distancia de 1-2 mBarrera física si hay disponibilidad |
| Sala de espera | Mascarilla quirúrgicaDistancia de 1-2 m |
PAPR: powered air purifying respirator.
En línea con la American Gastroenterological Association, recomendamos la utilización de mascarillas FFP2-3/N95-N99 en pacientes clasificados como de bajo riesgo de infección45. El uso de mascarillas FFP3 es preferible en pacientes con alta sospecha o infección confirmada. Las mascarillas deben cumplir con la norma UNE-EN 149:2001+A1:200950. Si hay disponibilidad, se recomienda utilizar una mascarilla FFP2-3/N95-99 por paciente, ya que la endoscopia genera aerosoles que pueden contaminar la superficie de la mascarilla. No existe evidencia que avale la seguridad de la reutilización (> 5 usos) o el uso prolongado (> 8-12 h) en la pandemia por SARS-CoV-245,55. La OMS y el Ministerio de Sanidad sugieren que la vida útil de la mascarilla podría prolongarse en situación de escasez de recursos50,54. La colocación de una mascarilla quirúrgica desechable por encima es otra medida que reduce el riesgo de contaminación de la mascarilla FFP2-3/N95-99 y podría servir para prolongar su vida útil55. La desinfección y la reutilización de mascarillas solo debe considerarse como último recurso55. En este escenario, es fundamental que dichas acciones se lleven a cabo dentro de un protocolo avalado a nivel institucional.
Bata protectoraSe debe asegurar la protección del uniforme del trabajador de la posible salpicadura de fluidos biológicos o secreciones. Aunque las GPC no especifican el tipo de bata de elección para la endoscopia, este material debe cumplir con la norma UNE-EN 14126:2004 que contempla ensayos específicos de resistencia a la penetración de microorganismos50. Se recomienda que estas batas sean desechables para evitar el potencial contagio entre pacientes50. Los Centers for Disease Control and Prevention (CDC) y el ECDC recomiendan utilizar una bata impermeable por procedimiento generador de aerosoles en pacientes con alta sospecha o infección confirmada (no necesariamente con categoría de bata quirúrgica)49,56. Si no existe esta disponibilidad de recursos, se contempla la posibilidad de emplear batas reutilizables tratadas mediante protocolos de lavado estandarizados o batas plásticas desechables por encima de batas de mayor impermeabilidad56.
Todos los profesionales sanitarios de las UE deben recibir formación sobre la utilización de EPI. El entrenamiento en el uso de EPI ha demostrado disminuir el riesgo de contaminación inadvertida y es un requisito para su utilización57–59.
Protector ocular o facialEs fundamental garantizar la adecuada protección facial y ocular durante la endoscopia. Un estudio reciente demostró que las salpicaduras inadvertidas a la cara del endoscopista son relativamente frecuentes. La tasa de exposición a microorganismos con capacidad infectiva fue de 5,6 por cada 100 días de endoscopia60. El tipo de exposición que tiene lugar durante la endoscopia digestiva hace que los dispositivos recomendados sean las gafas integrales (conforme a normativa UNE-EN 166:2002) y las pantallas faciales50.
GuantesLos guantes deben ser desechables y cumplir con la normativa UNE-EN ISO 374.5:2016. El uso de doble guante frente a guante único ha demostrado disminuir el riesgo de contaminación durante la retirada del EPI45,61. El uso de guantes no es necesario en el personal administrativo que no mantenga contacto con el paciente50.
Se recomienda en contra de realizar un procedimiento endoscópico si no se dispone de los equipos de protección necesarios para garantizar la seguridad de la endoscopia.
El personal sanitario implicado en la endoscopia digestiva presenta un alto riesgo de infección62,63. La utilización de EPI adecuados es fundamental no solo para salvaguardar la salud del personal sanitario, sino para evitar que se conviertan en trasmisores del virus. Se debe exigir a las autoridades competentes que garanticen la disponibilidad de EPI adecuados. En línea con las recomendaciones del ECDC, recomendamos asegurar la disponibilidad de 3-6 EPI completos por procedimiento para asegurar la protección de todo el personal sanitario49.
En los procedimientos con alta probabilidad de generación de aerosoles, ¿es recomendable emplear métodos de barrera adicionales sobre el área nasobucal del paciente o sobre las válvulas del endoscopio?Se recomienda no utilizar de forma sistemática barreras adicionales sobre el área nasobucal del paciente o sobre las válvulas del endoscopio. La utilidad y la eficiencia de estas medidas deben evaluarse en el seno de protocolos de investigación.
No se han encontrado recomendaciones a este respecto ni estudios que demuestren el beneficio de dispositivos adicionales sobre el área nasobucal. Se han publicado series de casos y casos clínicos de endoscopia urgente realizada durante la epidemia en las que se utilizaron dispositivos de barrera adicionales64,65. Sin embargo, se desconocen el beneficio y la eficiencia de estas medidas.
¿Se debe adoptar alguna precaución especial durante la oxigenoterapia en la sedación?Se recomienda que en pacientes con alta sospecha o infección confirmada por SARS-CoV-2 que se realicen una colonoscopia, la oxigenoterapia se suplemente con mascarillas con filtro de exhalado. Si no se dispone de estos dispositivos, recomendamos colocar una mascarilla quirúrgica por encima de las gafas nasales o la mascarilla tipo Venturi.
La oxigenoterapia suplementaria durante la sedación genera aerosoles. Cuando se utilizan gafas nasales, la distancia que alcanzan las partículas exhaladas es directamente proporcional al flujo de oxígeno, por lo que es importante adecuar el flujo a las necesidades fisiológicas, independientemente del riesgo de infección60,61.
En pacientes de alto riesgo o infección confirmada por SARS-CoV-2, el Ministerio de Sanidad recomienda la utilización de mascarillas con filtro de exhalado66. Estos dispositivos son compatibles con la realización de la colonoscopia, por lo que recomendamos su uso en este escenario. Si no se dispone de estos dispositivos, recomendamos colocar una mascarilla quirúrgica por encima de las gafas nasales o de la mascarilla tipo Venturi67.
¿Quién debe realizar los procedimientos endoscópicos?Se recomienda que los procedimientos en pacientes confirmados o con alta sospecha de infección por SARS-CoV-2 sean realizados por personal experimentado estratégicamente asignado.
El personal en la sala de endoscopia debe reducirse al mínimo para reducir el riesgo de exposición y transmisión. Es aconsejable que los procedimientos sean realizados por endoscopistas experimentados e independientes en la técnica. Existe unanimidad en esta recomendación por parte de las sociedades científicas6,27,45. Además, se recomienda que el personal de enfermería y los técnicos auxiliares dispongan de formación y experiencia previa en el procedimiento que se vaya a realizar. Se recomienda que el personal en formación no intervenga en estos procedimientos para disminuir el riesgo de infección y el tiempo del procedimiento.
Se recomienda que los residentes en Aparato Digestivo participen en los procedimientos endoscópicos en pacientes con bajo riesgo de infección por SARS-CoV-2, siempre y cuando se disponga de los recursos necesarios que garanticen la seguridad del procedimiento.
No se han encontrado recomendaciones específicas sobre cómo debe realizarse la formación en endoscopia en el contexto epidemiológico actual. Es fundamental promover y garantizar la continuidad de la formación académica tras el pico de la pandemia. Las sociedades firmantes de este documento se posicionan a favor de que los residentes en Aparato Digestivo continúen realizando procedimientos bajo supervisión directa en pacientes de bajo riesgo de infección por SARS-CoV-2. La reincorporación de los residentes a la sala de endoscopia debe hacerse de forma escalonada en función de las competencias previas adquiridas y la complejidad prevista del procedimiento. Esta recomendación queda sujeta a la disponibilidad de recursos humanos y materiales, y a la situación epidemiológica local.
Adicionalmente, recomendamos que se promueva la formación teórica, la utilización de herramientas de aprendizaje online y el entrenamiento en simuladores de endoscopia cuando estén disponibles.
¿Cómo se debe realizar el procesamiento de biopsias endoscópicas?Se recomienda que el procesamiento de muestras biológicas se realice siguiendo los protocolos estandarizados de bioseguridad para sustancias con alta capacidad infectiva.
En nuestra búsqueda, no se ha encontrado ninguna recomendación específica para el manejo de las biopsias endoscópicas. La OMS sugiere que la ruta fecal-oral no desempeña un papel relevante a nivel comunitario. No obstante, esta organización indica que la transmisión fecal-oral es posible basándose en datos indirectos28,43,68. En este sentido, se ha notificado el cultivo del virus vivo en muestras fecales69. En un metaanálisis reciente, el 48,1% de los pacientes con infección por SARS-CoV-2 presentaban ARN viral en las heces. La presencia del ARN fecal se mantuvo en un 70,3% de los pacientes a pesar de la negativización del ARN en el exudado nasofaríngeo, incluyendo pacientes en los que la sintomatología había comenzado 33 días antes28.
Hasta que se disponga de un mayor conocimiento, consideramos que todas las muestras obtenidas durante la endoscopia deben ser procesadas como potencialmente infectivas de SARS-CoV-2. El procesamiento y el transporte de estas muestras debe realizarse siguiendo las recomendaciones de la OMS para material biológico con capacidad infectiva o protocolos locales estandarizados y consensuados con otros servicios70. Es recomendable que todo el personal de la UE implicado en la manipulación o el transporte de las muestras vista los equipos de protección detallados en este documento. Además, se recomienda detallar en el volante de petición destinado al servicio receptor si la muestra procede de un paciente con sospecha o infección confirmada por SARS-CoV-271.
Se recomienda evitar la toma de muestras biológicas durante la endoscopia cuando el impacto clínico del resultado sea previsiblemente marginal.
La toma de biopsias innecesarias durante la endoscopia es una práctica documentada en estudio previos que conduce a un incremento del coste y del riesgo de eventos hemorrágicos72,73. Se recomienda optimizar la toma de biopsias siguiendo las indicaciones establecidas por las GPC. Esta premisa cobra especial relevancia considerando el potencial infectivo de las muestras biológicas y la necesidad de optimizar los recursos materiales.
Posprocedimiento¿Cómo debe realizarse la desinfección de dispositivos, material, superficies y salas de endoscopia? ¿Y la gestión de residuos?Se recomienda que la desinfección y reprocesamiento de los endoscopios se realice siguiendo los protocolos habituales.
El SARS-CoV-2 es un virus con una envuelta que lo hace sensible a los desinfectantes utilizados habitualmente74. No existe evidencia que apoye la necesidad de una desinfección y reprocesamiento diferencial en los pacientes con infección por SARS-CoV-2. Todas las sociedades científicas coinciden en que las pautas de desinfección previas a la pandemia siguen siendo válidas en el contexto actual6,27,45,51,74,75. Se recomienda que en todos los centros se revise y asegure la correcta implementación de estas recomendaciones.
Se recomienda en contra de la reutilización de los dispositivos de un solo uso.
La GPC de la ESGE del 2018 recomienda no reutilizar los accesorios endoscópicos de un solo uso75. Esta recomendación es especialmente relevante en la situación actual. Si existe disponibilidad de recursos, es aconsejable priorizar el uso de accesorios endoscópicos de un solo uso frente a los reutilizables6,75.
Se recomienda la aplicación de protocolos para la limpieza y la desinfección de las salas de endoscopia y de los materiales que hayan contactado con el paciente o con sus secreciones.
Los agentes de limpieza comúnmente utilizados que cumplan con la normativa europea EN 14885 son válidos en el contexto actual y pueden consultarse en otras fuentes74,75. Para los pacientes con alta sospecha o infección confirmada por SARS-CoV-2, es recomendable una desinfección en profundidad de la sala después de cada endoscopia6,27. Si no se dispone de un sistema de presión negativa, se debe ventilar la sala durante al menos 1-3 h entre procedimientos74. Si dicha sala no tiene ventanas al exterior, se recomienda utilizar filtros de partículas de alta eficiencia HEPA o métodos alternativos de desinfección, como rayos ultravioleta u ozono74,76.
En los pacientes considerados como de bajo riesgo de infección, se recomienda seguir con los protocolos estándar de limpieza6,27. Después de cada procedimiento de debe asegurar la desinfección de todas las superficies, incluyendo cama y barandillas, suelo, torre de endoscopia, material de monitorización de constantes vitales y cualquier otro dispositivo que haya podido contactar con el paciente. Al final del turno, se recomienda una limpieza en profundidad incluyendo paredes, mobiliario y todo el material presente en la sala6,74.
Se recomienda la asignación de personal de limpieza dedicado exclusivamente a la UE.
Ante la previsión de mayores requerimientos de tareas de desinfección, la AEG y la SEED se posicionan a favor de la asignación de personal de limpieza dedicado exclusivamente a la UE. Esta medida facilita la correcta formación del personal de limpieza y reduce la demora en la limpieza de las salas.
Se recomienda que la gestión de residuos se realice siguiendo los protocolos locales cada centro para material con alta capacidad infectiva categoría B (UN3291).
La gestión de residuos de la UE digestiva no debe gestionarse de forma individualizada, sino enmarcarse en protocolos hospitalarios que cumplan con la normativa vigente. El ECDC recomienda que los residuos sean manejados como material de desecho con alta capacidad infectiva categoría B (UN3291)74. Los EPI desechables deben depositarse en los contenedores adecuados y ser manejados como residuos biosanitarios clase iii50.
¿Debe tomarse alguna medida adicional en las salas de recuperación tras la realización de una endoscopia?Se recomienda mantener la distancia interpersonal de 1-2 m, las medidas de higiene básicas y el flujo independiente de pacientes en las salas de recuperación.
Se debe garantizar que las medidas de protección e higiene básicas se mantengan después del procedimiento. La sala de recuperación para pacientes de alto riesgo de infección debe estar separada físicamente de la sala destinada a los pacientes de bajo riesgo6,22,26,38. Es recomendable instruir a los pacientes en la retirada de guantes y mascarilla quirúrgica e incentivar la higiene de manos a la salida de la UE.
El personal sanitario, ¿debe retirarse el EPI en la misma sala donde se realice el procedimiento o en una sala habilitada específicamente para tal uso?Se recomienda que la retirada del EPI se realice en una sala o antesala habilitada específicamente para tal uso. Si no hay disponibilidad, se recomienda retirar el EPI fuera de la sala de endoscopia, en un área de transición entre la zona limpia y la contaminada.
La retirada del EPI es un paso fundamental para garantizar la seguridad de la endoscopia. El EPI debe retirarse mediante una secuencia predefinida en un área fuera de la zona de exposición y de la zona limpia de la UE. El ECDC y el CDC coinciden en que la retirada del EPI no debe realizarse en la misma sala del procedimiento77,78. Esta retirada puede hacerse en una antesala o en una habitación habilitada a este fin. Si no existe disponibilidad, es recomendable retirar el EPI fuera de la sala de endoscopia, en un área de transición entre la zona limpia y la zona contaminada77. Si esta opción tampoco es factible, se recomienda retirar el EPI a la puerta de la sala de endoscopia. La mascarilla debe retirarse en último lugar y siempre fuera de la zona de la UE potencialmente contaminada. Es fundamental realizar una adecuada higiene de manos inmediatamente después de la retirada del EPI50.
¿Es necesario evaluar la aparición de infección por SARS-CoV-2 después del procedimiento endoscópico?Se recomienda considerar la implantación de programas de seguimiento de los pacientes entre los 7-15 días después del procedimiento para valorar la aparición de síntomas compatibles con COVID-19.
El principio de trazabilidad y el control de la infección postintervención es una máxima de la calidad de la endoscopia79. La mayoría de los autores y las sociedades coinciden en que es aconsejable evaluar la incidencia de infección por SARS-CoV-2 tras un procedimiento endoscópico6,23,25,27. El objetivo es detectar precozmente posibles focos de transmisión dentro de la UE. Asimismo, esta medida sirve para identificar de forma precoz al personal de la UE y a los pacientes que estuvieron en contacto con un caso de COVID-19 detectado tras el procedimiento. El contacto debe realizarse de forma no presencial, bien mediante contacto telefónico o por vía telemática.
Por otro lado, la implantación de esta medida plantea problemas logísticos y no hay evidencia directa que avale su beneficio. En un estudio reciente que incluyó 851 procedimientos realizados entre el 27 de enero y el 13 de marzo del 2020 en hospitales del norte de Italia, la tasa de respuesta fue del 94,1%. El contacto se realizó por vía telefónica por parte de enfermería y coordinadores del estudio. Ocho pacientes (1%) desarrollaron síntomas de COVID-19. Su naturaleza retrospectiva, la ausencia de evaluación de la infección mediante pruebas de laboratorio y el hecho de que el estudio no se realizara durante el pico de la pandemia son limitaciones mayores que obligan a interpretar estos resultados con cautela80.
Finalmente, el paciente que desarrolle COVID-19 podría asumir erróneamente que el contagio se produjo necesariamente en la UE, por lo que es fundamental informar al paciente sobre la finalidad de este contacto. Por todo ello, la decisión de establecer este circuito se debe realizar a nivel local en función de los recursos disponibles, contando con la implicación de otros servicios hospitalarios responsables del control de la infección y, preferiblemente, dentro de un protocolo de investigación para evaluar su eficiencia.
FinanciaciónNinguna.
Conflicto de interesesNinguno.
Comité de Revisión:
AEG: Francesc Balaguer, Luis Bujanda, Gloria Fernández-Esparrach, Begoña González Suárez y Angels Ginés.
SEED: Carlos Dolz Abadía, Maite Herráiz Bayod, Vicente Lorenzo-Zúñiga, Manuel Pérez-Miranda, Vicente Pons y Juan J. Vila.
Agradecimiento a los representantes de las sociedades científicas que se adhieren al documento: