El registro ENEIDA, promovido por el Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa (GETECCU), fue creado en 2005 por un grupo de gastroenterólogos interesados en mejorar el manejo de los pacientes con enfermedad inflamatoria intestinal. Los objetivos principales del registro fueron facilitar la recogida de datos clínicos de interés para la práctica clínica asistencial, así como la elaboración de estudios colaborativos a partir de datos clínicos y muestras biológicas. En sus 15 años de existencia, ENEIDA ha evolucionado en múltiples aspectos, desde su contenido o su soporte tecnológico hasta el número de centros participantes, para convertirse en uno de los registros de referencia para el estudio y cuidado de los pacientes con enfermedad inflamatoria intestinal, con una producción científica continua y de alta calidad que lo ha situado como ejemplo de explotación científica colaborativa en el ámbito internacional. En este artículo se revisan los objetivos, el diseño, las características estructurales, la monitorización y la explotación científica del registro ENEIDA.
The ENEIDA registry, promoted by the Spanish Working Group on Crohn's Disease and Ulcerative Colitis (GETECCU), was created in 2005 by a group of gastroenterologists interested in improving the management of patients with inflammatory bowel disease. The main objectives of the registry were to facilitate the collection of clinical data of interest for clinical care practice, as well as to carry out collaborative studies using clinical data and biological samples. In its 15 years of existence, ENEIDA has evolved in many aspects, from its content or technological support to the number of participating centres, to become one of the reference registries for the study and care of patients with inflammatory bowel disease, with a continuous and high quality scientific production that has positioned it as an example of collaborative scientific exploitation at an international level. This article reviews the objectives, design, structural characteristics, monitoring and scientific exploitation of the ENEIDA registry.
El Grupo Español de Trabajo en Enfermedad de Crohn y Colitis Ulcerosa (GETECCU) es una asociación sin ánimo de lucro con 30 años de trayectoria, cuya misión es mejorar la vida de las personas afectas por la enfermedad inflamatoria intestinal (EII), promoviendo la excelencia asistencial, docente, investigadora e influyendo en acciones políticas y sociales. En la actualidad GETECCU cuenta con casi 1.000 afiliados y constituye la sociedad científica de referencia en el ámbito de la EII a nivel español, además de ser cantera de formación de profesionales que se dedican a la atención de pacientes con EII. Tras unos primeros años en los que su actividad se centró en la formación y la docencia, GETECCU inició su actividad en investigación clínica. El registro ENEIDA, diseñado en 2005 por un grupo de gastroenterólogos miembros de GETECCU e interesados en mejorar el manejo de los pacientes con EII, nació con la finalidad de facilitar la recogida de datos clínicos que pudieran tener interés para la práctica clínica asistencial, así como la elaboración de estudios colaborativos a partir de datos clínicos y muestras biológicas.
Inicio del proyectoEl proyecto ENEIDA, cuyo acrónimo corresponde a Estudio Nacional en Enfermedad Inflamatoria Intestinal sobre Determinantes genéticos y Ambientales, fue aprobado en el año 2006 por el Comité Ético del Hospital Clínic i Provincial de Barcelona; como objetivo global del proyecto figuraba la creación de una infraestructura y de los procedimientos operativos necesarios para el desarrollo continuado de estudios multicéntricos de colaboración en torno a los factores implicados en la etiología y fisiopatología de la EII, incluyendo factores genéticos, ambientales y estudios epidemiológicos. Desde su inicio se establecieron los principios que rigen la participación y explotación del registro, que han sido mantenidos en todo momento. En primer lugar, la participación y el registro de datos son voluntarios y no remunerados; por tanto, el mayor o menor grado de cumplimentación de las variables depende del compromiso y la voluntad de los investigadores adscritos a cada centro, sin que pueda exigirse el registro de datos. En segundo lugar, el registro pretende tener potencialmente una triple función: ser herramienta de uso asistencial (fuente de búsqueda rápida de datos clínicos para elaborar informes o para asistencia presencial o telemática), ser registro para la explotación científica a nivel de centro y, por último, ser registro multicéntrico colaborativo para su explotación científica regulada por GETECCU.
Al principio, los centros participantes debían contar con un software específico de ENEIDA en el que introducían localmente la información que, con frecuencia periódica, debían volcar de forma anonimizada a la base central desde un acceso remoto para su potencial explotación en proyectos colaborativos de investigación. En ese momento, la adopción del registro por los centros enfrentó algunas limitaciones que condicionaron el crecimiento de la base de datos. En primer lugar, la probable desconfianza que generaba en algunos la participación en una iniciativa colaborativa y no remunerada, en la que se requería compartir de forma desinteresada datos de pacientes. En segundo lugar, la falta de personal dedicado con tiempo suficiente a la EII (lo que suponía una carga considerable de trabajo adicional) y una base incómoda y compleja de manejar desde el punto de vista técnico y visual supusieron limitaciones adicionales para su diseminación. Por último, debe tenerse en cuenta las limitaciones tecnológicas de esa época, en la que muchos centros no disponían del acceso a Internet que la aplicación requería, lo que a menudo suponía que el investigador tuviera que enviar los datos de sus bases locales por medios propios.
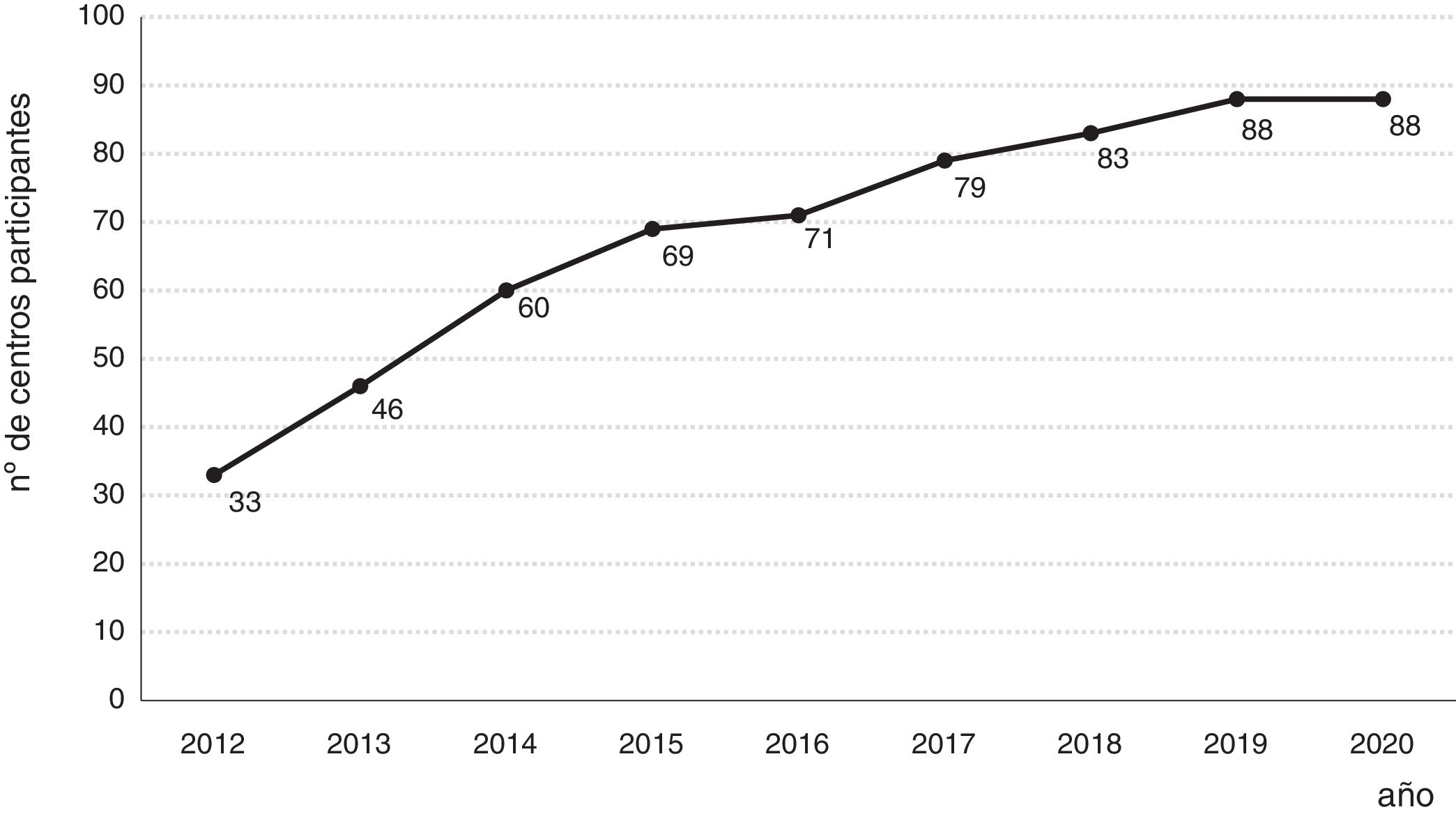
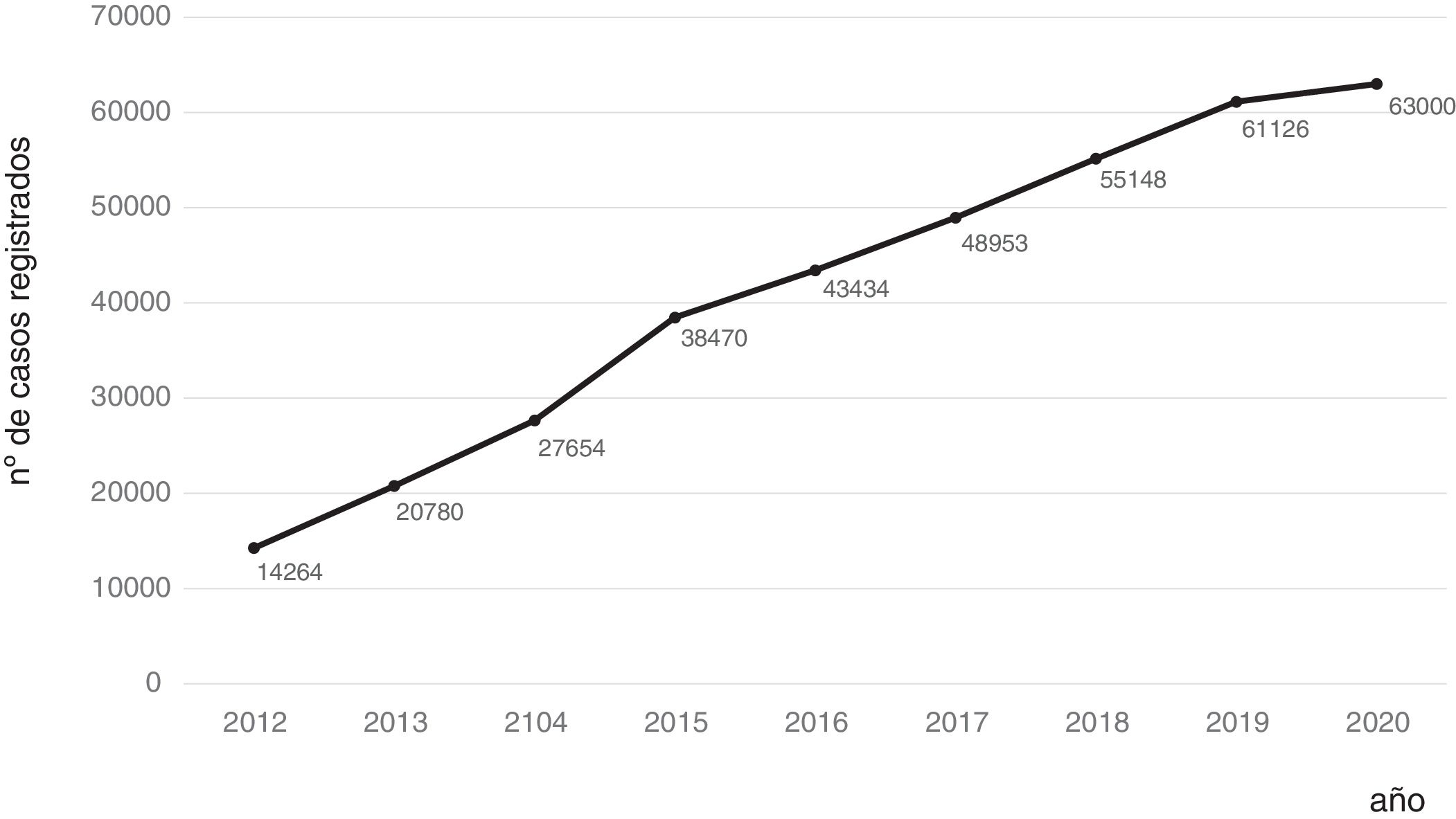
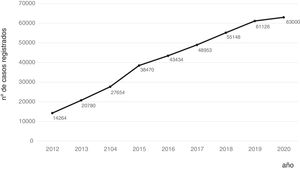
Consolidación del registroLa consolidación de forma definitiva como registro de referencia de GETECCU se produjo tras la creación de la versión en línea en el año 2012, sin necesidad del programa local y del posterior volcado periódico de datos. El cambio de sistema simplificó y dinamizó el registro. Cada centro hizo en una sola operación el volcado de todos los pacientes ya incluidos en la base local a la nueva base centralizada, introduciendo a partir de ese momento los datos directamente en línea. La necesidad de la firma de convenios entre GETECCU y cada una de las gerencias de los hospitales participantes del proyecto, así como de la aprobación por parte del comité ético de cada institución, supusieron cierta ralentización para la expansión del proyecto. En la actualidad, el proyecto cuenta con la participación de más de 80 centros (tabla 1) y más de 60.000 pacientes incluidos (figs. 1 y 2). Por último, el proyecto incluye una colección de muestras de ADN que cuenta con más de 8.000 en la actualidad. En el año 2020 se ha efectuado un último cambio tecnológico de la base, con la migración a una nueva plataforma con mayores prestaciones técnicas.
Listado de centros hospitalarios participantes en el registro ENEIDA
| Althaia Xarxa Assistencial Universitària de Manresa | Hospital San Pedro (Logroño) |
| Complejo Asistencial de Segovia | Hospital Santa Bárbara (Soria) |
| Complejo Asistencial Universitario de León | Hospital Santos Reyes (Aranda de Duero) |
| Complejo Asistencial Universitario de Palencia | Hospital Universitari de Bellvitge (L’Hospitalet de Llobregat) |
| Complejo Hospitalario de Jaén | Hospital Universitari Dr Josep Trueta (Girona) |
| Complejo Hospitalario de Navarra (Pamplona) | Hospital Universitari Germans Trias i Pujol (Badalona) |
| Complejo Hospitalario La Mancha Centro (Alcázar de San Juan) | Hospital Universitari Joan XXIII (Tarragona) |
| Complexo Hospitalario de Pontevedra | Hospital Universitari Mútua Terrassa |
| Complexo Hospitalario Universitario de Ourense | Hospital Universitario 12 de Octubre (Madrid) |
| Consorci Sanitari de Terrassa | Hospital Universitario Araba (Vitoria) |
| Consorcio Hospital General Universitario de Valencia | Hospital Universitario Arnau de Vilanova (Lérida) |
| Corporació Sanitària Parc Taulí (Sabadell) | Hospital Universitario Central de Asturias (Oviedo) |
| Gestión Sanitaria Este de Málaga-Axarquía | Hospital Universitario de Basurto |
| Hospital Universitario Infantil Niño Jesús (Madrid) | Hospital Universitario de Burgos |
| Hospital Álvaro Cunqueiro (Vigo) | Hospital Universitario de Cabueñes (Gijón) |
| Hospital Clínic i Provincial (Barcelona) | Hospital Universitario de Cáceres |
| Hospital Clínico de Valencia | Hospital Universitario de Canarias(Santa Cruz de Tenerife) |
| Hospital Clínico San Carlos (Madrid) | Hospital Universitario de Cruces (Baracaldo) |
| Hospital Clínico Universitario Lozano Blesa (Zaragoza) | Hospital Universitario de Fuenlabrada |
| Hospital Clínico Universitario de Santiago de Compostela | Hospital Universitario de Galdakao |
| Hospital Clínico Universitario de Valladolid | Hospital Universitario de La Princesa (Madrid) |
| Hospital Comarcal de Blanes | Hospital Universitario de Salamanca |
| Hospital Comarcal Sant Jaume (Calella) | Hospital Universitario de Torrejón |
| Hospital de Barbastro | Hospital Universitario Donostia (San Sebastián) |
| Hospital de Can Misses (Ibiza) | Hospital Universitario Fundación de Alcorcón |
| Hospital de La Santa Creu i Sant Pau (Barcelona) | Hospital Universitario Infanta Elena (Valdemoro) |
| Hospital de Manises (Valencia) | Hospital Universitario Infanta Sofía (San Sebastián de los Reyes) |
| Hospital del Mar (Barcelona) | Hospital Universitario La Paz (Madrid) |
| Hospital General de Granollers | Hospital Universitario Marqués de Valdecilla (Santander) |
| Hospital General San Jorge (Huesca) | Hospital Universitario Miguel Servet (Zaragoza) |
| Hospital General de Tomelloso | Hospital Universitario Nuestra Señora de La Candelaria (Santa Cruz de Tenerife) |
| Hospital General Universitario Gregorio Marañón (Madrid) | Hospital Universitario Puerta de Hierro (Majadahonda) |
| Hospital General Universitario de Alicante | Hospital Universitario Ramón y Cajal (Madrid) |
| Hospital General Universitario de Castellón | Hospital Universitario Reina Sofía (Córdoba) |
| Hospital General Universitario de Ciudad Real | Hospital Universitario Río Hortega (Valladolid) |
| Hospital General Universitario de Elche | Hospital Universitario Son Espases (Palma De Mallorca) |
| Hospital General Universitario de Elda | Hospital Universitario Son Llàtzer (Palma de Mallorca) |
| Hospital General Universitario de Santa Lucía (Cartagena) | Hospital Universitario Virgen Macarena (Sevilla) |
| Hospital General Universitario Reina Sofía (Murcia) | Hospital Universitario y Politécnico de La Fe (Valencia) |
| Hospital Marina Baixa (Villajoyosa) | Hospital Vega Baja (Orihuela) |
| Hospital Materno-infantil Sant Joan de Déu (Barcelona) | Hospital Viladecans |
| Hospital Moisès Broggi (Sant Joan Despí) | Hospital Virgen de la Concha (Zamora) |
| Hospital Regional Universitario Málaga | Hospital Virgen de la Luz (Cuenca) |
| Hospital Royo Villanova (Zaragoza) | Hospital Virgen de la Victoria (Málaga) |
El proyecto ha cumplido con creces el objetivo de generar conocimiento científico sobre la EII. El primer artículo colaborativo basado en los datos de ENEIDA fue publicado en 2011; hasta el momento se han publicado un total de 29 artículos1-29, sin incluir aquellos estudios desarrollados a partir de los datos del registro a nivel de centro. Cabe destacar que la producción no solo ha sido cuantiosa, sino de elevada calidad científica, lo que queda reflejado en el hecho de que el 30% del total se ha publicado en revistas de primer decil de la especialidad y el 89% en revistas de primer cuartil. En la página web de GETECCU pueden consultarse todos los estudios ya finalizados o todavía en marcha dentro del proyecto ENEIDA, así como los enlaces a sus respectivas publicaciones (http://geteccu.org/eneida/estudios-aprobados-en-eneida). Es precisamente la calidad de la producción científica de ENEIDA lo que ha reforzado el reconocimiento unánime e internacional de GETECCU como sociedad científica. La propia European Medicines Agency ha recomendado en diversas ocasiones la utilización del registro ENEIDA como base de registros de seguridad de nuevos fármacos en práctica clínica. Por último, queremos destacar la diversidad en el liderazgo de la explotación científica de ENEIDA, aspecto que desde el primer momento se ha estimulado desde GETECCU. Muestra de ello es el liderazgo de 9 grupos de investigación distintos y los 18 primeros autores distintos de los 29 artículos publicados.
Diseño, contenido y monitorización del registro ENEIDAENEIDA constituye un registro de pacientes diagnosticados de EII con seguimiento prospectivo. Una vez un centro decide su participación en la base, suele incluir a todos los pacientes de su centro con seguimiento activo; esto comporta que, al inicio de su participación, la inclusión sea fundamentalmente retrospectiva, si bien a partir de ese momento el seguimiento es siempre prospectivo. Lo mismo ocurre cuando un paciente inicia el seguimiento en un centro participante tras haber recibido el diagnóstico previamente en otro centro. Sin embargo, a los pocos meses de iniciarse la participación de cada centro, la inclusión es fundamentalmente prospectiva.
El registro permite seleccionar los pacientes por cualquiera de las múltiples variables que contiene. Por tanto, permite identificar a aquellos pacientes que se han seguido íntegramente de forma prospectiva y en los que la fecha de inclusión en el registro coincide con la fecha de diagnóstico.
Además de la fecha de inclusión (introducida de forma automática por el sistema en el momento en que se introducen los datos de filiación por primera vez en el registro y que no es modificable por el investigador), el investigador debe actualizar la fecha de la última visita en cada ocasión en que el paciente ha sido contactado. En caso de pérdida de seguimiento por cualquier causa (por fallecimiento, cambio de domicilio o cualquier otra causa), esta debe registrarse. Dado que uno de los objetivos del proyecto son los estudios epidemiológicos y ambientales, se decidió que el ámbito de la base se limitase a España, por lo que no incluye centros de otros países.
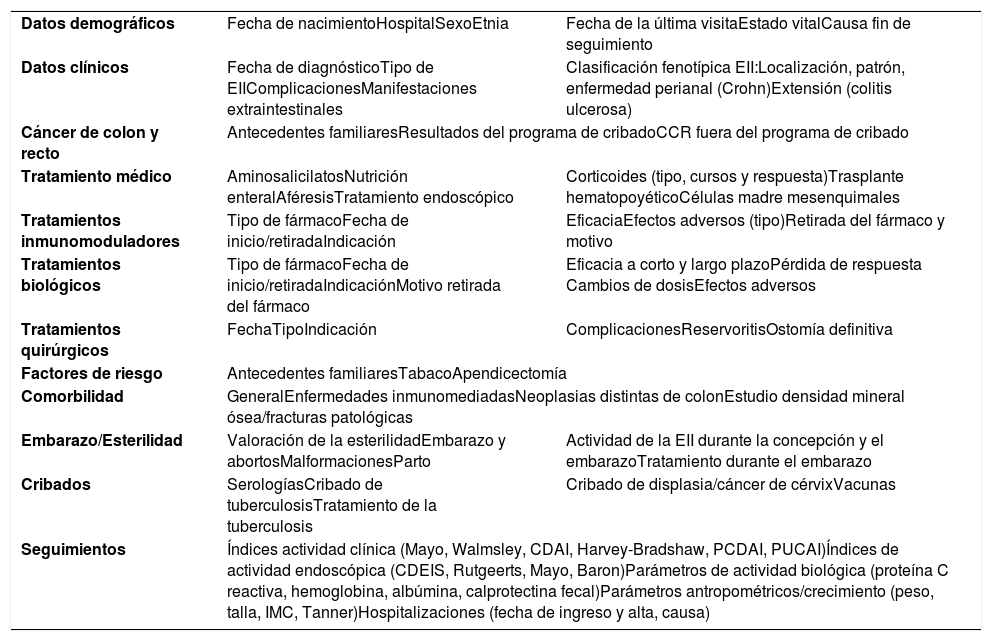
Las variables recogidas en el registro ENEIDA han sufrido diversas modificaciones a lo largo de su existencia, consistentes, sobre todo en la inclusión de nuevas variables, como consecuencia del avance en el conocimiento de las EII y de la disponibilidad de nuevas herramientas de diagnóstico y seguimiento y de nuevos tratamientos. La modificación de variables se ha efectuado siempre a criterio de un grupo de expertos, que incluye a los miembros del área de investigación y al presidente de la junta de GETECCU, así como a aquellos miembros de GETECCU que la junta designó en cada momento. La necesidad de estas modificaciones queda claramente demostrada en la aprobación de nuevos fármacos; desde el inicio del registro, se han incluido todas las nuevas opciones terapéuticas, incluyendo las moléculas biosimilares, aparecidas en el mercado español. En este sentido, la introducción de nuevas variables se ha hecho siempre de forma casi inmediata para asegurar la naturaleza prospectiva de los datos. Las variables se agrupan en 11 formularios: datos demográficos, características clínicas de la enfermedad (basadas en la clasificación de Montreal30), diagnóstico y cribado de neoplasia de colon, tratamientos médicos no inmunosupresores, tratamientos con fármacos inmunosupresores, tratamientos con agentes biológicos, tratamientos quirúrgicos, factores de riesgo familiares y ambientales, comorbilidades generales, inmunomediadas y neoplásicas, embarazo y fertilidad, cribado de infecciones y seguimiento (índices clínicos y endoscópicos, parámetros analíticos y hospitalizaciones). La tabla 2 resume las principales variables existentes en la actualidad.
Principales variables incluidas en el registro ENEIDA
| Datos demográficos | Fecha de nacimientoHospitalSexoEtnia | Fecha de la última visitaEstado vitalCausa fin de seguimiento |
| Datos clínicos | Fecha de diagnósticoTipo de EIIComplicacionesManifestaciones extraintestinales | Clasificación fenotípica EII:Localización, patrón, enfermedad perianal (Crohn)Extensión (colitis ulcerosa) |
| Cáncer de colon y recto | Antecedentes familiaresResultados del programa de cribadoCCR fuera del programa de cribado | |
| Tratamiento médico | AminosalicilatosNutrición enteralAféresisTratamiento endoscópico | Corticoides (tipo, cursos y respuesta)Trasplante hematopoyéticoCélulas madre mesenquimales |
| Tratamientos inmunomoduladores | Tipo de fármacoFecha de inicio/retiradaIndicación | EficaciaEfectos adversos (tipo)Retirada del fármaco y motivo |
| Tratamientos biológicos | Tipo de fármacoFecha de inicio/retiradaIndicaciónMotivo retirada del fármaco | Eficacia a corto y largo plazoPérdida de respuesta Cambios de dosisEfectos adversos |
| Tratamientos quirúrgicos | FechaTipoIndicación | ComplicacionesReservoritisOstomía definitiva |
| Factores de riesgo | Antecedentes familiaresTabacoApendicectomía | |
| Comorbilidad | GeneralEnfermedades inmunomediadasNeoplasias distintas de colonEstudio densidad mineral ósea/fracturas patológicas | |
| Embarazo/Esterilidad | Valoración de la esterilidadEmbarazo y abortosMalformacionesParto | Actividad de la EII durante la concepción y el embarazoTratamiento durante el embarazo |
| Cribados | SerologíasCribado de tuberculosisTratamiento de la tuberculosis | Cribado de displasia/cáncer de cérvixVacunas |
| Seguimientos | Índices actividad clínica (Mayo, Walmsley, CDAI, Harvey-Bradshaw, PCDAI, PUCAI)Índices de actividad endoscópica (CDEIS, Rutgeerts, Mayo, Baron)Parámetros de actividad biológica (proteína C reactiva, hemoglobina, albúmina, calprotectina fecal)Parámetros antropométricos/crecimiento (peso, talla, IMC, Tanner)Hospitalizaciones (fecha de ingreso y alta, causa) | |
CCR: cáncer colorrectal; CDAI: Crohn's disease activity index; CDEIS: Crohn's disease endoscopic index of severity; EII: enfermedad inflamatoria intestinal; IMC: índice de masa corporal; PCDAI: Pediatric Crohn's disease activity index; PUCAI: Pediatric ulcerative colitis activity index.
Para la creación de un nuevo registro de paciente es imprescindible cumplimentar el formulario de datos demográficos, sin el cual el sistema no permite introducir el resto de las variables. Los datos de filiación del paciente solo son visibles a nivel local para su uso asistencial y todos los registros son anonimizados a nivel central, siguiendo las normas de confidencialidad establecidas por la ley española. Asimismo, cada investigador solo tiene acceso directo a los datos de su propio centro. Dado el carácter voluntario de la participación en el registro, se estableció un sistema de monitorización indirecta de la cumplimentación de los registros. Para ello, se decidió que algunas de las variables eran necesarias para considerar que un caso disponía de un mínimo de información necesaria para ser incluido en estudios. Cada centro recibe mensualmente un informe detallado acerca de los pacientes con dichas variables incompletas: queda a voluntad del investigador el completarlas. Esto permite excluir de los estudios los casos incompletos, así como seleccionar aquellos centros buenos cumplidores si tienen más del 80% de los casos con información completa.
Dinámica del registro ENEIDAUna vez el comité ético del centro participante ha aprobado el proyecto y su gerencia ha firmado el convenio con GETECCU de conformidad con el reglamento relativo a la protección de datos y el reglamento sobre los ensayos clínicos de medicamentos de uso humano, GETECCU otorga las contraseñas necesarias al investigador principal del centro y a los investigadores colaboradores para acceder localmente al registro. Es necesario que cada paciente firme el consentimiento informado pertinente para la introducción de datos clínicos. GETECCU, como propietario del registro ENEIDA, se sirve de un proveedor tecnológico para la preservación e integridad de los datos, con las medidas de seguridad necesarias. El registro ENEIDA utiliza actualmente la plataforma de eHealth ClinicaaL® (Persei vivarium S.L., Madrid, España).
Además de las variables clínicas puede recogerse, de forma opcional y previa firma del consentimiento informado pertinente, una muestra sanguínea para la posterior extracción de ADN en el biobanco del Institut d’Investigació Biomèdica August Pi i Sunyer (IDIBAPS), donde se almacena para garantizar su conservación en óptimas condiciones. El envío de muestras biológicas al biobanco se rige por un procedimiento normalizado de trabajo (PNT) disponible para todos los investigadores de ENEIDA.
Explotación científica y diseminación informativa del registro ENEIDASi bien cada investigador es libre de utilizar sus datos locales ENEIDA para investigación sin precisar ninguna aprobación adicional, la explotación de los datos centrales está regulada por un PNT específico. Todos los investigadores participantes que aportan información clínica de un mínimo de 100 pacientes pueden solicitar a GETECCU la explotación de la información contenida en el registro. Los investigadores que, además, hayan aportado un mínimo de 50 muestras biológicas al proyecto, pueden asimismo solicitar estudios basados en estas muestras. Únicamente los socios de GETECCU cuyos centros participen en ENEIDA pueden solicitar un estudio con los datos de ENEIDA: quedan excluidos investigadores independientes, otras sociedades científicas o empresas públicas o privadas. Una vez aprobado el estudio por GETECCU, se entrega al investigador la información de las variables seleccionadas de forma anonimizada para su posterior explotación, análisis y publicación. Quienes solicitan estudios genéticos reciben, además de variables clínicas concretas, las muestras de ADN de los pacientes incluidos en el estudio, según se indica en otro PNT específico para la cesión de muestras. Existe una clara política de autorías (http://geteccu.org/eneida/politica-de-autorias), de forma que todos los investigadores del proyecto ENEIDA que hayan colaborado con los datos de algún paciente de su centro para cada estudio concreto tienen derecho a autoría. Tanto los artículos como las autorías deben ser aprobadas por el área de investigación de GETECCU, el coordinador de ENEIDA y los investigadores principales de los centros implicados. La gestión y control de todos estos procesos corren a cargo de una secretaría científica, el coordinador de ENEIDA y los vocales del área de investigación de la junta de gobierno de GETECCU.
Con el fin de diseminar el conocimiento generado a partir del registro ENEIDA, todos los investigadores reciben una boletín cuatrimestral en el que se informa de las comunicaciones a congresos y de las publicaciones derivadas de los estudios previamente aprobados y se comunican las modificaciones de la propia base de datos, de los PNT o de cualquier aspecto relacionado con el proyecto. Con periodicidad semestral, coincidiendo con las reuniones anuales de la Asociación Española de Gastroenterología y la de GETECCU, el coordinador de ENEIDA (designado cada 2años por la junta de gobierno de GETECCU) presenta una actualización del registro, así como de su producción científica.
ConclusionesEl proyecto ENEIDA constituye el mayor registro clínico prospectivo de pacientes con EII a nivel mundial y supone un ejemplo paradigmático del esfuerzo colaborativo en investigación clínica enmarcado en el seno de una sociedad científica. Asimismo, pone en valor la participación desinteresada de pacientes e investigadores, con una producción científica de alta calidad y que ha dado visibilidad y prestigio internacional a GETECCU como grupo consolidado.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses con el presente trabajo.
Los autores quieren agradecer a los presidentes de GETECCU, los doctores Miquel Àngel Gassull, Antoni Obrador y Joaquín Hinojosa, su contribución en la concepción del proyecto; a los doctores Joan Clofent, Antonio López Sanromán, Natalia Borruel, Francisco Guarner, Belén Beltrán, Ana Gutiérrez, Miguel Mínguez y María Chaparro, miembros destacados de GETECCU, el haber formado parte en algún momento de los distintos comités y grupos de trabajo vinculados a ENEIDA; a Maica Massamunt y Anna Casas, su eficaz labor al frente de la secretaría científica de ENEIDA; a la industria farmacéutica, su aporte económico, que ha permitido que este proyecto se haya hecho realidad, sin interferir en su contenido ni su explotación. Por último, los autores extienden su agradecimiento a todos los investigadores por su labor y a todos los pacientes por su colaboración, al facilitar el avance en el conocimiento de las enfermedades inflamatorias intestinales.