Mujer de 44 años, sin alergias medicamentosas ni hábitos tóxicos, con artritis seronegativa de inicio a los 18 años, en forma de oligoartritis asimétrica, de predominio en grandes articulaciones. A los 22 años inició coxitis derecha rápidamente destructiva, que precisó prótesis de cadera derecha (PTC) a los 42 años. Los estudios de factor reumatoide, anticuerpos antipéptido citrulinados, anticuerpos antinucleares y HLA-B27 fueron negativos. Continuó con tratamiento inductor de remisión con hidroxicloroquina, sales de oro (supendidos por ineficacia) y metotrexate (suspendido por intolerancia). En 2006 se inició tratamiento con adalimumab (suspendido a los 3 meses por rash cutáneo) y, posteriormente, con etanercept (2008-2009), con respuesta parcial y requerimiento de glucocorticoides en los brotes de artritis. Posteriormente recibió rituximab cada 6 meses (2009-2011, interrumpido para intervención de PTC). Por nuevo brote de artritis precisó infiltración del carpo derecho, y se reinició rituximab en junio del 2014 con repuesta parcial.
En julio de 2014 inicia pérdida ponderal, empeoramiento del estado general y de la artritis, anemización y elevación de reactantes de fase aguda VSG 64mm/h y PCR 56mg/l (valor normal: <5mg/l), por lo que se decidió cambio de tratamiento biológico. Por el marcado componente sistémico y la necesidad de utilizarlo en monoterapia (intolerancia a MTX), se decidió iniciar tratamiento con tocilizumab ev mensual, en octubre de 2014.
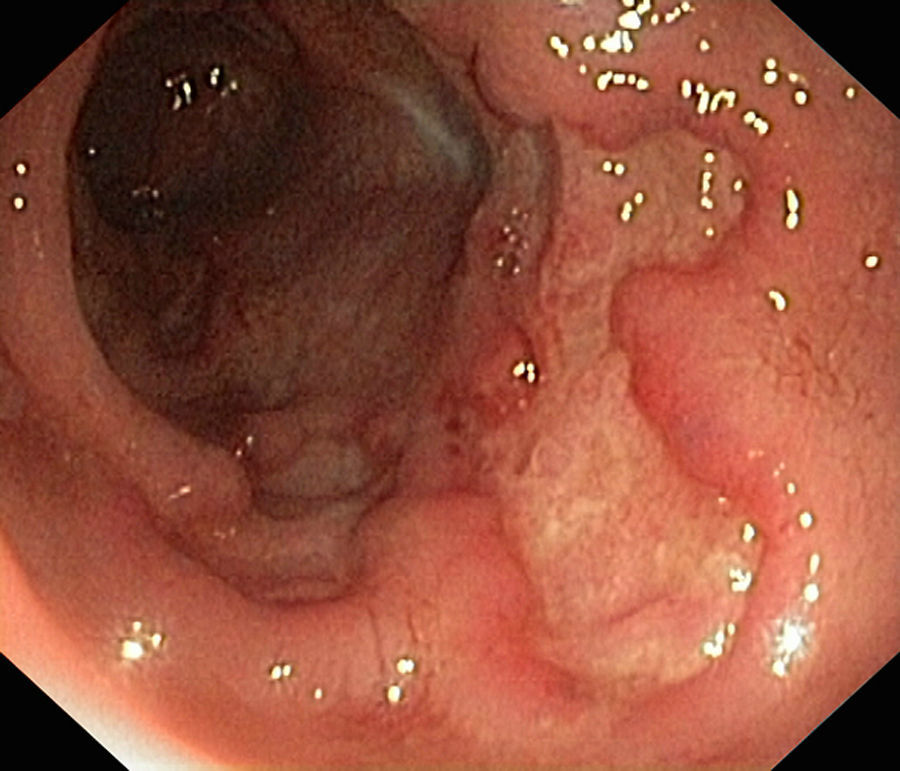
En enero de 2015, ingresa en el servicio de gastroenterología por cuadro de deposiciones diarreicas (5-7 día), sin productos patológicos, con dolor abdominal y pérdida de 10kg de peso, de un mes de evolución. En la exploración física destacaba dolor abdominal de predominio en flanco izquierdo, sin masas ni visceromegalias palpables. Analíticamente sin leucocitosis ni anemia (hemoglobina 14,2g/dl), PCR 0,24mg/l, albumina 44g/l. Para completar el estudio se realizó una fibrogastroscopia que resultó normal y una colonoscopia que mostró desde 12cm del margen anal hasta ciego úlceras extensas y profundas con mucosa interlesional sana, íleon terminal, afecto 15cm con aftas milimétricas (fig. 1). La anatomía patológica resultó compatible con EII. Posteriormente se cursan niveles de calprotectina fecal que resulta elevada 2.714mg/kg heces (VN<100mg/kg). Se orientó como un brote grave de enfermedad de Crohn (EC) íleo-cólica con artropatía periférica asociada. Se inició tratamiento con corticoterapia a dosis plena (40mg/día), azatioprina 150mg/dia y nutrición enteral total (NET), presentando correcta evolución clínica, con disminución en el número de deposiciones, así como resolución del dolor abdominal y articular, siendo dada de alta a domicilio.
Consideramos este caso clínico de especial interés, en primer lugar por la secuencia de presentación clínica, con artropatía periférica erosiva 20 años antes de la manifestación intestinal de la EC, situación que solo acontece en el 10% de los casos. En segundo lugar destaca la normalidad de los parámetros biológicos, a pesar de tener importante afectación de la mucosa en la colonoscopia. Se han descrito múltiples casos de infecciones graves con reactantes biológicos normales en pacientes con artritis reumatoide en tratamiento con tocilizumab, pero ninguno de pacientes con EC y reactantes biológicos normales en contexto de tratamiento con anti-IL-61–4.
Entre las manifestaciones extraintestinales de la EC, la clínica articular es la más frecuente (10-35%), bien en forma de espondiloartropatía axial (sacroileítis y espondilitis) o de artritis periférica, aguda o crónica. La artritis periférica suele estar relacionada con la actividad de la enfermedad inflamatoria intestinal (EII) y, generalmente, aparece de forma coincidente con los brotes de esta. Con frecuencia la afectación es pauciarticular, asimétrica, de curso transitorio y autolimitado, aunque existen formas con actividad crónica persistente como en el caso descrito. Si bien estas manifestaciones responden a la terapia de la EII, con frecuencia es necesario añadir fármacos inductores de remisión o realizar infiltraciones locales con glucocorticoides5.
La normalidad de los rectantes biológicos, a pesar de la importante afectación íleo-cólica por EC, podría explicarse por el efecto de la terapia anti-IL-6. La interleucina 6, es una citocina proinflamatoria producida por diversos tipos celulares, incluidos monocitos, linfocitos y fibroblastos, que participa en múltiples procesos biológicos como la formación de proteínas de fase aguda y hepcidina a nivel hepático, aumento de megacariocitos con trombocitosis sistémica, diferenciación de osteoclastos y por ende osteoporosis, activación de macrófagos, células B y T, que ocasionan la inflamación crónica. Todas estas acciones proinflamatorias, hace que se vincule a la fisiopatología de múltiples enfermedades inflamatorias, autoinmunes, como la EC.
El tocilizumab (TCZ) es un anticuerpo monoclonal humanizado dirigido contra el receptor, tanto soluble como de membrana de la IL-6. En Europa ha sido aprobado, en monoterapia o en combinación con MTX para el tratamiento de pacientes adultos con AR moderada-severa con respuesta inadecuada o intolerancia al menos a un FAME o a un agente anti-TNF-α6. Sin embargo, no es eficaz para la EC, ya que la IL-6 parece no estar implicada directamente en el mecanismo fisiopatológico en la EC, y de hecho en los resultados de diferentes estudios en pacientes con EII, tratados con tocilizumab, se ha evidenciado respuesta clínica en más del 50% de los casos, pero no remisión endoscópica ni histológica al comparar con el grupo placebo7–9.
En este caso una herramienta útil y sencilla para aclarar el diagnóstico es la calprotectina fecal (CF), que es una proteína con propiedades antimicrobianas, que constituye el 60% de las proteínas citosólicas de los granulocitos; su presencia en las heces es directamente proporcional a la actividad de los neutrofilos en la luz intestinal.
Ha sido propuesta como biomarcador de inflamación intestinal ya que presenta una mejor correlación con el grado de inflamación que los marcadores serológicos e índices clínicos, con una sensibilidad para detectar actividad mucosa que varía en rango del 70 al 100% con una especificidad del 44 al 100% en función del punto de corte en diferentes estudios10.
A modo de conclusión, ante un paciente con sospecha clínica de EII, la normalidad de los reactantes biológicos no permite descartarla, en este caso la CF parece ser una excelente prueba diagnóstica para seleccionar aquellos pacientes que deben ser estudiados.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.