Las tiazolidindionas favorecen la captación de glucosa por los tejidos periféricos (músculo y tejido adiposo) al ser agonistas del receptor que activa la proliferación de peroxisomas (PPAR)1. En la actualidad, hay 2 moléculas disponibles comercialmente —rosiglitazona y pioglitazona—, que fueron aprobadas en EE.UU. en 1999 y en Europa en 2000 para el tratamiento de la hiperglucemia en pacientes con diabetes mellitus tipo 2. Las tiazolidindionas no sólo actúan en el metabolismo glucídico, sino que también ejercen una acción antiinflamatoria, con mejoría del funcionalismo endotelial y reducción del riesgo cardiovascular, independientemente de su acción hipoglucemiante2. Este efecto es especialmente importante, ya que más del 65% de los fallecimientos en estos pacientes se deben a estas causas, principalmente a la enfermedad cardíaca isquémica3.
Por el contrario, los efectos en el perfil lipídico son controvertidos, y se han descrito variaciones en la concentración y el tamaño de las lipoproteínas, que podrían ser distintos si se usa pioglitazona o rosiglitazona4. Las lipoproteínas de baja densidad (LDL) pequeñas y densas son más susceptibles de oxidación y, por tanto, de ser atraídas por los macrófagos en la íntima vascular, lo que favorece la progresión del proceso aterosclerótico. Incluso se ha propuesto que son mejores predictores de enfermedad cardiovascular que el propio colesterol LDL (cLDL) total en pacientes con diabetes mellitus tipo 24. Nuestro objetivo ha sido analizar los cambios en el perfil lipídico, en especial en la concentración y el tamaño de las partículas LDL, en un grupo de pacientes con diabetes mellitus tipo 2 en tratamiento con antidiabéticos orales, a los que se añadió rosiglitazona a su tratamiento inicial. También hemos estudiado la evolución de los parámetros glucídicos, de la proteína C reactiva (PCR), como marcador inflamatorio, y del riesgo cardiovascular estimado.
Pacientes y métodoSe estudió a 30 pacientes (17 varones y 13 mujeres) con edades comprendidas entre 43 y 79 años, diagnosticados de diabetes mellitus tipo 2, con un tiempo medio (desviación estándar) de evolución de la enfermedad de 10,7 (6,8) años. De ellos, el 13,3% eran fumadores, el 96,7% presentaban obesidad (peso medio de 79 [18,2] kg y perímetro de cintura medio de 104 [12,2] cm) y el 63,3% eran hipertensos. Los pacientes procedían del Área Sanitaria I de la Región de Murcia y estaban en tratamiento con antidiabéticos orales —metformina, meglitinidas o sulfonilureas—, en monoterapia o en politerapia. A todos los pacientes se les realizó una extracción sanguínea antes y después de 6 meses del inicio del tratamiento con rosiglitazona (4 mg/día), que se añadió a su tratamiento inicial. El estudio cumplió las normas éticas del comité de investigación de nuestro centro, así como la Declaración de Helsinki de 1975, y todos los pacientes dieron su consentimiento.
Se determinaron las pruebas siguientes: glucosa, colesterol total, colesterol unido a lipoproteínas de alta densidad (cHDL), triglicéridos y PCR por espectrometría y turbidimetría en un autoanalizador bioquímico modular DP (Roche Diagnostic®); lipoproteína (a) (Lp[a]) por inmunonefelometría en un nefelómetro BN Prospec (Dade Behring®); hemoglobina glucosilada (HbA1C) por cromatografía líquida de alta resolución en un cromatógrafo Variant™ Turbo (Bio-Rad®) y cLDL estimado según la fórmula de Friedewald. Además, se calculó el diámetro medio de las partículas LDL mediante electroforesis en gel de poliacrilamida Lipoprint LDL System (Quantimetrix Corporation®), que permite separar 7 subfracciones de LDL. Tras la electroforesis, las fracciones electroforéticas se identifican según su movilidad o índice de retención en el gel, a partir de las lipoproteínas de muy baja densidad (VLDL) como punto de referencia inicial y las de alta densidad (HDL) como punto de referencia final. La concentración de las distintas subfracciones se calculó determinando el área bajo la curva de cada pico a partir de la gráfica de electroforesis5.
Se calculó la probabilidad de episodios cardiovasculares a 10 años según el modelo Framingham y SCORE6 (adaptado a países con riesgo cardiovascular bajo, como es el caso de España). Para el análisis estadístico, se calculó la prueba de la t de Student para muestras paramétricas relacionadas, con el software SPSS v.12.0.
ResultadosEn la tabla 1 se reflejan las concentraciones iniciales de los distintos parámetros, así como el incremento de éstas después de añadir rosiglitazona para el control glucémico a su tratamiento inicial. Encontramos una reducción estadísticamente significativa de los valores de glucosa, HbA1C y PCR, y un aumento de las concentraciones de colesterol total, cLDL total y triglicéridos, aunque sólo con significación estadística para el colesterol total. No encontramos variaciones importantes en las concentraciones de cHDL, Lp(a) ni tampoco en el diámetro medio de las partículas LDL. Al estudiar por separado la concentración y el tamaño de las subfracciones de LDL grandes y pequeñas, no observamos variación en el tamaño, aunque sí un ligero aumento de ambas concentraciones, que no fue significativo (tabla 1).
Tabla 1. Variación de los parámetros evaluados tras el tratamiento con rosiglitazona.
| Valor iniciala | Incrementob | ICc | DTd | p-valore | |
| Glucosa (mg/dl) | 181,6 (55,5) | −34,3 | (−50,6 a −18,0) | 54,3 | 0,002 * |
| HbA1C (%) | 8,3 (1,0) | −0,9 | (−1,3 a −0,6) | 1,2 | 0,0002 * |
| Colesterol total (mg/dl) | 191,9 (32,4) | 17,3 | (6,2 a 28,4) | 36,9 | 0,016 * |
| Triglicéridos (mg/dl) | 175,0 (89,1) | 24,9 | (3,4 a 46,4) | 71,7 | 0,067 |
| cHDL (mg/dl) | 50,1 (15,3) | 1,8 | (−1,0 a 4,6) | 9,1 | 0,299 |
| cLDL (mg/dl) | 107,8 (27,6) | 12,1 | (2,2 a 21,9) | 31,1 | 0,054 |
| LDL pequeñas (mg/dl) | 9,3 (11,1) | 0,7 | (−3,2 a 4,6) | 12,6 | 0,777 |
| LDL grandes (mg/dl) | 99,1 (23,6) | 6,0 | (−1,3 a 13,4) | 23,6 | 0,187 |
| Diámetro medio LDL total (Å) | 266,9 (6,6) | −0,6 | (−2,6 a 1,3) | 6,2 | 0,598 |
| Diámetro medio LDL pequeñas (Å) | 241,6 (6,3) | 1,4 | (−1,1 a 3,9) | 6,8 | 0,356 |
| Diámetro medio LDL grandes (Å) | 271,0 (2,1) | −0,4 | (−0,9 a 0,2) | 1,8 | 0,285 |
| Lp(a) (mg/dl) | 44,9 (53,6) | −2,3 | (−5,7 a 1,2) | 10,8 | 0,288 |
| PCR (mg/dl) | 0,5 (0,7) | −0,3 | (−0,5 a −0,1) | 0,6 | 0,018 * |
| RCV Framingham (%) | 13,9 (9,1) | 3,1 | (1,1 a 5,0) | 6,5 | 0,017 * |
| RCV total SCORE (%) | 5,1 (4,5) | 0,4 | (0,1 a 0,7) | 1,0 | 0,038* |
HbA 1C: hemoglobina glicada; cHDL: colesterol unido a lipoproteínas de alta densidad; cLDL: colesterol unido a lipoproteínas de baja densidad; Lp(a): lipoproteína (a); PCR: proteína C reactiva; RCV: riesgo cardiovascular. Los valores señalados con asterisco muestran significación estadística (p<0,05).
a Valor inicial representado por la media y la desviación estándar.
b Promedio del incremento.
c Intervalo de confianza al 90% del incremento.
d Desviación típica del incremento.
e Valor de p para un IC del 95%.
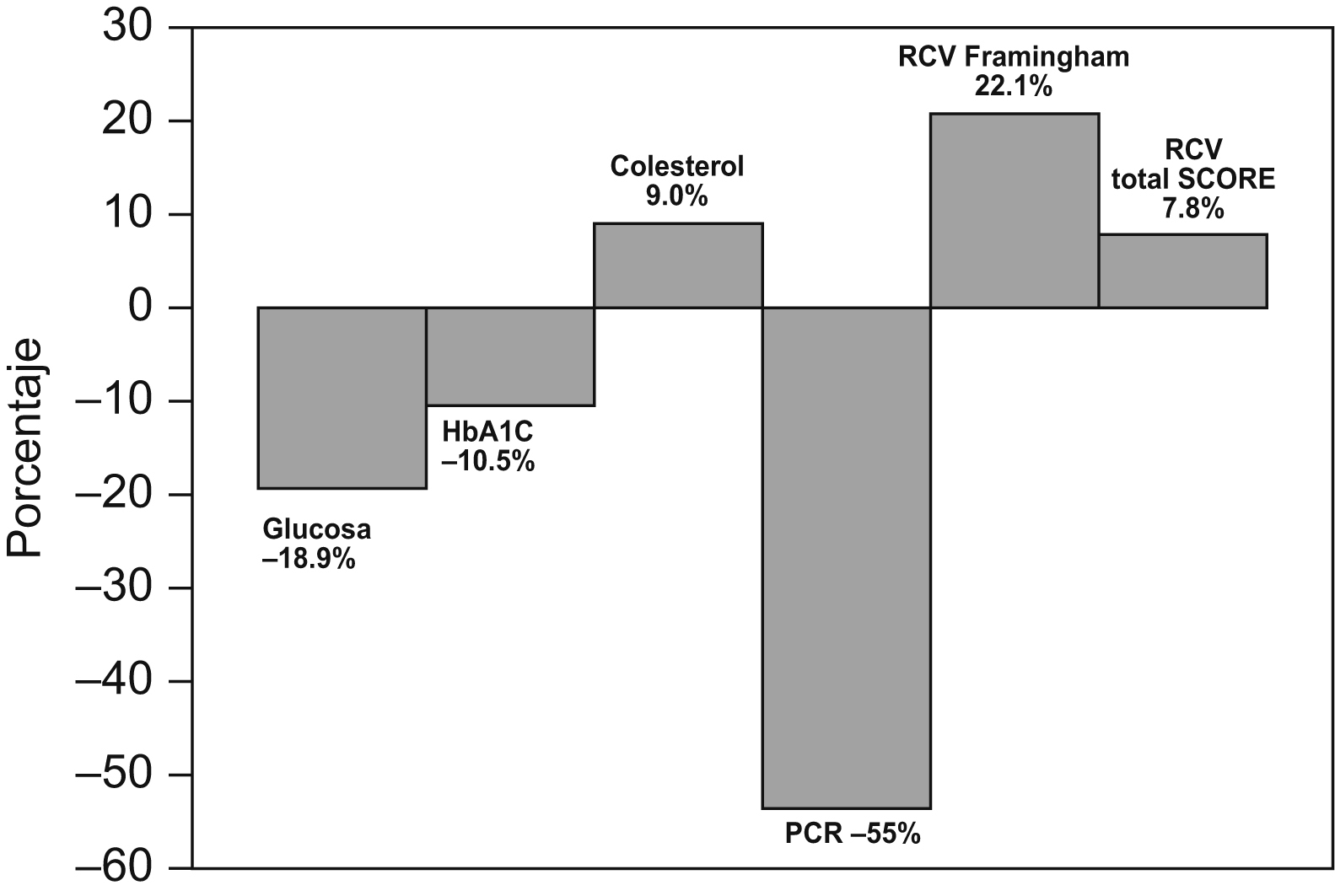
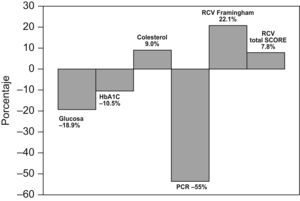
Observamos un incremento estadísticamente significativo en la estimación del riesgo cardiovascular a 10 años según el modelo Framingham y SCORE (adaptado a España). En la figura 1 se representa el porcentaje de modificación de los parámetros, así como su significación estadística.
Figura 1. Porcentaje de variación de los parámetros con significación estadística. HbA1C: hemoglobina glicada; RCV: riesgo cardiovascular.
DiscusiónEl efecto hipoglucemiante de la rosiglitazona está claramente establecido. Se ha descrito una mejoría de la resistencia a la insulina, que parece más eficaz en pacientes obesos, como es el caso de nuestra población de estudio7. Hemos encontrado una reducción media en los valores de glucosa del 18,9% (34,3 mg/dl) y en la HbA1C de 10,5% (0,9 unidades). Esto concuerda con lo descrito por autores como Yki-Järvinen1, que relata una reducción media de la HbA1C de 1–1,5 unidades en un estudio placebo-control en el que se emplea tanto pioglitazona como rosiglitazona.
El efecto antiinflamatorio descrito para ambas glitazonas se refleja en un descenso medio de 55,7% de los valores de PCR en nuestro estudio. Al valorar el riesgo cardiovascular a 10 años —tanto siguiendo el modelo Framingham como el SCORE—, éste aumenta de forma más acusada en el primer caso, por la sobreestimación que este modelo hace en países con riesgo cardiovascular bajo, como es el caso de España6. La elevación del colesterol total es la causa principal del incremento en el riesgo cardiovascular, y va unido a un aumento del cLDL, sin elevación del cHDL. Se ha descrito un aumento de episodios de isquemia miocárdica con el uso de rosiglitazona, y un análisis aún en curso, el ensayo RECORD (Rosiglitazone Evaluated for Cardiac Outcomes and Regulation of Glycaemia in Diabetes), establece una asociación entre rosiglitazona y el incremento en el riesgo de enfermedad cardíaca, aunque no muestra de momento un aumento estadísticamente significativo en el riesgo cardiovascular de los pacientes que reciben el fármaco8.
Observamos un incremento medio de 12,1 mg/dl en la concentración de cLDL total, que no va acompañado de un aumento en el tamaño medio de la partícula (anterior 266,90 Å y posterior 266,28 Å), junto con un incremento del 14,2% en los valores de triglicéridos. En un estudio con 325 pacientes con diabetes mellitus tipo 2 a los que se administró rosiglitazona, Deeg et al4 también encontraron un aumento en la concentración de colesterol total, cLDL y triglicéridos, aunque el aumento fue únicamente de las partículas de LDL grandes, sin cambios en la concentración de las LDL pequeñas. Nuestro grupo de estudio no es muy amplio; esto, junto al hecho de no haber utilizado un grupo control, no nos permite afirmar que el tamaño de las partículas no se modifique con el tratamiento.
Las partículas LDL pequeñas son más susceptibles de experimentar modificaciones cualitativas que las hacen más aterogénicas9, y se ha descrito una asociación a largo plazo entre el tamaño medio de la partícula de LDL y la enfermedad isquémica cardíaca, de tal forma que un descenso en el tamaño medio de las partículas LDL sería un predictor de enfermedad coronaria más potente incluso que parámetros lipídicos, como los valores de cLDL o de cHDL, en pacientes con diabetes mellitus tipo 24. En nuestro caso, el aumento del cLDL total no va acompañado de un cambio en el tamaño medio de la partícula LDL, ni de una disminución de las partículas LDL pequeñas. No obstante, se ha descrito una disminución del riesgo de desarrollar enfermedad cardiovascular en pacientes con valores menores de PCR y similar fenotipo de LDL pequeñas y densas10.
Aunque el riesgo cardiovascular calculado es mayor tras la inclusión de la rosiglitazona, y observamos un aumento de la concentración de colesterol total, sin variación en el tamaño medio de la partícula LDL, es clara la reducción de la PCR y, con ella, de la inflamación, que previene la progresión de la aterosclerosis.
Autor para correspondencia.
María Dolores Albaladejo Otón
Dirección: mariad.albaladejo@carm.es