Comparados con los antiinflamatorios no esteroides (AINE) clásicos, los nuevos AINE selectivos sobre la ciclooxigenasa-2 (COX-2) se asocian a una menor incidencia de efectos gastrointestinales graves1-4.
En este trabajo se describen las primeras notificaciones de sospechas de efectos adversos atribuidas a rofecoxib y celecoxib recibidas en el Centro de Farmacovigilancia de Cataluña.
Material y método
Los métodos aplicados en el Sistema Español de Farmacovigilancia han sido descritos con detalle5. Se analizaron las siguientes características de las notificaciones de sospechas de efectos adversos del rofecoxib y celecoxib recibidas durante los primeros 18 y 12 meses de comercialización respectivamente (hasta el 31 de marzo de 2001): sexo y edad de los pacientes, fármacos sospechosos, tratamientos concomitantes y dosis administradas, efecto adverso y su gravedad, y factores posiblemente contributivos. Se comparó la información citada con la contenida en las notificaciones de sospechas de efectos adversos atribuidos a los AINE no selectivos comercializados a partir de enero de 1983 (fecha de inicio de la Tarjeta Amarilla), excluyendo nabumetona, meloxicam y nimesulida (que tienen cierta selectividad por la COX-2), recibidas durante los dos primeros años tras su comercialización. Para la comparación de proporciones de efectos adversos de rofecoxib y celecoxib con los de otros AINE, se aplicó la prueba de la *2 o una prueba exacta, ajustadas para comparaciones múltiples. Se utilizó el programa estadístico PEPI, versión 4.0.
Resultados
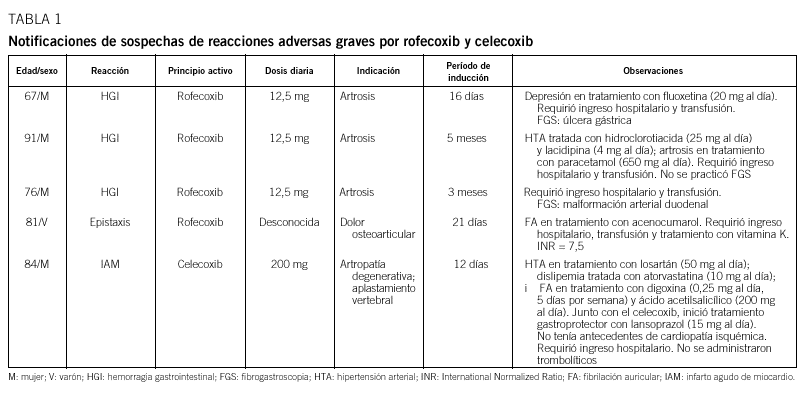
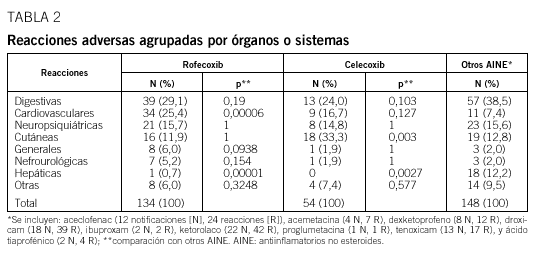
Se recibieron 92 notificaciones (70 relativas a mujeres) de efectos adversos con rofecoxib. En un 58% los afectados eran mayores de 65 años (mediana: 70; extremos: 29-92 años). Los efectos adversos notificados fueron leves en 81 casos, de gravedad moderada en siete, y graves en cuatro (tabla 1). No hubo casos mortales. Las 92 notificaciones describían 134 efectos adversos; los más frecuentes fueron los digestivos (en una proporción no significativamente diferente de la observada con otros AINE), seguidos de los cardiovasculares, en una proporción significativamente superior a la registrada con otros AINE (tabla 2). Dieciséis de los 23 pacientes con efectos adversos gastrointestinales recibían rofecoxib a dosis de 12,5 mg al día. Hubo 4 casos de hemorragia gastrointestinal (HGI), 18 de dolor abdominal y/o dispepsia, y uno de gastritis. Sólo un paciente tenía antecedente de enfermedad ulcerosa. Treinta y dos pacientes (mediana de edad: 74 años; extremos: 45-92), de los que 23 recibían 25 mg al día de rofecoxib, desarrollaron edemas (n = 21), oliguria (n = 5) y/o hipertensión arterial (de nueva aparición en 5 casos, descompensada en 6). De estos pacientes, 11 eran hipertensos conocidos; 5 de ellos recibían diuréticos, dos inhibidores de la enzima conversiva de la angiotensina (IECA), y dos diuréticos e IECA. También se notificó un caso de trombosis de la arteria femoral, que requirió trombectomía, en una paciente de 91 años tratada con rofecoxib a dosis de 12,5 mg al día desde hacía dos meses. Otros efectos adversos de rofecoxib notificados fueron erupción cutánea y/o prurito (en 9 pacientes), mareo (n = 5), cefalea (n = 4) y confusión (n = 4). Se registró un caso de eritema multiforme.
Se recibieron 41 notificaciones (36 relativas a mujeres) de efectos adversos de celecoxib. Un 63% de estos pacientes eran mayores de 65 años (mediana: 69,5; extremos: 31-85 años). Los efectos adversos notificados fueron leves en 38 casos y moderados en dos; uno fue grave y se recuperó (tabla 1). No hubo casos mortales. Las 41 notificaciones describían 54 efectos adversos; los más frecuentes fueron los cutáneos (en 15 casos, entre ellos 5 erupciones eritematosas o maculopapulares, 5 urticarias, tres angioedemas y un eritema multiforme), en una proporción significativamente superior a la observada con otros AINE (tabla 2). Siguieron en frecuencia las reacciones digestivas (7, entre ellas dispepsia o dolor abdominal), cardiovasculares (6, entre ellas edemas e hipertensión) y neuropsiquiátricas (7, las más frecuentes mareo y cefalea), en proporciones no significativamente diferentes de las registradas con otros AINE.
Durante los dos primeros años de comercialización de los AINE no selectivos sobre la COX-2, se recibieron en conjunto 82 notificaciones que describían 148 reacciones adversas; las más frecuentes fueron las digestivas, seguidas de las neuropsiquiátricas y las cutáneas (tabla 2).
Discusión
El principal problema de seguridad de los AINE es su gastrotoxicidad mediada por la reducción de la síntesis de prostaglandinas con funciones citoprotectoras en la mucosa gástrica, como consecuencia de la inhibición de la COX-1. En nuestra serie los efectos adversos gastrointestinales fueron los más notificados para los AINE no selectivos y para rofecoxib, y el segundo grupo más frecuente para celecoxib. Estos resultados coinciden con los de series procedentes de notificación voluntaria en otros países6-9. Aunque la notificación voluntaria de reacciones adversas a medicamentos no permite cuantificar riesgos, estos resultados confirman que los AINE selectivos sobre la COX-2 no están desprovistos de toxicidad digestiva.
Los efectos adversos cutáneos por AINE suelen ser frecuentes, aunque la incidencia real, la patogenia, el aspecto morfológico y la gravedad pueden ser muy diferentes para cada fármaco. En nuestra serie se observó una elevada proporción de efectos adversos cutáneos con celecoxib, lo que también coincide con los resultados de la notificación espontánea en otros países8,9. Las reacciones cutáneas y/o de hipersensibilidad por celecoxib se han atribuido a que su molécula contiene un grupo sulfamida8.
También de manera análoga a lo observado en otras series6-9, los efectos adversos cardiovasculares constituyeron una proporción importante de todos los notificados para los AINE selectivos sobre la COX-2, especialmente para rofecoxib, en comparación con los AINE no selectivos. Los AINE pueden producir edemas e inducir o descompensar la hipertensión arterial o la insuficiencia cardíaca, porque inhiben la síntesis de prostaglandinas renales, con lo que aumentan las resistencias vasculares sistémicas, se reduce la perfusión renal y se inhibe la excreción de sodio y agua. Tanto la COX-1 como la COX-2 contribuyen al mantenimiento de la homeostasis renal, pero la importancia relativa de cada isoforma no está bien definida. La presente serie incluye un caso de trombosis femoral y otro de infarto agudo de miocardio. En otros países también se han notificado casos de cardiopatía isquémica6-8 y de otros episodios trombóticos. Estos efectos protrombóticos se han observado con rofecoxib en un ensayo clínico3, y un reciente metaanálisis10 ha apuntado que éste sería un efecto de clase, no limitado exclusivamente a rofecoxib; no obstante, el citado metaanálisis adolece de problemas metodológicos que confieren incertidumbre a esta hipótesis. Los AINE selectivos sobre la COX-2 pueden desplazar el equilibrio entre los eicosanoides protrombóticos y los antitrombóticos a favor de los primeros, porque dan lugar a una disminución de la producción de prostaciclina en el endotelio vascular sin inhibir la formación del tromboxano plaquetario; esto puede dar lugar a un incremento del riesgo trombótico. Además, comparado con naproxeno, el rofecoxib da lugar a un mayor incremento de la presión arterial (de más de 3 mmHg en la sistólica y más de 1,5 mmHg en la diastólica)10, lo que puede determinar incrementos del riesgo de ictus y de infarto agudo de miocardio del 40 y del 25%, respectivamente.
A pesar de que se ha apuntado que la COX-2 podría ser constitutiva en el cerebro, en nuestra serie se registró una proporción de efectos adversos neuropsiquiátricos similar para rofecoxib, celecoxib y AINE no selectivos.
En resumen, la experiencia adquirida en los primeros meses de comercialización de celecoxib y rofecoxib en nuestro medio confirma que estos fármacos no están desprovistos de toxicidad digestiva, que pueden dar lugar a acontecimientos cardiovasculares adversos, y que el celecoxib presenta un perfil de efectos indeseados diferente de rofecoxib, debido a una mayor proporción de efectos adversos cutáneos con el primero. El perfil de efectos indeseados de estos fármacos es provisional y puede modificarse en el futuro, a medida que se acumule experiencia clínica. La notificación sistemática de las sospechas de efectos indeseados mediante la Tarjeta Amarilla permitirá avanzar en su conocimiento. Dadas las dudas recientemente planteadas sobre el posible incremento del riesgo de acontecimientos cardiovasculares graves asociados a los AINE inhibidores selectivos de la COX-2, y dado su elevado consumo, sería muy conveniente aclarar con ensayos clínicos apropiados si estos fármacos se asocian realmente a un riesgo cardiovascular superior al de los AINE clásicos, y si este riesgo compensa el menor riesgo de toxicidad digestiva.
Agradecimiento
Agradecemos la colaboración de los notificadores. Este trabajo ha sido realizado con el apoyo del Servei Català de la Salut y del Departament de Sanitat de la Generalitat de Catalunya.