El carcinoma escamoso es el tumor maligno más frecuente en cabeza y cuello. Su etiología se debe fundamentalmente al consumo de tabaco y alcohol1. El diagnóstico temprano de los pacientes con esta afección es de especial dificultad dada la escasa expresividad clínica de estos tumores, y en muchos casos se produce el diagnóstico en estadios avanzados de la enfermedad. El diagnóstico y el seguimiento clínicos se basan en la clínica, la exploración física y las técnicas de imagen. El tratamiento quirúrgico a menudo produce una distorsión anatómica que dificulta la detección de recidiva y/o segundas neoplasias. Desde los años setenta, se han estudiado diferentes marcadores tumorales en el carcinoma escamoso de cabeza y cuello (CECC), en un intento de mejorar las posibilidades en el diagnóstico y el seguimiento, sin que, hasta el momento se haya probado su eficacia clínica. Los marcadores clásicamente estudiados han sido el antígeno de célula escamosa2 y los fragmentos solubles de citoqueratina 19 (cyfra 21.13) que, pese a mostrar cierta especificidad por el epitelio escamoso, no muestran un potencial diagnóstico suficiente. Hay nuevos marcadores que aún no se han evaluado de manera precisa en el CECC.
Las cadherinas son proteínas de membrana dependientes del calcio que participan en la formación de uniones adherentes4. Hasta la fecha, se ha podido demostrar un papel supresor de invasividad para un miembro de esta familia, la E-cadherina, también conocida como L-CAM o uvomorulina5. Esta proteína, causante de la adhesión celular, puede determinarse en tejido y en suero, y su pérdida de función se puede relacionar con la invasión tumoral y las metástasis. Se piensa que el gen de la E-cadherina es un gen supresor que interviene en la diferenciación tumoral, pues la proteína no se expresa en el CECC poco diferenciado, y aumenta progresivamente en los CECC moderados y bien diferenciados. Los tumores sin expresión son más agresivos y con mayor incidencia a metastatizar6,7.
La forma soluble de la E-cadherina (80-84 kD) se descubrió en el sobrenadante del medio de cultivo liberado por la línea tumoral de células tumorales humanas MCF-78. Esta forma soluble es el producto de degradación de la forma intacta de la E-cadherina (120 kD) generada por una proteólisis dependiente del calcio. También se ha demostrado su presencia en fluidos biológicos de individuos sanos, aunque los valores séricos estaban más elevados en pacientes con cáncer9-11. Las metaloproteasas o matrixinas (MMP) son endopeptidasas de matriz extracelular. Su determinación se hace en suero mediante anticuerpos específicos. Se ha establecido una clasificación de 4 grupos: colagenasas, estromelisinas, gelatinasas y MMP de membrana12,13. Aunque se pensaba que intervenían sólo en la rotura física de la matriz extracelular por el tumor (invasión local), actualmente se sabe que están implicadas también en el crecimiento del tumor primario y de sus metástasis14,15. Se ha visto un aumento de la expresión de MMP-2 y MMP-9 en el CECC16. En el cáncer de laringe con sobreexpresión de colagenasa 3 (MMP-13) hay mayores tasas de progresión local y metástasis17.
La expresión de anticuerpos (Ac) anti-p53 se puede determinar en tejido y en suero. La mutación de p53 es la alteración genética más común en los cánceres humanos y se ha demostrado por inmunohistoquímica en el CECC. Los anticuerpos séricos de p53 son muy específicos, y no se expresan en individuos sin cáncer, pero no determinan el tipo de tumor18. En el suero de pacientes con CECC se ha observado Ac p53 en el 18-44%, que se ha asociado a la expresión nuclear de la proteína detectada. A pesar de tener una sensibilidad limitada, podría ser útil en el pronóstico, ya que su presencia resultó ser un marcador independiente del riesgo de recidivas y supervivencia19,20. El presente estudio tiene como objetivo evaluar el potencial preliminar de la determinación preoperatoria de nuevos marcadores tumorales en pacientes con CECC.
Material y métodos
Se incluyó en el estudio a los pacientes con CECC diagnosticados y tratados por los servicios de otorrinolaringología de los hospitales Central de Asturias (HUCA de Oviedo) y Valle del Nalón (HVN de Langreo) de la Comunidad Autónoma del Principado de Asturias, entre junio de 2003 y septiembre de 2005, estudio que se cerró en diciembre de 2005. El tiempo de seguimiento fue de 30 meses. Los criterios de selección fueron los siguientes: disponer de una historia que permitiera extraer los datos clínicos y de seguimiento, diagnóstico histopatológico de CECC en el tumor primario, indicación quirúrgica sobre el tumor primario y realización de vaciamiento cérvico-ganglionar, ser el primer diagnóstico de la enfermedad y no haber realizado tratamientos previos con radioquimioterapia.
El diagnóstico clínico se hizo por los procedimientos clínicos (endoscopia, biopsia) y de imagen (tomografía computarizada y resonancia magnética) habituales. Se siguieron las recomendaciones para los estudios de precisión diagnóstica STARD21. El comité ético de investigación clínica aprobó el estudio y se planteó según protocolos establecidos y consensuados. Para la clasificación del estadio tumoral se utilizó el sistema TNM (Tumor, Node, Metastasis Stage Grouping) de la Unión Internacional Contra el Cáncer. A partir de estos criterios, se seleccionó a 39 pacientes, 5 correspondientes al HUCA (12%) y 34 al HVN (88%). La toma de las muestras de sangre se realizó inmediatamente antes de la extirpación quirúrgica, durante la inducción anestésica, previo consentimiento informado. Como muestras de control se incluyeron 10 muestras de sangre procedentes de donantes del Banco de Sangre del Principado de Asturias, todos ellos mayores de 50 años y fumadores. Se realizó una consulta clínica a cada uno de ellos para descartar lesiones displásicas y/o CECC. Se obtuvo una muestra de 10 ml de sangre en un tubo, se esperó el tiempo necesario para que la muestra coagulase y, posteriormente, se centrifugó para separar el suero, se alicuotó y congeló a 80 °C hasta su procesamiento en el Servicio de Análisis Clínicos del HVN. Las variables cuantitativas se expresaron utilizando la media, que se compararon con la t de Student o mediante la U de Mann-Whitney en caso de no seguir una distribución normal. Las variables cualitativas se expresaron como porcentaje y se compararon mediante el test de la x2, con corrección de continuidad de Yates en los casos de tablas de 2 3 2, o bien por la prueba exacta de Fisher en los casos de tablas poco pobladas. Se estableció como nivel de significación estadística un valor de p < 0,05. La supervivencia se analizó mediante las curvas de Kaplan-Meier, utilizando la prueba log-rank. Los puntos de corte de las variables cuantitativas se determinaron utilizando curvas ROC. Los cálculos estadísticos se realizaron mediante el programa estadístico Medcalc® v8.1.1 (MedCalc Software, Mariakerke, Belgium).
Resultados
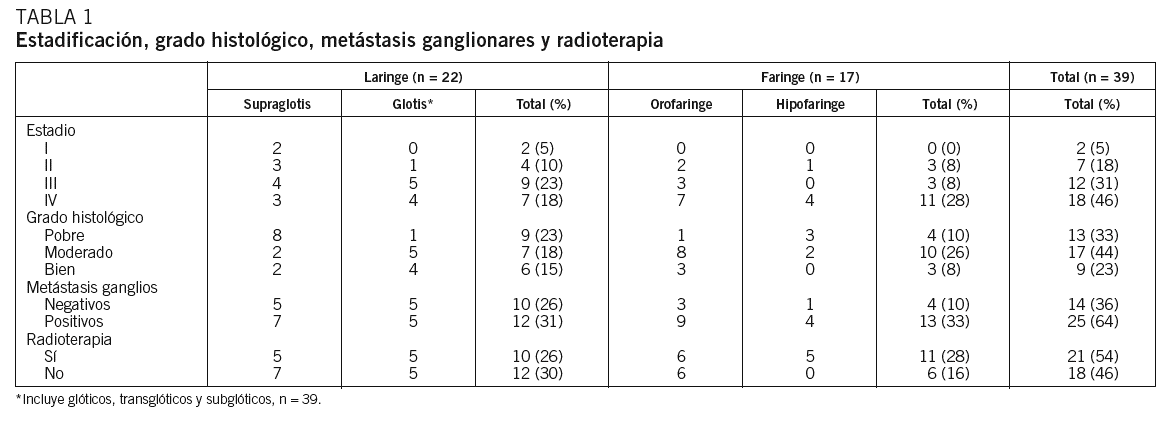
El grupo de 39 pacientes estudiados estaba formado por 37 varones y 2 mujeres. La edad media fue de 61 años, con un rango entre 34 y 80. Casi todos eran fumadores (97,4%) y bebedores de alcohol (89,7%). En cuanto a la localización más frecuente, fue la laringe (22 casos), y en el resto, la faringe (17 casos). Otras de las características clínicas más relevantes de los pacientes se muestran en la tabla 1.
A continuación se muestran los resultados de cada marcador.
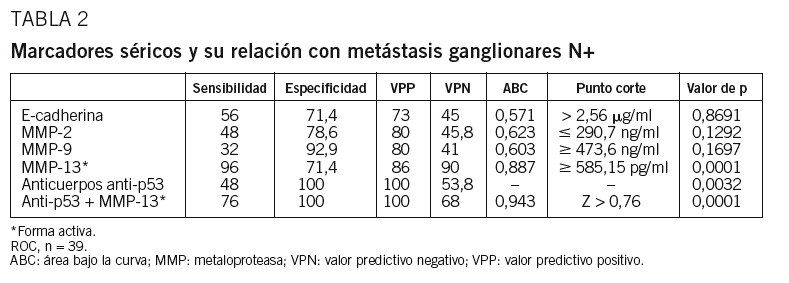
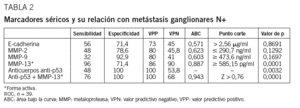
La comparación de los valores de E-cadherina entre pacientes (media 2,97 mg/ml; intervalo de confianza [IC], 2,42-3,51 mg/ml) y controles (media 1,87 mg/ml; IC, 1,66-2,07 mg/ml) mostró diferencias estadísticamente significativas (p = 0,0483). El análisis mediante curva ROC, donde se fijó como punto de corte óptimo 2,56 mg/ml, reveló una sensibilidad del 56% (IC, 34,9-75,6) y una especificidad del 71,4% (IC, 41,9-91,4) (tabla 2); no obstante, no hubo diferencias estadísticamente significativas entre los valores de E-cadherina de los pacientes N positivos (media 2,99; IC, 2,35-3,65) frente a los N negativos (media 2,889; IC, 1,76-4,04), donde p = 0,8691. Las concentraciones de E-cadherina no difirieron en función de la localización tumoral, el grado histológico, el estadio o la supervivencia.
Los valores de MMP-2 entre pacientes (media 355,6 ng/ml; IC, 310,1-401,1) y controles (media 430,1 ng/ml; IC, 331,9-528,3) no mostraron diferencias estadísticamente significativas (p = 0,1393). El análisis ROC fijó como punto de corte óptimo en una concentración de MMP-2 menor o igual a 290,7 ng/ml, para una sensibilidad del 48% (IC, 27,8-68,7) y una especificidad del 78,6% (IC, 49,2-95,1) (tabla 2) para demostrar la presencia de metástasis ganglionares. Sin embargo, no hubo diferencias estadísticamente significativas entre los valores de MMP-2 de pacientes con metástasis (media 330,0; IC, 284,2-375,8) frente a las que no las presentaron (media 401,3; IC, 299,2-503,5), con una p = 0,1292. Por el contrario, se observa una menor supervivencia utilizando el punto de corte ya citado, en los pacientes con concentraciones inferiores o iguales a 290,7 ng/ml, donde la mediana de la supervivencia es de 16 meses, mientras que con valores superiores alcanzó los 35 meses. El estudio comparativo de ambas curvas de supervivencia mostró diferencias estadísticamente significati-vas para la prueba log-rank (x2 = 7,168; gl = 1; p = 0,0074).
Las concentraciones de MMP-9 de pacientes (mediana 243,2 ng/ml; IC, 177,8-332,7 ng/ml) y controles (mediana 159,9 ng/ml; IC, 109,1-236,3 ng/ml) también mostraron diferencias estadísticamente significativas (p = 0,0445). Fijando como punto de corte óptimo 473,6 ng/ml, el análisis ROC para predecir la presencia de metástasis mostró una sensibilidad del 32% (IC, 15-53,5) y una especificidad del 92,9% (IC, 66,1-98,8) (tabla 2) sin que hubieran diferencias estadísticamente significativas entre los valores de MMP-9 de pacientes N positivos (media 345; IC, 247,2-442,7) frente a los N negativos (media 246,6; IC, 160,4-332,9), tomando p el valor de 0,1697.
En cuanto a la MMP-13 activa, sus valores en pacientes (mediana 648,12; IC, 597,39-688,70) y controles (mediana 534,49; IC, 349,06-678,99) mostraron diferencias estadísticamente significativas (p = 0,0151). Para tratar de predecir la presencia de metástasis con este marcador, se fijó un punto de corte óptimo en 585,15 pg/ml, con una sensibilidad del 96% (IC, 79,6-99,3) y una especificidad del 71,4% (IC, 41,9-91,4) (tabla 2). El valor predictivo positivo (VPP) fue del 86%, mientras que el valor predictivo negativo (VPN) del 90%. Un total de 25 pacientes con valores superiores al punto de corte presentaron N positivo, por 4 que no. Todos los pacientes con valores superiores a 689,76 pg/ml tenían metástasis ganglionares. En este caso sí hubo diferencias estadísticamente significativas (p = 0,0001) entre los valores de MMP-13 de los pacientes con N positivo (mediana 679,63; IC, 628,6-742,6) frente a los que no las presentaron (mediana 536,62; IC, 461,3-640,7).
El último marcador evaluado individualmente fueron los Ac anti-p53. En la tabla 3 se muestran los diferentes resultados encontrados en pacientes y en controles.
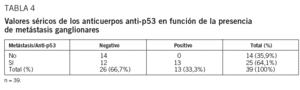
La presencia de estos anticuerpos fue exclusiva de pacientes, sin que se encontraran en controles. El análisis estadístico mostró diferencias estadísticamente significativas (x2 = 2,99, p = 0,030). En la tabla 4 se exponen los resultados de los Ac anti-p53 en función de la presencia de metástasis.
No hubo ningún paciente sin metástasis ganglionares que tuviese los Ac anti-p53 positivos, aunque hubo 12 pacientes con metástasis ganglionares en los que no se detectaron anticuerpos séricos. La sensibilidad de la prueba para el diagnóstico de N positivo fue del 48% y la especificidad del 100%. El VPP fue del 100% y el VPN, del 53,8%. El valor de x2 fue 8,705, y se hallaron diferencias estadísticamente significativas (p = 0,0032). El resto de los resultados de los Ac anti-p53 se muestran en la tabla 5.
En cuanto a supervivencia en función de la presencia o ausencia de Ac anti-p53 en suero, la mediana de la supervivencia de los pacientes sin Ac anti-p53 séricos fue de 35 meses, mientras que si los tenían, se reducía a 17 meses. Estos resultados eran estadísticamente significativos para la prueba log-rank (x2 = 5,28; gl = 1; p = 0,0216).
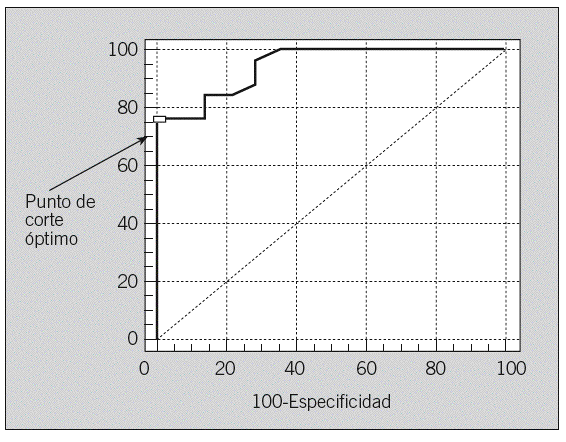
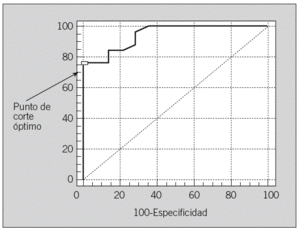
Los 2 únicos marcadores con potencial para predecir la presencia de metástasis ganglionares fueron los Ac anti-p53 y la MMP-13 activa. Mediante regresión logística binaria, evaluamos el potencial de ambos marcadores de manera conjunta para el diagnóstico de metástasis ganglionares. Al utilizar los resultados obtenidos, se consiguió la ecuación siguiente: Z = 11,86 + 0,019 X2 + 20,443 X1, donde X1 = Ac anti-p53 (cualitativo) y X2 = MMP-13 activa. De cada paciente se calcularon los valores de Z y posteriormente la posibilidad de metástasis mediante la ecuación: probabilidad de N+ = eZ/1+ eZ. La curva ROC obtenida utilizando ambos marcadores se puede observar en la figura 1.
Fig. 1. Curva ROC para los valores de Z (Ac anti-p53 +MMP13 activada) frente N+, (n = 39).
La sensibilidad obtenida fue del 76%(IC, 54,9-99,6) y la especificidad del 100% (IC, 76,7-100) (tabla 2) para un valor de Z > 0,76. El VPP fue del 100% y el VPN, del 70%.
Discusión
Uno de los principales retos en el tratamiento del cáncer es cómo poner de manifiesto la presencia de metástasis en distintos tejidos. Esto es especialmente difícil si se utilizan marcadores tumorales, los cuales son en el mayor número de casos proteínas presentes en individuos sanos. Todavía se conoce poco sobre cuáles serían lo marcadores tumorales ideales en el CECC. Este hecho, unido a la inexistencia de perfiles de marcadores tumorales aplicables en el CECC, justificó este estudio.
Los valores de la fracción soluble de la E-cadherina solamente mostraron diferencias estadísticamente significativas con la población control, como parece que también ocurre en el cáncer de próstata22; en cambio, no se asoció a la presencia de metástasis, hecho que contrasta con los resultados obtenidos mediante inmunohistoquímica, donde su mayor expresión se relacionaría con su menor número de metástasis23.
Los resultados de la MMP-2 fueron algo contradictorios, no había diferencia estadísticamente significativa ni con la población control, ni con la presencia de metástasis, ni con el resto de parámetros clínicos de interés, como habían publicado otros autores24,25; sin embargo, sí hubo diferencias con la supervivencia. Pensamos que el hecho de presentar una peor supervivencia con valores bajos de MMP-2 pueda deberse al tamaño muestral. Otra posible causa de ello podría ser que la MMP-2 predominara en su forma activa en el suero de pacientes con CECC. No obstante, estos datos deben contrastarse con estudios más amplios, pues se han descrito muchas variaciones de los valores de MMP-2 en los pacientes con CECC26,27.
Los valores séricos de MMP-9 difirieron de modo estadísticamente significativo en comparación con la población control. Este hecho ya lo habían recogido diversos estudios26-28, por lo que parece claro que la MMP-9 está implicada en la patogenia del CECC; sin embargo, los valores de MMP-9 no mostraron diferencias significativas con el resto de parámetros clínicos estudiados, por lo que son necesarios nuevos estudios para confirmar estos hallazgos.
Los resultados de la forma activa de la MMP-13 mostraron diferencias significativas con el grupo control y con el grupo de pacientes con metástasis gangliolares. Hasta la fecha no hemos encontrado ningún otro estudio sobre la forma activa de la MMP-13 en CECC; sin embargo, hay otros estudios que asocian valores elevados de MMP-13 con diseminación metastásica en cáncer de próstata29, y otros que refieren que la forma activa de esta MMP predomina en pacientes con melanoma metástasico30. El hecho de que no haya datos en la bibliografía a este respecto nos hace ser prudentes en la valoración de los resultados, por lo que son necesarios estudios más amplios.
La presencia de Ac anti-p53 se ha determinado en distintos trabajos sobre CECC, en los que se han mostrado resultados contradictorios. Nuestros resultados muestran la presencia de Ac anti-p53 circulantes en el 33% de los pacientes con CECC, sin que aparecieran en ninguno de los controles. Otros trabajos publican resultados similares31,32, por lo que parece que la determinación de estos Ac podría tener cierto potencial. La presencia de estos Ac se asoció con la presencia de metástasis ganglionares, que están presentes en todos los pacientes que presentaban Ac anti-p53 circulantes; sin embargo, en 12 pacientes con metástasis no se pudo detectar su presencia. La confirmación de estos hallazgos sería de especial interés dado que ya hay precedentes que confirman estos resultados32,33.
La presencia de estos Ac circulantes también se ha asociado con tumores faríngeos, los cuales parecen mostrar mayor expresión de la proteína p53, en comparación con otras zonas como la laringe34.
También hemos encontrado una asociación positiva entre la presencia de Ac anti-p53 y estadios avanzados de la enfermedad (III y IV) frente a estadios iniciales (I y II). Nuevos estudios también podrían aclarar la relación entre la presencia de Ac anti-p53 y el grado de diferenciación histológico, debido a los resultados contradictorios encontrados en la bibliografía35.
La información pronóstica puede ser de especial utilidad en este tipo de pacientes. La presencia de Ac anti-p53 se asoció a una peor supervivencia. Estos hallazgos están en la misma dirección que otros trabajos ya publicados32. Sin embargo, otros autores no obtuvieron resultados similares36,37, por lo tanto son precisos nuevos estudios.
El análisis multimarcador nos dio la posibilidad de obtener una resolución diagnóstica mejor, en comparación con la utilización de un marcador solo. El uso combinado de la MMP-13 activa y los Ac anti-p53 mejoró nuestra capacidad para esclarecer la presencia de metástasis ganglionares, y los verdaderos positivos aumentaron del 33 al 44%, con un número de falsos negativos menor (30 al 15%). Sin embargo, todavía hay un 30% de pacientes con metástasis que no pudimos detectar. Este trabajo refleja que, si bien el trabajo con marcadores tumorales es muchas veces complicado, la utilización de marcadores de forma conjunta puede ser útil para vencer algunas de las limitaciones existentes. El contraste de estos resultados con estudios de mayor tamaño muestral y la adición de nuevos marcadores son los pasos siguientes para conseguir un conocimiento mejor del CECC.