El SARS-CoV-2 es un virus RNA perteneciente a la familia de los coronavirus que causa la COVID-19. Desde que se describieron los primeros casos en China hasta la actual pandemia, esta enfermedad ha supuesto un reto clínico importante para el sistema sanitario de todos los países. Desde el punto de vista clínico, se puede manifestar de diversas formas: desde asintomáticos, pasando por neumonías bilaterales hasta síndromes de distrés respiratorio del adulto1. Hasta la fecha, su diagnóstico se ha basado sobre todo en pruebas que confirmen la presencia del SARS-CoV-2, ya que la sintomatología que presentan los pacientes puede ser común a otros virus, bacterias o incluso a algunas bacterias atípicas y no debemos olvidarnos de evaluarlos para descartarlos como posibles agentes causales de la enfermedad que observemos. Ante la sospecha del SARS-CoV-2 como causante de la infección, la determinación mediante la reacción en cadena de la polimerasa inversa (del inglés reverse-transcription polymerase chain reaction [RT-PCR]) en tiempo real ha sido hasta el momento la prueba gold-standard2. Sin embargo, a pesar de que las RT-PCR suelen poseer una alta sensibilidad y especificidad, los clínicos nos hemos encontrado en varias ocasiones con pacientes con alta sospecha clínica (criterios epidemiológicos, clínicos, analíticos y radiológicos) y con resultados de PCR reiteradamente negativos. Por ello, nos preguntamos, en primer lugar, si la fuente desde la que se ha obtenido la muestra era la idónea, ya que se realiza a través de un exudado nasofaríngeo debido a que es en esa región donde el virus experimenta una tasa de mayor replicación. Sin embargo, también se podrían emplear otras muestras alternativas como el exudado orofaríngeo, esputo, saliva o el lavado broncoalveolar (esta última implicando mayor riesgo para el personal que realiza su obtención). En segundo lugar, nos planteamos si la muestra ha sido obtenida y transportada hacia el laboratorio de forma adecuada y sin contaminación y, en tercer lugar, si la muestra ha sido procesada de manera óptima para obtener el máximo rendimiento de la prueba.
Dado que la RT-PCR es una prueba que requiere al menos 4-6 h en su realización y sus costes son elevados, los esfuerzos recientes en el diagnóstico de la COVID-19 se han centrado también en los inmunoensayos (del inglés enzyme-linked immunosorbent assay [ELISA]) y en los test rápidos de antígenos y anticuerpos (tabla 1). Por un lado, el test ELISA es una prueba inmunoenzimática que determina la presencia de anticuerpos IgM e IgG, o una combinación de IgM+IgA. El coste de esta prueba es bajo, y se realiza en unas 3,5-4 h. Por otro lado, los test rápidos realizan una cromatografía en formato de ensayo de flujo lateral y permiten obtener de manera sencilla resultados en 20-60 min, pero con una baja sensibilidad.
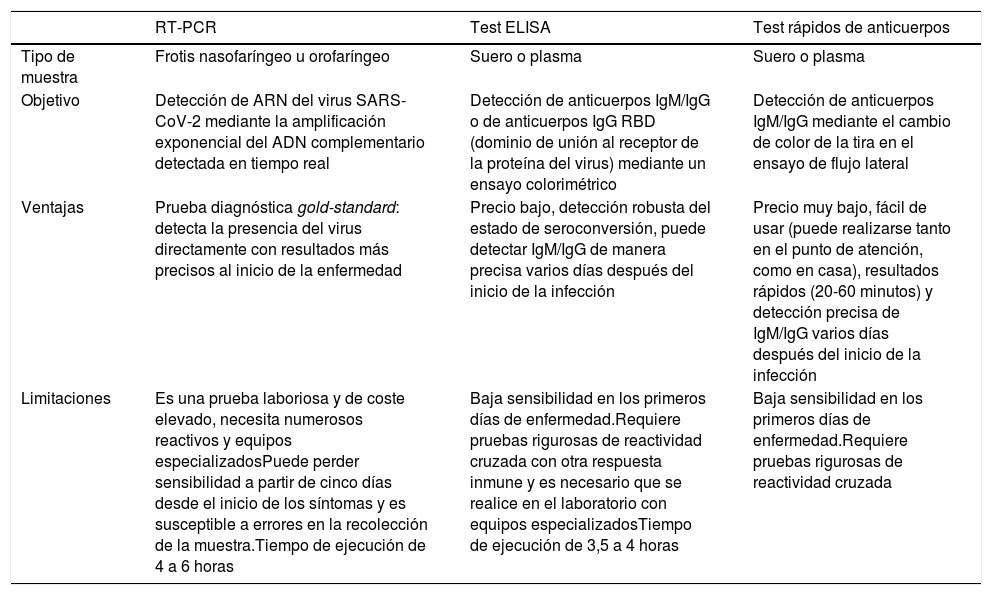
Comparativa de las diferentes pruebas diagnósticas principales frente a la COVID-19
| RT-PCR | Test ELISA | Test rápidos de anticuerpos | |
|---|---|---|---|
| Tipo de muestra | Frotis nasofaríngeo u orofaríngeo | Suero o plasma | Suero o plasma |
| Objetivo | Detección de ARN del virus SARS-CoV-2 mediante la amplificación exponencial del ADN complementario detectada en tiempo real | Detección de anticuerpos IgM/IgG o de anticuerpos IgG RBD (dominio de unión al receptor de la proteína del virus) mediante un ensayo colorimétrico | Detección de anticuerpos IgM/IgG mediante el cambio de color de la tira en el ensayo de flujo lateral |
| Ventajas | Prueba diagnóstica gold-standard: detecta la presencia del virus directamente con resultados más precisos al inicio de la enfermedad | Precio bajo, detección robusta del estado de seroconversión, puede detectar IgM/IgG de manera precisa varios días después del inicio de la infección | Precio muy bajo, fácil de usar (puede realizarse tanto en el punto de atención, como en casa), resultados rápidos (20-60 minutos) y detección precisa de IgM/IgG varios días después del inicio de la infección |
| Limitaciones | Es una prueba laboriosa y de coste elevado, necesita numerosos reactivos y equipos especializadosPuede perder sensibilidad a partir de cinco días desde el inicio de los síntomas y es susceptible a errores en la recolección de la muestra.Tiempo de ejecución de 4 a 6 horas | Baja sensibilidad en los primeros días de enfermedad.Requiere pruebas rigurosas de reactividad cruzada con otra respuesta inmune y es necesario que se realice en el laboratorio con equipos especializadosTiempo de ejecución de 3,5 a 4 horas | Baja sensibilidad en los primeros días de enfermedad.Requiere pruebas rigurosas de reactividad cruzada |
Cabe destacar que los test rápidos de anticuerpos y las pruebas de ELISA proporcionan información adicional del estado inmunitario del paciente con respecto a la prueba RT-PCR3 (tabla 1), aunque aún se desconoce si pueden indicar que el paciente es inmune a futuras reinfecciones. Estas técnicas tienen como puntos débiles que poseen una baja sensibilidad (cercana al 50%) en los primeros 7 días de la enfermedad (aumentando con el paso de los días hasta el 88%) y que están afectadas por el estado inmunitario del paciente4. Por estos motivos, la información proporcionada por estos test es de poca utilidad en muchos casos y en algunos es incluso nula, como es el caso de pacientes con algunos tipos de inmunodeficiencias. Sin embargo, la rapidez de los test rápidos para proporcionar los resultados, su sencillez a la hora de su realización y su precio son sus virtudes más relevantes2. Además, la confirmación de casos sospechosos de COVID-19 mediante pruebas serológicas podría ayudar a reducir el riesgo de exposición de los pacientes, así como evitar la realización de RT-PCR y reservar así su uso para otros pacientes5.
Por todo ello, a pesar de que los actuales test diagnósticos para un nuevo virus poseen algunas deficiencias, poco a poco se van mejorando los rendimientos y subsanando los posibles errores de las tomas de muestras y de la localización del muestreo, haciendo de ellas un pilar fundamental para que el clínico disponga de ayuda en la toma de decisiones diagnóstico-terapéuticas.