El trasplante pulmonar es un procedimiento terapéutico, médico-quirúrgico, indicado en enfermedades pulmonares terminales e irreversibles con los tratamientos médicos actuales, excepto el carcinoma pulmonar. Es un tratamiento emergente en atención médica.
En esta revisión se analizan las complicaciones más frecuentes del trasplante pulmonar relacionadas con: el injerto (rechazo y disfunción crónica); la inmunosupresión (infecciones, hipertensión arterial, diabetes, etc.); otras especialmente frecuentes (gastrointestinales, osteoporosis, etc.) y la actitud terapéutica más razonable.
Se especifican los controles a realizar para vigilar la evolución del injerto y del paciente, las recomendaciones generales para la consecución de un estilo de vida saludable y de la mayor calidad posible y la supervivencia tanto del registro español como del registro internacional, su evolución histórica y las causas más frecuentes de muerte, para poder así analizar la utilidad real del trasplante.
The lung transplantation is a therapeutic procedure indicated for lung diseases that are terminal and irreversible (except lung cancer) despite the best medical current treatment. It is an emergent procedure in medical care.
In this review, an analyse is made of the most frequent complications of lung transplant related to the graft (rejection and chronic graft dysfunction), immunosuppression (infections, arterial hypertension, renal dysfunction, and diabetes), as well as others such as gastrointestinal complications, osteoporosis. The most advisable therapeutic options are also included.
Specific mention is made of the reviews and follow-up for monitoring the graft and the patients, as well as the lifestyle recommended to improve the prognosis and quality of life. An analysis is also made on the outcomes in the Spanish and international registries, their historical evolution and the most frequent causes of death, in order to objectively analyse the usefulness of the transplant.
Es una reacción antígeno-anticuerpo (inmunidad humoral) que se origina cuando el receptor está sensibilizado y tiene anticuerpos contra antígenos HLA del donante; es importante en el trasplante renal pero muy raro en el pulmonar, es un cuadro precoz, muy agudo y muy grave, y se evita haciendo un emparejamiento HLA donante-receptor.
Rechazo agudo humoralEs una reacción entre anticuerpos desarrollados por el receptor después del implante, contra los antígenos del sistema HLA del donante u otros desconocidos1; es un capítulo hoy en día mal conocido, en investigación, poco frecuente, aunque no excepcional, que se manifiesta como una capilaritis con depósito de complemento en los tabiques alveolares. Responde mal a los tratamientos.
Rechazo agudo celularEs la reacción natural de nuestro sistema inmune para eliminar el cuerpo extraño que supone el injerto1,2; en mayor o menor grado se produce casi siempre. Consiste en que los linfocitos del receptor se sensibilizan contra las primeras células que encuentran del donante, que son las del endotelio capilar, produciéndose un infiltrado inflamatorio que se extiende a arteriolas, tabiques alveolares y a todo el pulmón. Esta reacción, si no fuese controlada por la medicación, sería progresiva en el tiempo y acabaría destruyendo el órgano. Se diagnostica por biopsia transbronquial, que nos indica el grado de infiltración linfocitaria y se gradúa de 1 a 4. El tratamiento con bolos de esteroides es muy eficaz.
Es muy frecuente, afecta al 75% de los pacientes y a algunos varias veces a lo largo de su vida.
Al ser un cuadro progresivo, las manifestaciones clínicas también son progresivas y comienzan con síntomas leves como tos, opresión o leve dificultad respiratoria y febrícula, cuya intensidad va aumentando, lenta o rápidamente, hasta aparecer fiebre elevada, disnea intensa, leucocitosis, etc. La radiografía de tórax puede ser anodina al principio, o mostrar un leve patrón intersticial a veces con un pequeño derrame pleural que progresa a una opacificación total del pulmón. Es muy característico que curse con disminución de la saturación de oxígeno y la espirometría no muestra cambios inicialmente.
Es fundamental la sospecha o diagnóstico precoz. El retraso en el diagnóstico y el tratamiento supone un riesgo de que las lesiones se hagan irreversibles y repercutan negativamente en la función pulmonar o desencadene una bronquiolitis obliterante.
La sospecha inicial debe ser clínica y se debe confirmar por broncofibroscopia (BFC) y biopsia transbronquial, cuya rentabilidad es muy elevada. Si la sospecha clínica es bastante evidente o no se puede realizar una BFC por el estado del paciente, se realiza una prueba terapéutica administrando esteroides a dosis elevadas. Si el cuadro revierte en las primeras 24-48h se trata sin duda de un rechazo agudo; si no hay respuesta, se deben realizar todos los procedimientos necesarios para llegar a un diagnóstico.
Este cuadro no debe ser tratado ambulatoriamente, debe ser remitido al hospital.
InfeccionesSon las complicaciones más frecuentes. Se deben al estado de inmunosupresión del paciente y a otros factores3 (sutura bronquial, alteración del aclaramiento mucociliar, abolición del reflejo de la tos, etc.).
Son más graves en los primeros meses del trasplante por el estado de mayor inmunosupresión y la debilidad del paciente, y conforme pasan los meses/años se convierten en más benignas (sin que ello suponga la ausencia de riesgo) y por agentes más habituales3.
Los primeros meses los agentes productores pueden ser bacterias, hongos4, virus, protozoos, parásitos5, etc., y el órgano diana es el pulmón trasplantado o nativo si es un trasplante unipulmonar.
La presencia de fiebre y leucocitosis con o sin manifestaciones radiológicas obliga a ingresar en un hospital para un adecuado estudio y tratamiento.
Pasados los meses y reducida la inmunosupresión, las infecciones pueden ser similares a las producidas en la población general6; es muy frecuente la infección de vías respiratorias que cursa con tos, expectoración, febrícula y opresión torácica, cuadro que es indistinguible de un episodio leve de rechazo agudo. En estos casos se puede realizar una prueba terapéutica o antibioterapia empírica con un betalactámico o una quinolona; si pasados 2-3 días no ha habido mejoría o es escasa se debe remitir al equipo de trasplante para valoración del paciente, pues podemos estar ante un rechazo agudo o una infección por citomegalovirus (CMV) y un nuevo retraso en el diagnóstico por un segundo tratamiento empírico podría llevar al paciente a una situación de gravedad e irreversibilidad.
Unas notas sobre el citomegalovirusEs un virus del grupo herpes y, como todos ellos, afecta a la población general, quedando en estado latente de por vida.
En la población general la infección por CMV cursa de forma asintomática y solamente sabemos que se ha pasado porque la persona infectada ha producido anticuerpos contra el CMV del tipo IgG. El 80% de la población adulta española ha pasado en algún momento de su vida la infección asintomática por CMV y posee anticuerpos de tipo IgG; se denominan seropositivos, tienen el virus latente pero nunca se reactivará.
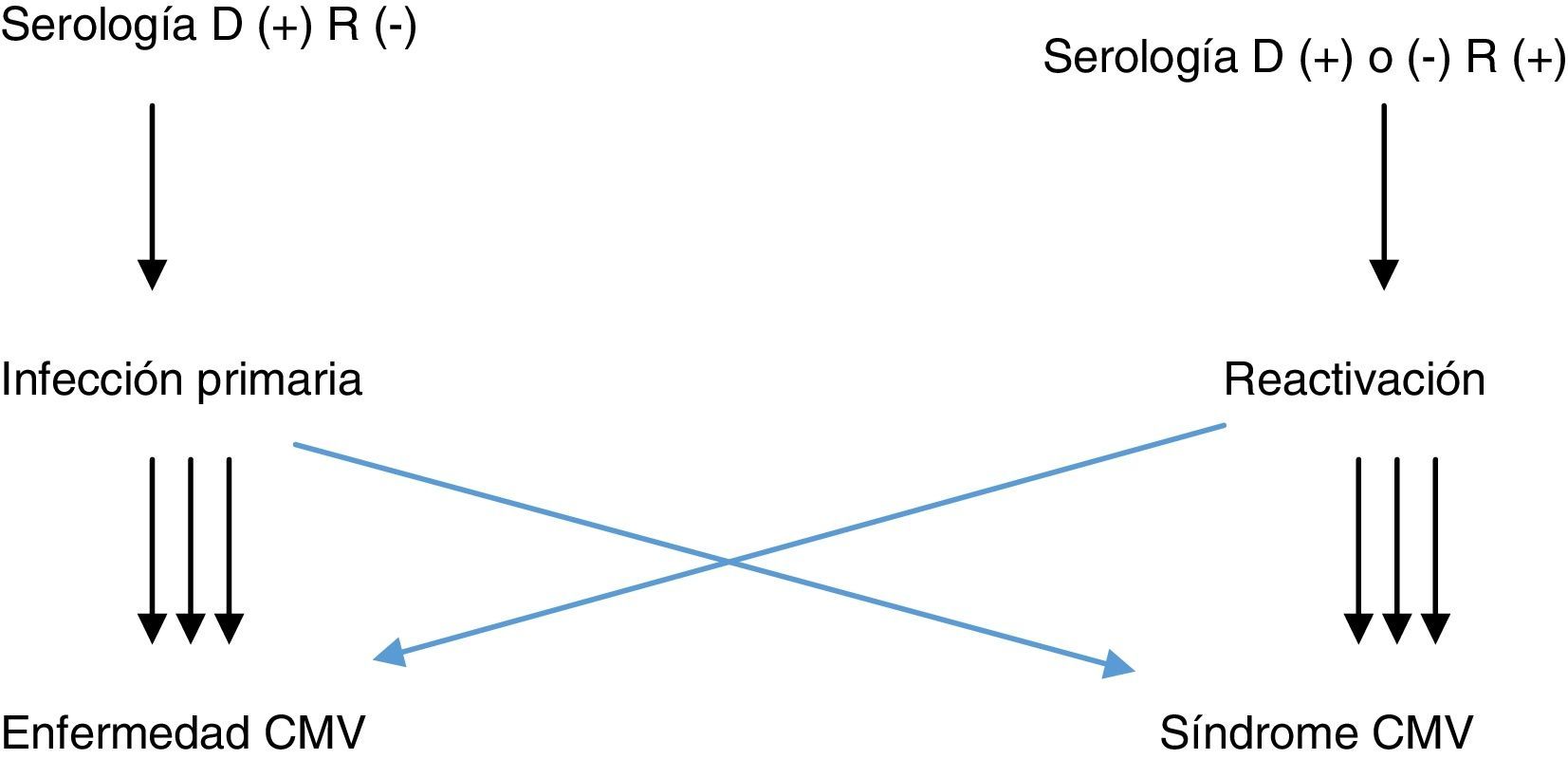
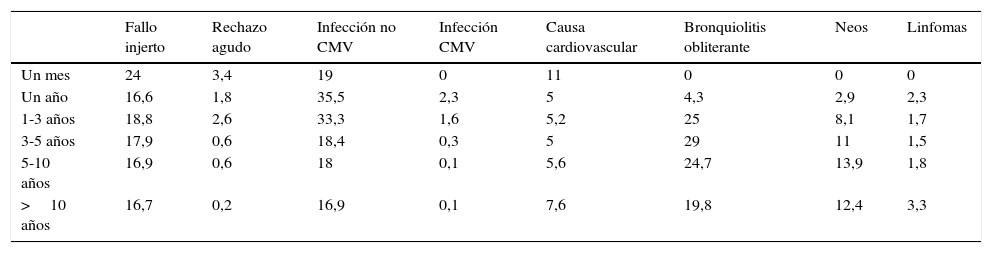
Un paciente trasplantado puede presentar una infección activa por 2 vías: por reactivación de su virus latente en receptores seropositivos o porque la haya adquirido en el pulmón trasplantado o por transfusión de hemoderivados de un donante seropositivo siendo él seronegativo (fig. 1).
En el primer caso se dice que tiene una reactivación, y en el segundo, una infección primaria; estos son, en principio, cuadros más graves, ya que el paciente no posee anticuerpos.
Tanto en uno como en otro, la afectación por el virus puede ser leve y cursar con fiebre, alteración del estado general y leucopenia –se denomina síndrome CMV–, o grave y afectar a cualquier órgano –se denomina enfermedad como miocarditis, hepatitis, esofagitis, colitis, encefalitis, neumonitis CMV–, y puede desencadenar insuficiencia respiratoria y muerte.
Afecta al 80% de los pacientes y por esa alta tasa se realiza profilaxis con ganciclovir/valganciclovir en todos los pacientes en los que donante y/o receptor sean seropositivos7–9.
El diagnóstico del síndrome o la enfermedad se realiza mediante estudios virológicos en sangre (antigenemia o PCR) o por biopsia del órgano afectado.
El tratamiento consiste en la administración de ganciclovir intravenoso y/o valganciclovir oral.
Disfunción crónica del injertoEs el deterioro de la función pulmonar de manera crónica e irreversible. Se define por una disminución irreversible del FEV1 por debajo del 80% del valor basal conseguido tras el trasplante, afecta a más del 30% de los pacientes e incluye 2 procesos diferentes: el síndrome restrictivo (RAS) y el síndrome de bronquiolitis obliterante (BOS)10,11.
El RAS cursa con patrón intersticial y fibrosis fundamentalmente de lóbulos superiores y disminución de la capacidad pulmonar total, se da en el 30% de las disfunciones crónicas del injerto, su mecanismo no está aclarado y tiene muy mal pronóstico, con mayor impacto en la sobrevida que el BOS.
El BOS es una disfunción crónica del injerto sin RAS; se da en el 70% de las disfunciones crónicas del injerto, se caracteriza por un síndrome obstructivo, con atrapamiento aéreo, TAC torácica con árbol en brotes y dilataciones bronquiales. Tiene mal pronóstico, aunque la sobrevida media es del doble con respecto a RAS.
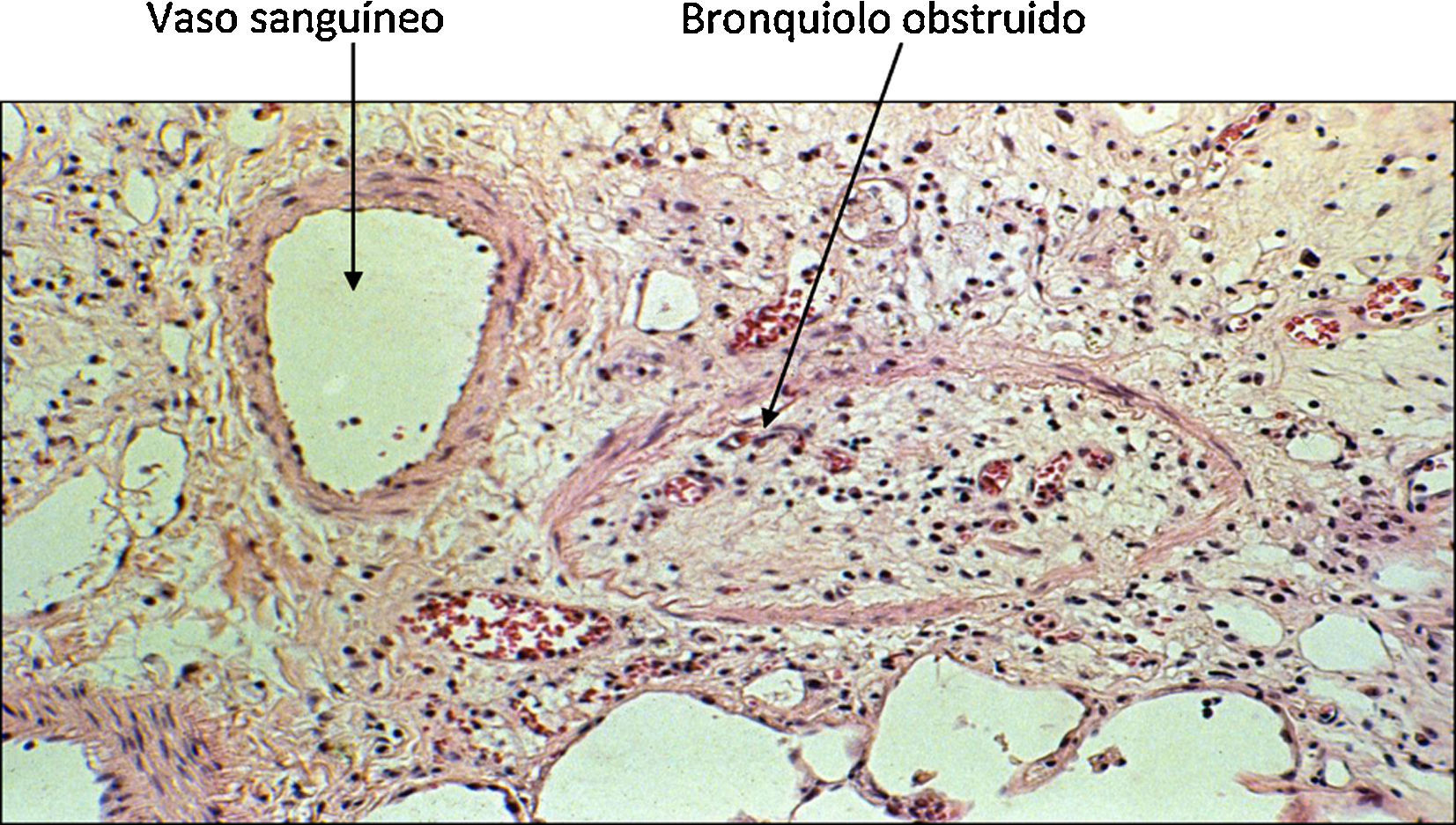
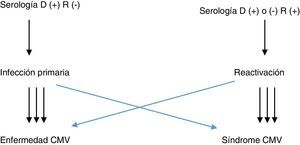
Se caracteriza por un cuadro de obstrucción bronquial (fig. 2) que se manifiesta por una disminución progresiva del flujo espiratorio, y cursa con disnea progresiva que no responde a broncodilatadores, e infecciones de vías aéreas de repetición. En los estadios avanzados se acompaña de insuficiencia respiratoria. El cuadro puede evolucionar de forma rápida y progresiva en uno o 2 años, o de forma lenta y escalonada a lo largo de varios años.
En general, responde mal a los diversos tratamientos ensayados (aumento o cambio de inmunosupresores, azitromicina, etc.), obteniéndose únicamente en algunos casos una estabilización de la función pulmonar12, pero casi nunca una reversión. La mayoría de los pacientes fallecen, siendo una de las principales causas de muerte a largo plazo, o hay que retrasplantar.
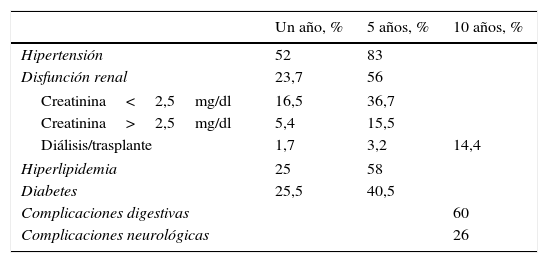
Complicaciones no neumológicas (tabla 1)13Hipertensión arterialAparece en algunas series hasta en el 50% de los pacientes trasplantados.
Complicaciones no neumológicas
| Un año, % | 5 años, % | 10 años, % | |
|---|---|---|---|
| Hipertensión | 52 | 83 | |
| Disfunción renal | 23,7 | 56 | |
| Creatinina<2,5mg/dl | 16,5 | 36,7 | |
| Creatinina>2,5mg/dl | 5,4 | 15,5 | |
| Diálisis/trasplante | 1,7 | 3,2 | 14,4 |
| Hiperlipidemia | 25 | 58 | |
| Diabetes | 25,5 | 40,5 | |
| Complicaciones digestivas | 60 | ||
| Complicaciones neurológicas | 26 | ||
Su control no supone ningún problema especial y puede ser tratada con las medidas habituales: antagonistas del calcio (amlodipino) o inhibidores de la enzima convertidora de angiotensina (enalapril); sin embargo, un control no adecuado supone un riesgo añadido para el desarrollo de insuficiencia renal crónica y progresiva por su efecto aditivo sobre la nefrotoxicidad de los anticalcineurínicos.
DiabetesLa aparición de diabetes es relativamente común en los pacientes con trasplante pulmonar, 25-33%, por el uso de esteroides en muchos de ellos antes del trasplante y en todos como tratamiento inmunosupresor, asociado al uso de anticalcineurínicos, fundamentalmente tacrolimus.
Es especialmente frecuente en pacientes con fibrosis quística (FQ)6.
Debe ser controlada con dieta, ejercicio físico, antidiabéticos orales y/o insulina para reducir el riesgo cardiovascular.
Insuficiencia renal crónicaEstá relacionada estrechamente con la nefrotoxicidad de los anticalcineurínicos, aunque puede ser agravada por otros factores, hemodinámicos, otros nefrotóxicos, etc. Un buen ajuste de niveles y dosis reduce su incidencia.
Una vez instaurada se debe consultar con el especialista correspondiente.
OsteoporosisLa población de pacientes candidata a trasplante pulmonar se compone mayoritariamente de enfermos crónicos, muchos de ellos con actividad física disminuida durante años, algunos con tratamiento esteroideo y los más jóvenes presentan FQ. Esto explica que la mayoría presenten osteopenia u osteoporosis ya antes del trasplante; se calcula que el 32-54% de los pacientes en lista de espera para trasplante tienen ya osteoporosis.
El tratamiento inmunosupresor acelera la pérdida de densidad ósea durante los 3-6 primeros meses y, por tanto, el riesgo de fracturas vertebrales que se estima es muy superior al de personas de la misma edad.
El tratamiento más efectivo para controlar esta situación es la asociación de suplementos de calcio y la administración de bifosfonato, y es más eficaz si se inicia antes del trasplante, mientras el paciente está en lista de espera, y se prolonga durante al menos 6 meses.
Los controles de densitometría que se realizan nos informarán de la conveniencia o no de su administración de por vida.
Alteraciones gastrointestinalesAunque las complicaciones que aparecen en los pacientes con trasplante pulmonar son múltiples y muy variadas, las que se refieren al aparato digestivo forman un grupo muy importante14.
Es de destacar la relativa frecuencia con la que se produce perforación de colon en los primeros días del trasplante. La frecuente aparición de gastroparesia, de mecanismo no bien conocido, repercute en la absorción de medicamentos, aunque es fácil corregir con procinéticos tipo domperidona o metoclopramida.
El reflujo gastroesofágico se ha asociado con la aparición de BOS en algunos pacientes.
Pueden aparecer náuseas, vómitos y diarrea relacionados con la medicación, aunque ocasionalmente son producidos por enfermedad asociada a CMV (esofagitis, gastritis, colitis, etc.).
Pancreatitis, colecistitis y diverticulitis son cuadros no infrecuentes y han obligado a ocasionales intervenciones quirúrgicas.
ControlesLa supervivencia de los pacientes trasplantados a corto plazo depende de múltiples factores15,16, como su estado antes del trasplante, lo compleja que haya resultado la intervención, la necesidad o no de reintervenirlo, las complicaciones médicas que hayan surgido, la necesidad de más medicación o de dosis altas de esta con respecto a lo habitual, lo tóxica que haya resultado para él, el tiempo que haya precisado de ventilación mecánica y de estancia en la Unidad de Cuidados Intensivos, y otros múltiples factores.
La supervivencia a largo plazo también depende de algunos de estos factores17, pero muy especialmente del acierto y la rapidez con la que seamos capaces de detectar y tratar los problemas que vayan surgiendo.
Para detectar y tratar estas complicaciones se ha diseñado un protocolo de seguimiento que incluye la monitorización y vigilancia del estado del injerto y la monitorización y vigilancia de la medicación, su iatrogenia y la aparición de complicaciones previsibles o frecuentes6.
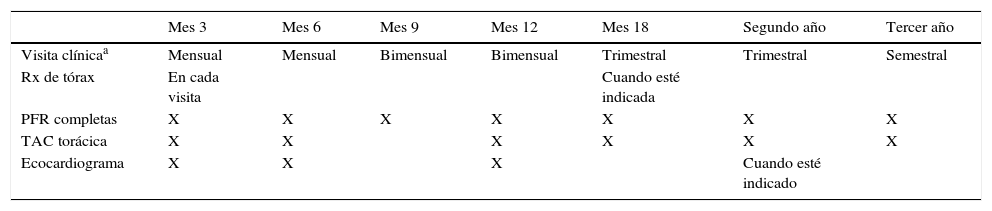
Esta monitorización (tabla 2) se realiza básicamente en el hospital, pero algunas pruebas pueden y deben ser realizadas por su neumólogo o por su médico de familia, con el fin de que el paciente realice una vida lo más normal posible, sea atendido por sus médicos y se eviten desplazamientos innecesarios.
Controles y periodicidad en el trasplante pulmonar
| Mes 3 | Mes 6 | Mes 9 | Mes 12 | Mes 18 | Segundo año | Tercer año | |
|---|---|---|---|---|---|---|---|
| Visita clínicaa | Mensual | Mensual | Bimensual | Bimensual | Trimestral | Trimestral | Semestral |
| Rx de tórax | En cada visita | Cuando esté indicada | |||||
| PFR completas | X | X | X | X | X | X | X |
| TAC torácica | X | X | X | X | X | X | |
| Ecocardiograma | X | X | X | Cuando esté indicado |
Incluye la realización de pruebas de función respiratoria, estudios radiológicos y/o BFC; deben ser realizadas por el equipo que llevó a cabo el trasplante u otro equipo neumológico con experiencia en trasplante.
Se realiza espirometría y radiografía de tórax como mínimo mensualmente durante los 6 primeros meses; la radiología se puede distanciar con posterioridad y adaptarla a las necesidades que se determinen en cada paciente. A partir del primer año se puede realizar trimestral o semestralmente.
Las pruebas de función respiratoria completas, que incluyen volúmenes, difusión y test de marcha, y la TAC torácica se realizan a los 3, 6, 9, 12, 18 y 24 meses, y con posterioridad, anualmente.
La BFC se realiza a la tercera semana del trasplante para valorar el estado de las suturas y realizar biopsia transbronquial para analizar el estado de rechazo o no del injerto. Con posterioridad solo se realiza si está clínicamente indicada.
Estas pruebas se realizan además cuando la clínica así lo aconseje.
Monitorización de la medicación, su iatrogenia y complicaciones frecuentesIncluye la realización de un hemograma completo, perfil bioquímico (glucosa, iones, lípidos, función renal y hepática), orina, determinación de niveles en sangre de los inmunosupresores y determinación de la antigenemia CMV en sangre o mejor carga viral.
Se realiza mensualmente durante el primer año y, una vez estabilizado, se puede distanciar cada 2-3 meses, dependiendo de si la evolución ha sido compleja o no.
Pasado el primer o segundo año, algunos de estos controles pueden ser asumidos por su médico.
Se realizan estudios de densidad ósea y ecocardiogramas de forma periódica.
Estilo de vidaEl objetivo del trasplante es que el paciente sobreviva a una grave enfermedad pulmonar y que, además, llegue a realizar una vida normal; para ello se le debe permitir la realización de actividades habituales, aunque de forma lenta y progresiva, siempre y cuando estas no atenten contra su salud. Está terminantemente prohibido fumar.
AlimentaciónDebe ser sana y equilibrada. Hay que evitar alimentos ricos en colesterol. No se deben hacer comidas excesivamente copiosas; hay que repartir la alimentación a lo largo del día. No se deben consumir bebidas alcohólicas, aunque no importa su uso excepcional para conmemorar algo.
Ejercicio físicoDurante los 3 primeros meses solamente realizará los ejercicios que le mande el equipo de fisioterapia; es necesario que la cicatriz cure perfectamente. Se debe evitar levantar peso –incluido niños– y empujar objetos pesados; se suspenderá cualquier actividad que agrave su dolor en la cicatriz.
Después del tercer mes: evitar competiciones deportivas, aunque algún paciente pueda realizarlas. Monitorice su frecuencia cardiaca y respiratoria durante el ejercicio. Reduzca la actividad si nota fatiga.
La natación es un ejercicio excelente.
Algunos consejos para el ejercicio físico son:
Vista y calce de forma confortable.
Realice los ejercicios de forma regular no anárquica.
La respiración debe ser relajada, si nota dificultad respiratoria significa que el ejercicio es demasiado intenso.
Utilice el test de hablar. Debe ser capaz de hablar de forma cómoda mientras realiza el ejercicio, si no es así, reduzca su intensidad.
Espere por lo menos 2h después de las comidas.
Progrese de forma gradual y lenta. ¡No tenga prisa!
Viajes y vacacionesEstán contraindicados los 3-6 primeros meses postrasplante.
A partir del sexto mes tiene perfecta libertad, pero hay que tener en cuenta lo siguiente:
- -
Planifique el viaje o vacación muy cuidadosamente.
- -
Debe obtener un informe del equipo de trasplante con un número de teléfono al que poder llamar en caso de urgencia.
- -
Si va a subir a un avión, debe obtener un permiso para llevar la medicación en cabina, no debe facturarse en la maleta porque podría extraviarse.
- -
Debe llevar suficiente medicación pensando en retrasos, demoras o contratiempos.
- -
Debe estar preparado para regresar si se encuentra mal.
- -
Si viaja al extranjero, consulte si debe vacunarse.
Algunos equipos vacunan a sus pacientes antes del trasplante y este calendario vacunal se considera finalizado, haya llegado hasta donde haya llegado, una vez realizado el trasplante.
La vacunación antigripal, en general, no se administra durante los 2 primeros años del trasplante, ya que al administrarse virus atenuados pueden reactivarse y originar un cuadro gripal grave a consecuencia del tratamiento inmunosupresor.
Se recomienda la vacunación de todos los miembros de su familia y personas que estén en estrecho contacto con el paciente para disminuir el contagio a ellos y evitar que lo transmitan al paciente. Pasados los 2 primeros años del trasplante, se recomienda la vacunación antigripal anualmente.
Cremas solaresDebe minimizarse la exposición al sol, nunca exponerse directamente. Debe utilizar sombrero o similar. No pasear entre las 12 y 17h en verano, hay que utilizar cremas de protección solar de alta numeración.
TrabajoNo es posible la incorporación al trabajo hasta pasado al menos un año del trasplante; posteriormente no hay impedimento.
Actividad sexual (información para el paciente)Recuperará su actividad sexual, perdida por su enfermedad terminal, cuando se encuentre bien; inicialmente debe ser moderado, quizás sean necesarios ciertos cambios en sus costumbres. No existe ninguna limitación, excepto que le recomendamos la utilización de preservativos ya que está muy expuesto a enfermedades de trasmisión sexual18.
Embarazo (información para el paciente)La enfermedad terminal que padecía produce en la mujer la anovulación y la ausencia de menstruación, y en el hombre, la disminución de esperma. La recuperación de su salud lleva consigo, muchas veces, la recuperación de estas funciones fisiológicas, por tanto, existe riesgo de embarazo.
No se recomienda el embarazo, pero si se desea, es usted libre; en este caso le recomendamos que discuta con el equipo de trasplante los pros y contras19. Existe riesgo de rechazo del injerto o pérdida de función pulmonar y BOS. El embarazo puede ser complicado, se requiere hospitalización al final y existe el riesgo de que el niño sea prematuro. Hay una mayor incidencia de alteraciones congénitas en niños de padres que están sometidos a tratamiento inmunosupresor.
Si no desea el embarazo, le recomendamos la doble barrera, preservativo y cremas; los fracasos de la doble barrera son excepcionales. No se recomienda el uso de anovulatorios por su interacción con la medicación. No se recomienda DIU por el riesgo de infecciones.
Es recomendable que se realice una revisión ginecológica anualmente.
SupervivenciaLos datos del registro español20 correspondiente a 950 pacientes trasplantados entre 2006 y 2010 muestran una supervivencia a uno y 3 años del 72 y el 60%, respectivamente; si se excluyen los fallecidos en los 3 primeros meses, del 89,7 y el 75,2%. Los factores que inciden en la supervivencia son la edad del receptor y el diagnóstico.
Según los datos del último registro de la Sociedad Internacional de Trasplante de Corazón y Pulmón, publicado en 201421, sobre un total de 47.647 trasplantes pulmonares registrados, 3.719 realizados en 2012 en 156 centros, el 38% de los trasplantes se han realizado a pacientes con enfisema (33% no déficit alfa 1 AT), 28% con enfermedad intersticial, fibrosis, etc., 16,4% con FQ, 3,8% a pacientes con hipertensión arterial pulmonar, 2,5% con sarcoidosis, 5% con retrasplantes. En los últimos 15 años el porcentaje de enfisemas ha descendido del 40 al 33%, mientras que el porcentaje de enfermedad intersticial ha aumentado del 17 al 28%.
La supervivencia media del registro es de 5,7 años, 80% al año, 65% a 3 años, 53% a 5 años y 32% a 10 años. Los pacientes que sobreviven el primer año tienen una supervivencia media de 7,9 años.
La supervivencia media en el registro de 200922 era de 5,4 años, y si excluimos los que fallecen durante el primer año, de 7,4 años.
El trasplante bipulmonar tiene mejor supervivencia que el unipulmonar, 7 vs. 4,5 años, y los que sobreviven el primer año, 9,6 vs. 6,5. La supervivencia en relación con el procedimiento está influida por múltiples factores, como la edad del receptor, la comorbilidad, la preferencia del equipo y las características del donante. En relación con la edad del receptor, la supervivencia en el grupo de 18-34 años es de 7,3 años, en el de 35-49 años es de 7,1 años, en el de 50-59 años es de 5,6 años, y por encima de 60 años la supervivencia media es de 4,4 años; en las gráficas se detecta una subida exponencial de la mortalidad por encima de 55 años. En relación con el diagnóstico o indicación de trasplante, la mayor mortalidad en los 3 primeros meses se da en hipertensión arterial pulmonar, y la menor, en enfisema; excluidos los que fallecen el primer año, la supervivencia media por indicación es de 11 años en FQ, 10,1 años en hipertensión arterial pulmonar, 8,9 años en sarcoidosis, 8,7 años en enfisema por déficit AAT, y 7 años en enfisema no AAT y fibrosis pulmonares.
Las causas de muerte se exponen en la tabla 3.
Causas de muerte (%)
| Fallo injerto | Rechazo agudo | Infección no CMV | Infección CMV | Causa cardiovascular | Bronquiolitis obliterante | Neos | Linfomas | |
|---|---|---|---|---|---|---|---|---|
| Un mes | 24 | 3,4 | 19 | 0 | 11 | 0 | 0 | 0 |
| Un año | 16,6 | 1,8 | 35,5 | 2,3 | 5 | 4,3 | 2,9 | 2,3 |
| 1-3 años | 18,8 | 2,6 | 33,3 | 1,6 | 5,2 | 25 | 8,1 | 1,7 |
| 3-5 años | 17,9 | 0,6 | 18,4 | 0,3 | 5 | 29 | 11 | 1,5 |
| 5-10 años | 16,9 | 0,6 | 18 | 0,1 | 5,6 | 24,7 | 13,9 | 1,8 |
| >10 años | 16,7 | 0,2 | 16,9 | 0,1 | 7,6 | 19,8 | 12,4 | 3,3 |
A la pregunta teórica sobre cuánto puede durar un pulmón trasplantado, podemos asegurar que al menos 22 años, que es lo que lleva viva una paciente con FPI trasplantada en marzo de 1994.
Conflicto de interesesLos autores declaran que no existe ningún conflicto de intereses.