En España aproximadamente el 25% de los pacientes anticoagulados por fibrilación auricular no valvular llevan un anticoagulante de acción directa (ACOD). Es previsible que la mayor parte de ellos en algún momento de su vida deban someterse a procedimientos invasivos o tratamientos quirúrgicos, por lo que el manejo del ACOD en estas situaciones es esencial para realizar el procedimiento con la máxima seguridad y minimizar al máximo el riesgo de hemorragia y de trombosis. El manejo de esta situación se basa en la valoración del riesgo hemorrágico del paciente y del procedimiento que se va a realizar, del riesgo de tromboembolia del paciente, su función renal y de las características farmacocinéticas de los ACOD, especialmente su vida media, el grado de eliminación renal y su pico de acción.
In Spain, approximately 25% of patients anticoagulated due to non-valvular atrial fibrillation use a direct-acting anticoagulant (DOAC). It is foreseeable that most of them at some point in their lives should undergo invasive procedures or surgical treatments. This makes the management of DOAC in these situations essential in order to perform the procedure with maximum safety and minimise the risk to the maximum of haemorrhage and thrombosis. The management of this situation is based on the evaluation of the haemorrhagic risk of the patient, and the procedure to be performed, the risk of thromboembolism, and renal function. The pharmacokinetic characteristics of the DOAC also should be taken into account, especially its half-life, the degree of renal elimination and its peak action.
Juan es un paciente de 74 años de edad, con antecedentes de diabetes mellitus tipo 2, hipertensión arterial, ictus sin secuelas en 2005, gastrectomía por cáncer gástrico diagnosticado y tratado en el año 2006 sin evidencia de recidiva en la actualidad, artritis reumatoide en el 2010, fibrilación auricular no valvular (FANV) en el 2016, actualmente en tratamiento con edoxabán, con un CHAD2DS2Vasc de 5 puntos. En la analítica presenta una función renal con creatinina de 0,85mg/dl y filtrado glomerular de 78ml/min. Nos es remitido desde digestivo para adecuar el tratamiento anticoagulante para realizar una colonoscopia y gastroscopia para estudio de una anemia ferropénica.
Ante esta situación nos surgen las siguientes preguntas que debemos abordar: 1. ¿Es necesario suspender el anticoagulante de acción directa (ACOD)? 2. En caso afirmativo: cuándo interrumpir y reanudar el tratamiento con ACOD, y si hay que hacer terapia puente.
Para la mayoría de estas preguntas no disponemos de estudios prospectivos y controlados y las recomendaciones se basan en resultados de estudios retrospectivos o consensos de opiniones de expertos, por lo tanto, disponemos solo de evidencia de calidad baja1 y las recomendaciones son diferentes en las distintas sociedades médicas. Es una situación clínica frecuente y compleja, genera confusión y la práctica clínica varía ampliamente2.
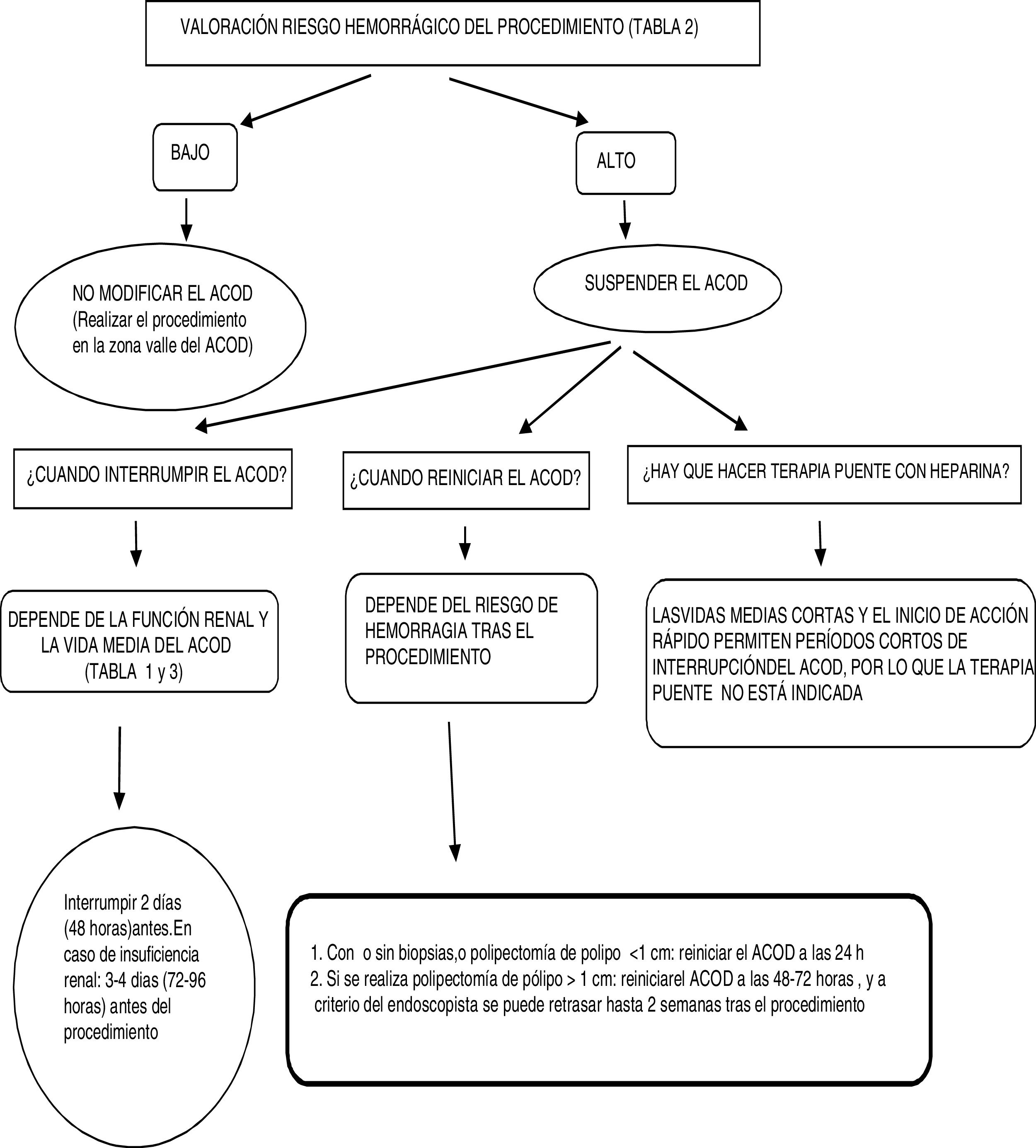
Nuestra discusión se centrará solo en pacientes con FANV anticoagulados con ACOD a los que se va a realizar una endoscopia digestiva diagnóstica. Tras la revisión del tema, aportamos un algoritmo de ayuda para el manejo de esta situación (fig. 1).
Recientemente se ha publicado un consenso nacional sobre manejo del tratamiento antitrombótico en el periodo perioperatorio y periprocedimiento, en el que han participado 23 sociedades científicas españolas implicadas en el manejo de estos pacientes, y en el que nosotros hemos basado la resolución del caso6.
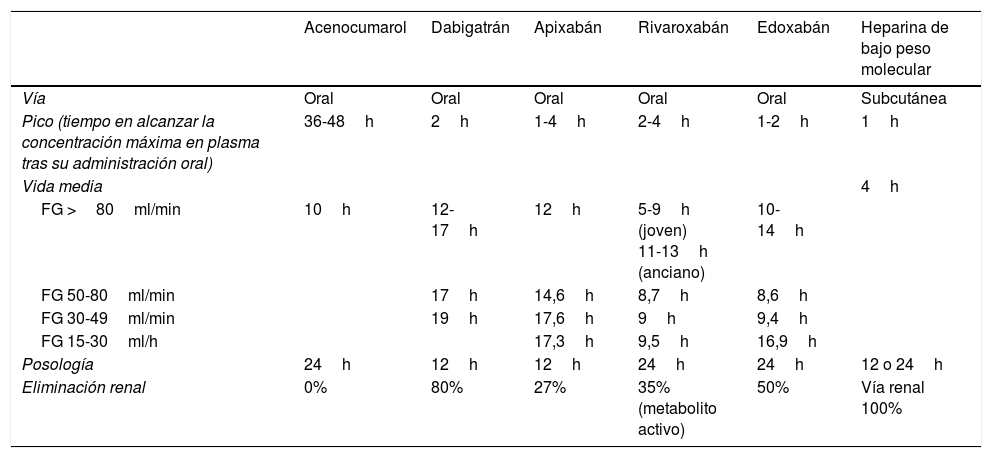
El número de pacientes tratados con ACOD es cada vez más frecuente en nuestras consultas, generalmente en la indicación de FANV. Se entiende por FANV aquella que aparece en un paciente sin estenosis mitral reumática moderada o severa, y no portador de prótesis valvular mecánica. En pacientes portadores de prótesis cardiacas valvulares mecánicas o con estenosis mitral reumática moderada o grave los ACOD están contraindicados3. Para reducir el riesgo de accidente cerebrovascular y embolia sistémica en la FANV hay 4 ACOD aprobados: dabigatrán 2008, rivaroxabán 2008, apixabán 2011, edoxabán 2015. Sus propiedades farmacocinéticas son especialmente interesantes (tabla 1), dado que se caracterizan por un inicio de acción rápido (1-4h tras su administración oral) y una duración corta de su efecto farmacológico (12-24h)3.
Características farmacocinéticas de los anticoagulantes
| Acenocumarol | Dabigatrán | Apixabán | Rivaroxabán | Edoxabán | Heparina de bajo peso molecular | |
|---|---|---|---|---|---|---|
| Vía | Oral | Oral | Oral | Oral | Oral | Subcutánea |
| Pico (tiempo en alcanzar la concentración máxima en plasma tras su administración oral) | 36-48h | 2h | 1-4h | 2-4h | 1-2h | 1h |
| Vida media | 4h | |||||
| FG >80ml/min | 10h | 12-17h | 12h | 5-9h (joven) 11-13h (anciano) | 10-14h | |
| FG 50-80ml/min | 17h | 14,6h | 8,7h | 8,6h | ||
| FG 30-49ml/min | 19h | 17,6h | 9h | 9,4h | ||
| FG 15-30ml/h | 17,3h | 9,5h | 16,9h | |||
| Posología | 24h | 12h | 12h | 24h | 24h | 12 o 24h |
| Eliminación renal | 0% | 80% | 27% | 35% (metabolito activo) | 50% | Vía renal 100% |
FG: filtrado glomerular.
Fuente: Adaptada de la European Heart Rhythm Association3.
Para valorar qué hacer en pacientes que se encuentran en tratamiento con ACOD y van a requerir una cirugía o procedimiento invasivo electivo necesitamos conocer 3 cosas: el riesgo de sangrado del procedimiento, el riesgo tromboembólico del paciente (equivalente en la práctica al de la indicación del tratamiento anticoagulante) y la función renal del paciente2.
Si el procedimiento o intervención quirúrgica que se van a realizar es de muy alto riesgo hemorrágico o el paciente es de muy alto riesgo trombótico, la valoración de la pauta se realizará en la consulta de hematología4. En los pacientes con FANV, que no sean de muy alto riesgo trombótico, a los que se les vaya a realizar una endoscopia digestiva con intención diagnóstica podemos hacer la recomendación desde la atención primaria.
1. ¿Es necesario suspender el ACOD?
Lo primero que debemos valorar es el riesgo hemorrágico del procedimiento que se va a realizar. En general, la anticoagulación se debe suspender cuando el riesgo de sangrado es alto, limitando al menor tiempo posible el tiempo sin anticoagulante oral. En procedimientos de bajo riesgo de sangrado, como son la mayoría de procedimientos quirúrgicos menores, y en aquellos procedimientos donde el sangrado es fácilmente controlable con medidas locales, como son las extracciones dentales, la cirugía de cataratas y glaucoma, y las cirugías de la piel, se recomienda no suspender el tratamiento anticoagulante. En general, estos procedimientos pueden realizarse 12-24h después de la última administración del ACOD (en la zona valle del fármaco, antes de la siguiente dosis) y reiniciar 6h después del procedimiento, sin omitir ninguna dosis del fármaco4. Ante cirugías o procedimientos invasivos cuyo riesgo de sangrado es mayor (riesgo de sangrado moderado o alto) se recomienda interrumpir transitoriamente el tratamiento anticoagulante2.
Centrándonos en el caso que nos ocupa, cualquier procedimiento endoscópico digestivo tiene un riesgo de hemorragia digestiva. Se considera que es de bajo riesgo si la probabilidad de sangrado es <1%, y alto si es superior al 1% (tabla 2). El riesgo es diferente si la prueba es solo diagnóstica (bajo riesgo) o terapéutica (en general alto riesgo), y según el procedimiento que se realice durante la misma. En las endoscopias con intención diagnóstica hay posibilidad de realizar en el mismo acto, si se precisa, biopsias o polipectomías si se encuentran pólipos. Las biopsias son consideradas de bajo riesgo de sangrado por la mayoría de sociedades científicas, pero la polipectomía es de alto riesgo cuando el pólipo tiene un tamaño mayor de 1cm5. De hecho, la hemorragia es la complicación grave más frecuente de la polipectomía endoscópica, y se produce con mayor frecuencia al reintroducir la medicación anticoagulante. Puede ser desde leve (la mayoría) a grave y puede llegar a requerir transfusión e ingreso, y aunque la mayoría de ellas pueden ser solucionadas con métodos terapéuticos endoscópicos, algún caso puede llegar a requerir cirugía. Puede suceder de forma inmediata (durante el procedimiento y poner remedio en el mismo momento) o de forma diferida (se puede iniciar el sangrado hasta 2 semanas tras la polipectomía). El tamaño del pólipo (mayor de 1cm) constituye el factor de riesgo independiente más importante para hemorragia pospolipectomía. La mayoría de las hemorragias ocurren dentro de las primeras 48h. La gran mayoría de pólipos son pequeños (<9mm), por lo que el riesgo de hemorragia es bajo. Sin embargo, la incidencia de hemorragia en la resección de lesiones de tamaño igual o superior a 10mm oscila entre el 2 y el 10%6.
Riesgo de sangrado según procedimiento endoscópico
| Bajo riesgo hemorrágico | Alto riesgo hemorrágico |
|---|---|
| Endoscopia digestiva alta/colonoscopia con o sin biopsia | Resección mucosa, disección submucosa, ampulectomía |
| Polipectomía <10mm | Polipectomía >10mm |
| Ecoendoscopia diagnóstica con o sin punción de lesión sólida | Ecoendoscopia con punción de lesión quística |
| CPRE con colocación de prótesis o papiloplastia sin esfinterotomía | CPRE con esfinterotomía |
| Dilatación de estenosis | Ligadura de varices esofágicas |
| Electrocoagulación con argón | Colocación de gastrostomía endoscópica percutánea |
| Prótesis intestinal |
CPRE: colangiopancreatografía endoscópica retrógrada.
Fuente: Documento de consenso de SEC, SEDAR, SEACV, SECTCV, AEC, SECPRE, SEPD, SEGO, SEHH, SETH, SEMERGEN, SEMFYC, SEMG, SEMICYUC, SEMI, SEMES, SEPAR, SENEC, SEO, SEPA, SERVEI, SECOT y AEU6.
Según el consenso español6 de acuerdo con este riesgo de hemorragia, no es necesario suspender el tratamiento anticoagulante para gastroscopias ni colonoscopias con biopsias ni con polipectomía de pólipos pequeños, y al igual que para otros procedimientos de bajo riesgo, la mayoría de guías actuales recomiendan continuar el tratamiento anticoagulante y especialmente en el caso de los pacientes con alto riesgo tromboembólico. Cuando se trata de los antagonistas de la vitamina K (AVK), el INR debe estar en rango terapéutico antes del procedimiento, mientras que en el caso de los ACOD es preferible realizar la endoscopia cuando el fármaco alcanza su nivel sérico más bajo (valle, antes de la siguiente dosis), para minimizar el efecto anticoagulante4. Un procedimiento realizado en el nivel valle del fármaco (final de un intervalo de dosificación, corresponde a partir de las 10h de la última dosis de ACOD si su administración oral es cada 12h, o partir de las 20h si se administra cada 24h) minimiza el riesgo de sangrado sin disminuir la protección antitrombótica del ACOD. Por el contrario, en el caso de pólipos mayores de 10mm, las guías actuales recomiendan la interrupción del tratamiento anticoagulante con objeto de realizar el procedimiento con una coagulación normalizada6.
En resumen, los procedimientos diagnósticos endoscópicos, con o sin biopsia, se clasifican como de bajo riesgo de hemorragia. Pero no es raro encontrar pólipos, por lo que se opta por clasificar a la colonoscopia como un procedimiento de alto riesgo ante la imposibilidad de saber a priori si habrá algún pólipo de gran tamaño. Por lo que, en nuestro paciente, suspendimos el ACOD.
2. Si se suspende el ACOD hay que decidir: cuándo lo interrumpimos, cuándo lo reintroducimos, y si precisa terapia puente con heparina.
A. El tiempo de suspensión del ACOD previo al procedimiento dependerá del riesgo de hemorragia, de la función renal y de la vida media del fármaco. Entre los ACOD hay diferencias en cuanto a su vida media y la eliminación renal. En general, dado que la vida media de los ACOD es corta (entre 9 y 14h en pacientes con función renal normal), el efecto anticoagulante disminuye rápidamente tras suspender la medicación. Para entender este punto, es importante saber que la vida media plasmática es el tiempo necesario para eliminar el 50% del fármaco del organismo, es decir, el tiempo que tarda la concentración plasmática del fármaco en reducirse a la mitad de sus niveles iniciales. Con 2 vidas medias se calcula que se ha eliminado el 75% del fármaco, y se requieren 5 vidas medias para eliminar >95% de la concentración de un fármaco. Por lo que, este último (5 vidas medias) será, en general, el tiempo orientativo necesario para interrumpir el ACOD previo al procedimiento. Si un fármaco se elimina vía renal, en caso de insuficiencia renal aumentará su vida media y se requerirá más tiempo para eliminar el fármaco. La función renal hay que tenerla en cuenta porque los ACOD se eliminan vía renal en grado variable dependiendo del ACOD, sobre todo el dabigatrán, ya que es el ACOD con mayor eliminación renal3.
En general, ante un procedimiento de alto riesgo de sangrado el ACOD deberá suspenderse 48h (2 días) antes en sujetos con función renal normal. En caso de insuficiencia renal la suspensión deberá efectuarse entre 72-96h (3-4 días) antes (tabla 3)2,6.
Tiempo mínimo de interrupción del ACOD antes del procedimiento, en función del filtrado glomerular, en procedimientos invasivos de alto riesgo de sangrado
| Dabigatrán | |
| FG>80ml/min | 2 días (48h) |
| FG 50-79ml/min | 3 días (72h) |
| FG 30-49ml/min | 4 días (96h) |
| Rivaroxabán, apixabán, edoxabán | |
| FG>30ml/min | 2 días (48h) |
| FG 15-29ml/min | 3 días (72h) |
ACOD: anticoagulante de acción directa; FG: filtrado glomerular.
(Interpretación de la tabla: ¿Qué quiere decir 48h? Ejemplo: si al paciente le operan el jueves día 4 de enero, quiere decir que el último día que tomará el ACOD antes de la colonoscopia será el lunes día 1 de enero).
Fuente: Adaptado del Documento de consenso de SEC, SEDAR, SEACV, SECTCV, AEC, SECPRE, SEPD, SEGO, SEHH, SETH, SEMERGEN, SEMFYC, SEMG, SEMICYUC, SEMI, SEMES, SEPAR, SENEC, SEO, SEPA, SERVEI, SECOT y AEU6.
B. Tras el procedimiento, y una vez asegurada la hemostasia, y dado el rápido pico de acción de entre 1-4h tras la administración oral de los ACOD, en procedimientos de bajo riesgo de hemorragia se sugiere reiniciar el ACOD a las 12- 24h, y si el procedimiento o cirugía es de alto riesgo hemorrágico se esperará 48-72h (2-3 días)2,5. El efecto anticoagulante pleno reaparece con rapidez (pico de acción) aproximadamente a las 2-3h de su administración si la absorción intestinal es normal.
Tras una polipectomía el riesgo de sangrado, dependiendo del tamaño del pólipo resecado, puede persistir hasta 2 semanas, por lo que en algunos casos habrá que valorar este tiempo para reiniciar el ACOD, por lo que será el endoscopista el que indique al paciente cuándo debe reiniciar el ACOD6.
Así pues, tras una polipectomía endoscópica con hemostasia completa, el ACOD a dosis plenas podría reiniciarse a las 48-72h. No obstante, el endoscopista podría recomendar una interrupción más prolongada por el alto riesgo de hemorragia en caso de resección de los pólipos de gran tamaño.
C. ¿Precisa terapia puente con heparina?
El objetivo de la terapia puente es minimizar el riesgo trombótico durante la interrupción temporal de la anticoagulación oral (mientras no hay actividad del fármaco anticoagulante oral) y solamente está indicada cuando el riesgo tromboembólico es alto. La terapia puente se realiza con heparina por su vida media corta (en el caso de la heparina de bajo peso molecular [HBPM] subcutánea la vida media es de 4h y la de la heparina no fraccionada endovenosa es de 1h; la heparina no fraccionada endovenosa se interrumpe 4h antes de la cirugía y la HBPM subcutánea se interrumpe 24h antes del procedimiento) e inicio de acción rápido (tras la administración de heparina fraccionada endovenosa el efecto anticoagulante aparece inmediatamente y en el caso de la HBPM subcutánea, en 1h).
El riesgo tromboembólico se clasifica en alto, medio y bajo, en función de la probabilidad de que se produzca un evento tromboembólico anual: >10%, entre el 5 y el 10% y <5%, respectivamente. En el caso de la FANV se utiliza la escala CHAD2DS2Vasc, que valora el riesgo de accidente cerebrovascular en pacientes sin terapia antitrombótica7. Esta escala de estratificación del riesgo asigna los puntos de la siguiente forma: ictus o accidente isquémico transitorio, 2 puntos; edad mayor o igual a 75 años, 2 puntos; insuficiencia cardiaca, un punto; hipertensión, un punto; diabetes, un punto; enfermedad vascular (p. ej., enfermedad arterial periférica, infarto de miocardio, placa aórtica), un punto; edad de 65 a 74 años, un punto; mujer, un punto. Una puntuación de 7 a 9 estima un riesgo >10% de accidente cerebrovascular en un año. Se considera que un paciente con FANV tiene un riesgo tromboembólico muy alto cuando CHAD2DS2Vasc es de 7 a 9, o ha presentado un ictus o accidente isquémico transitorio en los últimos 3 meses6.
En 2015 se publicó el estudio BRIDGE8, único ensayo clínico aleatorizado y doble ciego, realizado con el objetivo de valorar la terapia puente en pacientes tratados con AVK (warfarina) por FANV, y concluye que la terapia puente en pacientes con FANV con bajo o moderado riesgo de trombosis no debe realizarse, ya que aumenta de forma significativa las hemorragias mayores con el mismo número de eventos trombóticos, respecto a los pacientes que no hacían terapia puente. En la misma línea, otros estudios, como un subanálisis del estudio cohortes ORBIT-AF9 que analiza la terapia puente en pacientes con FA en tratamiento con warfarina, observó más hemorragias y eventos adversos en el grupo de terapia puente, llegando a la conclusión de que con los datos de que se dispone actualmente no se sostiene la indicación de llevar a cabo un periodo puente. No disponemos de este tipo de estudios con los ACOD.
Las vidas medias cortas y el inicio de acción rápido permiten periodos cortos de interrupción de ACOD, por lo que la terapia puente en general no está indicada en pacientes tratados con ACOD. Por el contrario, el efecto anticoagulante de un AVK (warfarina o acenocumarol) tarda más en desaparecer cuando se interrumpe y más tiempo en alcanzar la dosis terapéutica cuando se reinicia. En consecuencia, los pacientes con un AVK que tengan un alto riesgo de eventos tromboembólicos pueden beneficiarse de los puentes usando heparina parenteral en el entorno periprocedimiento2,6.
A raíz de la evidencia disponible, el consenso español6 no recomienda terapia puente en pacientes tratados con ACOD. El uso de terapia puente con heparina solamente se debería considerar en pacientes tratados con AVK con alto riesgo de ictus o de embolia sistémica, que en el caso de la la FANV serían aquellos pacientes con un CHAD2DS2Vasc de 7-9 o que hayan tenido un ictus isquémico o accidente cerebrovascular isquémico transitorio reciente, hace menos de 3 meses.
En nuestro paciente, se interrumpió el edoxabán 48h antes de las endoscopias. Las endoscopias fueron normales, no se realizaron biopsias ni polipectomías. El endoscopista recomendó al paciente reiniciar el ACOD al día siguiente. Si se hubiese hecho una polipectomía de un polipo >1cm el reinicio del ACOD sería a los 2-3 días, pudiéndose alargar este tiempo hasta 2 semanas en función del tipo de pólipo extirpado. No se hizo terapia puente.
ConclusiónLas recomendaciones de las distintas sociedades médicas carecen de la evidencia de estudios controlados y se basan en opiniones de expertos. La colonoscopia se considera a priori un procedimiento de alto riesgo de sangrado, no por la prueba en sí misma —que es de bajo riesgo—, sino por la posibilidad de que haya que realizar una polipectomía. Por lo que, se recomienda suspender el ACOD en general 2 días antes de la prueba (aunque el tiempo es variable dependiendo del ACOD y de la función renal, en el caso de dabigatrán con FG entre 30 y 50ml/min: 4 días antes) y reiniciarlo en 6-8h (o en las primeras 12-24h) si no se ha realizado polipectomía de un pólipo mayor de 1cm; y si se ha realizado este tipo de polipectomía, no será antes de 2-3 días, o incluso hasta 2 semanas después dependiendo del tamaño de los pólipos. Por lo que, el momento en que se reintroduce el ACOD debería ser valorado por el endoscopista. En general, por las características farmacocinéticas de los ACOD, con un inicio y fin de acción rápidos, no hay indicación de terapia puente.
FinanciaciónNo hay.
Conflicto de interesesNo tenemos.