El asma es una enfermedad crónica de las vías aéreas que se ha convertido en un asunto prioritario y un importante problema mundial de salud pública por su prevalencia y su capacidad de afectar a individuos de cualquier edad y sexo, llegar a ser progresiva, grave e incluso fatal. En la actualidad, la mayoría de los expertos está de acuerdo en considerarla una enfermedad inflamatoria crónica de las vías aéreas que implica a numerosas células (mastocitos, eosinófilos y linfocitos) y sus mediadores. Esta inflamación aumenta la respuesta bronquial a los posibles desencadenantes (hiperrespuesta) y provoca la aparición recurrente de sibilancias, fatiga, opresión torácica, disnea o tos, especialmente por la noche y a primera hora de la mañana. Estos episodios o crisis se asocian a una variabilidad de la obstrucción bronquial (estrechamiento de las vías aéreas) que suele ser reversible de forma espontánea o con el tratamiento.
Epidemiología
No se ha podido establecer las causas específicas que justifiquen el aumento ininterrumpido de la prevalencia del asma bronquial en los países industrializados en las últimas dos décadas, aunque hoy se acepta como un hecho probado sólo a partir de numerosos estudios transversales de amplia consistencia repetidos en una misma área geográfica. Esta enfermedad afecta a un 4-8% de la población mundial (aproximadamente dos millones de pacientes en España), de los que un 60-70% usa fármacos inhalados con regularidad, casi un 30% acude a urgencias o es ingresado en un hospital al menos una vez al año y ocupa hasta el 14,4% de las consultas realizadas por los neumólogos.
Diagnóstico
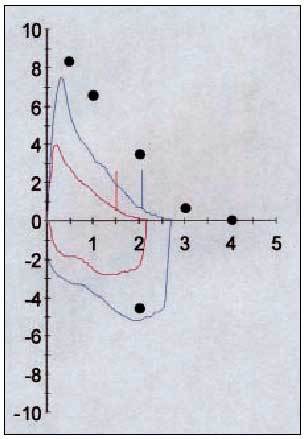
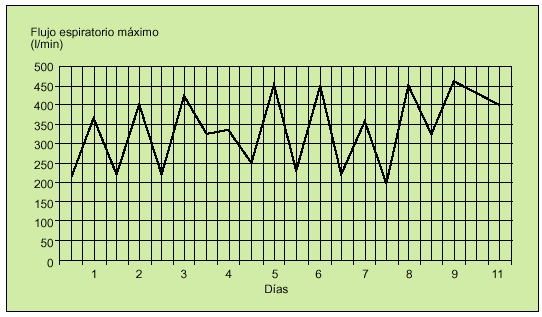
Sigue basándose en los mismos criterios clínicos y de las pruebas funcionales respiratorias. Una historia clínica intencionada es fundamental para sospechar esta enfermedad, especialmente en un paciente que combine la presencia de síntomas, como disnea, sibilancias, tos u opresión torácica, que suelen aparecer de forma variable y episódica (tabla 1). No obstante, hasta un 36% de los pacientes no presentan un cuadro típico y su ausencia no permite excluirla. En todos los casos, la sospecha clínica debe acompañarse de la realización de una espirometría con prueba broncodilatadora y la monitorización del flujo espiratorio máximo para confirmar una obstrucción bronquial variable y reversible. Un aumento de la capacidad vital forzada (FVC) o el flujo espiratorio máximo en el primer segundo (FEV1) superior al 12% después del broncodilatador (fig. 1) o una variación diaria del flujo espiratorio máximo superior al 20% confirman el diagnóstico de la enfermedad. En caso contrario, ante la presencia de una espirometría basal normal y una clínica compatible o dudosa, está indicada la realización de una prueba de provocación bronquial inespecífica con metacolina o histamina para confirmarla.
Fig. 1. Curva flujo/volumen de un paciente asmático donde se demuestra la mejora de los flujos espiratorios con el broncodilatador (color rojo prebroncodilatador y color azul posbroncodilatador).
Pilares básicos del tratamiento del paciente asmático
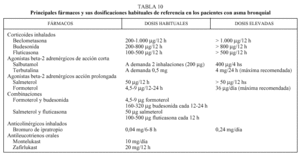
En la tabla 2 se presentan los pilares básicos que en la actualidad sustentan el tratamiento adecuado de los pacientes con asma bronquial. Todos estos pasos deben valorarse de forma secuencial en este tipo de pacientes y serán revisados en el resto de este manuscrito.
Para conseguir un buen control de esta enfermedad es necesario partir de un diagnóstico correcto, conocer la gravedad o intensidad de la enfermedad, evitar los factores desencadenantes, realizar un tratamiento correcto y organizar un seguimiento regular a largo plazo. No obstante, esto no asegura un buen control o el cumplimiento de las pautas terapéuticas por parte del paciente (índices habituales de cumplimiento terapéutico en las enfermedades crónicas con fármacos inhalados, sólo del 15-30%, atribuibles al exceso de número de fármacos o de tomas diarias, una mala interpretación, una realización deficiente de los sistemas de inhalación, etc., que suelen asociarse con ideas erróneas sobre el asma o el tratamiento que el paciente evita por miedo a los efectos secundarios). Para solventar este problema es necesario establecer una buena comunicación entre el personal sanitario y el paciente o su familia, ofreciendo al enfermo la posibilidad de expresar sus miedos o dudas y facilitar que el personal que lo atienda proporcione unos conocimientos específicos sobre la enfermedad, los distintos fármacos disponibles y sus acciones, la habilidad en realizar el tratamiento y sobre cómo actuar en caso de deterioro. La enseñanza de estos conceptos o habilidades es lo que se entiende por educación y tiene como finalidad la mejora del cumplimiento del tratamiento o la cooperación activa del paciente en el control de su enfermedad.
Factores predisponentes y precipitantes
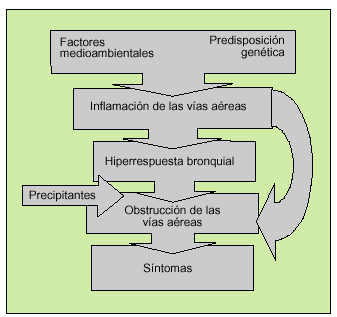
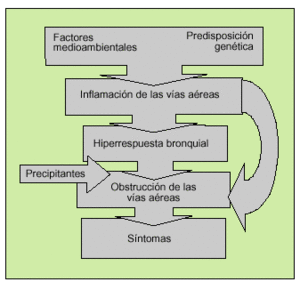
El aumento de la respuesta bronquial que se produce en los pacientes con asma está relacionado con una amplia variedad de estímulos o factores de riesgo. A pesar de la existencia de amplias áreas de incertidumbre sobre la patogenia de esta enfermedad, hay evidencias científicas para aceptar que surge de la conjunción o interacción de una predisposición genética y la presencia de estímulos medioambientales, asociados o no con factores precipitantes que favorecen la aparición de síntomas y las agudizaciones (fig. 2). Los factores propios del huésped están relacionados con el desarrollo de la enfermedad, mientras que los ambientales también podrían influir en su desarrollo en los pacientes predispuestos, provocar las exacerbaciones y justificar la persistencia de los síntomas. En la tabla 3 se exponen los principales factores personales y ambientales que se debe tener en cuenta por su implicación en el asma (fig. 3).
Fig. 2. Principales mecanismos patogénicos implicados en el asma.
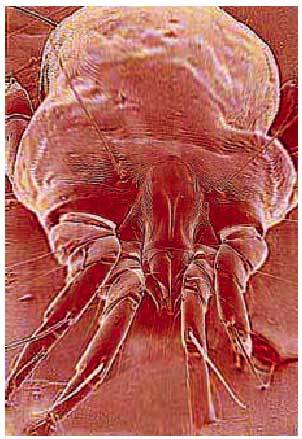
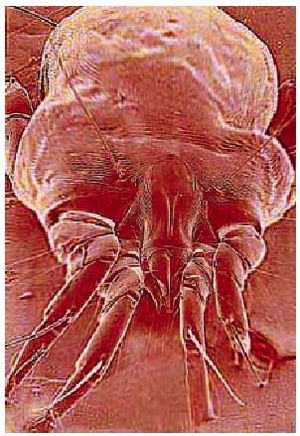
Fig. 3. Dermatophagoides pteronyssimus. Ácaro presente en el polvo doméstico que actúa como alergeno.
Valoración del paciente asmático
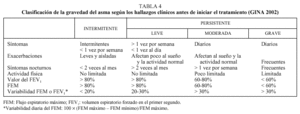
Una vez confirmado el diagnóstico de asma es obligado definir su intensidad o gravedad a partir de unos criterios clínicos, las necesidades terapéuticas y las medidas objetivas de la obstrucción. A partir de estos parámetros, el consenso de la GINA (Global Initiative for Asthma 2002) ha establecido una clasificación clínica muy útil desde el punto de vista pronóstico y terapéutico, que divide la enfermedad en intermitente y crónica o persistente, y esta última con tres grados de intensidad que incluyen las formas leves, moderadas y graves (tabla 4). En los casos más graves o de difícil control es fundamental la confirmación de la obstrucción bronquial a través de la espirometría o de los medidores de flujo máximo (figs. 4 y 5), ya que la valoración clínica es más difícil o inadecuada por la ansiedad, exageración, dificultad o falta de percepción de los propios pacientes, en los que la presencia de una obstrucción bronquial mantenida se acompaña de una grado elevado de tolerancia que reduce la intensidad sensorial.
Figs. 4 y 5. Medición y medidor del flujo espiratorio máximo en una paciente con asma bronquial.
Finalmente, también es siempre necesario excluir otras enfermedades que pueden confundirse con o superponerse al asma (tabla 5) y la evaluación de los posibles factores etiológicos o su relación con la aparición de los síntomas. La aparición de síntomas durante la primavera sugiere una alergia a pólenes y su persistencia o falta de control también pueden relacionarse con el contacto con animales, irritantes específicos, el aire frío, el tabaco, el ejercicio físico y algunos fármacos.
¿Qué asmáticos presentan mayor riesgo vital?
Los pacientes con un asma de riesgo vital son aquellos que llegan a una situación extremadamente grave, que cursa con un importante deterioro ventilatorio, una acidosis respiratoria aguda y, en ocasiones, parada respiratoria. Este tipo de pacientes sigue dos tipos diferenciados de crisis:
1. Crisis súbitas caracterizadas por su rápida instauración (generalmente menos de 6 h) en pacientes con un asma previamente estable y con una buena respuesta al tratamiento convencional.
2. Crisis subagudas, de instauración lenta hacia un fracaso lentamente progresivo en individuos con asma crónica grave y de mala evolución.
Existe un elevado interés en delimitar los factores de riesgo de este tipo de pacientes para establecer el perfil que se relaciona directamente con una mayor probabilidad de fallecer por asma. En la tabla 6 se especifican los principales factores asociados, cuya presencia debe interpretarse con cautela por la dificultad de interpretar los estudios realizados a partir de metodologías muy distintas. Entre los múltiples factores sigue siendo preocupante el elevado número de pacientes de riesgo que desconocía que sufría esta en fermedad y un número no despreciable de casos diagnosticados previamente que seguía un tratamiento incorrecto. No obstante, una vez identificados, todos estos pacientes deberían ser seguidos por unidades especializadas de fácil acceso y contar con planes escritos de actuación ante una situación de emergencia, con lo que probablemente disminuiríamos el riesgo de mortalidad.
Tratamiento del asma bronquial
Los nuevos conocimientos establecidos en la patogenia del asma han hecho que una enfermedad que hace años entendíamos como la presencia de crisis agudas aisladas pase a ser considerada un proceso crónico variable y, por tanto, deba tratarse y controlarse de forma continua en la mayoría de los casos. El establecimiento de cualquier estrategia terapéutica se basará en conseguir los siguientes objetivos:
1. Control de la enfermedad (control de los síntomas, las exacerbaciones y optimización de las medidas o la variabilidad de flujo espiratorio máximo y la espirometría).
2. Mantener una buena calidad de vida o clase funcional (optimización de la calidad de vida y minimizar su repercusión).
3. Mejorar o normalizar la función pulmonar.
4. Evitar la cronificación, las crisis graves o exacerbaciones, la irreversibilidad o la progresión de la obstrucción y el riesgo vital o la mortalidad.
5. Utilizar una vía inhalatoria de tratamiento y la mínima medicación y reducir al máximo los efectos secundarios.
En todos los casos, el concepto de inflamación como elemento patogénico fundamental en el asma ha quedado plenamente establecido y ha permitido diseñar distintas líneas de actuación mediante la introducción simultánea de estrategias, farmacológicas o no, que dependerán del estado y la gravedad de la enfermedad en cada momento, estableciendo planes escalonados que varían entre los pacientes y en un mismo paciente con el tiempo. En estos últimos años, ha cobrado una gran relevancia el conocimiento de la posibilidad del remodelado de la vía aérea, mediante la presencia de fenómenos de reparación y cicatrización que posibilitan el mantenimiento de la hiperrespuesta y el deterioro u obstrucción bronquial progresiva. Este riesgo o proceso demostrado en los pacientes con asma obliga a su control y el inicio temprano del tratamiento cuando aparecen los síntomas o su inestabilidad.
Tratamiento no farmacológico
Existe un grupo no despreciable de medidas que ayudan a disminuir o eliminar algunos de los desencadenantes y facilitan el control del asma bronquial. Su aplicación permitirá la disminución del consumo excesivo de medicamentos, la gravedad de las crisis y un control óptimo de la enfermedad (tabla 7).
Es esencial evitar el tabaquismo activo o pasivo, este último especialmente en el asma infantil por su relación directa con el número de crisis asmáticas, ingresos hospitalarios y la necesidad de más medicación para su control. Es útil evitar otros agentes como el humo de leña, los aceites de cocina, las pinturas o los aerosoles, que han sido reconocidos como desencadenantes inespecíficos de hiperreactividad. La adecuada ventilación de los ambientes, una temperatura de 24 oC durante el día (18 oC durante la noche) y una humedad relativa del 30-50% son recomendables.
Los animales domésticos, especialmente los gatos, deben ser evitados por los pacientes sensibilizados. Aunque es imposible evitar de forma completa los pólenes ambientales, su exposición puede reducirse evitando un mayor contacto los días de viento, cerrando las ventanas, utilizando aire acondicionado y suprimiendo las actividades al aire libre durante determinadas épocas según las características de cada región, sobre todo a primera hora de la mañana y al final de día, cuando las concentraciones son mayores. El elevado porcentaje de sensibilizantes del polvo doméstico puede evitarse con una limpieza periódica mediante aspiradoras con filtros especiales, controlando aquellos materiales capaces de acumularlos (alfombras, moquetas, cortinas, colchones y cojines de lana), exponiéndolos al sol, reduciendo la humedad ambiental y mejorando la ventilación diaria. La simple utilización de fundas de plástico sobre estos materiales impide el paso de los ácaros y, en algunos casos, puede acompañarse de la aplicación de acaricidas manteniendo un adecuado control ambiental. De forma ocasional, podría considerarse el uso de la inmunoterapia en asmáticos leves con una sensibilización única, en la que las medidas de control ambiental y un tratamiento farmacológico adecuado no son suficientes. No obstante, la inmunoterapia no debe utilizarse en pacientes mal controlados, no reemplaza las medidas de evitación ambiental y siempre debe realizarla personal experimentado.
Debe evitarse, o tomar medidas farmacológicas preventivas, un ejercicio intenso o prolongado por la posibilidad de provocar un broncospasmo, sobre todo cuando el ambiente es seco y frío. Las carreras son las de mayor riesgo, mientras que el ciclismo, la marcha y especialmente la natación suelen ser mejor toleradas. La presencia de un reflujo gastroesofágico sintomático aconseja su control para mejorar el tratamiento del asma por la posibilidad de compartir mecanismos fisiopatológicos.
En todos los asmáticos con crisis frecuentes de una intensidad moderada o grave es recomendable la vacuna antigripal anual si no existe una sensibilización previa a sus componentes. En algunos pacientes más graves o de difícil control se ha recomendado la vacuna antineumocócica y la posibilidad de iniciar un programa de rehabilitación respiratoria. Es aconsejable la realización controlada de ejercicio al aire libre y el entrenamiento muscular sobre técnicas de relajación o posturas que faciliten la espiración y puedan utilizarse durante las crisis.
¿Qué fármacos son útiles en el tratamiento del asma?
En la actualidad el tratamiento farmacológico del asma bronquial queda cubierto gracias a la posibilidad de utilizar un número amplio de fármacos muy efectivos que se caracterizan por un efecto broncodilatador (dilatación bronquial o relajación de la musculatura lisa bronquial) y antiinflamatorio. Los principales fármacos pueden dividirse en dos grandes grupos: los de rescate o aliviadores y los de mantenimiento, controladores o preventivos (tabla 8). Los primeros son los que actúan de forma más rápida y son capaces de mejorar inmediatamente al paciente actuando sobre la broncoconstricción. Los controladores son medicaciones que suelen tomarse a diario y son útiles para el mantenimiento del control a largo plazo de los síntomas de asma sin tener efectos tan inmediatos como los anteriores.
Fármacos de rescate o aliviadores
Agonistas beta-2 adrenérgicos inhalados de acción rápida. El salbutamol, la terbutalina y el fenoterol son los fármacos inhalados de elección en el tratamiento sintomático agudo del asma. Suelen utilizarse a demanda según los síntomas del paciente y actúan como tratamiento de rescate o de primera línea durante las exacerbaciones o aumentos puntuales de los síntomas, gracias a su mayor eficacia y capacidad de mejorar la obstrucción a una velocidad lo suficientemente rápida para evitar su progresión.
Los efectos indeseables importantes o que obligan a su retirada son infrecuentes y, con el tiempo, la mayoría son bien tolerados.
Anticolinérgicos inhalados. La acción broncodilatadora de los anticolinérgicos como el bromuro de ipratropio está relacionada con su antagonismo por los receptores muscarínicos. Su efecto broncodilatador es menos potente que el de los agonistas beta-2 adrenérgicos de acción rápida y necesitan unos 30-60 min para conseguir un efecto máximo. Su utilidad en el asma es más limitada y constituyen un tratamiento de segunda línea, sobre todo en los pacientes que no toleran los agonistas beta-2 adrenérgicos o en el broncospasmo inducido por los bloqueadores beta. No obstante, su utilización por vía inhalada, los pocos efectos secundarios a pesar de utilizar dosis elevadas y la posibilidad de una sinergia con los mismos agonistas beta-2 adrenérgicos pueden ser útiles en determinados casos.
Fármacos controladores o de mantenimiento
Corticoides inhalados. Los principales fármacos comercializados para su uso por vía inhalatoria son el dipropionato de beclometasona, el propionato de fluticasona y la budesonida, y son el pilar fundamental del tratamiento actual del asma bronquial, por su mayor potencia antiinflamatoria, sobre la que existen numerosos estudios que la confirman. Estos fármacos mejoran la función pulmonar y la hiperreactividad bronquial a partir de las 1-3 y 4-6 semanas, respectivamente. Su inicio temprano es importante y debe mantenerse en el tiempo hasta conseguir un buen control de la enfermedad para evitar la reaparición de los síntomas.
La mayoría de los efectos secundarios locales están relacionados con la disfonía, la irritación laríngea o la candidiasis orofaríngea, y pueden minimizarse al mejorar los sistemas o técnicas de inhalación y con la higiene bucal después de utilizarlos. Sus efectos sistémicos suelen ser mínimos a las dosis necesarias para el control del asma bronquial y con la beclometasona sólo suelen aparecer a partir de 400 µg al día en los niños y 800 µg en los adultos.
Corticoides sistémicos. El mecanismo de acción es similar al de los inhalados, aunque con un mayor número de efectos secundarios que obliga a minimizar sus indicaciones. Su utilización ha sido propuesta durante las exacerbaciones importantes y en algunos pacientes para facilitar el control de un asma grave persistente. Deben administrarse a las mínimas dosis durante el menor tiempo posible y preferiblemente en su forma oral, evitando la parenteral y aconsejando la utilización de la prednisona, prednisolona o metilprednisolona, por su menor efecto mineralocorticoide, su vida media relativamente corta o sus efectos limitados sobre la musculatura estriada.
Agonistas beta-2 adrenérgicos inhalados de acción prolongada. El salmeterol y el formoterol son los principales fármacos de este grupo que actúa como broncodilatador aunque manteniendo su efecto durante un mínimo de 12 h. Como el resto de los agonistas beta-2, relajan la musculatura lisa bronquial, mejoran el aclaramiento mucociliar, disminuyen la permeabilidad vascular y modulan la liberación de mediadores de los mastocitos o los basófilos, actuando posiblemente como antiinflamatorios. Las diferencias entre salmeterol y formoterol no son tan importantes para definir una única elección y en la mayoría de los casos dependerá de aspectos individuales, aunque el formoterol aportaría un inicio de acción más rápido y la posibilidad de actuar como tratamiento de rescate.
Estos fármacos han sido introducidos en el tratamiento del asma en aquellos pacientes que necesitan aumentar la dosis de corticoides inhalados para conseguir su control. La utilización de agonistas beta-2 de larga duración antes de aumentar las dosis de corticoides ha demostrado mejorar el control, los síntomas, la disnea nocturna, la función pulmonar, el número de exacerbaciones o la necesidad de los agonistas beta-2 de acción corta. Además, la disponibilidad de corticoides y agonistas beta-2 de acción prolongada en un mismo dis-
positivo ha facilitado su realización y cumplimiento con una eficacia terapéutica o efectos secundarios similares, recomendando su utilización cuando sean necesarios.
Cromonas inhaladas: nedocromil sódico y cromoglicato disódico. Estos fármacos son estabilizadores de la membrana de los mastocitos y se han utilizado como ahorradores de la administración de corticoides con una eficacia moderada. No se ha demostrado que tengan capacidad para modificar la enfermedad y sus principales indicaciones son el asma inducida por el ejercicio o el frío, y la mejora del control del asma persistente leve antes de aumentar los corticoides inhalados. Su principal ventaja es la práctica carencia de efectos secundarios y entre sus desventajas destaca su menor eficacia o la necesidad de administración hasta cuatro veces al día durante un mínimo de 4-6 semanas para esperar un efecto terapéutico.
Teofilinas. Actúan principalmente como broncodilatadores, aunque también se les han atribuido efectos inmunomoduladores o antiinflamatorios que tendrían su influencia en el manejo del asma. La principal desventaja y el motivo fundamental de su menor uso está en relación a la necesidad de la medición periódica de valores sanguíneos (márgenes terapéuticos de 5-15 µg/ ml) y la posibilidad de interacciones o un mayor número de efectos secundarios que otros fármacos.
En el asma se consideran como fármacos de mantenimiento de segunda línea y sus indicaciones quedarían más restringidas. En la agudización del asma estarían indicadas ante la falta de respuesta del tratamiento convencional y en las formas crónicas, a la ausencia de control por los medicamentos de primera línea, la dificultad de adherencia al tratamiento inhalado y al riesgo o efectos secundarios de los otros fármacos.
Antileucotrienos. El montelukast, el pranilukast y el zafirlukast constituyen un nuevo grupo de fármacos antiasmáticos capaces de modular la producción y los efectos de los leucotrienos sobre los que no influirían los corticoides. Los leucotrienos actuarían como intermediarios de los mecanismos inflamatorios y en la broncoconstricción de los pacientes con asma, y estos nuevos fármacos los controlarían inhibiendo su producción o como antagonistas específicos de sus receptores celulares. En España se ha comercializado el montelukast y el zafirlukast, ambos antileucotrienos o inhibidores de los receptores.
Su eficacia ha sido demostrada en la broncoconstricción causada por alergenos (respuestas inmediatas o tardías), el ejercicio y el ácido acetilsalicílico, y han sido introducidos en el tratamiento del asma persistente moderado o grave con la intención de reducir la dosis de corticoides inhalados.
¿Cómo utilizar y combinar todos los fármacos?
En la actualidad son numerosas las guías editadas a partir de múltiples consensos o sociedades que sitúan el asma como un proceso crónico y variable, que cursa con distintas fases o grados de gravedad y cuyo tratamiento debe realizarse de forma escalonada. El tratamiento es flexible y se correlaciona con la gravedad de la enfermedad, recomendando un aumento del tipo de fármacos, su dosis y su frecuencia hasta conseguir el control con un mínimo de dosis y efectos secundarios. En ocasiones, una primera evaluación encuentra al paciente en una situación claramente inestable y es aconsejable utilizar un ciclo oral de corticoides o corticoides inhalados a altas dosis junto a los agonistas beta-2 de acción prolongada, para conseguir su control de forma precoz y seguir valorando sus necesidades en controles posteriores.
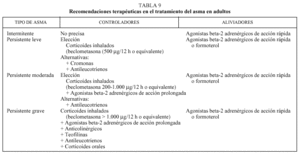
Una de las guías más conocidas es la GINA, que ha sido realizada por expertos de todo el mundo y actúa como una referencia internacional en el tratamiento de esta enfermedad a partir de un conjunto de escalones de gravedad establecidos según la clínica, la función pulmonar y la necesidad de medicación (tabla 4), con los que, una vez ubicado al paciente, éste recibe más o menos tratamiento (tablas 9 y 10).
Control y seguimiento del paciente asmático
La gravedad y la evolución del asma bronquial puede evaluarse con la medición de los síntomas, la función pulmonar y el número de fármacos necesarios en el tratamiento. Cada visita o control del paciente diagnosticado debe incluir un interrogatorio intencionado sobre la presencia de los principales síntomas relacionados con el asma (tos, disnea, sibilantes y opresión torácica) y se debe compararlos con los controles previos, registrar su evolución y añadir los cambios para conocer la situación clínica. Es fundamental conocer si ha sufrido alguna exacerbación y la forma en que la ha controlado, así como la calidad de vida que sigue el paciente, especialmente en cuanto a la presencia de síntomas durante la noche, a primera hora de la mañana, durante el esfuerzo y ante cualquiera de los desencadenantes que puedan relacionarse con su enfermedad como primer signo de inicio de una descompensación o de un empeoramiento del control.
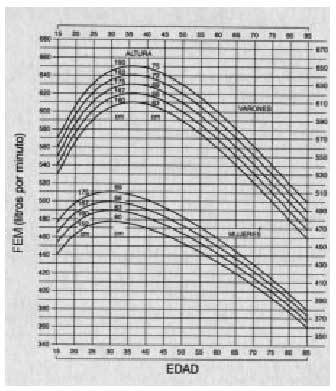
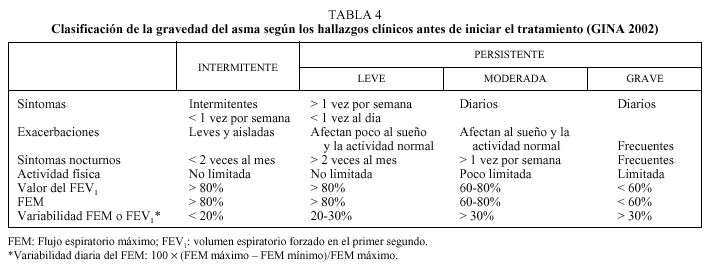
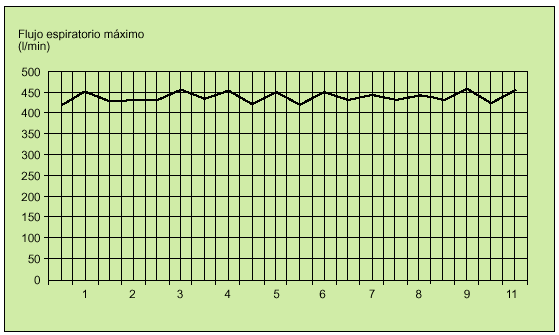
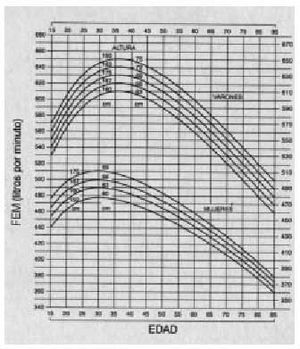
La espirometría aportará una información más detallada de la presencia y evolución de la obstrucción, especialmente en aquellos pacientes con mayor dificultad de reconocimiento de los síntomas. Sin embargo, sólo se recomienda en una valoración inicial para confirmar el diagnóstico y periódicamente para un seguimiento cada 6 meses o anual, en función de la evolución del paciente o para confirmar las mediciones del flujo espiratorio máximo obtenidas con los medidores de uso domiciliario (figs. 4 y 5). El medidor del flujo espiratorio máximo es un instrumento portátil, muy útil, barato, de manejo sencillo y cuyos resultados son muy reproducibles para valorar la evolución del paciente y conocer de forma continua el grado de obstrucción registrado en su domicilio, la consulta, en urgencias durante una exacerbación o en el hospital gracias a su buena correlación con el FEV1. La simple realización de una espiración forzada máxima con el instrumento permite al paciente asegurar la relación entre la presencia de algunos síntomas y el grado de obstrucción, evitando el peligro de sobredimensionar una situación de ansiedad o no percibir un empeoramiento asintomático por un grado elevado de tolerancia. Su registro regular, una o dos veces al día, antes y después de los broncodilatadores, permitirá reconocer la respuesta al tratamiento y la presencia de factores desencadenantes a evitar en un futuro. La mayoría de los adultos y niños mayores de 5 años puede realizarlo y su resultado debe ser comparado con el establecido en las tablas de referencia en función de la edad, el sexo y otros parámetros antropométricos (tabla 11). Este valor podrá actuar como guía, aunque es más aconsejable establecer un valor personal de referencia y de variabilidad diaria para cada paciente cuando está estable y bajo un tratamiento efectivo durante aproximadamente dos semanas, realizando un mínimo de dos mediciones diarias, y posteriormente utilizarlo para las comparaciones o decisiones terapéuticas. El registro del flujo espiratorio máximo no es necesario en todos los pacientes con asma pero es recomendable en aquellos de difícil control, asma persistente, pacientes más graves o con asma de riesgo vital y en los que perciben mal la presencia de síntomas. Así, siempre deberemos valorar la presencia de un valor por debajo del 80% de su referencia y una variabilidad superior al 20% para considerar un cambio, habitualmente con una terapia más agresiva. Aunque el valor absoluto o la variabilidad sean los parámetros más útiles para considerar la presencia de gravedad o inestabilidad, también son interesantes los valores que comparan una medición antes y después de broncodilatador o la comparación de todos los valores matutinos como índice de labilidad bronquial (figs. 6, 7 y 8).
Fig. 6. Tablas de referencia del FEM en función de la edad, el sexo y la talla de los pacientes.
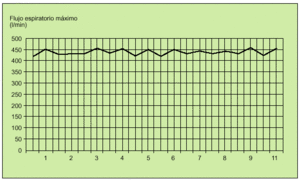
Fig. 7. Registro de una gráfica de mediciones de flujo espiratorio máximo en un paciente con un asma bronquial estable (flujo espiratorio máximo superior al 80% y variabilidad inferior al 20%).
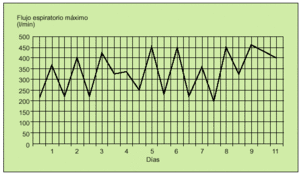
Fig. 8. Registro de una gráfica de mediciones de flujo espiratorio máximo en un paciente con un asma bronquial lábil (flujo espiratorio máximo inferior al 80% y variabilidad superior al 20%).
Una vez valorado el paciente, iniciado el tratamiento y conseguido el control de la enfermedad durante aproximadamente tres meses, deberíamos plantearnos la posibilidad de la reducción del tratamiento o, en caso contrario, mantener o variar el escalón a otro más agresivo. Cualquier cambio deberá ser confirmado periódicamente en un plazo similar hasta conseguir mantener el control de la enfermedad con el mínimo tratamiento. En todos los casos y especialmente en los pacientes que no mejoran a pesar de una tratamiento correcto, siempre deberemos considerar otros factores añadidos (tablas 5 y 11).
Bibliografía recomendada
Antó JM, Sunyer J. Epidemiología del asma. Med Clin (Barc) 2002;3(Supl 1):3-5.
Bone RC, and the International Clinical Respiratory Group. Assessment of therapeutic benefit in asthmatic patients. Chest 1993;103:914-16.
Bone RC. Goals of asthma management. A step-care approach. Chest 1996;109:1056-65.
Cabrera P, Caminero JA. Factores de riesgo en asma. Arch Bronconeumol 2001;37:248-56.
Diego A. Tratamiento de la crisis asmática. ¿Qué debemos hacer? Arch Bronconeumol 2001;37(Supl 5):8-11.
López A, Casán P, Diego A, Duce F, Gáldez JB, Manresa F, et al. Recomendaciones para educar a los pacientes con asma. Arch Bronconeumol 1996;32(Supl 1):10-4.
National Institutes of Health. GINA Global Strategy for Asthma management and prevention 2002. Disponible en: www.ginasthma. com
NHLBI. International consensus report on diagnosis and treatment of asthma. Eur Respir J 1992;5:601-41.
Patel AM, Axen DM, Bartling SL, Guarderas JC. Practical considerations for managing asthma in adults. Mayo Clin Proc 1997; 72:749-56.
Pellicer C. Asociación de fármacos en el tratamiento del asma. ¿Son realmente útiles? Arch Bronconeumol 2000;36:491-3.
Picado C. Asma: retos para el 2000. Arch Bronconeumol 2000; 36(Supl 3):24-6.
Pueyo A, Viejo JL. Presente y futuro del tratamiento del asma. Med Clin (Barc) 2002;3(Supl 1):41-5.
SEPAR (Grupo de Trabajo). Recomendaciones para la atención del paciente con asma. Arch Bronconeumol 1998;34:394-9.
Sobradillo V, Gómez A, Chic S. Enfoque actual del diagnóstico del asma. Med Clin (Barc) 2002;3(Supl 1):18-22.
Weinberger M, Hendeles L. Theophyline in asthma. N Engl J Med 1996;334:1380-8.