El cáncer cervical es una de las enfermedades malignas más comunes que afectan al sexo femenino y se estima que origina el fallecimiento de unas 200.000 mujeres al año. Constituye el primer cáncer más frecuente en los países no industrializados y ocupa el décimo lugar entre las neoplasias de los países desarrollados.
Durante los últimos 20 años se ha demostrado que el mismo carcinógeno, el virus del papiloma humano (HPV), causa casi todos los casos de cáncer cervical, estimulando a los científicos a una comprensión más completa de las fases de la carcinogénesis y a buscar estrategias de prevención vinculadas al HPV. Estas fases incluyen: infección por HPV, progresión a lesiones premalignas de alto grado e invasión. La infección por el HPV es una infección de transmisión sexual muy común, con más de 30 tipos genitales, aunque sólo los tipos 10 a 15 causan cáncer. La infección actual se mide con mayor precisión mediante la detección del ADN. La mayoría de infecciones, incluyendo las que presentan anormalidades citológicas, se resuelven espontáneamente, virando a la negatividad en el ADN del HPV (a menudo con seropositividad). En ocasiones, una infección por HPV progresa a lesión preinvasiva de alto grado (incluyendo los estadios más avanzados de carcinoma in situ [CIS]). Es característico que las lesiones de alto grado contengan tipos carcinógenos de HPV; una vez establecidas, estas lesiones tienen tendencia a persistir. Muchas lesiones de alto grado se convierten en carcinomas de cérvix invasivos, marcados por una frecuencia superior de alteraciones genéticas.
Antecedentes epidemiológicos
Antes de la introducción del cribado, las tasas de frecuencia y mortalidad eran poco representativas, si bien el cáncer cervical se consideraba como el segundo tipo de cáncer más habitual en el género femenino.
En 1943, cuando Papanicolaou y Traut publicaron su estudio, en los EE.UU. había el equivalente a 50.000 casos de cáncer cervical. En 1950, 8.000 mujeres murieron de cáncer cervical. En las estadísticas de cáncer en EE.UU., el cáncer cervical es hoy día el octavo en incidencia (13.700 casos) y el undécimo en mortalidad (4.900 casos). Estas estadísticas apuntan reducciones de un 75 y de un 73%, respectivamente, atribuidas sobre todo al diagnóstico y tratamiento de lesiones precancerosas secundarios a la aplicación de la citología Papanicolaou (Pap).
En nuestro país, el cáncer de cuello de útero tiene una incidencia y mortalidad muy bajas. Durante el año 1990 causó la muerte de 93 mujeres en Cataluña, con una tasa bruta de mortalidad de 3,03 por 100.000 habitantes, no habiéndose notificado ninguna muerte por cáncer in situ.
En relación con la incidencia de nuevos casos, y a partir de los datos del registro de cáncer de Tarragona (período 1980-1985), se estima que cada año aparecen aproximadamente unos 700 casos de cáncer invasivo, correspondiente a una tasa bruta de 11,2 por 100.000 mujeres y año (8,4, tasa ajustada a la población mundial). Ésta es la cifra más alta entre los registros existentes en España, que se sitúan en cifras de 5,7 a 7,4 de las tasas ajustadas a la población mundial. El registro monográfico de Gerona presentaba una tasa bruta de 8,16 casos de cáncer invasivo por 100.000 y una tasa ajustada de 6,07 por 100.000 en el período de 1980-1989.
Los tumores malignos de cuello uterino figuran entre las causas de muerte innecesariamente prematuras y sanitariamente evitables en Cataluña, causando 148 defunciones acumuladas en el trienio 1994-1996, con una tasa anual de 2,35 por 100.000 mujeres del grupo de edad comprendido entre los 15 y los 64 años. Su detección, tratamiento y control en mujeres de 25 a 64 años atendidas por los servicios sanitarios se encuentra entre las intervenciones y acciones prioritarias del Plan de Salud de Cataluña 1999-2001.
Globalmente, la incidencia del cáncer invasivo de cuello de útero en nuestro país se sitúa entre las tasas más bajas del mundo. Así, las más elevadas se presentan en Cali (Colombia) con 48,2, Sao Paulo (Brasil) con 35,1 y la antigua República Democrática Alemana (24,6), que es la primera de Europa. La incidencia más baja se encuentra entre las poblaciones de Israel (3-5,1) y Finlandia (5,5); después aparecen los datos correspondientes al Registro de Navarra (5,7) y al de Zaragoza, con una tasa del 6,1. Los valores de Tarragona y de Gerona también se sitúan entre los más bajos del mundo. La media de edad en el momento del diagnóstico era de 57,3 años en Tarragona. En el caso del cáncer in situ, la media de edad era de 38,6 años en el momento del diagnóstico, aunque se han de considerar con precaución estos datos dada la circunstancia de falta de registro que puede existir.
La supervivencia del cáncer de cuello de útero invasivo es muy variable en función del grado invasivo en el momento del diagnóstico. Las cifras obtenidas en el registro de Gerona son del 44% de supervivencia global a los 5 años en el cáncer de cuello de útero invasivo.
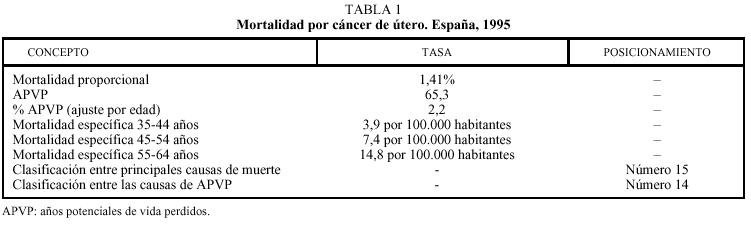
En la tabla 1 se exponen los principales indicadores sanitarios de cáncer de útero correspondientes a 1995 para España.
Cribado. Test de Papanicolaou (Pap)
Las pruebas de cribado deben ser validadas antes de generalizar su aplicación a poblaciones, no debiendo ser mesuradas en resultados sustitutivos sino en términos de reducción de la morbilidad y la mortalidad especí ficas.
El cribado cervical no cumpliría satisfactoriamente algunos de los criterios que han sido considerados como un requisito necesario para su publicación a escala masiva. Los aspectos más problemáticos incluyen la precisión del Pap, la incertidumbre sobre la historia natural de la enfermedad, el desacuerdo sobre lo que constituye la población de riesgo definida, el desacuerdo sobre el manejo de las anormalidades cervicales, y la falta de datos fiables para la evaluación de la eficacia en relación con el coste.
Papanicolaou y Traut describieron en 1943 un procedimiento de toma citológica consistente en la obtención de exfoliación o rascado suave de células provenientes del endocérvix, exocérvix y vagina. La toma de citologías Pap no es un procedimiento simple, y su interpretación pertenece a una de las áreas de la microscopia más complejas. La exfoliación debe ser fijada rápidamente para evitar la formación de artefactos celulares que se confunden con discariosis y aumentan la posibilidad de que una citología sea informada como anormal. Una citología negativa no garantiza la ausencia de una anormalidad patológica. La citología no sustituye la inspección visual del cuello uterino. Estudios iniciales demostraron que la distinción entre la displasia histológicamente demostrada y el CIS es artificial, ya que las diferencias conductuales entre ambos grupos de lesiones no son relevantes.
Anatomopatólogos experimentados han puesto de manifiesto marcadas diferencias intraobservador e interobservador en la interpretación de citologías y biopsias, comprometiendo la fiabilidad de la técnica.
Como promedio de las diferentes experiencias se estima que la sensibilidad del test de Papanicolaou es del 70% (oscilaría entre un 55 y un 90%); teniendo en cuenta que la displasia y el carcinoma in situ parecen necesitar años para su progresión, se calcula que alrededor del 90% de los casos preinvasivos deberían ser detectados si el cribado se realizara correctamente y fuera repetido al menos cada 3 años.
El concepto de resultado «falso positivo» en una citología Pap es significativo sólo si se relaciona con el propósito del cribado, es decir, la detección de verdaderas anormalidades premalignas que conducirían a la enfermedad invasiva si se dejaran sin tratar. Por tanto, todas las citologías positivas que exceden de la prevalencia esperada de la enfermedad en ausencia de cribado son falsos positivos. Como este criterio es aplicable a la mayoría de las citologías positivas, el valor predictivo positivo de la citología cervical es muy bajo.
Una citología falsamente negativa, según la bibliografía, se refiere a tres tipos de error: a) una citología anormal se informa como normal; b) la citología es inadecuada o la lesión no libera células anormales, y c) el carcinoma invasivo aparece después de la última citología normal. El índice de falsos negativos para lesiones con relación incierta con el carcinoma invasivo (displasias, CIS, neoplasia cervical intraepitelial [CIN]) oscila entre un 20 y un 40%.
Historia natural de la enfermedad
A principios del siglo xx, el cáncer cervical era responsable de alrededor del 20% de las muertes por cáncer en mujeres y se conocía como morbus miserias, porque afectaba particularmente a los pobres. Se reconocía la necesidad del diagnóstico precoz, aun considerando los inconvenientes de los excesos en el diagnóstico y el tratamiento.
La secuencia de la historia natural identificada en el proceso evolutivo del cáncer de cérvix sería: displasia leve, moderada, grave, carcinoma in situ y carcinoma invasivo. La filosofía del cribado se ha basado en esta visión secuencial continua para conseguir un diagnóstico precoz, efectuado cuando la paciente está asintomática y en la fase donde las expectativas de supervivencia al proceso se acercan al 100%.
De todas formas, hay cuestiones fundamentales de la historia natural que todavía no se han clarificado. ¿Es verdad el modelo continuo? Y si es así, ¿cuál es la escala temporal de los cambios progresivos? ¿Qué proporción de lesiones revierten a la normalidad si se dejan sin tratar? ¿Influye el tratamiento de las lesiones precursoras en la mortalidad por enfermedad invasiva? ¿Cuál es el papel del virus del papiloma humano en la génesis y progresión de la enfermedad?
La Canadian Task Force informó acerca de la distribución modal de la prevalencia de displasia, CIS y carcinoma invasivo compatible con el modelo continuo y postuló un intervalo de 10 años entre displasia y CIS, y un intervalo de 35 años entre CIS y carcinoma invasivo. De todas formas, otros estudios no han conseguido confirmar esta hipótesis. Dado que el cribado lleva al diagnóstico de displasia y CIS con mucha mayor frecuencia que la incidencia esperada de carcinoma invasivo, muchas lesiones anormales deben regresar espontáneamente sin tratamiento. Cuanto más alto es el índice de regresión más elevado es el riesgo de sobretratamiento. Diferentes estudios han cuestionado la idoneidad del modelo continuo en la historia natural de esta enfermedad.
Este alejamiento del modelo continuo es confirmado por estudios histopatológicos, que documentan negativamente el papel de la displasia como precursora del carcinoma in situ, ya que su localización es diferente, demostrándose que tumores precozmente invasivos provienen con relativa frecuencia de epitelios displásicos, incluso de las formas más leves. El problema para el profesional que realiza el cribado es la incapacidad actual para distinguir entre la displasia verdaderamente precancerosa y aquellas que son proliferaciones inespecíficas.
No se sabe la proporción de CIS que son verdaderos precursores de carcinoma invasivo. En el estudio más extenso de la historia natural del CIS, en el cual se hizo un seguimiento de hasta 20 años a más de 1.000 mujeres, en un 86% el tratamiento normal llevó a la curación, mientras que en el restante 14% las lesiones siguieron reapareciendo o persistieron con independencia del tratamiento utilizado. El hecho de que las lesiones sean o no completamente extirpadas parece no influir en la posibilidad de que la invasión ocurra con posterioridad. Por consiguiente, el seguimiento clínico y citológico regular de las pacientes aparentemente tratadas con éxito no previno el desarrollo de carcinoma invasivo. En la mayoría de estas mujeres, el carcinoma apareció ya de novo o a los pocos meses de la primera nueva anormalidad citológica, indicando que la invasión no había progresado por la esperada fase premaligna prolongada.
Dado que el carcinoma invasivo es raro en mujeres jóvenes y el CIS frecuente, mientras que en mujeres de edad avanzada hay un déficit de CIS para la incidencia esperada de la enfermedad invasiva, la relación entre CIS y enfermedad invasiva no está clara. Recientes estudios no han evidenciado correlación entre el índice de detección y posterior tratamiento y la reducción posterior de carcinoma invasivo en los años posteriores.
Llegados a este punto hay que hacerse la siguiente pregunta: ¿cuál es el estadio premaligno más precoz de la enfermedad?
El profesional que realiza el cribado se enfrenta a una elección alternativa: se basa en la citología y el seguimiento citológico de anormalidades menores, con el riesgo de pasar por alto lesiones importantes, o bien aplica la colposcopia a todas las anormalidades citológicas menores, lo cual sobrepasa al sistema de cribado y aumenta el sobretratamiento. El problema con el frotis Pap es que no reúne todas las características ideales para un test de cribado.
La repetición de la citología no es la respuesta a los test de Pap erróneos, ya que incluso los frotis levemente atípicos, que resultan normales al ser repetidos, pueden ser obtenidos en presencia de CIN II o CIN III. En un programa australiano 123 de 256 (48%) de frotis de tipo II (sin evidencia de displasia) fueron posteriormente rediagnosticados de displasia (62 casos), CIS (53 casos) y 8 casos de carcinoma invasivo. En un 5% de los frotis puede estar presente una citología bor derline.
Son notables las implicaciones de esta línea de razonamiento en referencia a las políticas de recomendación de la colposcopia, con gran sobretratamiento de lesiones benignas en mujeres jóvenes, utilización inadecuada de recursos sanitarios e insatisfacción social.
Objetivo del diagnóstico precoz
El diagnóstico de las lesiones más precoces se centra en el carcinoma in situ, pero muchos problemas nacen de que este diagnóstico no es fácil y que, en realidad, depende en gran medida del criterio subjetivo de cada histopatólogo, puesto que no existe ninguna alteración que sea específica de esta lesión, si bien, como en todo diagnóstico de neoplasia, el hallazgo de anomalías arquitecturales y de alteraciones celulares es decisivo.
El descubrimiento de estas lesiones depende fundamentalmente de los medios de diagnóstico empleados. El hallazgo de un estadio precoz con la biopsia a ciegas es poco menos que una casualidad y carece, por tanto, de todo valor. Si queremos obtener un rendimiento eficaz hay que recurrir a la práctica de biopsias múltiples en varias localizaciones, a la biopsia selectiva en el punto indicado por la colposcopia o a la conización cervical y estudio de cortes seriados.
En la tabla 2 se presentan las diferentes estrategias a seguir en la detección del cáncer de cuello uterino. No cabe duda de que la primera posibilidad es, en teoría, la ideal, pero (consideraciones económicas al margen) para ello es preciso cumplir tres etapas: a) educación del médico práctico; b) creación de centros de detección, y c) educación de la población en general.
Población de riesgo
El protocolo de actuación más recomendable sería el siguiente:
1. Citología inicial a todas las mujeres mayores de 18 años que hayan tenido relaciones sexuales. El límite inicial de edad es controvertido y, en caso de necesitar una estrategia de priorización, se ha apuntado que la efectividad del frotis (cara a reducir la mortalidad por cáncer de cérvix) no es tan evidente en el grupo de mujeres menores de 30 años de edad. Asimismo, se considera de interés prioritario la realización de las oportunas pruebas de cribado a mujeres que se consideren de alto riesgo y que son, entre otras, las que toman anticonceptivos orales, las que consultan por enfermedad venérea, las que han tenido embarazos múltiples, las de clase social baja y las que se caracterizan por una mayor promiscuidad sexual.
2. En el caso de que no se detecte atipia, se tomará una segunda muestra al año siguiente.
3. Si persiste el test negativo, se continúa con una periodicidad de 3-5 años.
4. Se considera como generalmente innecesario realizar examen en mujeres que tengan más de 60 años de edad y hayan presentado dos frotis previos negativos.
Limitaciones del diagnóstico precoz
Pese a la mejoría de las técnicas exploratorias y a la intensificación de las campañas de diagnóstico, hay un elevado número de limitaciones en la consecución del objetivo del diagnóstico precoz.
1. Naturaleza asintomática del cáncer: la primera y gran dificultad radica en el hecho de que no hay síntomas que indiquen el comienzo de la enfermedad, pues los considerados clásicamente como tales (leucorrea, metrorragias por contacto, dolor) suelen presentarse cuando ya el carcinoma se halla en una fase bastante avanzada.
2. Conducta de las pacientes: la dejadez y abandono de las propias pacientes es, en gran parte, la responsable de que la propaganda del diagnóstico precoz no sea demasiado eficaz, en especial en los estratos sociales bajos. Entre la aparición de los primeros síntomas y los requerimientos de consulta puede pasar una media de un año, según diferentes trabajos.
Un grupo que ha merecido varios estudios es el de las mujeres obesas. Dado que las mujeres con sobrepeso y obesidad tienen índices más altos de mortalidad por cáncer cervical (y de mama), deberían ser un objetivo de los programas de cribado.
3. Carencia de exámenes periódicos sistematizados: ante la ausencia de síntomas precoces se impone la práctica de revisiones periódicas, pero éstas se encuentran con las dificultades derivadas de la falta de educación sanitaria de la población en general y, a veces, también de los médicos, lo que se traduce en un inadmisible retraso en el diagnóstico.
4. Conducta del médico: la discreta colaboración del médico general se deduce del hecho de que la mayoría de las pacientes han sido sometidas a tratamientos hormonales más o menos anodinos antes de proceder a un reconocimiento. El ginecólogo también tiene su cuota de responsabilidad, tanto por la infravaloración en la interpretación de los síntomas o hallazgos explora torios, como por relajar el control sistemático de al menos toda paciente que sobrepase los 35 años. Así, se explica que sólo un 46% de los carcinomas sean diagnosticados en la primera visita.
5. Problemas de educación profesional: cierto número de fracasos en el descubrimiento del cáncer de cuello uterino dependen de insuficiencias en la enseñanza oncológica en general y, más especialmente, de la oncología ginecológica.
6. Insuficiencia de las técnicas diagnósticas: todos los procedimientos diagnósticos empleados tienen su porcentaje de error, e incluso la biopsia (único método válido para discernir si realmente se trata de un proceso carcinomatoso) puede presentar un cierto porcentaje de falsos negativos. Aunque estos fallos sean menos frecuentes con las conizaciones de cuello, tampoco esta técnica queda libre de errores y, en cambio, son relativamente frecuentes las complicaciones.
Sin embargo, hay que señalar que el empleo correcto y sistemático de los medios de que disponemos en la actualidad logra mejorar los resultados de manera extraordinaria.
7. Ausencia de campañas sanitarias: es preciso desarrollar amplias campañas sanitarias para proporcionar una cierta cultura médica a la población en general y sensibilizar al colectivo femenino de la necesidad de someterse a controles periódicos de su aparato genital; es especialmente importante proporcionar la información suficiente sobre la oportunidad de los exámenes en masa. Esta educación sanitaria debe ir dirigida en mayor grado a los líderes sociales.
Por otra parte, faltan también en nuestro país las instalaciones adecuadas, si no en calidad sí en cantidad, para poder controlar no ya a toda la población femenina, sino tan sólo a aquella parte de las mujeres que por su edad o por los factores epidemiológicos personales, constituyen el grupo más expuesto al carcinoma.
En relación con el coste-beneficio de la intervención, un editorial publicado en The Lancet comentaba de todas formas que desde que se introdujo el cribado citológico a gran escala en la década de los sesenta, la mortalidad había descendido un 1% anual; pero éste parece ser el índice al que había estado descendiendo durante varias décadas anteriores, por lo que no ha habido ningún cambio evidente. Concediendo, a lo sumo, un 2,5% de efectividad por cada vida salvada con el cribado, se llevaban a cabo 40.000 frotis y 200 biopsias escisionales (un índice coste-beneficio penosamente escaso). Incluso si se dobla la efectividad, sólo se prevendría una muerte al año por cada 160.000 mujeres de 25 o más años.
Inconvenientes del cribado
Los errores en el cribado ocurren por una técnica inadecuada en la toma de los frotis, por resultados falsos negativos y falsos positivos, por fallo en el seguimiento de frotis anormales y por sobretratamiento de lesiones benignas.
Se han documentado graves efectos adversos psicológicos y psicosexuales tras ser comunicada a la paciente la positividad de su test. Las biopsias en cono pueden causar infección posterior, o hemorragia primaria o secundaria, a veces suficientemente graves como para requerir transfusión, mientras que otras mujeres desarrollan estenosis cervical sintomática e infertilidad.
También pueden considerarse como efectos adversos los problemas medicolegales derivados del cribado. El marido de una paciente que murió de cáncer cervical tras dos frotis positivos que no fueron correctamente seguidos tuvo que ser indemnizado económicamente. Los ginecólogos que realicen seguimiento, en vez de remitir directamente para coloposcopia y tratamiento de pacientes con discariosis leve a moderada, pueden ser demandados por basarse en un diagnóstico citológico no fiable.
Consideraciones éticas
Los defensores del cribado, con una correcta línea argumental, concluyen que la evidencia preexistente más el sentido común demandan programas masivos de cribado. Al «mantener la fe», los defensores del cribado pueden verse forzados a aceptar o rechazar la evidencia, no tanto por sus méritos científicos como por el grado en que apoya o rechaza la afirmación de que el cribado es bueno. No es ética la exageración de los beneficios y la omisión de perjuicios al invitar a las mujeres a participar en este tipo de programas. Existe una diferencia ética entre ofrecer el cribado a una población sana, sin evidencia fuerte de que los beneficios superan a los perjuicios, y la práctica médica ordinaria de responder a las solicitudes de ayuda de los pacientes. En este último caso, el médico no es responsable de los defectos del conocimiento médico y el tratamiento que ofrece refleja la práctica del momento, a menudo sin beneficios probados.
Cuando se pide a personas sanas que participen en un cribado es imperativo disponer de una evaluación cuantitativa de los beneficios esperados y de los posibles perjuicios, de manera que la persona pueda hacer una elección racional entre aceptar o rechazar la oferta del proceso. Esta información actualmente no está disponible en el cribado cervical. Un mejor conocimiento de la etiología y la historia natural del cáncer cervical permitirá disponer de una prueba que identifique a personas con un riesgo elevado.
Nuevas perspectivas
El cáncer de cuello de útero ocupa el segundo lugar mundial entre los tumores más frecuentes en las mujeres, con unos 400.000 casos diagnosticados al año. En algunas zonas de Asia, África y Latinoamérica es el primer cáncer femenino. Aunque en un 70% de las mujeres de los países de rentas altas se efectúa cribado para el cáncer cervical, éste sólo se realiza en el 5% de las mujeres de los países de rentas medias y bajas, normalmente en clínicas privadas y en algunos núcleos urbanos.
Los profesionales de la salud podrían realizar el cribado a las mujeres para el cáncer de cérvix usando una nueva técnica sencilla que no requiere equipos médicos complejos, descubierta por investigadores en Zimbabwe y los EE.UU. La técnica, probada en un estudio sobre casi 11.000 mujeres en 15 clínicas de Zimbabwe, conlleva una inspección visual del cérvix después de lavarlo con una solución diluida de ácido acético. El ácido acético vuelve blanco cualquier tejido que esté desarrollando lesiones precancerosas.
Usado por las enfermeras-comadronas, el test del ácido acético detectó con precisión más del 75% de los cánceres potenciales entre las participantes en el estudio. El método también llevó a los profesionales de la salud a identificar un cierto número de falsos positivos, posiblemente por las altas prevalencias de otras enfermedades de transmisión sexual en la población de estudio. De todas formas, los investigadores creen que el número de falsos positivos podría reducirse con un mayor entrenamiento de los profesionales. Además, señalan que todavía hay muchas barreras para proporcionar tratamiento efectivo una vez las mujeres ya han sido diagnosticadas.
Aunque el test de Papanicolaou es la base principal para la prevención del cáncer cervical, el nuevo modelo de carcinogénesis cervical sugiere que un test de ADN del HPV sensible puede ser útil en la prevención (tanto primaria como secundaria) del cáncer cervical, pero está en discusión. Las mujeres de los países desarrollados están protegidas (si bien de forma imperfecta) mediante el cribado con test de Pap, por el cual se detectan cambios celulares microscópicos en el cérvix causados por HPV que se sabe que preceden o acompañan al cáncer cervical. El objetivo final debe ser la erradicación del HPV mediante vacunación, pero una expectativa mucho más inmediata es la detección y monitorización del virus como parte del proceso de cribado y diagnóstico. El test del HPV podría tener tres funciones potenciales: selección de pacientes con células escamosas atípicas de significación indeterminada y frotis cervicales de bajo grado; vigilancia de neoplasias cervicales intraepiteliales de alto grado y enfermedad (micro) invasiva localizada, tras tratamiento; cribado primario, ya sea solo o en combinación con la citología.
El debate sobre el uso del test de HPV para prevenir el cáncer cervical debe iniciarse con datos fiables. Casi todas las lesiones de alto grado y los cánceres contienen HPV carcinogénicos, pero se debe evitar el exceso de exámenes de HPV porque la infección es un proceso común (y típicamente transitorio), en especial al nivel más sensible de detección del ADN.
Cada uno de los diferentes tipos de HPV genital carcinogénico implica un riesgo distinto para el paciente, con una carga mayor de riesgo atribuida al tipo 16. En cualquier caso, las graduaciones entre los riesgos se superponen, y si los costes lo permiten, parece deseable un examen para todo el grupo con el fin de conseguir una máxima sensibilidad, aunque una restricción a menos tipos aumentaría su especificidad.
De todas formas, no se conoce el grado analítico de sensibilidad que optimiza la efectividad del test de HPV. Los ensayos iniciales de HPV fueron poco sensibles y sólo identificaron algunos tipos.
En el estudio de Schiffman et al, con un punto de corte en 1,0 pg/ml mediante ensayos de segunda generación se consiguió una detección sensible de lesiones cervicales de alto grado y cáncer, consiguiendo un balance óptimo entre alta sensibilidad y una especificicdad razonable de este test. La prueba funcionará mejor en lugares donde es esencial la detección sensible de las lesiones de alto grado y del cáncer. Como la prevalencia de HPV varía según la población, el valor predictivo positivo del test de HPV para la detección de lesiones de alto grado y cáncer variará de forma acorde, con implicaciones para la utilidad en relación a otros métodos de cribado del cáncer cervical.
Un test de PHV autoaplicado que fuera preciso podría tener enormes implicaciones. Un test así abre la posibilidad de evaluar a mujeres que de otra manera no están dispuestas a someterse a exámenes pélvicos. No está claro si en las áreas subdesarrolladas esto ofrecería alguna ventaja respecto al control por parte de una enfermera formada que realice inspecciones visuales y test de HPV en la comunidad. En áreas donde se realiza un cribado organizado, la automuestra ofrece una vía adicional para alcanzar a mujeres que rechazan el cribado convencional y puede tener también un papel en la vigilancia o la monitorización después del tratamiento de mujeres positivas para HPV y citología negativa, en las que es preciso hacer tests de seguimiento a intervalos cortos. Sin embargo, esta teórica mayor aceptación y facilidad de uso podría tener también efectos negativos. Por ejemplo, algunas mujeres que previamente habrían pasado los exámenes rutinarios podrían ahora escoger un test casero menos sensible. Una prioridad clara es determinar las razones de la sensibilidad más baja y encontrar maneras de hacer un test autónomo tan bueno como el realizado por el clínico.
El hecho de situar el HPV en la cadena causal del cáncer cervical ha permitido una aproximación más racional al cribado para el cáncer cervical mediante el test de HPV. Para dilucidar si es factible y económicamente viable, y si a la larga se conseguirá disminuir el número de casos de cáncer cervical o la morbilidad y mortalidad por la enfermedad, serán necesarios más estudios para identificar y tratar de manera óptima a la población de mujeres con riesgo.
Existen suficientes evidencias que apoyan la efectividad del cribado del cáncer de cuello de útero. Esta evidencia procede de los cambios en la incidencia tras la introducción del cribado y de diferencias en incidencia entre las pacientes que han sido cribadas y las que no lo han sido dentro de una misma población.
El cribado cervical y el tratamiento de lesiones de alto grado detectadas no es perfecto, pero sí previene muchos cánceres que se habrían desarrollado en ausencia de la prueba.
Bibliografía recomendada
Anónimo. Cancer of the cervix: death by incompetence [editorial]. Lancet 1985; 2: 363-364.
Boletín Epidemiológico Semanal 1998; 6: 105-116.
Boletín Epidemiológico Semanal 1998; 6: 117-128.
Borràs JM Iglesias X. Cribado del cáncer de cuello de útero. Med Clin (Barc) 1994; 102 (Supl 1): 80-84.
Bulletin of the World Health Organization. Simpler screening for cervical cancer. WHO 1999; 77: 448.
Cuzick J. Human papillomavirus testing for primary cervical cancer screening. JAMA. 2000; 283: 108-109.
Harris R. What is the right cancer screening rate? An Intem Med 2000; 132: 732-734.
MacCormac L, Lew W, King G et al. Gynaecological cytology screening in South Australia: a 23.year experience. Med J Australia 1988; 149: 530-536.
Mateu JM. Cáncer de útero. Diagnóstico precoz del carcinoma cervical y endometrial. Barcelona: JIMS, 1982.
McIndoe WA, McLean MR, Jones RW et al. The invasive potential of carcinoma in situ of the cervix. Obstet Gynecol 1984; 64: 451-458.
Piédrola G, Del Rey J, Domínguez M et al. Medicina preventiva y salud pública. Barcelona: Masson-Salvat, 1991.
Plan de Salud de Cataluña 1999-2001. Barcelona: Generalitat de Catalunya, 2000.
Raffle E, Thomas J. How long will screening myths sunive? Lancet 1999; 354: 431-432.
Sackett D, Holland WW. Controvertsy in detection of disease. Lancet 1975; 2: 357-358.
Schiffman M, Herrero R, Hildesheim A et al. HPV DNA testing in cervical cancer screening: results from women in a high risk province of Costa Rica. JAMA 2000; 283: 87-93.
Skrabanek P. Cervical cancer screening. En: Luesley DM, Barrasso R, editores. Cancer and pre-cancer of the cervix. Londres: Chapman & Hall, 1998.
Wee C, McCarthy E, Davis R et al. Screening for cervical and breast cancer: is obesity an unrecognized barrier to preventive care? Ann Intern Med 2000; 132: 697-704.