El déficit agudo de oxígeno se manifiesta, fundamentalmente, por cambios a nivel de los aparatos cardiovascular, respiratorio y cerebral que pueden ir ligados a efectos funestos, especialmente si la situación desencadenante se prolonga de forma indefinida o persiste su gravedad. Es importante diferenciar los conceptos de hipoxemia e hipoxia; el primero indica que existe una disminución de la concentración de oxígeno en la sangre, mientras que el segundo hace referencia a la probreza a nivel tisular de dicho gas. Cabe, así, distinguir cuatro tipos de hipoxia: hipoxémica (la que deriva de una deficiente oxigenación de la sangre arterial manifestándose, por tanto, por una disminución de la presión parcial de oxígeno y de la saturación de la hemoglobina), anémica (cuando falla el transporte de oxígeno por la sangre al haber una alteración cuantitativa o cualitativa de la hemoglobina), circulatoria (consecuencia de la alteración en la perfusión tisular ya sea por una disminución del gasto cardíaco o por unaumento de las demandas tisulares) e histotóxica (cuando el transporte de oxígeno es normal, pero no puede ser liberado en los tejidos al verse interferido por determinados tóxicos como, por ejemplo, el ácido cianhídrico).
Por tanto, no nos podemos olvidar de que, a excepción de aquélla cuyo origen obedezca a una disminución de la concentración de oxígeno ambiental, en el resto de las causas de hipoxia aguda la oxigenoterapia no es más que una medida paliativa para mantener vivo al paciente en espera de que se consiga la corrección del factor etiológico que motivó dicha deuda de oxígeno.
Indicaciones y objetivo
Lo que se pretende con la oxigenoterapia es satisfacer las necesidades de oxígeno a los tejidos. Esta medida terapéutica se basa en aumentar la fracción inspirada de oxígeno (FiO2) y consecuentemente el contenido arterial de oxígeno (pO2, SaO2) para así mejorar el transporte de este gas y, en definitiva, evitar la hipoxia tisular.
Es importante recordar que el transporte de oxígeno está en función de tres factores, que son la saturación de oxígeno de la hemoglobina, la concentración de hemoglobina y el volumen minuto. Por tanto, las condiciones patológicas que los alteren serán, lógicamente, las indicaciones de oxigenoterapia:
1) Disminución de la saturación de oxígeno: insuficiencia respiratoria aguda.
2) Disminución de la hemoglobina: anemia severa.
En este apartado podemos incluir la intoxicación por monóxido de carbono, ya que la afinidad de este gas por la hemoglobina es muchísimo mayor que la del oxígeno, formándose así carboxihemoglobina. Por tanto, aunque en realidad no disminuye la hemoglobina, deja de estar disponible para el transporte de oxígeno.
3) Disminución del volumen minuto: insuficiencia cardíaca, shock.
4) Por último, en todo enfermo en situación crítica.
En la tabla 1 se detallan las situaciones clínicas que requieren oxigenoterapia.
¿Cuál es el objetivo de la oxigenoterapia urgente? Dependerá, evidentemente, de la patología a la que nos estemos enfrentando:
1) En la insuficiencia respiratoria aguda no hipercápnica será suficiente una pO2 >=60 (saturación >=90%), mientras que si se produce retención de carbónico nos conformaremos con una pO2 en torno a 55-60 mmHg (saturación: 85%-90%).
2) En la intoxicación de monóxido de carbono se pretende reducir a valores mínimos la carboxihemoglobina, por lo que se administrará la mayor concentración de oxígeno posible (lo ideal 100%), haciendo así que se desplace el monóxido de carbono al competir con él.
3) En el paciente crítico se administra oxígeno siempre, aunque la pO2 no esté en rango de insuficiencia respiratoria, pretendiendo que la saturación de la hemoglobina se acerque lo más próximo al 100% para compensar al máximo posibles deficiencias en las otras situaciones responsables del transporte de oxígeno, a saber: concentración de hemoglobina y volumen minuto.
Es importante tener en cuenta que el adecuado abastecimiento no sólo depende del transporte de oxígeno, sino que también se originarán problemas si hay un aumento de la demanda de dicho gas. Se entiende que cobran entonces importancia las estrategias que reducen el consumo de oxígeno. La causa más frecuente de consumo de oxígeno elevado que nosotros vemos, y además podemos tratar, es la fiebre, cosa que haremos siempre en todo paciente febril con insuficiencia respiratoria.
También debemos tener presente que la oxigenoterapia aguda contribuye a salir del paso ante una situación patológica, pero en la mayor parte de las veces no es un tratamiento curativo ni etiológico, sino una simple «muleta». En consecuencia, habrá que tratar el problema agudo de forma global: causa, repercusiones, etc.: «de poco sirve colocarle una mascarilla con oxígeno a un ahorcado si no se le afloja la cuerda».
Sistemas de administración de oxígeno
El criterio más utilizado para clasificar los sistemas de administración de oxígeno es la cantidad de flujo de la mezcla gaseosa que llega al paciente, y así se habla de sistemas de alto flujo y de bajo flujo. Pero, ¡atención!, el flujo al que nos referimos no es el marcado a la entrada del sistema en el caudalímetro de la pared o de la bombona, sino el que hay a la salida del sistema, delante de la vía aérea del enfermo.
Sistemas de bajo flujo
Se caracterizan porque el flujo de oxígeno que proporcionan es insuficiente para satisfacer los requerimientos inspiratorios del paciente, por lo que éste toma además aire ambiente. La cantidad de oxígeno que se mezcla con el aire es variable, ya que depende de varios factores: flujo de oxígeno, patrón respiratorio y características anatómicas del paciente, y tipo de dispositivo, esto explica que la FiO2 sea impredecible.
Los sistemas manejados habitualmente son las gafas nasales y las máscaras con reservorio.
Gafas nasales
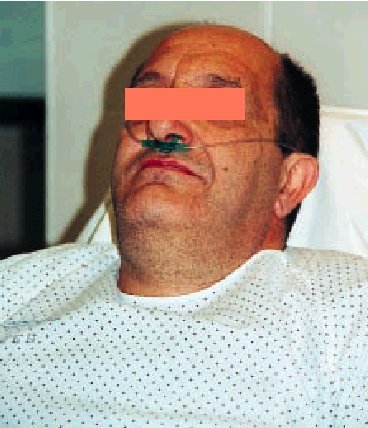
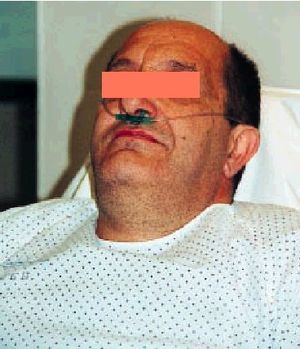
Es el sistema más barato y cómodo para el paciente (fig. 1): permite comer sin interrumpir el aporte de oxígeno, expectorar y hablar sin trabas, y quizá desempeñe un papel psicológico favorable en algunos casos al ser percibido su empleo como signo de menor gravedad. Por supuesto, el enfermo tiene que poder respirar por la nariz y tener en cuenta que la FiO2 será mayor cuando respira tranquilo que cuando hiperventila.
Fig. 1. Gafas nasales
Son el recurso ideal para aquellos enfermos con una buena respiración nasal y que no están en insuficiencia respiratoria (aguda) ni en estado crítico.
El enriquecimiento de oxígeno en el aire inspirado no sólo es debido al oxígeno proporcionado por el sistema durante el tiempo inspiratorio, sino también al relleno del reservorio nasofaríngeo natural durante la parte final del tiempo espiratorio. Por tanto, existen dos condi cionantes fundamentales de la FiO2, que son el tamaño de dicho reservorio y el patrón respiratorio del pacien-te, de tal manera que reservorios pequeños, volúmenes corrientes altos o frecuencias respiratorias altas disminuirán la FiO2 y viceversa. De ahí que esta variable sea impredecible, aunque, como norma general, por cada 1 l/m, aproximadamente, aumenta la concentración de oxígeno en un 4%. El flujo continuo administrado llena el reservorio natural, así con un flujo de 6 l/m dicho espacio está lleno y se consigue una FiO2 en la tráquea en torno a 0,35-0,45. Incrementos adicionales del flujo no conseguirán elevar la FiO2, ya que la capacidad del reservorio (que ya está lleno) permanece invariable. Por tanto, jamás administraremos oxígeno en gafas a flujos superiores a 6 l/m, pues el exceso «se lo lleva el viento» (nunca mejor dicho).
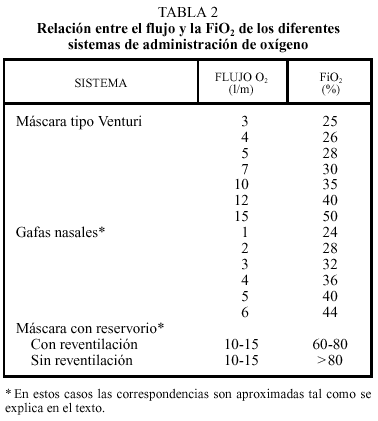
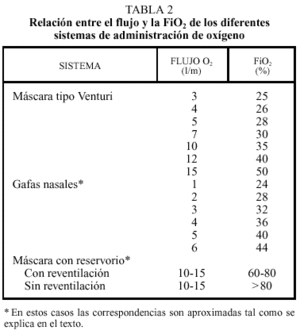
Modificando el flujo del caudalímetro, la FiO2 varía, de forma aproximada, tal como se muestra en la tabla 2.
Si se requiere una FiO2 mayor del 45% será necesario aumentar el tamaño del reservorio, y dado que la anatomía de cada paciente no se puede modificar, será necesario recurrir a otro tipo de aparato.
Mascarillas con reservorio
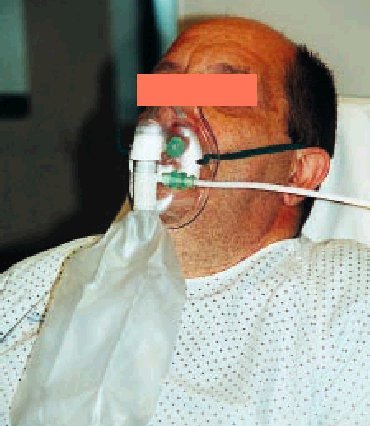
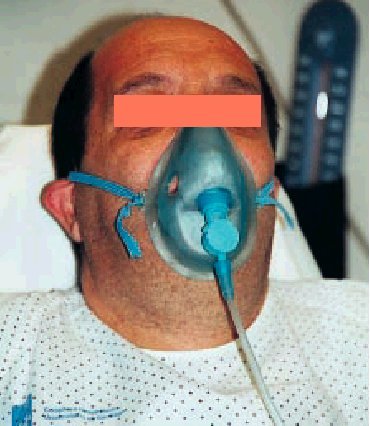
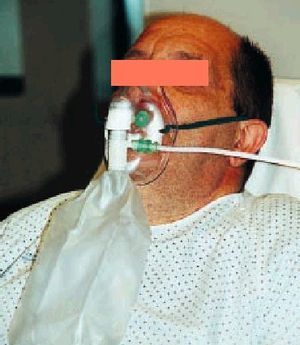
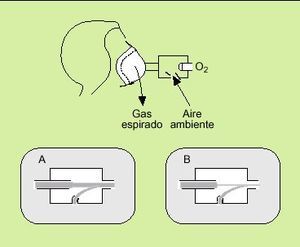
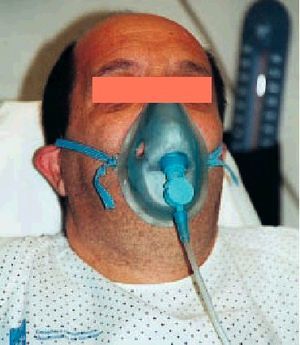
Se trata también de un sistema de bajo flujo, pero, a diferencia de las gafas nasales, de alta capacidad y con el que se pueden conseguir FiO2 muy altas, próximas al 90% en condiciones óptimas. ¿Qué quiere decir alta capacidad? Pues, en esencia, que se ha colocado un artilugio que aumenta la capacidad del reservorio natural y además con unos mecanismos sencillos que permiten esas FiO2 tan altas como al mismo tiempo desconocidas. Estos mecanismos son un reservorio (bolsa) de al menos 1 litro de capacidad situado entre la fuente de oxígeno y la mascarilla de la que está separada por una válvula unidireccional que impide la entrada del aire espirado y se abre al crearse durante la inspiración una presión negativa dentro de la mascarilla; ésta debe sellar perfectamente sobre la cara del paciente y tener también válvulas unidireccionales que impidan el fenómeno de rerrespiración y la entrada de aire ambiente durante la inspiración (fig. 2). Para impedir que la bolsa reservorio pueda llegar a vaciarse (lo que indicaría que no estamos satisfaciendo las necesidades ventilatorias del enfermo) debemos marcar unos flujos altos en el caudalímetro, al menos de 7-8 litros por minuto, de ahí que no tenga sentido utilizar en las mascarillas con reservorio flujos menores de dichas cantidades. En definitiva, la bolsa debe estar siempre llena (no colapsada).
Fig. 2. Mascarilla con reservorio.
Sus indicaciones fundamentales son la insuficiencia respiratoria grave y la intoxicación por monóxido de carbono. La causa más frecuente de fallo es el sellado imperfecto entre los bordes de la mascarilla y la cara del paciente; dado que éste se mueve, la mascarilla se desplaza, de ahí que el sellado deba comprobarse periódicamente. Otra causa frecuente de fallo es la pérdida de uno de los disquitos que hacen de válvula unidireccional en la mascarilla.
Sistemas de alto flujo
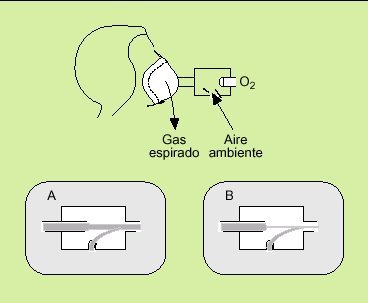
Las necesidades se logran mezclando aire y oxígeno mediante el efecto Venturi que se basa en el principio de Bernouilli: al pasar un flujo de oxígeno a gran velocidad por un orificio central arrastra gas ambiental por otro orificio al interior de la corriente tal como muestra la figura 3. Así, el flujo de salida será el resultado de la suma del marcado en el caudalímetro más el flujo de aire ambiente arrastrado por succión de los alrededores de la mascarilla.
Fig. 3. Efecto Venturi.
Los artilugios usados habitualmente como sistemas de alto flujo son las mascarillas tipo Venturi (fig. 4). La FiO2 que proporcionan será conocida, fija e independiente del patrón respiratorio del paciente. Es conocida porque nosotros mismos fijamos la cantidad que quere mos y es fija, ya que los flujos de la mezcla gaseosa que entran en la mascarilla son tan altos que es imposible que la mezcla sea «rebajada» por entrada de aire ambiente durante el tiempo inspiratorio a través de los orificios de la mascarilla (siempre está tan llena que le sobra, por muy difícil que lo ponga el patrón ventilatorio).
Fig. 4. Mascarilla tipo Venturi.
El oxígeno entra en la mascarilla a través de un orificio más estrecho, lo que crea un efecto Venturi que, merced a unas aperturas laterales en la conducción entre la zona de la estrechez y la mascarilla, arrastra aire ambiente hacia el interior de ésta; según el diámetro del orificio y el flujo de oxígeno procedente de la fuente varía la intensidad del efecto, de forma que para un orificio de un diámetro dado el efecto Venturi crece con el flujo hasta un punto a partir del cual se mantiene constante y, por tanto, con este orificio cuando usamos ese flujo crítico o más conseguimos un flujo mezcla final con una FiO2 constante. Las mascarillas que usamos tienen una ruedecilla en cuyo interior hay varios orificios que podemos seleccionar girándola y en el exterior tiene grabados los flujos mínimos que se deben marcar en el caudalímetro para conseguir la FiO2 deseada. Al final todo se reduce, una vez decidida la FiO2 que queremos administrar, a girar la ruedecilla y la llave del caudalímetro según las indicaciones grabadas en la mascarilla.
Se emplean en las insuficiencias respiratorias en que no estén indicadas por una u otra razón las gafas ni la mascarilla con reservorio, bien porque las gafas no consigan una FiO2 suficiente y continuada, bien porque el paciente no esté tan mal como para necesitar una mascarilla con reservorio o bien porque consideramos muy importante emplear una FiO2 ideal y mantenerla.
¿Cómo pautar la oxigenoterapia?
La FiO2 se selecciona por ensayo y error. Es decir, se inicia con la cantidad que creamos oportuna y al cabo de un tiempo comprobamos bien clínicamente, con gasometría o pulsioximetría que es eficaz. Para ello hay que tener en cuenta una serie de factores:
1) Edad. Hipoxemia no es sinónimo de insuficiencia respitatoria. Entre otras cosas hay que recordar que la pO2 cambia con la edad de tal manera que, por ejemplo, a los 80 años se considera que la pO2 normal es de 60 mmHg, valor evidentemente bajo para un paciente de 20 años.
2) Antecedentes. ¿Se trata de un paciente con enfermedad pulmonar obstructiva crónica (EPOC), cardiópata, anémico, etc.? ¿Necesita oxigenoterapia domiciliaria?
3) Esfuerzo respiratorio. Con dicho término se hace referencia a una serie de signos: frecuencia respiratoria, tiraje, pulso paradójico, dificultad para hablar, incoordinación toracoabdominal, aleteo nasal, uso de musculatura respiratoria accesoria, etc. Es corriente en el apartado de las historias clínicas correspondiente a la exploración física escribir «paciente disneico» sin hacer alusión a la descripción del esfuerzo respiratorio. Se
comete así un doble error al confundir el síntoma «disnea» con un signo y no precisar los signos que son justamente la expresión visible de ese síntoma. En definitiva, un enfermo que tiene una pO2 aceptable, pero su frecuencia respiratoria es de 40, con tiraje y es incapaz de decir su nombre, es un paciente que mantiene esa pO2 a costa de un tremendo esfuerzo respiratorio que probablemente no podrá mantener durante mucho tiempo, por lo que la oxigenoterapia en este caso debe ser agresiva.
4) Estado mental. Hemos de valorar el nivel de conciencia o si hay confusión o agitación y relacionarlos con la insuficiencia respiratoria o sepsis, lo que significaría estar ante un paciente grave.
5) Otros signos posibles de insuficiencia respiratoria. La cianosis, diaforesis (si no hay otras causas es un signo ominoso y amenazante de parada respiratoria), taquicardia, hipertensión, asterixis (que apunta a retención de CO2), etc.
6) Estado hemodinámico. Atendemos a la presión arterial, a la perfusión periférica, estado mental, etc. Si está comprometido: oxigenoterapia agresiva.
7) Anemia conocida o probable. Dado que es un problema añadido al transporte de oxígeno, además de pensar en la posibilidad de transfusión, inicialmente administramos oxígeno de forma agresiva.
8) Estado cardíaco. Si la causa de la insuficiencia respiratoria es un fallo cardíaco o aun sin ser la causa principal es coadyudante: oxigenoterapia agresiva.
9) Criterios de sepsis. Es necesario pre star especial atención a este estado clínico habida cuenta que muchas insuficiencias respiratorias son desencadenadas por infecciones bacterianas que pueden causar cuadros de sepsis graves y en cuyos casos la oxigenoterapia será agresiva una vez más.
Situaciones prototipo
Paciente «leve»
Consulta con mucha frecuencia y es importante identificarlo para no actuar en exceso en el plan diagnóstico ni en el terapéutico (oxigenoterapia incluida). Se trata de enfermos que no están en insuficiencia respiratoria y que no tienen criterios de gravedad, aunque consultan por disnea. En ellos, el oxígeno lo administramos en gafas nasales a dos o tres litros por minuto, caso de que nos decidamos a emplearlo.
Paciente «intermedio»
El que se halla en insuficiencia respiratoria o el que sin estarlo reúne criterios de gravedad. Utilizamos el oxí-geno por ventimask, ¿a qué FiO2?, por ensayo y comprobación con pulsioximetría de que la saturación de oxígeno está por encima del 90%. Si el enfermo tiene una pO2 menor de 50 y además otros signos de gravedad comenzamos por una FiO2 alta (mayor del 31%) y los ajustes posteriores se hacen a la baja si se puede; si la situación no fuera ésta empezaremos con una FiO2 de 26%-28% y después ajustamos a la alta si es necesario.
Paciente «grave»
Aquel que pese a la oxigenoterapia con FiO2 del 50% no llega o incluso ni se aproxima a una saturación del 90%. Recurrimos entonces a la mascarilla con reservorio y debe tenerse en cuenta la posibilidad de que próximamente necesite medidas más agresivas como la intubación endotraqueal.
Paciente retenedor de CO2
Caben dos posibilidades :
1) Retención aguda sin retención crónica, lo que comprobamos por la ausencia de compensación metabólica de la acidosis; el centro respiratorio de estos pacientes responde de igual manera que el de cualquier otra persona a los mismos estímulos. Las causas más frecuentes de este estado son la crisis grave de asma y el edema agudo de pulmón. Son enfermos que requieren oxígeno administrado a la mayor concentración posible bien con ventimask al 50% o mascarilla con reservorio.
2) Agudización real o presunta de la insuficiencia respiratoria de un paciente retenedor crónico de CO2. La batalla a propósito de la oxigenoterapia en estos enfermos es la posibilidad de deprimir el centro respiratorio al administrar oxígeno, dado que se entiende que el déficit de este gas se ha convertido en ellos en el principal estímulo del centro respiratorio y su administración puede deprimirlo y causar hipoventilación; en espera de que «los científicos se pongan de acuerdo», debemos tener presentes dos cosas: a la hora de tratar siempre prima la hipoxemia (que es de lo que se mueren), y si «el caso no está muy bravo» administraremos el oxígeno «suavecito» (saturación en torno al 90%), con lo que no causaremos mayores problemas. Por «suavecito» entendemos mascarilla Venturi al 24%; no debemos usar gafas nasales a bajo flujo en esta situación, ya que frecuentemente se consiguen FiO2 más altas y no desadas. No obstante, hay que insistir en que nunca estará justificada una deficiente oxigenación por el peligro de provocar una mayor retención de CO2. En la valoración inicial y seguimiento de estos pacientes ocupa un lugar principal el examen del nivel de conciencia.
Efectos secundarios de la administración de oxígeno
En función del tiempo que tardan en aparecer se clasifican en precoces y tardíos. Un caso especial que no procede en el comentario pormenorizado en este trabajo son los cuadros clínicos asociados a la toxicidad del oxígeno en los neonatos.
Precoces
Dentro de los efectos secundarios precoces están los siguientes:
Hipercapnia. Como ya vimos antes, ocurre en algunos enfermos que ya son retenedores crónicos de CO2 cuando se administra oxígeno a altas dosis, ya que se atenúa el estímulo que éste ejerce sobre el centro respiratorio.
Atelectasias. La administración de oxígeno a altas concentraciones (superiores al 80%) durante más de 24 horas provoca desnitrogenación de los alvéolos, que puede originar colapsos en los mismos por disminución de volumen.
Tardíos
La hiperoxia mantenida produce aumento de los radicales libres y ello conlleva toxicidad pulmonar.
Contraindicaciones
En la intoxicación por paraquat la administración de oxígeno produce radicales libres, por lo que este gas se comporta como un sustrato del tóxico. Ocurren efectos similares con otras sustancias como la bleomicina, la ciclofosfamida, el ozono y el óxido nitroso, por ello en ausencia de hipoxia demostrada la oxigenoterapia está contraindicada en este grupo de intoxicaciones.
Control de la eficacia de la oxigenoterapia
Lo que pretendemos es saber si estamos logrando lo que nos proponemos o no, por lo que, en definitiva, el control de la eficacia nos permitirá adoptar dos tipos de decisiones: ajuste preciso de la dosis (FiO2) dependiendo del objetivo propuesto (recordar que para decidir la saturación de oxígeno necesaria nos basamos en el «ensayo y error») y valoración de la necesidad de medidas más agresivas.
Para esta verificación nos basaremos en:
La clínica
Indudablemente el control clínico es de un valor inestimable y es el que más rápidamente nos dará información: ¿han mejorado los signos y síntomas que estimamos que son causados por la hipoxemia? Aunque su eficacia está limitada por ser totalmente dependiente del observador, está claro que es esta valoración clínica de la respuesta a la oxigenoterapia la primera que tendremos en cuenta e incluso la última hasta la fecha si trabajamos en el medio extrahospitalario.
Gasometría arterial
Es indispensable en el paciente crítico o con insuficiencia respiratoria grave que retiene CO2 y muchas veces en los servicios de urgencias constituye la indicación objetiva de ingreso o de alta (en este último caso cuando los valores de la pO2 sean aceptables tras haber estado cierto tiempo sin oxígeno suplementario). Es muy precisa y aporta información fidedigna acerca del estado de oxigenación y equilibrio ácido-base. Los principales inconvenientes radican en ser invasiva y, además, no proporcionar información continua. Por otra parte, es una técnica no disponible en los servicios de urgencias extrahospitalarios.
Pulsioximetría
En buena medida ha sido un recurso que en los últimos años ha revolucionado esta cuestión. La pulsioximetría se basa en el principio de Beer-Lambert, según el cual podemos conocer la concentración de un soluto que absorbe selectivamente luz de una determinada longitud de onda cuando esa luz atraviesa la solución. En el caso que nos ocupa usamos generalmente un dedil que en una de sus caras internas tiene un diodo emisor de luz roja e infrarroja; la luz roja es absorbida selectivamente por la hemoglobina reducida y la infrarroja por la oxihemoglobina. En la cara opuesta hay un sensor para las dos longitudes de onda y que se estimula más o menos según la cantidad de radiación que le llega. Es evidente que si el dedo no sufriera variación alguna en composición, grosor, etc., la cantidad de luz absorbida sería constante y no tendría utilidad, lo que se la da es la variación del «grosor» del dedo con cada onda de pulso y es justamente la oxigenación de la sangre arterializada, que con cada onda de pulso engorda el dedo, la que nosotros queremos conocer. Así, con cada onda de pulso una cantidad variable de radiación roja e infrarroja no llegará al sensor, lo que es expresión de la concentración de hemoglobina reducida y oxihemoglobina en la sangre arterial que ha llegado al dedo. Finalmente el pulsioxímetro elabora los datos y ofrece una cifra de saturación de oxígeno funcional que es el resultado del cociente entre la oxihemoglobina y la suma de ésta con la hemoglobina reducida.
La mayoría de estos aparatos también muestran en la pantalla la frecuencia cardíaca y una onda de pulso que no es sino el resultado de una elaboración de las variaciones de la radiación absorbida.
Se trata de un recurso para valorar la oxigenación que es objetivo, incruento, continuo, barato y portátil. Estamos absolutamente convencidos de que debe formar parte del utillaje tecnológico de todo centro de salud, servicio de urgencias o sistemas de transporte urgente de pacientes.
Su única limitación consiste en no proporcionar información alguna sobre la pCO2.
Bibliografía recomendada
Alía I, Esteban A. Oxigenoterapia. En: De Latorre FJ, ed. Medicina crítica práctica. ABC de la insuficiencia respiratoria. Barcelona: Edika Med, 1995; 39-52.
Baker WE, Lanoix R, Field DL, Hedges JR. Noninvasive assessment and support of oxygenation and ventilation. En: Roberts/Hedges, ed. Clinical procedures in emergency medicine (3.a ed). Philadelphia: Saunders Company, 1998; 82-107.
Casanova C, Hernández MC, Medina A, Acosta O. Oxigenoterapia. En: Caminero JA, Fernández L, eds. Manual de neumología y cirugía torácica. Volumen 1. SEPAR. Madrid: Editores Médicos, 1998; 567-577.
Herrera M, Mora D. Oxigenoterapia. En: Montejo JC, García A, Ortiz C, Planas M, eds. Manual de medicina intensiva. Madrid: Mosby/ Doyma, 1996; 10-13.
Mora D, Herrera M. Insuficiencia respiratoria aguda. En: Herrera M, ed. Medicina crítica práctica. Iniciación a la ventilación mecánica. Puntos clave. Barcelona: Edika Med, 1997; 105-118.
Muriel C. Liberación y protección de la vía aérea. Oxigenación. En: Muriel C, eds. Emergencias médicas. Madrid: ELA, 1992; 388-390.
Serrano A. Exploración clínica del aparato respiratorio. Oxigenación y valoración de la ventilación. Técnicas y procedimientos empleados en la urgencia respiratoria pediátrica. En: Casado J, Serrano A, eds. Urgencias y transporte del niño grave. Madrid: Ergon, 1997; 33-44.