El nódulo pulmonar solitario (NPS) es una entidad que cada vez se observa con más frecuencia en la práctica clínica habitual. En Estados Unidos se diagnostican unos 150.000 nuevos casos de nódulos pulmonares al año, estimándose en 0,2% la prevalencia de esta entidad en la población general; esta proporción llega hasta un 2% en la población seguida de manera habitual en una consulta externa de neumología. El nódulo pulmonar solitario se define como la presencia de una sombra radiográfica de no más de 3 cm en su diámetro mayor, siendo la lesión bien definida necesariamente, con cualquier forma o contorno, mostrando calcificación o no, con o sin cavitación, acompañándose en ocasiones de lesiones satélites y estando el nódulo o bien rodeado de pulmón aireado o bien, si está adyacente a la pleura visceral, al menos dos tercios de su circunferencia se muestran contiguos a pulmón aireado.
El 60-65% de todos los nódulos pulmonares solitarios son benignos, aumentando hasta un 90% la proporción de benignidad en determinadas zonas endémicas para determinadas infecciones, como la tuberculosis o determinadas infecciones fúngicas.
Etiología
La etiología es variada (tabla 1), y la causa más frecuente de NPS benignos la constituyen los granulomas, que representan hasta un 40% de todos los nódulos pulmonares solitarios. El cáncer es la segunda causa de NPS, aunque para algunos autores es la primera, con hasta un 44% del total, iniciándose el 25% de todos los carcinomas broncogénicos como NPS y siendo el adenocarcinoma el tipo histológico que tiene habitualmente esta forma de presentación.
Los hamartomas suponen la tercera causa global de NPS, representando entidades en principio benignas pero que, dada la posibilidad de malignización descrita en algunas series, es conveniente adoptar actitudes diagnósticas y terapéuticas agresivas.
Se han descrito hasta 80 entidades nosológicas responsables de NPS (tabla 2), y las causas infecciosas y neoplásicas son las más habitualmente descritas, aunque, como veremos, existen muchos tipos diferentes que deben tenerse en cuenta en la práctica clínica.
Procesos infecciosos
En cuanto a la presencia de procesos infecciosos responsables de nódulos pulmonares solitarios, en zonas endémicas debe tenerse en cuenta en primer lugar la presencia de infección por Mycobacterium tuberculosis, que es relativamente común y afecta con mayor frecuencia a los lóbulos superiores, más el derecho que el izquierdo, con un 25% de casos en donde aparecen lesiones lobuladas con calcificación frecuente y con rara cavitación. Las lesiones satélites pueden aparecer en hasta un 80% de los casos, produciéndose a veces en el bronquio de drenaje un engrosamiento irregular y, en ocasiones, broncostenosis.
Con bastante menos frecuencia se describe la presencia de NPS debidos a otras micobacterias que, a pesar de ser atípicas, deben tenerse en cuenta y proceder a su identificación por parte del laboratorio de microbiología.
En zonas endémicas como la que nos ocupa es importante también, dentro del contexto epidemiológico adecuado, valorar la posibilidad de infección por Brucella, que puede producir NPS en cualquier localización; la presencia de cavitación es muy rara, pero no la de calcificación.
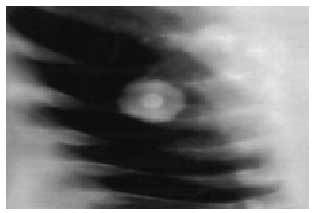
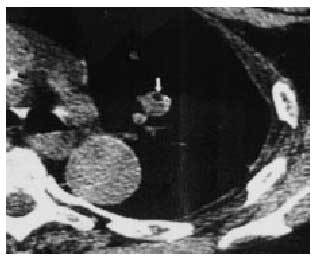
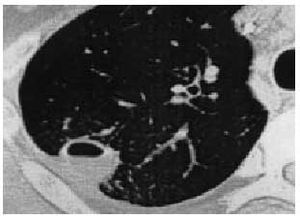
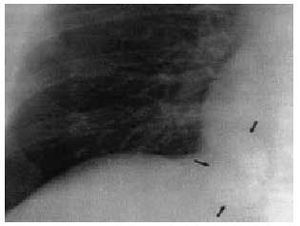
La presencia de infección por Histoplasma capsulatum (fig. 1) es más común en zonas endémicas y aparece con más frecuencia en los lóbulos inferiores; suele ser redonda u ovalada, bien circunscrita, con la zona central con aspecto de diana; la cavitación es rara, con presencia de lesiones satélites comunes que pueden ser múltiples y asocian de manera habitual la calcificación con los ganglios hiliares.
Fig. 1. Nódulo pulmonar solitario por Hystoplasma capsulatum.
Coccidioides immitis no suele presentarse como un NPS, y aparece por lo general en el lóbulo superior, con nódulos bien redondeados u ovalados con calcificación en algún caso, cavitación común; las paredes del nódulo son más gruesas que delgadas.
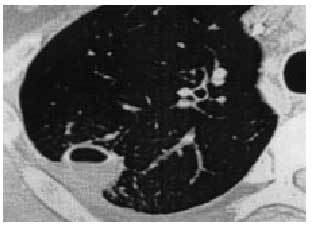
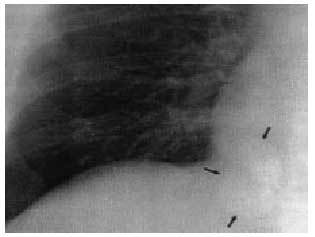
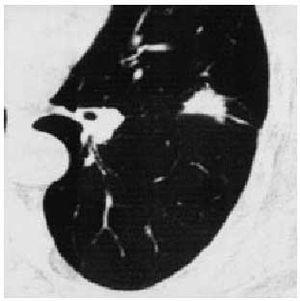
Aspergillus (fig. 2) puede producir imágenes compatibles con NPS en aquellos individuos en los que se produce un impacto mucoide, aunque es poco común, y básicamente se asocia a la producción de broncospasmo; se localiza en el lóbulo superior y adopta una imagen en forma de dedo, Y o V, sin calcificación, aunque en ocasiones aparecen niveles hidroaéreos que simulan cavitación, e incluso a veces se produce la atelectasia del segmento afectado. Mucho más rara es la producción de un micetoma que, cuando aparece, se localiza por regla general en el lóbulo superior, de forma redonda u ovalada sin calcificar y con cavitación siempre dentro de la cavidad, que adopta en ocasiones la forma de una bola micótica intracavitaria.
Fig 2. Aspergillus como causa de nódulo pulmonar solitario.
En cuanto a los diferentes parásitos responsables de la producción de NPS podemos destacar Equinococcus granuloso que aparece en áreas endémicas, en el lóbulo inferior, más en el derecho que en el izquierdo, con imágenes circunscritas y claras con calcificación muy rara y cavitación común.
Dilofilaria immitis es muy rara, no presenta predilección por uno u otro lóbulo y aparece con ausencia de calcificación y a veces de cavitación; en ocasiones puede simular un infarto pulmonar.
Neoplasias
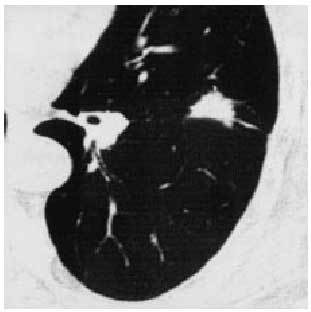
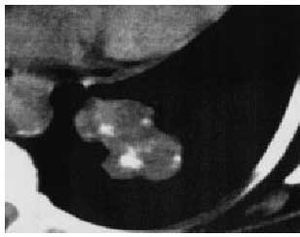
Los procesos neoplásicos (fig. 3) son, para algunos autores, la primera causa de NPS, y este matiz constituye un importante factor a tener en cuenta, dado que va a condicionar un cambio en la actitud de «esperar y ver» que hasta ahora se venía adoptando, pasando a una actitud diagnóstica y terapéutica más agresiva. Así, en la actualidad se considera maligno todo nódulo pulmonar solitario de menos de 3 cm, dada la prevalencia en el carcinoma pulmonar, mientras no se demuestre lo contrario. Ello comporta agresividad a la hora de las exploraciones diagnósticas.
Fig. 3. Neoplasia pulmonar.
La localización en estos casos de NPS por neoplasia pulmonar es básicamente los lóbulos superiores, con presencia de márgenes muy mal definidos, lobulados y umbilicados, con calcificación muy rara, cavitación del 2 al 10% y presencia de lesiones satélite poco comunes.
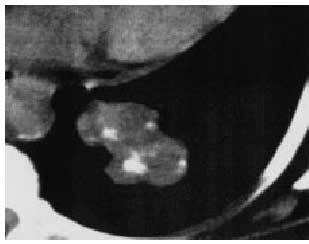
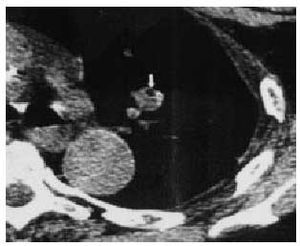
El tumor carcinoide (fig. 4) tiene una incidencia de 1 a 50 con respecto al carcinoma pulmonar como responsable de NPS, presentándose el 20-25% de los tumores carcinoides como NPS; afecta básicamente al lóbulo superior y medio con imágenes redondeadas que se van a cavitar del 2 al 10%, y el 80% restante empieza como atelectasia o neumonitis obstructiva del segmento afectado.
Fig. 4. Tumor carcinoide.
Tumores benignos
El hamartoma (fig. 5) es para algunos autores la tercera causa global de NPS, representando hasta un 5% de todos los nódulos. Por definición es considerado benigno, pero dado que está constituido por una mezcla heterogénea de los diferentes tejidos que habitualmente constituyen el pulmón, en la bibliografía se ha descrito en alguna ocasión malignización del epitelio celómico que separa los diferentes tejidos constitutivos del hamartoma. No muestra predilección lobular, con imagen bien definida más lobulada que lisa, sin cavitación, y es muy frecuente, aunque menos de lo que inicialmente se pensaba y sólo en una cuarte parte de los casos.
Fig. 5. Hamartoma pulmonar.
Existen otros tumores con diferente histología que pueden producir nódulos pulmonares solitarios, y así se describen tumores derivados de tejido muscular, cartilaginoso, celómico y neural, todos ellos muy raros, con forma generalmente bien definida, que rara vez se calcifican y no se cavitan, sin localización definida y, por regla general, de características benignas, siendo muy rara la obstrucción bronquial o la atelectasia.
Existen también casos de metástasis solitarias de tumores primarios desconocidos que comienzan como NPS desde cualquier lugar de la economía, representando del 3 al 5% de todos los nódulos pulmonares; aparecen con más frecuencia en los lóbulos pulmonares inferiores, son de aspecto liso o lobulado bien definido y la calcificación es rara, en ocasiones hay cavitación, y hasta en un 25% de los casos en los que se encuentran alcanzan metástasis pulmonares solitarias. Según la histología del tumor originario hay un mayor grado de malignidad en las imágenes nodulares solitarias, alcanzando hasta un 90% de malignidad en los casos de NPS por melanoma y hasta un 60-70% de malignidad en los casos donde el tumor primario sea el de colon.
Procesos autoinmunes
En cuanto a las causas inmunológicas responsables de NPS, se puede describir la granulomatosis de Wegener. Su frecuencia es muy baja, con imagen bien definida, sin calcificación, cavitándose en un tercio o la mitad de los casos y apareciendo en forma de nódulos pulmonares múltiples con más frecuencia que solitarios que no pasan del 4 al 20% de los casos. Entre las causas inmunológicas también se describe el nódulo reumatoideo, que es muy raro y se localiza habitualmente en una zona subpleural periférica bien definida; es de aspecto liso, sin calcificación y con cavitación común, aunque por regla general suele aparecer de forma múltiple y no en solitario, asociado a derrame pleural, eosinofilia, y con mayor evidencia en aquellos casos en que la artritis reumatoide se asocia a mayor actividad.
Linfomas
Los linfomas son muy raros, pero también es preciso tenerlos en cuenta en el diagnóstico diferencial. La posibilidad de que los nódulos pulmonares sean producidos por linfoma del tipo no hodgkiniano y por el mieloma múltiple es muy rara, y no presentan predilección en cuanto a los lóbulos pulmonares.
Miscelánea
En el contexto de traumatismo pulmonar se describe también la presencia de hematomas pulmonares responsables de NPS; son muy poco comunes y suelen adoptar una disposición subpleural periférica.
Es preciso considerar causas metabólicas, entre las que se considerará la amiloidosis broncopulmonar, que es muy rara, lógicamente dentro del contexto clínico típico y sin predilección en cuanto a la localización pulmonar.
Asimismo se describe una serie de entidades, como el quiste bronquial pulmonar, que aparece en la tercera década de la vida, sobre todo en varones judíos, y se localiza en el tercio medial del lóbulo inferior; su aspecto es redondeado, liso y bien definido, con presencia muy rara vez de calcio en la pared, aunque sí en el quiste, con frecuencia cavitado y con aspecto de lesión homogénea hasta que se establece contacto con el pulmón contiguo por infección.
La fístula arteriovenosa pulmonar (fig. 6) aparece en dos tercios de los casos en forma de lesiones únicas, más en lóbulos inferiores, con aspecto bien definido y redondeado; no se cavita y a veces se calcifica, y se encuentra en el 40 al 60% de los enfermos con diagnóstico de telangiectasia hemorrágica hereditaria.
Fig. 6. Fístula arteriovenosa responsable de nódulo pulmonar solitario.
La varicosidad de una vena pulmonar es una entidad muy rara que aparece en el tercio medial del pulmón, sin cavitación ni calcificación, con presencia de cambio de tamaño con la maniobra de Valsalva; la arteriografía confirma el diagnóstico diferencial con la fístula arteriovenosa.
La atresia bronquial congénita con impacto mucoide es muy rara y aparece en el bronquio apicoposterior del lóbulo pulmonar superior izquierdo, sin cavitación ni calcificación; es muy típica la presencia de moco dentro del bronquio con parénquima distal a la oclusión sobreinsuflado por desplazamiento de aire colateral.
Evaluación diagnóstica
Ante un nódulo pulmonar solitario es preciso efectuar una historia clínica y un examen físico rigurosos, incluyendo antecedentes de tuberculosis, posibilidad epidemiológica en cuanto a la posibilidad de determinadas infecciones fúngicas, exposición a riesgos laborales, presencia o no de hábito tabáquico y coexistencia de determinadas infecciones sistémicas.
Las pruebas de laboratorio consisten en efectuar una citología seriada de esputo, indicada sobre todo en la evaluación de lesiones grandes de localización central y que resulta muy poco útil en lesiones periféricas y pequeñas, ya que presentan hasta un 80% de falsos negativos. También es obligatorio efectuar la prueba de la tuberculina para descartar una exposición previa a tuberculosis.
La radiografía de tórax es la prueba que permite descubrir los NPS en la mayor parte de los casos, y es muy importante comparar con radiografías previas, puesto que la falta de crecimiento de un NPS en dos años es un claro indicador de benignidad.
La tomografía computarizada torácica, sobre todo si es de alta resolución, puede proporcionar de 10 a 20 veces más información que una radiografía convencional sobre el patrón de calcificación, las características del nódulo, la presencia de nódulos adicionales así como de la presencia de grasa, prácticamente diagnóstica de hamartoma.
La tomografía de emisión de positrones tiene una sensibilidad del 80-90%, pero su poca especificidad para lesiones malignas muestra una elevada proporción de falsos positivos en los procesos inflamatorios pulmonares y su elevado coste hacen que sea poco utilizada en la actualidad.
Las técnicas invasivas están indicadas cuando, tras realizar las pruebas indicadas hasta ahora, el diagnóstico permanezca sin definirse, y se puede recurrir a la fibrobroncoscopia, que va a mostrar poca sensibilidad para lesiones menores de 2 cm. La punción-aspiración con aguja fina puede diagnosticar hasta un 50-60% de NPS, pero presenta un elevado riesgo de iatrogenia y no es infrecuente la aparición de neumótorax y, en grado variable según las series descritas, la presencia de muestra insuficiente en hasta un 18-20% de casos. La toracotomía y resección del nódulo será necesaria si todavía no se ha establecido el diagnóstico. Últimamente se ha descrito la posibilidad de realizar minitoracoscopia, que presenta menor morbilidad y que, acompañada por determinadas técnicas tinción con metileno, utilización del arpón guiado por tomografía computarizada y en manos de cirujanos expertos, va a permitir el diagnóstico en aproximadamente el 90-92% de los NPS.
Actitud ante un nódulo pulmonar solitario
Ante pacientes con riesgo bajo de malignización, menores de 35 años, no fumadores y sobre todo con ausencia de crecimiento de la lesión en dos años o la presencia de un patrón de calcificación benigno, entendiendo como tal la presencia de una calcificación homogénea, concéntrica, en láminas o en forma de palomitas de maíz, la actitud adoptada por la mayor parte de los autores es la vigilancia expectante.
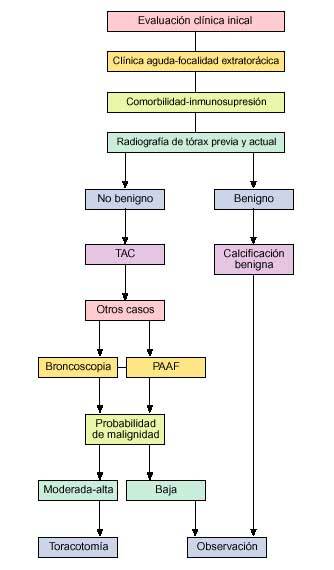
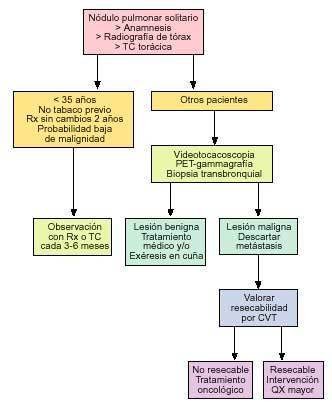
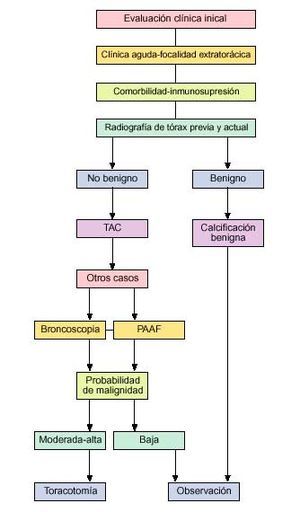
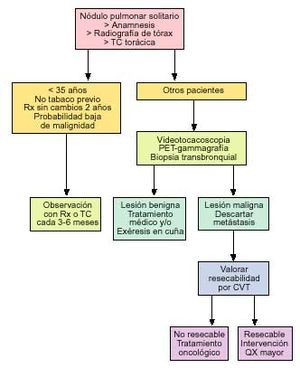
Por el contrario, un paciente fumador, mayor de 35 años, con tiempo de duplicación del nódulo pulmonar entre 30 y 400 días, con ausencia de calcificación o con calcificación no sugerente de benignidad, se precisan técnicas de diagnóstico más agresivas, recomendándose efectuar un algoritmo diagnóstico (figs. 7 y 8).
Fig. 7. Algoritmo diagnóstico hasta el desarrollo de la videotoracoscopia.
Fig. 8. Algoritmo diagnóstico tras videotoracoscopia.
En cualquier caso, como ya se ha comentado anteriormente, en el momento actual, y dada la gran prevalencia que muestra el carcinoma pulmonar, se ha pasado de la actitud de esperar y ver a una actitud que en principio considera a todo NPS de más de 2 cm como un carcinoma pulmonar, por lo que, en la medida de lo posible, se debe conseguir una anatomía patológica.
En la actualidad existe una serie de calculadores bayesianos para el cálculo de la probabilidad de malignización de un determinado NPS, los cuales tienen en cuenta diversos factores (tabla 3), aunque no dejan de ser modelos matemáticos. Por ello, en la práctica clínica habitual es preciso efectuar una individualización de las actitudes diagnósticas, valorando los pros y los contras.
Bibliografía general
Casali C, Stefani A, Paci M, Morandi U, Lodi R. Surgical management of solitary pulmonary nodules. An unexpected lucky case. J Cardiovasc Surg 2001;42:271-3.
Congregado Loscertales M, Girón Arjona JC, Jiménez Merchán R, Arroyo Tristán A, Arenas Linares C, Ayarra Jarne J, et al. Utilidad de la cirugía videotoracoscópica en el diagnóstico de los nódulos pulmonares solitarios. Arch Bronconeumol 2002;38:415-20.
Erasmus JJ, Connolly JE, McAdams, HP, Roggli, VL. Solitary pulmonary nodules. Part I. Morphologic evaluation for differentiation of benign and malignant lesions. Radiographics 2000;20:43-58.
Erasmus JJ, McAdams HP. Solitary pulmonary nodules. Part II. Evaluation of the indeterminate nodule. Radiographics 2000; 20:59-66.
Gjevre JA, Myers JL, Prakasch UB. Pulmonary hamartomas. Mayo Clin Proc 1996;71:14-20.
Gurney JW, Lidon DM, Mckay JA. Determining the likelihood of malignancy in solitary pulmonary nodules with Bayesian analysis. Part II. Application. Radiology 1993;186:415-22.
Higgashita R, Ichikawa S, Ban T, Suda Y, Hayasshi K, Takeuchi Y. Coexistence of lung cancer and hamartoma. Jpn J Thorac Cardiovasc Surg 2001;49:258-60.
Jaurena Churi J, Varela Ugarte A, González Hernando C, Ramos Martínez A, Martín Jiménez T, Portero Navío L, et al. Nódulo pulmonar solitario: aplicación del teorema de Bayes en la predicción de malignidad. Arch Bronconeumol 1998;34:4-8.
Jurado B, Díaz F, Ysamat R. Manejo del nódulo pulmonar solitario. Rev Clin Esp 1998;198(1):44-7.
Khouri NF, Meziane MA, Zerhouni EA, Fishmann EK, Siegelman SS. The solitary pulmonary nodule. Chest 1987;91:128-33.
Lillington GA, Caskey CI. Evaluation and management of solitary multiple pulmonary nodules. Clin Chest Med 1993;14:111-9.
López Serrano B, Zufia García J. Estudio del nódulo pulmonar solitario. Jano, Medicina y Humanidades 2001;61:51-2.
Midthun DE, Swensen SJ, Jett JR. Approach to the solitary pulmonary nodule Mayo Clin Proc 1993;68:378-85.
Sánchez Martín E, Fernández Peláez JM, Vila Meiroso B, Martín Doimeadios P, Sobrino Hernández M, Saez Méndez L. Masa pulmonar asintomática. Rev Clin Esp 1999;199(8):535-6.