La enfermedad de Erdheim-Chester (EEC) es una forma rara de histiocitosis no-Langerhans, que cursa con una infiltración xantogranulomatosa multiorgánica por histiocitos CD68+/CD1−. Dos signos altamente sugestivos de esta enfermedad son la esclerosis corticomedular de huesos largos y la infiltración de la grasa perirrenal1. La afectación del sistema nervioso central (SNC) sucede en el 30-50% de los casos y constituye el principal factor de mal pronóstico1,2. Se ha propuesto como tratamiento de primera línea el interferón α a dosis elevadas cuando hay afectación del SNC3,4. Otras alternativas terapéuticas se basan en la publicación de casos aislados en los que se ha obtenido respuesta con fármacos inmunomoduladores como imatinib5 (potente inhibidor de tirosin cinasas) y anakinra6 (forma recombinante del antagonista del receptor de la interleucina-1), o con inmunosupresores como cladribina7. Recientemente, el vemurafenib (potente inhibidor del gen BRAF) ha demostrado eficacia en pacientes refractarios portadores de la mutación V600E del gen BRAF8.
Se presentan 2 pacientes con EEC con afectación neurológica y se describen las manifestaciones clínicas y de neuroimagen, así como, la evolución de la enfermedad con los distintos tratamientos empleados.
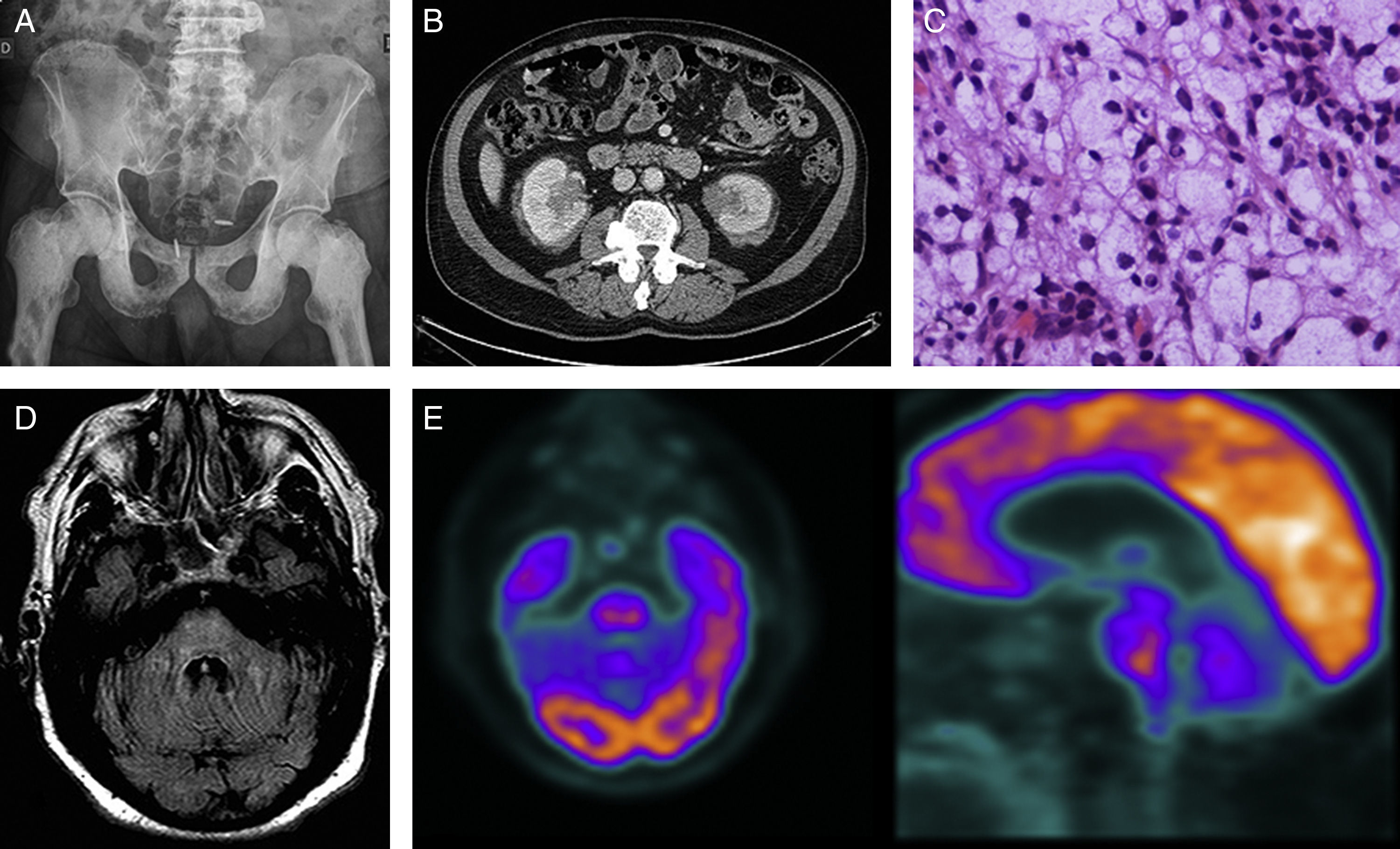
Caso 1Varón de 68 años con antecedentes de cardiopatía isquémica y un carcinoma de próstata tratado en el 2008. Ingresó en junio del 2011 por unas lesiones óseas osteoescleróticas de 5 años de evolución con biopsia inicial no diagnóstica (fig. 1A). Presentaba disartria e inestabilidad progresivas de varios meses de evolución. Se observó un síndrome pancerebeloso siendo el resto de la exploración normal. VSG de 56mm. Resto de los parámetros analíticos sanguíneos y LCR normales. En la RM cerebral se objetivó una alteración de señal en la protuberancia interpretada como de probable naturaleza gliótica-isquémica residual. En la TAC-body se observó una masa infiltrativa perirrenal bilateral (fig. 1B) cuya biopsia mostró un infiltrado histiocitario (fig. 1C) con inmunohistoquímica positiva para CD68 y negativa para CD1a y S100; hallazgos compatibles con una EEC. El paciente recibió tratamiento con prednisona (1mg/kg/d) e interferón α (3-6 millones sc/d, 3 veces por semana). A los 6 meses se retiró el tratamiento por progresión de la clínica neurológica con agravamiento del síndrome cerebeloso hasta impedirle la deambulación y aparición de signos piramidales y alteraciones de conducta (fig. 1D y E). Los tratamientos con imatinib (400mg/d) y cladribina fueron ineficaces. Es portador de la mutación V600 del gen BRAFF, por lo que se inicia hace 2 meses tratamiento con vemurafenib sin cambios clínicos.
A) Rx simple de pelvis: osteosclerosis diáfiso-epifisario de ambos fémures y pubis. B) TAC abdominal: masa hipercaptante infiltrativa perirrenal. C) Tinción hematoxilina-eosina: infiltrado histiocitario con citoplasma amplio claro espumoso. D) RM cerebral, FLAIR axial: a los 9 meses: alteración de señal en la protuberancia que se insinúa hacia los pedúnculos cerebelosos medios. E) PET-TC con 18F-FDG: imagen anular en la protuberancia con centro hipometabólico y moderada actividad periférica.
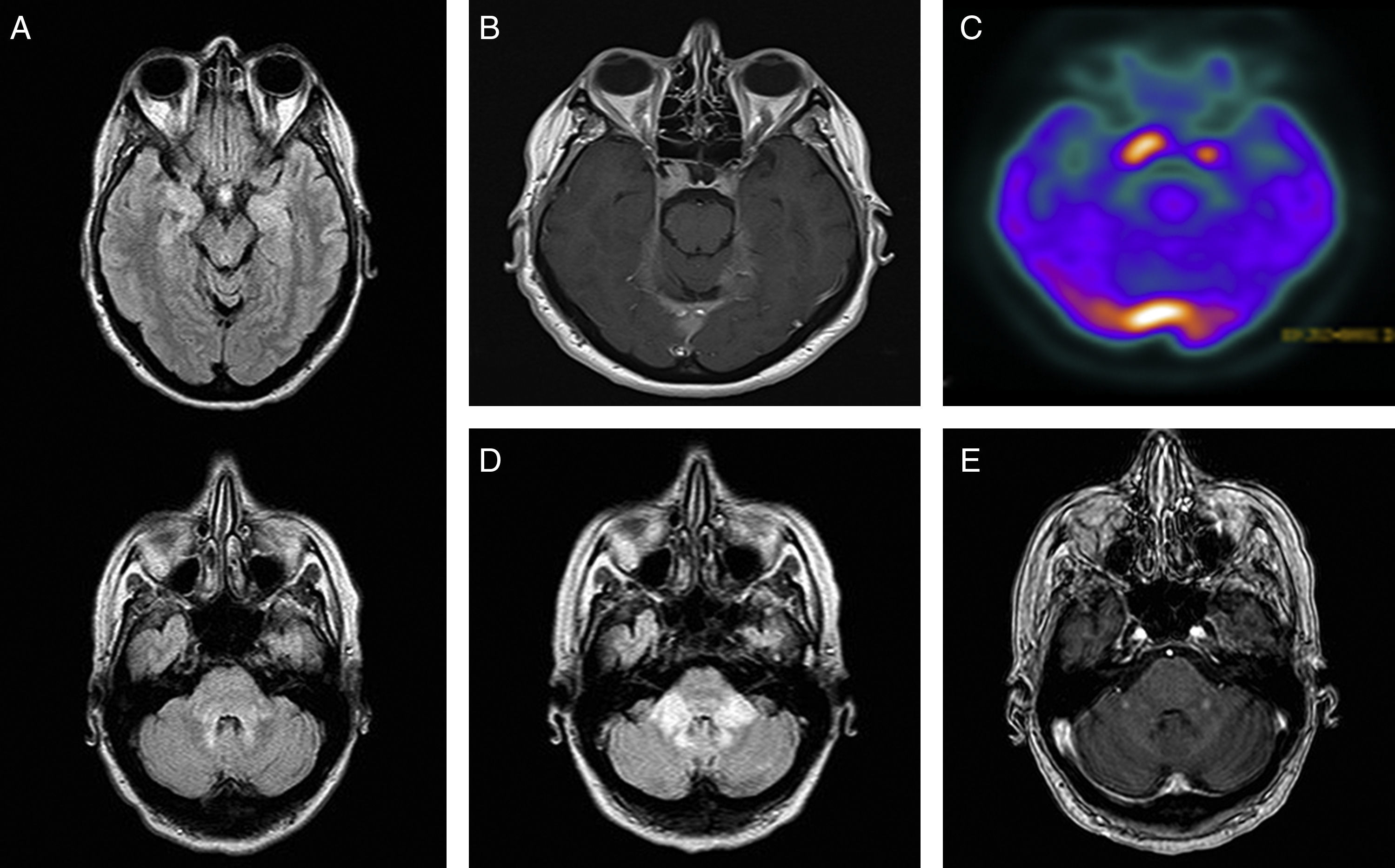
Mujer de 50 años con antecedentes de un síndrome depresivo de larga evolución. Diagnosticada en diciembre del 2010 de una diabetes insípida de origen central con engrosamiento hipotálamo-hipofisario y masas paraselares bilaterales, así como, alteración de señal a nivel del troncoencéfalo y uncus temporales (fig. 2A y B). La exploración neurológica fue normal salvo una leve disartria. VSG de 82mm. Resto de análisis generales y LCR normales. En la TAC-body se objetivó una infiltración perirrenal y periaorta abdominal, y en la gammagrafía ósea se hallaron focos hipercaptantes en la diáfisis de ambas tibias y peronés. La biopsia ósea confirmó la sospecha de una EEC. En la PET-TC con 18F-FDG cerebral se objetivó un incremento de la actividad metabólica en aquellas regiones cerebrales que mostraban engrosamiento y realce de contraste por RM (fig. 2C). El tratamiento con interferón α (3 millones sc/d, 3 veces por semana) se retiró a los 6 meses por intolerancia y progresión de la enfermedad sistémica. Anakinra y cladribina fueron ineficaces y la paciente desarrolló un síndrome cerebeloso y piramidal hasta el encamamiento y fallecimiento a los 2 años del diagnóstico (fig. 2D y E).
A) RM cerebral, FLAIR axial: hiperintensidad en pedúnculos cerebelosos medios (PCM), protuberancia dorsal, periacueductal mesencefálico y uncus temporales. B) RM cerebral, T1 axial con gadolinio: lesiones paraselares bilaterales que se realzan con contraste, mayor en el lado derecho, y en la tórcula y tentorio bilateral. C) PET-TC con 18F-FDG: aumento de captación en el área hipofisaria y tórcula. D) RM cerebral, FLAIR axial, a los 18 meses: progresión de la alteración de señal a nivel de los PCM. E) RM cerebral, T1 axial con gadolinio: captación nodular de contraste a nivel de PCM.
Los síndromes cerebeloso y piramidal progresivos constituyen las principales manifestaciones neurológicas en la EEC. El hallazgo de una hiperintensidad que se extiende de forma difusa afectando a la protuberancia y pedúnculos cerebelosos medios es característico, aunque se han descrito distintos patrones neurorradiológicos9,10. El diagnóstico correcto es difícil si no se conoce la enfermedad sistémica. La PET-TC con 18F-FDG es una herramienta útil en el diagnóstico y la valoración de la respuesta al tratamiento11. Sin embargo, como se observa en ambos casos, no todas las lesiones cerebrales muestran el mismo comportamiento. Una posible explicación para estos hallazgos es que exista un patrón neurodegenerativo además de la infiltración tumoral que, por otro lado, podría justificar la progresión neurológica y la escasa respuesta al tratamiento12,13.