Introducción La epilepsia es la enfermedad neurológica más común en la infancia; dependiendo de la definición de epilepsia farmacorresistente la incidencia varía del 10 a 23% en la población pediátrica. El objetivo de este estudio fue contabilizar la disminución en la frecuencia y/o duración mensual de crisis epilépticas en pacientes pediátricos con epilepsia farmacorresistente tratados con antiepilépticos, antes y después de la adición de inmunoglobulina G intravenosa (IgG iv).
MétodosEstudio analítico, observacional retrospectivo de casos-controles. Se estudiaron pacientes pediátricos con epilepsia farmacorresistente atendidos en el Centro Médico Nacional 20 de Noviembre de la Ciudad de México durante el período 2003-2013 y que recibieron tratamiento con IgG iv.
ResultadosCiento sesenta y siete pacientes (19,5%) presentaron epilepsia farmacorresistente y 44 (5,1%) iniciaron tratamiento adyuvante con IgG iv. La edad media de los pacientes al inicio del tratamiento fue de 6,12 años (±5,14); 28 (73,6%) tuvieron una etiología estructural adquirida, 5 (13,1%) genética, uno (2,6%) inmune y 4 (10,5%) desconocida. A los 2 meses de la aplicación de inmunoglobulina la duración de las crisis se redujo al 66,66% y la frecuencia de las crisis alcanzó una reducción del 64% a los 4 meses de iniciado el tratamiento(p<0,001).
ConclusionesLa IgG iv puede ser una terapia eficaz para la disminución en la frecuencia y duración de las convulsiones en pacientes pediátricos con epilepsia farmacorresistente, como lo demuestran los resultados de este estudio.
Epilepsy is the most common neurological disease in childhood; depending on the definition of drug-resistant epilepsy, incidence varies from 10% to 23% in the paediatric population. The objective of this study was to account for the decrease in the frequency and/or monthly duration of epileptic seizures in paediatric patients with drug-resistant epilepsy treated with antiepileptic drugs, before and after adding intravenous immunoglobulin G (iIV IgG).
MethodsThis is an analytic, observational, retrospective case-control study. We studied paediatric patients with drug-resistant epilepsy who were treated with IV IgG at the Centro Médico Nacional 20 de Noviembre, in Mexico City, from 2003 to 2013.
ResultsOne hundred and sixty seven patients (19.5%) had drug-resistant epilepsy and 44 (5.1%) started adjuvant treatment with IV IgG. The mean age of patients at the beginning of treatment was 6.12 years±5.14); aetiology was structural acquired in 28 patients (73.6%), genetic in 5 (13.1%), immune in 1 (2.6%), and unknown in 4 (10.5%). At 2 months from starting IV IgG, seizure duration had reduced to 66.66%; the frequency of seizures was reduced by 64% at 4 months after starting treatment (P<.001).
ConclusionsAccording to the results of this study, intravenous immunoglobulin may be an effective therapy for reducing the frequency and duration of seizures in paediatric patients with drug-resistant epilepsy.
La epilepsia es una enfermedad neurológica común en la infancia y afecta del 0,5-1% de los niños; aproximadamente uno de cada 150 niños será diagnosticado con epilepsia durante los primeros 10 años de vida1,2. Cada año se reportan 3,5 millones de casos nuevos de epilepsia y de estos el 40% corresponde a menores de 18 años; más del 80% de ellos se encuentran en países en desarrollo. Desafortunadamente del 6-14% de estos niños con epilepsia desarrollarán epilepsia farmacorresistente3. En la población pediátrica, la incidencia de epilepsia farmacorresistente varía del 10 a 23% dependiendo de la definición empleada en diferentes estudios4.
La epilepsia farmacorresistente fue definida por la International League Against Epilepsy (ILAE) como el fallo de 2 esquemas antiepilépticos para obtener y mantener al paciente libre de crisis5. Dentro de los factores de riesgo para desarrollar epilepsia farmacorresistente en niños se pueden mencionar: los menores de un año de edad, epilepsia sintomática, retardo del neurodesarrollo, estudio de neuroimagen patológico, entre otros6,7. El uso de inmunoglobulina intravenosa (IgG iv) ha sido reportado en diversos estudios como un tratamiento adyuvante eficaz para la epilepsia pediátrica farmacorresistente; es bien conocido que la persistencia de las crisis epilépticas, así como la ausencia de un adecuado control de las mismas tienen un impacto negativo psicosocial, conductual, cognitivo y económico además de estar asociado con un incremento de la morbimortalidad8.
MetodologíaDiseño del estudioSe empleó una muestra a conveniencia. Se trata de un estudio analítico, observacional, retrospectivo, caso-control en donde cada sujeto fue su propio control. El estudio fue aprobado por el comité de ética e investigación del Hospital Centro Médico Nacional (CMN) 20 de Noviembre, ISSSTE.
Pacientes y definicionesSe revisaron los expedientes electrónicos de los pacientes menores de 18 años atendidos en el servicio de Neurología Pediátrica del CMN 20 de Noviembre, ISSSTE durante enero 2003 a diciembre del 2013. Los pacientes con epilepsia farmacorresistente y que recibieron tratamiento con inmunoglobulina fueron considerados para el análisis, independientemente del tipo de epilepsia que presentaran.
Mediante la revisión de los expedientes clínicos, se identificaron 856 pacientes con epilepsia atendidos en el servicio de Neurología Pediátrica durante los años 2003 al 2013, de los cuales 167 (19,5%) desarrollaron epilepsia farmacorresistente. El CMN 20 de Noviembre es un centro de referencia de alta especialidad y la mayoría de los pacientes atendidos residen en otros estados del país. De los 167 pacientes con epilepsia farmacorresistente, se describe en el expediente que 44 (5,1%) aceptaron iniciar tratamiento con IgG iv; 6 pacientes recibieron una sola dosis de IgG iv y no se presentaron nuevamente para recibir el tratamiento por este motivo no se incluyeron en el análisis.
La definición de epilepsia farmacorresistente empleada fue la recomendada por la ILAE (fallo de 2 antiepilépticos), así como la definición pediátrica que además considera la presencia de al menos una crisis en un mes durante un período de 18 meses9–11. Todos los pacientes cumplieron con la definición de epilepsia farmacorresistente y se consideró reducción significativa en la frecuencia y/o duración (minutos) mensual de las crisis cuando esta fue≥50% al compararla con la basal (3 meses antes del inicio de IgG iv).
Cada sujeto fue su propio control 3 meses previo al inicio de IgG iv y se comparó la frecuencia y duración de las crisis mensuales a los 2, 4 y 6 meses de la administración de IgG iv.
EvaluacionesLos pacientes recibieron IgG iv durante 5 días consecutivos a una dosis de 0,4g/kg y posteriormente durante 5 ocasiones con intervalos de 3 semanas. Se empleó IgG humana donde cada frasco contenía 6g de inmunoglobulina diluidos en cloruro de sodio al 0,9%. La evaluación clínica neurológica, ajuste de antiepilépticos y cálculo de la dosis de IgG iv fue realizada por neurólogos pediatras del servicio de Neurología Pediátrica, de acuerdo a lo referido en el expediente clínico.
Análisis estadísticoLos datos se cargaron en una hoja de datos de Excel y posteriormente se exportaron a R (V 3.0.1) para su análisis. Las variables categóricas se describieron en frecuencias absolutas y relativas, las variables continuas se describieron como medianas (mín-máx). Dado que no hubo una distribución normal en cuanto a las comparaciones antes y después (pareadas) de las variables continuas, el análisis se hizo mediante la prueba de Friedman.
Se reportan intervalos de confianza al 95%; un valor p a 2 colas<0,05 se consideró como estadísticamente significativo.
ResultadosSe identificaron 856 pacientes con epilepsia atendidos en el servicio de Neurología Pediátrica del 2003 al 2013, de los cuales 167 (19.5%) desarrollaron epilepsia farmacorresistente y 44 (5,1%) recibieron tratamiento con IgG iv. No se consideraron en el análisis 6 pacientes, debido a que no completaron el tratamiento.
La edad media de los pacientes a la que comenzaron con epilepsia fue de 2 años y la edad media al inicio del tratamiento con IgG iv fue de 6,12 años (±5,14); 26 pacientes fueron masculinos (68,4%) y 12 femeninos (31,6%).
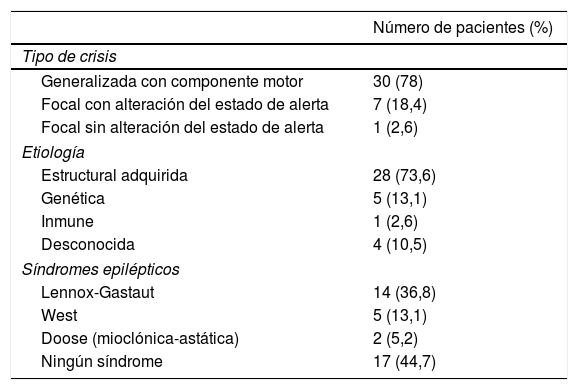
En cuanto a la etiología de la epilepsia, 28 (73,6%) pacientes tuvieron una causa estructural adquirida, 5 (13,1%) genética, uno (2,6%) inmune y 4 (10,5%) desconocida. Los síndromes epilépticos más frecuentes fueron el síndrome de Lennox-Gastaut, síndrome de West y de Doose, en orden descendente de frecuencia (tabla 1).
Frecuencias de crisis epilépticas y epilepsia según su clasificación
| Número de pacientes (%) | |
|---|---|
| Tipo de crisis | |
| Generalizada con componente motor | 30 (78) |
| Focal con alteración del estado de alerta | 7 (18,4) |
| Focal sin alteración del estado de alerta | 1 (2,6) |
| Etiología | |
| Estructural adquirida | 28 (73,6) |
| Genética | 5 (13,1) |
| Inmune | 1 (2,6) |
| Desconocida | 4 (10,5) |
| Síndromes epilépticos | |
| Lennox-Gastaut | 14 (36,8) |
| West | 5 (13,1) |
| Doose (mioclónica-astática) | 2 (5,2) |
| Ningún síndrome | 17 (44,7) |
El tipo de crisis epiléptica más frecuente fue la generalizada con componente motor, 30 pacientes (78%), seguido de la focal con alteración del estado de alerta 7 (18,4%) y focal sin alteración del estado de alerta 1 (2,6%).
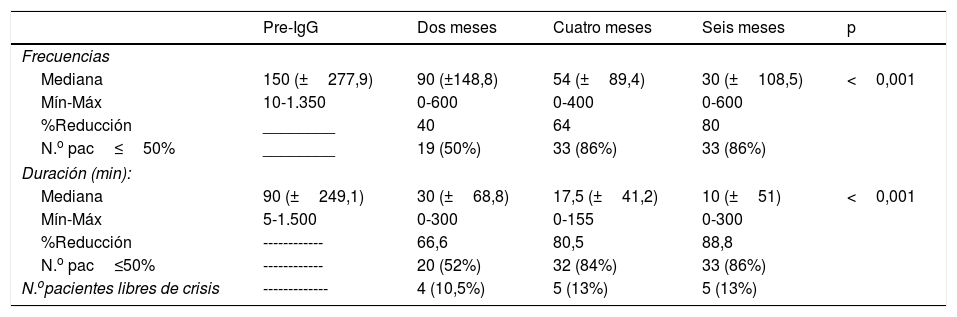
A los 2 meses de la aplicación de inmunoglobulina la duración (en minutos) de las crisis se redujo al 66,66% y la frecuencia de las crisis alcanzó una reducción del 64% a los 4 meses de iniciado el tratamiento (p<0,001) (tabla 2).
Reducción de las crisis en el tiempo
| Pre-IgG | Dos meses | Cuatro meses | Seis meses | p | |
|---|---|---|---|---|---|
| Frecuencias | |||||
| Mediana | 150 (±277,9) | 90 (±148,8) | 54 (±89,4) | 30 (±108,5) | <0,001 |
| Mín-Máx | 10-1.350 | 0-600 | 0-400 | 0-600 | |
| %Reducción | ________ | 40 | 64 | 80 | |
| N.o pac≤50% | ________ | 19 (50%) | 33 (86%) | 33 (86%) | |
| Duración (min): | |||||
| Mediana | 90 (±249,1) | 30 (±68,8) | 17,5 (±41,2) | 10 (±51) | <0,001 |
| Mín-Máx | 5-1.500 | 0-300 | 0-155 | 0-300 | |
| %Reducción | ------------ | 66,6 | 80,5 | 88,8 | |
| N.o pac≤50% | ------------ | 20 (52%) | 32 (84%) | 33 (86%) | |
| N.opacientes libres de crisis | ------------- | 4 (10,5%) | 5 (13%) | 5 (13%) | |
El número de antiepilépticos empleados antes y después del inicio de IgG iv fue del 2,65% y del 2,84% respectivamente, no hubo diferencia estadísticamente significativa en el número de antiepilépticos empleados antes y después del tratamiento con inmunoglobulina (p=0,655).
De los 5 (13,1%) pacientes que recibieron tratamiento quirúrgico a 3 se les colocó neuroestimulador (en 2 pacientes esto sucedió uno y 2 años previo a la administración de IgG iv, en el tercer paciente esto fue un año posterior a la IgG iv), y a 2 se les realizó callosotomía (uno 6 años previo a la administración de IgG y el otro un año después de la IgG).
DiscusiónEn el presente estudio se encontró que el porcentaje de pacientes que desarrolló epilepsia farmacorresistente fue del 19,5% y de estos el 5,1% recibió tratamiento con inmunoglobulina, lo cual concuerda con lo reportado en la literatura por Yilmaz et al.3 y con otros estudios que emplean diversas definiciones de epilepsia farmacorresistente (10 al 23%)4.
Geerts et al.12 reportan que el 22,6% de los pacientes que desarrollan epilepsia farmacorresistente son de causa sintomática y en el presente estudio se encontró que la principal causa de epilepsia farmacorresistente es estructural adquirida (73,6%). A pesar de que el estudio de Geerts emplea la antigua clasificación de etiología de epilepsia, existe una correspondencia entre causas sintomáticas y estructurales adquiridas. En nuestro estudio la mayoría de los pacientes con etiología estructural fue debido a daño hipóxico-isquémico perinatal.
En lo que respecta a la respuesta al tratamiento adyuvante con IgG iv, a los 2 meses se encontró que la mitad de los pacientes habían alcanzado una reducción del 40% de las crisis epilépticas y a los 4 meses el 86% de los pacientes alcanzó una reducción≥50% lo cual se mantuvo a los 6 meses de seguimiento, con un valor de p estadísticamente significativo (<0,01). Al comparar esto con la literatura se puede observar lo siguiente: Granata13 (15 pacientes en el 2003) reporta reducción en el 86% de los pacientes, Billiau et al.14 en el 31% (13 pacientes en el 2007), Mikati et al.15 en el 43% (37 pacientes en el 2009), Geva-Dayan et al.16 en el 15% (64 pacientes en el 2012), y Bello-Espinosa et al.11 en el 81% (27 pacientes en el 2015).
En las revisiones sistemáticas más recientes reportadas en el Cochrane Database, se encontró solamente un estudio clínico controlado aleatorizado, placebo-control en pacientes adultos y pediátricos tratados con inmunoglobulina donde se obtuvo una respuesta al tratamiento en el 52,5% versus el 27,78% del grupo placebo (p=0,095)17,18.
Con lo anterior podemos constatar que existe una amplia variabilidad en el porcentaje de pacientes que responden al tratamiento con inmunoglobulina9, independientemente de la etiología de la epilepsia19 incluyendo la existencia de alteraciones inmunológicas; en este aspecto el presente estudio concuerda con los datos de los estudios previamente publicados.
En cuanto al número de antiepilépticos empleados antes y después del inicio del tratamiento con IgG iv, no se encontró una reducción significativa, lo cual apoya el concepto de uso de esta terapia como adyuvante.
Dado que el diseño del presente estudio es observacional, retrospectivo en el cual cada paciente fue su propio control, las desventajas que se pueden mencionar son: falta de aleatorización, limitación en cuanto a los datos obtenidos mediante la revisión de los expedientes clínicos y la falta de control de ciertas variables, así como la comparación con grupo control que haya recibido placebo. Sin embargo, los estudios observacionales a pesar de tener un menor nivel de evidencia clínica son una vía válida de añadir información acerca de enfermedades donde es difícil realizar un ensayo clínico. Este es el primer estudio en donde se toma en cuenta para el análisis de respuesta al tratamiento la variable del tiempo (duración de las crisis) además de la frecuencia de las mismas, ya que los estudios previos solamente hablan del porcentaje de reducción en frecuencia.
Lo que se encontró en este estudio es que existe una correlación de reducción tanto en frecuencia como en la duración de las crisis, sin embargo, la reducción≥50% se manifestó primero en la duración y posteriormente en frecuencia (a los 2 meses el 52% de los pacientes ya tenía una reducción del 66% con una p significativa<0,001).
Esto nos habla del impacto que tiene la inmunoglobulina como terapia adyuvante en la epilepsia farmacorresistente y de la importancia que tiene llevar una adecuada contabilización de ambos parámetros antes de concluir una falla de respuesta al tratamiento.
ConclusionesLos resultados del presente estudio pueden indicar una efectividad en el tratamiento adyuvante con IgG iv en la epilepsia farmacorresistente pediátrica, esto es aplicable tanto en los pacientes con etiología conocida, así como en aquellos en los cuales no se logra llegar a un diagnóstico etiológico.
Este estudio añade información acerca de un tema poco conocido y marca un precedente en la importancia de la realización de ensayos clínicos en esta área.
FinanciaciónEl presente estudio no tuvo ningún tipo de financiación.
Conflicto de interesesNinguno de los autores declara conflicto de intereses.