Los pacientes con diabetes tipo 1 necesitan tres o más inyecciones diarias de insulina para controlar su glucemia. Los pacientes con diabetes tipo 2 necesitan insulina cuando los antidiabéticos orales y otras medidas no farmacológicas han dejado de ser eficaces para controlar sus valores sanguíneos de glucosa. Es evidente, por tanto, la importancia de este compuesto en el abordaje farmacoterapéutico de la diabetes.
Por otra parte, en la pasada década varios acontecimientos mejoraron notablemente las posibilidades de tratamiento del paciente diabético:
- Los resultados de dos grandes estudios1 demostraron inequívocamente la relación existente entre un buen control metabólico y el descenso de las complicaciones vasculares.
- El desarrollo de nuevas formas de insulina, caracterizadas por una mayor rapidez en el inicio de la acción y una mayor duración: los denominados análogos de la insulina.
- La aparición de nuevas formas de liberación de insulina (bombas de infusión y aerosoles).
- Los avances en la monitorización de la glucemia.
Desde del punto de vista de la estructura, la insulina es un polipéptido de 51 aminoácidos que se disponen formando dos cadenas, unidas por diferentes puentes disulfuro. La insulina es sintetizada a partir de un precursor de cadena única conocido como proinsulina. Esta síntesis y su posterior almacenamiento tienen lugar en el páncreas, y más en concreto, en las células beta de los islotes de Langerhans.
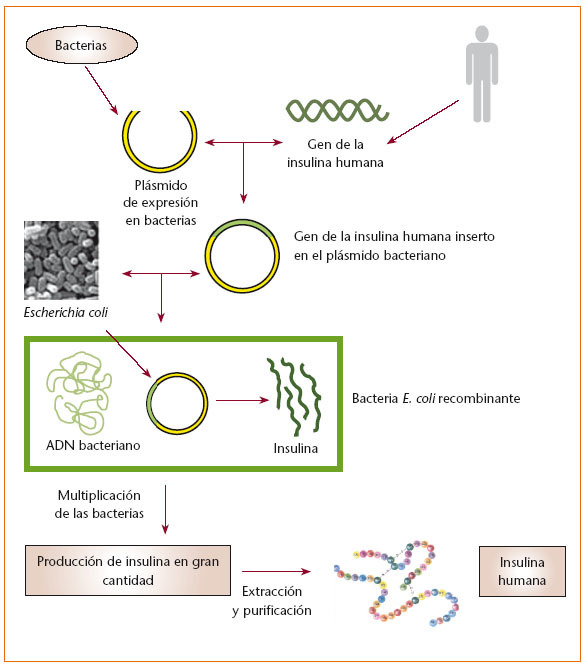
Inicialmente las insulinas utilizadas eran de origen animal: porcino y bovino. Posteriormente ha sido posible sintetizar insulina humana, dando lugar a la insulina semisintética (obtenida a partir de insulina porcina por sustitución en la cadena B del aminoácido alanina por treonina) y a la insulina biosintética (obtenida por bioctenología con ADN recombinante de origen bacteriano o de levadura) (fig. 1).
fig. 1. Esquema de obtención de la insulina.
Los últimos estudios han conducido a los análogos de la insulina cuyo objetivo es mejorar el perfil farmacocinético de las insulinas convencionales y superar así las limitaciones que éstas presentaban en algunos pacientes para mantener un control glucémico adecuado.
La secreción de insulina fisiológica tiene dos componentes, uno basal continuo y otro agudo desencadenado por la hiperglucemia. En sujetos sanos, inmediatamente después de ingerir alimentos, se secreta insulina desde las células beta a la circulación portal, alcanzando insulinemias elevadas, con niveles máximos de hasta 80 µU/ml a los 30 min, seguido por una disminución a los valores basales al cabo de 2-3 h. La insulina secretada se une a las células del tejido adiposo, hígado y músculo, estimulando la entrada de nutrientes a la célula y evitando así un ascenso excesivo de la glucemia posprandial. La dificultad para imitar la secreción fisiológica en pacientes con diabetes tipo 1 viene dada por la necesidad de conseguir un ascenso rápido de insulina después de las comidas, ascenso que debe ir en paralelo con el aumento de la glucemia.
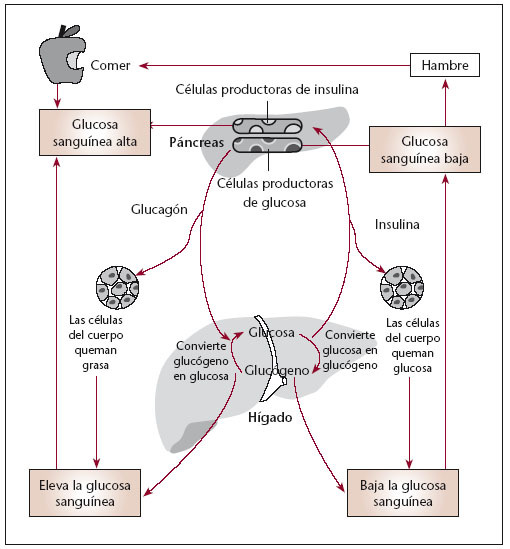
Por otro lado, durante el período de ayuno, la insulina, conocida en esta fase como insulina basal, desempeña un papel crucial, ya que inhibe la neoglucogénesis hepática y evita la hiperglucemia en ayunas. Otra de sus funciones durante este período es la de inhibir la lipólisis desde el tejido adiposo, lo que produce un descenso en el aporte de ácidos grasos al hígado, evitándose así la cetogénesis. Es evidente, por tanto, que la deficiencia de insulina basal acarrea hiperglucemia en ayunas y cetosis (fig. 2).
fig. 2. fisiología de la insulina.
La secreción basal de insulina al sistema porta se produce de forma continua, aunque en niveles muy bajos, alcanzando directamente el hígado donde ejerce su principal función. Si bien la secreción de insulina es continua durante el período comprendido entre dos comidas, los valores varían durante el día, de modo que los requerimientos de insulina basal son un 30% superiores en la madrugada, respecto a las primeras horas de la noche.
Cuando se administra insulina exógena a pacientes con diabetes tipo 1, dicha insulina no se libera de forma directa a la circulación portal, ni imita las variaciones en los niveles de insulina basal, tal y como ocurre en el sujeto sano.
Indicaciones de tratamiento insulínicoAdemás de la diabetes tipo 1, la principal indicación para tratamiento insulínico es la insuficiencia definitiva en el funcionamiento de las células beta pancreáticas, fenómeno también conocido como fracaso secundario a hipoglucemiantes orales. Este fracaso se justifica atendiendo a los siguientes criterios clínicos:
- Ineficiente control glucémico empleando dosis máximas de dos o más antidiabéticos orales.
- Pérdida de peso acelerada, como consecuencia de esta descompensación permanente.
- La presencia de infección concomitante no debe ser el desencadenante de la descompensación.
- Presencia o no de cetoacidosis.
En algunos casos puede ser necesaria una insulinización transitoria en diabéticos tipo 2 con el fin de mejorar el control glucémico, reduciendo así el riesgo de complicaciones diabéticas.
A modo de resumen, puede decirse que las indicaciones de tratamiento insulínico en España son las siguientes:
- Diabetes tipo 1.
- Diabetes tipo 2 cuando se produce fracaso primario o secundario con hipoglucemiantes orales.
- Control inicial de la diabetes en situaciones tales como fiebre, infecciones graves, acidosis significativa, cirugía mayor, traumatismo severo, quemaduras graves, cuidados intensivos y coma diabético.
- Diabetes durante el embarazo.
Cabe hablar aquí de las insulinas convencionales, las premezcladas y los análogos de insulina.
Insulinas convencionalesDado que la insulina tiene una vida media muy corta, usualmente se recurre a distintas técnicas que incrementen la duración de su acción. Estas técnicas incluyen la unión a proteínas tipo protamina y la cristalización controlada, técnica esta que permite la formación de cristales más o menos grandes, de modo que cuanto mayor sea el tamaño del cristal, más lentamente se liberará la insulina.
Las insulinas convencionales incluyen:
- insulina regular o rápida. Esta insulina es obtenida por recristalización de la insulina, sin adición de sustancias retardantes. Sus cristales corresponden a hexámeros de insulina producidos por agregados de la hormona unidos entre sí a través de la cadena B. Su aspecto se caracteriza por ser una solución transparente. En caso necesario puede administrarse por vía intravenosa. Su lenta absorción determina un retraso en el inicio de su acción, que comienza al cabo de 30-60 min, lo que obliga a los pacientes a inyectársela entre 20 y 30 min antes antes de las comidas. El efecto máximo se consigue al cabo de 1-3 h y la duración de su acción es de 5-8 h, lo que incrementa el riesgo de hipoglucemia posprandial. Esta insulina actúa casi inmediatamente cuando se inyecta por vía intravenosa. La insulina soluble neutra humana es insulina humana obtenida biosintéticamente por tecnología de ADN recombinante y es equivalente a la insulina humana desde el punto de vista inmunológico.
- insulina de acción intermedia. La insulina de acción intermedia también es conocida como isofánica o NPH (insulina Hagedorn Protamina Neutra) y se caracteriza por una lenta absorción debido a la adición de protamina a la insulina regular. La insulina NPH es insulina humana con cantidades equimolares de protamina, una proteína básica extraída del esperma de los peces. Su acción se inicia a las 2 h y tiene una duración total del efecto de 13-18 h, con una acción máxima entre las 5-7 h siguientes a su administración. La inyección vespertina de insulina NPH tiene su efecto máximo en las primeras horas de la madrugada, siendo causa frecuente de hipoglucemia nocturna. Otra desventaja de la insulina NPH son las variaciones intraindivuales de su efecto de hasta el 40-50%, reflejando una respuesta clínicamente impredecible.
Este tipo de insulinas está compuesto por mezclas en proporciones fijas de insulina de acción rápida y de acción intermedia. Están indicadas en la terapia insulínica convencional, actuando tanto como insulinas basales como preprandiales. Suelen administrarse antes del desayuno y antes de la cena. Las mezclas prefijadas tienen el inconveniente de su limitada flexibilidad, de modo que dosis que son idóneas habitualmente, pueden resultar incorrectas por cambios puntuales en las actividades o comidas usuales.
Análogos de insulinaEn el pasado, las características farmacocinéticas de los preparados de insulina eran modificadas añadiendo sustancias que retardaban su absorción (protamina y cinc) y mediante la formación de cristales de diferentes tamaños.
Durante los últimos años, la tecnología de ADN recombinante ha hecho posible el desarrollo de análogos de insulina con un perfil farmacocinético diferente al de las preparaciones de insulina intacta existentes.
Usualmente los análogos de insulina se clasifican en análogos de acción rápida y de acción lenta.
Análogos de insulina de acción rápidaLos análogos de acción rápida tienen menor tendencia a agruparse en complejos hexaméricos en relación con la insulina humana y se absorben con más facilidad, por lo que su comienzo de acción es más precoz, el pico más elevado y la desaparición más rápida. En este grupo se enmarcan las insulinas lispro, aspart y glulisina.
Insulina lisproFue el primer análogo desarrollado e introducido en el mercado en la década de los noventa. Este compuesto debe su nombre a la inversión de los residuos prolina en posición B-28 y lisina en B-29. Este cambio estructural en la cadena B reduce 300 veces la dimerización de las cadenas proteicas. Su espectro de acción es el siguiente: actúa a los 5-15 min de su inyección, presenta un nivel de concentración máximo a los 60 min, y desaparece a las 2-4 h. La absorción más rápida de la insulina lispro origina un pico de insulina más rápido, más alto y más corto en comparación con la insulina regular, lo cual es más adecuado para compensar la elevación glucémica que sigue a la ingesta de alimento. Esta insulina debe administrarse inmediatamente antes de empezar a comer.
Durante los últimos años, la tecnología de aDN recombinante ha hecho posible el desarrollo de análogos de insulina con un perfil farmacocinético distinto del de las preparaciones de insulina intactas existentesUna ventaja de este tipo de insulina es la reducción de las colaciones necesarias para evitar la hipoglucemia.
Sus principales inconvenientes incluyen su mayor coste y la falta de efecto al cabo de 4-6 h, lo que obliga a aumentar la dosis de insulina basal. Si bien la insulina lispro no es idéntica a la insulina natural, no produce reacciones alérgicas, aunque induce una mayor síntesis de anticuerpos en pacientes sin insulinoterapia previa.
Insulina aspartEs idéntica estructuralmente a la insulina humana regular salvo por la sustitución del residuo de prolina en posición 28 de cadena B por un ácido aspártico, lo que reduce la tendencia a la agregación de los monómeros. Su apariencia es clara e incolora. Presenta un tiempo de inicio, efecto máximo y duración idénticos a los de la insulina lispro. En relación con la insulina humana regular, se absorbe el doble de rápido, alcanza una concentración sérica dos veces mayor y dura la mitad del tiempo. Sus características farmacocinéticas no se afectan significativamente en caso de disfunción hepática o renal, si bien las concentraciones de insulina pueden incrementarse en dichas situaciones, lo que obliga a un control más frecuente en estos pacientes. Dichas características tampoco se ven afectadas en caso de obesidad.
En lo que respecta a la afinidad de este análogo por los distintos receptores, su afinidad por el receptor de insulina y por el receptor de IGF-1 es similar a la de la insulina humana regular.
Otra de sus características es una menor variabilidad intra e interindividual en comparación con la insulina humana regular. Esta insulina debe administrarse inmediatamente antes de las comidas, si bien también está autorizada su administración posprandial cuando sea necesario.
Se recomienda precaución cuando se administre en embarazadas y durante la lactancia.
Los beneficios de la insulina aspart se traducen en una mejor calidad de vida, una disminución de las hipoglucemias y de la hemoglobina glucosilada. Esta insulina induce menos reacciones inmunológicas que la insulina NPH y la insulina humana regular.
Insulina glulisinaLa insulina glulisina es el último análogo de insulina rápida comercializado. Al igual que los anteriores presenta modificaciones estructurales, en concreto, cambio del residuo de lisina en B-29 por ácido glutámico y reemplazo de asparragina en B-3 por lisina. Sus características farmacocinéticas son similares a las de los dos análogos anteriores.
Son escasos los estudios clínicos acerca de su eficacia, si bien en algunos de ellos se ha demostrado que con este análogo se logran valores de hemoglobina glucosilada más bajos que con la insulina regular humana.
Actualmente se desconoce su efecto en embarazadas y en niños, por lo que no debe usarse en estos colectivos.
Se han descrito algunas reacciones alérgicas locales como eritema, dolor y edema.
Análogos de insulina de acción lentaLos análogos de acción lenta producen una liberación de insulina más lenta y sin picos, por lo que disminuye la frecuencia de hipoglucemias nocturnas. En este grupo se enmarcan glargina y detemir.
Insulina glarginaLa insulina glargina es un análogo de insulina de acción larga que se produce al añadir a la insulina humana, por técnicas de recombinación genética, dos argininas en la región C-terminal de la cadena B, y sustituir la asparragina por glicina en la posición A-21de la cadena
A. Estos cambios dan lugar a una insulina estable que es soluble en el pH ácido del vial, pero que precipita en el pH neutro del lugar de inyección. El precipitado se disocia lentamente en hexámeros y posteriormente en dímeros y monómeros, dando lugar a una absorción sostenida y lenta que determina niveles plasmáticos planos. Esta insulina se caracteriza por presentar una menor variabilidad en su absorción desde el sitio de inyección en comparación con las insulinas basales convencionales; su acción se inicia aproximadamente 1 h después de su administración y se alcanza una concentración máxima a las 4-5 h. La duración de su efecto es de aproximadamente 24 h, por lo que puede administrarse en dosis única diaria, a cualquier hora del día, consiguiéndose así una insulinemia basal, asociada a análogos rápidos que se administrarán con las comidas.
A diferencia del resto de insulinas de acción intermedia y prolongada, la insulina glargina es transparente al igual que la insulina regular, lo que debe ser tenido en cuenta para evitar posibles errores.
El cambio de tratamiento desde insulina NPH a insulina glargina permite una disminución de la dosis de insulina basal en 20-30%. Por otra parte, pacientes que tienen hipoglucemias con insulina NPH mejoran su control y reducen las hipoglucemias, especialmente las nocturnas, tras cambiar al análogo glargina. Estos resultados pueden justificarse atendiendo a la ausencia de pico de acción máxima que tiene la insulina glargina.
La administración de este tipo de insulina se realiza por vía subcutánea y no debe usarse la vía intravenosa. Se recomienda disminuir la dosis en casos de insuficiencia hepática o renal. No se aconseja su utilización en mujeres gestantes ni en madres lactantes, ya que no existen todavía suficientes ensayos clínicos para asegurar su inocuidad.
La dosis de insulina glargina debe adaptarse individualmente en función del tratamiento insulínico anterior y las cifras de glucemia.
No se aconseja diluir la glargina con otra insulina, ya que su pH es ácido, y por tanto, no puede mezclarse con insulinas con pH neutro.
Entre sus principales inconvenientes se incluyen los siguientes:
- Debido a su perfil farmacocinético, algunos pacientes pueden necesitar dosis mayores de insulina rápida antes de las comidas.
- Al no poder mezclarse en la misma jeringa con otras insulinas, son necesarias varias inyecciones.
En lo que respecta a la respuesta inmunológica, no se ha observado una mayor respuesta inmunogénica a la insulina glargina en comparación con la insulina NPH.
Insulina detemirLa insulina detemir debe su efecto prolongado a un mecanismo diferente a los otros análogos: la adición de ácido mirístico, un ácido graso de 14 carbonos, a la lisina en B-29 le confiere capacidad para unirse a la albúmina y de esta forma actúa como un reservorio de insulina, prolongando su efecto. La remoción de una treonina en B-30 facilita la formación de hexámeros, alargando su acción.
Este análogo está unido a la albúmina en más de un 98% y sólo su fracción libre puede unirse a los receptores de insulina de las células diana. Es soluble a pH neutro, por lo que tras su administración mediante inyección subcutánea permanece líquida, lo que probablemente produce menor variabilidad en su absorción. Esto la convierte en la insulina basal con menor variabilidad intraindividual entre las dosis.
Su potencia hipoglucemiante es inferior respecto a la de la insulina NPH, lo que obliga a administrarla en una dosis mayor que la anterior para conseguir una potencia hipoglucemiante equivalente.
En cuanto a su farmacocinética, la insulina detemir presenta una duración de acción de aproximadamente 20 h, un perfil más plano que la insulina NPH, ninguna alteración de su espectro en personas con insuficiencia renal o hepática y menor variabilidad de absorción que la insulina NPH.
La insulina detemir se relaciona con valores mayores y menor variabilidad de la glucemia en ayunas, menor riesgo de hipoglucemias totales y nocturnas y menor ganancia de peso que la insulina NPH.
Sistemas de administración de insulinaLa insulina puede administrarse a través e distintos sistemas: viales, plumas, jet, bombas de infusión continua.
VialesSon los primeros sistemas de administración de insulina que salieron al mercado. Incluyen el vial propiamente dicho, junto con una aguja y una jeringa graduada y desechable. Una de sus principales características es su precio sumamente económico en comparación con otros sistemas de administración de insulina, unido a la posibilidad de realizar mezclas manuales de insulinas. Su mayor inconveniente es la dificultad de su manejo, especialmente en aquellos pacientes con problemas de visión.
En el mercado actualmente existen diferentes tipos de insulina (regular, NPH, lispro, etc.) con esta forma de presentación.
PlumasEs un sistema de administración de insulina más moderno, en comparación con los viales anteriormente citados. En las plumas la insulina va cargada en un cartucho. Tras su uso puede cambiarse por otro nuevo o se desecha todo el dispositivo. Estos sistemas permiten realizar varias aplicaciones cambiando de aguja.
El cartucho contiene 300 unidades de insulina. Su sistema de graduación para medir la dosis de insulina es más sencillo y útil, especialmente en pacientes con problemas de visión. Otra de sus características es la facilidad y la comodidad que implica su transporte. Como principal inconveniente destaca su precio más elevado.
JetEste dispositivo es un pequeño aparato similar a un bolígrafo que mediante un sistema de alta presión introduce la insulina subcutáneamente sin que sea necesario utilizar una aguja. Es especialmente útil en aquellos sujetos con poca tolerancia a las agujas. Sus principales inconvenientes incluyen su precio, unido a la poca experiencia existente sobre su uso.
Bombas de infusión continuaLa bomba o sistema de infusión subcutánea continua de insulina consiste en un aparato electrónico del tamaño de una baraja de cartas que bombea insulina desde un reservorio a un ritmo prefijado.
Un programa permite mantener tanto los valores basales de insulina como la introducción de bolos rápidos que aumentan los niveles posprandiales, con el objetivo de conseguir un mejor control metabólico, minimizar el riesgo de hipoglucemias y mejorar la calidad de vida de los pacientes.
Estas bombas representan una técnica prometedora en pleno desarrollo, que utiliza insulinas de acción rápida. Se dispone de algunas evidencias en las que los análogos lispro y aspart han mostrado una eficacia similar y menor frecuencia de hipoglucemias que con la infusión de insulina regular humana. Usualmente, con el uso de estas bombas, se administra en glúteos o abdomen.
Sus principales ventajas son las siguientes:
- No hay limitación de edad.
- Facilidad de administración, con disminución del número de pinchazos e inserción no dolorosa de la cánula.
- Pueden administrarse dosis muy pequeñas.
- Mejor control glucémico, con disminución de las oscilaciones glucémicas.
- Mayor facilidad para ajustar la insulina según la ingesta de hidratos de carbono.
- Mayor flexibilidad.
Sus principales inconvenientes incluyen:
- Incidencia controvertida de complicaciones agudas.
- Olvido de los bolos.
- Obstrucción de la cánula por sangre o doblamientos.
- Salida de la aguja de la zona de punción.
- Puede dificultar las relaciones sexuales.
- Alteración de la imagen corporal.
- Dificultades tecnológicas.
- Sistema muy costoso.
Actualmente las bombas de insulina están indicadas en los siguientes pacientes con diabetes tipo 1:
- Mujeres cuya glucemia no se controla con insulina inyectada por vía subcutánea y embarazadas.
- Diabéticos no controlables con tratamiento habitual subcutáneo o que producen importantes hiperglucemias en ayunas o nocturnas.
- Pacientes dependientes de insulina con múltiples ingresos hospitalarios por descompensaciones.
- Pacientes dependientes de insulina con necesidades específicas por su desarrollo profesional.
En la actualidad, algunos investigadores están intentando desarrollar insulinas que se administren por vías más agradables que la inyección subcutánea. La insulina oral está limitada por la acidez del estómago y las enzimas digestivas del intestino. La insulina nasal presenta varios problemas, entre ellos su variable absorción y la irritación de las mucosas. La insulina inhalada es la más prometedora desde el punto de vista clínico; de hecho en enero de 2006, la Agencia Europea del Medicamento autorizó la comercialización en toda la Unión Europea de la primera insulina disponible por vía inhalatoria.
Se trata de un análogo de la insulina humana de acción rápida, que se presenta como polvo para su administración en forma de aerosol con cámara de inhalación. Genera pequeñas partículas que liberan la insulina en los alvéolos pulmonares, a través de los cuales se absorbe. En definitiva, utiliza un sistema de liberación parecido a los que se usan para el asma. Se presenta en dosis de 1 o 3 mg y se necesitan dosis mayores a las utilizadas por vía subcutánea para lograr el mismo efecto. Su farmacocinética es similar a la de los análogos aspart o lispro. Proporciona niveles de eficacia similares cuando se utiliza conjuntamente con insulina de acción prolongada. Su empleo no conlleva la supresión del tratamiento parenteral, ya que esta vía sigue siendo necesaria para la administración de insulinas basales. Por otra parte, parece importante señalar que la biodisponibilidad de la insulina inhalada es tan sólo del 8-13% con respecto a la insulina administrada por vía subcutánea. Los principales efectos adversos asociados a su uso incluyen: hipoglucemia, tos, disnea, dolores faríngeos y boca seca. Quedan por establecerse sus efectos sobre la función pulmonar. La insulina inhalada está indicada para el tratamiento de la diabetes tipo 1 y 2 en adultos sin problemas pulmonares conocidos. Su uso no está indicado en menores de edad, diabéticos con problemas pulmonares conocidos (asma, EPOC, enfisema) o alérgicos a alguno de los componentes de la formulación. Ya que el tabaco aumenta la tasa de absorción de insulina inhalada, no puede usarse en fumadores o en ex fumadores que lleven menos de 6 meses de abstinencia. Dada la falta de experiencia de uso y la ausencia de estudios, es pronto para establecer una clara comparación coste/ efectividad respecto a las insulinas subcutáneas disponibles.
Pautas de insulinizaciónLas pautas o regímenes de insulinización se clasifican en dos grandes grupos: pautas fisiológicas y pautas no fisiológicas.
Regímenes no fisiológicosEn estos regímenes, la administración de insulina exógena no reproduce el perfil de secreción de la insulina endógena. Se caracterizan por la administración de 1-2 dosis de insulina al día; puede ser insulina de acción intermedia o prolongada. Estas pautas de administración están especialmente indicadas en diabéticos tipo 1 de reciente diagnóstico y con células beta pancreáticas aún funcionantes, o en diabéticos tipo 2 al comienzo de la insulinización.
Regímenes fisiológicosEstos regímenes pretenden reproducir la secreción de insulina endógena, compensando hiperglucemias basales e hiperglucemias prandiales con diferentes insulinas. Se distingue entre: régimen convencional y régimen intensivo. El régimen convencional se basa en la mezcla de insulina rápida e insulina intermedia administrada, en general, antes del desayuno y antes de la cena. Su ventaja radica en un menor número de pinchazos diarios, aunque tiene como contrapartida un estricto control de los horarios, de modo que un retraso en el horario de las comidas puede generar hipoglucemias. El régimen intensivo es el más empleado con objeto de aproximarse más al patrón de glucemia del sujeto sano. Este régimen se basa en la administración de 1-2 dosis diarias de insulina de acción intermedia o prolongada y bolos de insulina de acción rápida en relación con las comidas. Obviamente este régimen requiere un mayor número de inyecciones, si bien tiene la ventaja de permitir una mayor flexibilidad en los horarios de las comidas. La puesta en práctica de esta pauta implica pacientes motivados y una adecuada educación diabetológica.
Consejos desde la farmaciaSeguidamente se citan una serie de recomendaciones básicas
que el farmacéutico puede dar a aquellos pacientes que reciban
tratamiento insulínico:
- Es fundamental que el paciente conozca el tipo o los tipos de insulina que está utilizando (nombre comercial, fabricante, duración del efecto…). Las dosis siempre deberán ser individualizadas y ajustadas en función del nivel de actividad física desarrollado por
el sujeto. - El paciente debe conocer cómo preparar la insulina prescrita o cómo realizar las mezclas en caso de que use varias insulinas. Si el paciente tiene dificultades de visión que le impiden ver correctamente la escala de la jeringa, es conveniente que use una lupa, o bien que otra persona supervise que la dosificación es correcta.
- Es básico que el paciente sepa que debe administrarse la dosis justa de insulina, ni un poco más, ni un poco menos, porque pequeñas oscilaciones pueden afectar gravemente a su glucemia.
- Conviene recalcar al paciente la necesidad de que compruebe que lleva la insulina correcta antes de salir de la farmacia.
- El paciente ha de saber cómo debe guardar la insulina. Es sumamente importante que sepa que todas las insulinas mantienen su potencia durante más tiempo si permanecen en la nevera antes de ser usadas por primera vez. Una vez que se ha empezado a utilizar un determinado vial de insulina, puede mantenerse a temperatura ambiente, pero no durante más de un mes.
- El paciente debe conocer dónde y cómo administrarse la insulina, así como también debe ser capaz de reconocer los síntomas de la hipoglucemia y cómo responder ante ellos. n Por último, el paciente tiene que saber que debe medir su insulina periódicamente y es fundamental que sepa cómo.manejar el aparato medidor.
Anónimo. Actualización en insulinas. Infac. 2005;3:11-6.
Anónimo. Actualización del tratamiento insulínico de la diabetes. SaludMadrid. 2007;2:3-8.
Anónimo. Insulinas: clasificación y usos. Sacylite 2005, nº 1, (consultado el 24 de junio de 2007). Disponible en: http://www.sanidad.jcyl.es/ SACYLITE_05_1_INSULINAS_I.pdf
Aragón A, Olivan B, Manzano P, Lucas T. Las nuevas insulinas: revisión. Información Terapéutica del Sistema Nacional de Salud. 2004;2:41-9.
Cadime. Nuevas insulinas. Boletín Terapéutico Andaluz. 2006;5.
(Consultado el 24 de junio de 2007). Disponible en: http://www.easp.es/web/documentos/BTA/0001034documento.pdf
Cervera-Casino P, Royo-Garrido A. Análogos de insulina: un pequeño paso para el hombre, un gran «peso» para la sociedad. Atención Primaria. 2006;6:363-4.
Díaz-Maroto S, Martínez de Lecea ML. Insulinas. Nuevas formulaciones y esquemas terapéuticos en la diabetes mellitus tipo 1. Offarm. 1999;9:98-110.
Espinosa TM, Marichal S. Avances en terapia insulínica en la diabetes mellitus tipo 1. Aciertos y desaciertos. Revista Cubana de Endocrinología. 2007;1. (Consultado el 24 de junio de 2007). Disponible en: http://bvs.sld.cu/revistas/end/vol18_1_07/end07107. htm
Eyzaguirre F, Corner E. Análogos de insulina: en búsqueda del reemplazo fisiológico. Revista Médica de Chile. 2006;134:239-50.
Fain JA. Desvelar los misterios del tratamiento con insulina. Nursing. 2005;1:21-3.
Gómez FJ. Tratamiento con insulina. Alternativas actuales. Revista de Endocrinología y Nutrición. 2005;3:S31-S36.
Mata M, Muñoz M. Nuevas insulinas. Atención Primaria. 2005;3:126-8.
Muñoz S. Nuevas insulinas en el tratamiento de la diabetes mellitus tipo 2. Medwave. 2005;11. (Consultado el 24 de junio de 2007). Disponible en: http://www.medwave.cl/congresos/ Nutricionclinica/5/1.act
Roura P, Mata M, Cano JF. Nuevas perspectivas en el tratamiento de la diabetes mellitus. Atención Primaria. 2005;5:229-32.
The Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. The Diabetes Control and Complications Trial Research Group. New England Journal of Medicine 1993;329:977-86.
UK Prospective Diabetes Study Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes. Lancet. 1998;352:837-53.