En Estados Unidos se estima que la epidemia estacional de gripe provoca una media de 226.000 hospitalizaciones y 36.000 fallecimientos anuales1,2. La infección por el virus de la gripe puede causar morbilidad grave y mortalidad a cualquier edad, pero las máximas tasas de complicaciones graves de la gripe se observan en los niños menores de 2 años de edad, los adultos de más de 65 años de edad y los enfermos crónicos1-5.
Aunque la propia infección por el virus de la gripe puede provocar la muerte, la mayoría de los fallecimientos relacionados con la gripe son consecuencia, bien de una exacerbación, bien de una alteración subyacente o una coinfección invasora por otro patógeno infeccioso1,2. En muchos estudios se ha observado una neumonía bacteriana grave, a veces fatal, después de la gripe, que se sospecha es causa importante del aumento de la mortalidad durante la pandemia de gripe6-8. Más del 90% de las muertes atribuibles a la gripe en Estados Unidos ocurre en personas de 65 años de edad o más2. Los datos de la mortalidad asociada con la gripe en los niños son limitados. Un estudio que utilizó los datos del certificado de defunción y de la supervisión de la gripe estimó unos límites de 28-92 muertes anuales asociadas con la gripe en niños estadounidenses menores de 5 años de edad entre 1990 y 19992.
La mortalidad pediátrica asociada con la gripe es una alteración de notificación obligatoria nacional en Estados Unidos. En octubre de 2004 se instauró una revisión nacional de la mortalidad pediátrica asociada con la gripe, tras una estación de gripe grave en la que se notificaron 153 muertes pediátricas asociadas con la gripe9. Durante los inicios de 2007, los CDC observaron un aumento del número de informes de muertes pediátricas relacionadas con la gripe asociadas con una coinfección por Staphylococcus aureus, comparado con las estaciones anteriores. En este informe describimos la mortalidad pediátrica asociada con la gripe desde 2004 a 2007, y un aumento de los informes de coinfección por S. aureus durante la estación de 2006-2007.
MÉTODOSLa muerte pediátrica asociada con la gripe se define como el fallecimiento de un niño de < 18 años de edad con una enfermedad clínicamente compatible y una gripe confirmada por laboratorio. La confirmación de la infección por el virus de la gripe puede ocurrir antes o después de la muerte, y necesita del hallazgo de influenza A o B en al menos uno de los siguientes métodos de laboratorio: una prueba de diagnóstico rápido del virus de la gripe, o determinación inmunoenzimática, el aislamiento del virus en un cultivo tisular, la tinción de anticuerpos fluorescentes, la reacción en cadena de la polimerasa de transcripción inversa (RT-PCR) o la tinción inmunohistoquímica de las muestras tisulares. La mayoría de las muestras se estudió respecto a la gripe en los laboratorios del hospital, la sanidad local o la estatal, y se pudo determinar el subtipo de algunos virus influenza A.
A efectos de la supervisión de la gripe, la estación de la gripe se define entre el 1 de octubre y el 30 de septiembre del año siguiente. Los servicios de salud estatal y local informan al CDC de los casos de mortalidad pediátrica asociada con la gripe mediante impresos de notificación normalizados que incluyen información demográfica, la fecha y el lugar del fallecimiento, los resultados de los estudios de laboratorio, la historia clínica, el estado de la vacuna contra la gripe, la asistencia médica recibida en relación con la enfermedad y la coinfección bacteriana o fúngica de puntos no estériles y otras informaciones clínicas relevantes. Los niños con enfermedades crónicas reconocidas por el Advisory Committee on Immunization Practices (ACIP) como indicación de la vacuna contra la gripe fueron calificados como afectados por una alteración de alto riesgo definido por el ACIP10*. En la estación de la gripe 2004-2005 se recomendaba la vacuna anual contra la gripe a todos los niños de 6-23 meses de edad; desde la estación de 2006-2007 se recomienda la vacuna contra la gripe de todos los niños de 6-59 meses de edad. El ACIP recomienda que los niños de < 9 años de edad reciban 2 dosis de vacuna contra la gripe en la primera estación en la que se vacunen. El niño se consideró totalmente vacunado cuando disponía de documentación que verificase que había recibido la vacuna contra la gripe en el número adecuado de dosis al menos 14 días antes del inicio de la enfermedad. Además, los niños de < 9 años de edad se calificaron de “totalmente vacunados” por la definición anterior; “totalmente vacunados según la historia” si se habían vacunado contra la gripe actual al menos 14 días antes del inicio de la enfermedad actual y se habían vacunado en el año anterior según la historia, pero sin documentación; “parcialmente vacunados” si se habían vacunado contra la gripe actual al menos 14 días antes del inicio de la enfermedad pero sin vacunación previa y “parcialmente vacunados con falta de información” si se habían vacunado contra la gripe actual al menos 14 días antes del inicio de la enfermedad y se carecía de información sobre la vacunación previa.
Los datos se introdujeron en Microsoft Access 2002 y se analizaron en SPSS (versión 15). Se utilizó el estadístico µ2 para evaluar las diferencias estadísticamente significativas entre las proporciones de dos o más grupos. Cuando estuvo indicado, se utilizó la corrección de Yates por continuidad para evitar la sobrevaloración de la significación estadística por el tamaño de la celda. Todas las comparaciones fueron bilaterales, y los valores de p < 0,05 se consideraron significativos.
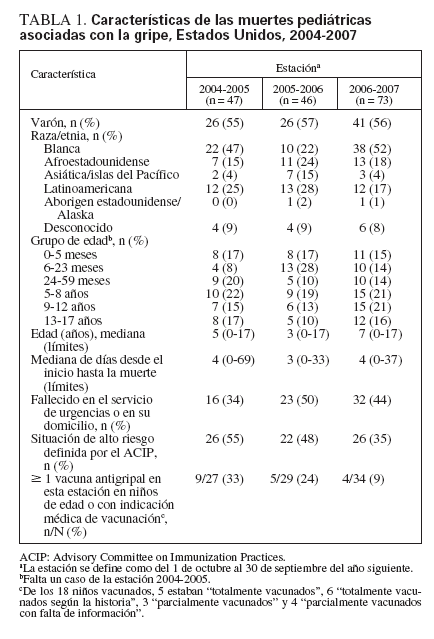
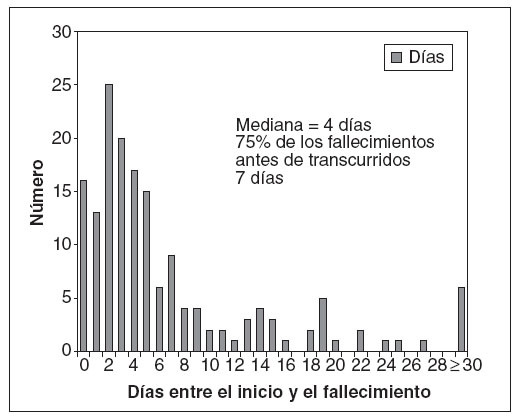
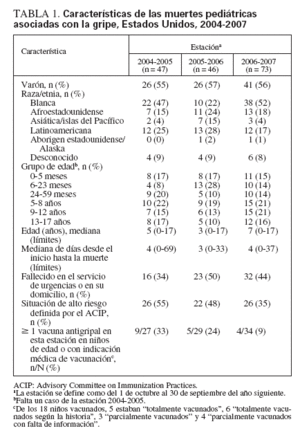
RESULTADOSEntre el 1 de octubre de 2004 y el 30 de septiembre de 2007, 41 jurisdicciones (39 servicios de salud estatales y 2 locales) informaron de 166 muertes pediátricas asociadas con la gripe. El número de fallecimientos fue casi igual durante las dos primeras estaciones de la revisión y aumentó en la tercera (n = 47, 46 y 73, respectivamente) (tabla 1). Algo menos de la mitad de los fallecidos fueron niños y la mayoría eran de raza blanca, afroamericanos o latinoamericanos. La mediana de edad en años varió según la estación y fue máxima (7 años) en la estación de 2006-2007. La mediana del número de días transcurrido entre el inicio de la gripe y el fallecimiento osciló entre 3 y 4 días, y el 75% de las muertes ocurrió antes de transcurridos 7 días (fig. 1). El cuarenta y cuatro por ciento de los niños falleció en el domicilio o en el servicio de urgencias. Durante tres estaciones, 74 niños (45%) tenían una alteración de alto riesgo definida por el ACIP (26, 22 y 26 niños, respectivamente, en estas estaciones). La proporción de niños con una enfermedad crónica subyacente de alto riesgo disminuyó desde el 55% en la estación de la gripe de 2004-2005 y el 34% en la de 2006-2007. Las alteraciones de alto riesgo informadas con mayor frecuencia fueron el asma (n = 23), el trastorno convulsivo (n = 16) y el trastorno neuromuscular, incluyendo la parálisis cerebral (n = 15). Algunos niños tuvieron más de una alteración de alto riesgo.
TABLA 1. Características de las muertes pediátricas asociadas con la gripe, Estados Unidos, 2004-2007
Fig. 1. Número de días entre el inicio de la gripe y el fallecimiento asociado con la gripe, Estados Unidos, 2004-2007.
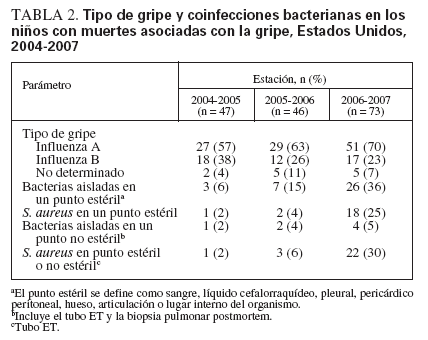
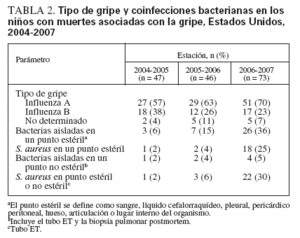
Pocos niños con indicación de vacuna contra la gripe habían sido vacunados en la estación en la que murieron. De los 90 niños con una alteración de alto riesgo, relacionada con la edad o definida por el ACIP, a quienes se recomienda la vacuna, 18 (20%) estaban al menos parcialmente vacunados µ14 días antes del inicio de la enfermedad (33%, 24% y 9% por estación en 2004-2005, 2005-2006 y 2006-2007, respectivamente) (tabla 1). Un niño parcialmente vacunado no sufrió alteración de riesgo relacionada con la edad ni definida por el ACIP de vacunación recomendada. Se dispuso de los datos de las complicaciones de la gripe en 73 niños; las más frecuentes fueron neumonía (n = 59), coinfección bacteriana invasora (n = 36), SDRA (n = 30), convulsiones (n = 23), encefalopatía (n = 18) y shock (n = 16). No se dispuso de la información sobre el tratamiento antiviral. Las infecciones por el virus de la gripe, tanto A como B, se asociaron con muerte pediátrica. No se identificó un tipo predominante de virus de la gripe entre los fallecidos y la distribución de los tipos del virus de la gripe no fue distinta entre los casos de las tres estaciones (tabla 2).
TABLA 2. Tipo de gripe y coinfecciones bacterianas en los niños con muertes asociadas con la gripe, Estados Unidos, 2004-2007
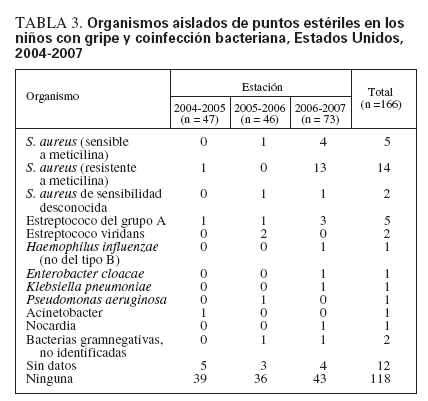
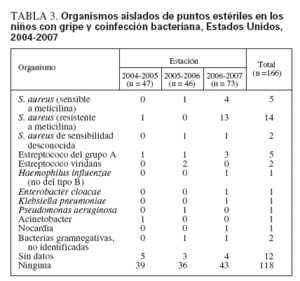
La coinfección bacteriana aumentó sustancialmente durante las tres estaciones de la gripe (6%, 15% y 33%, respectivamente). S. aureus fue la bacteria patógena identificada con mayor frecuencia, y produjo una gran proporción del aumento de la coinfección bacteriana en 2006-2007, comparado con las dos estaciones anteriores (tabla 2). S. aureus se aisló de un punto estéril en un niño (2%) en 2004-2005, dos niños (4%) en 2005-2006 y 18 niños (25%) en 2006-2007 (tabla 2). S. aureus se aisló del cultivo del tubo endotraqueal en un niño en 2005-2006 (2%) y en 4 niños en 2006-2007 (6%). En conjunto, S. aureus se aisló de un lugar estéril o en el cultivo del tubo endotraqueal en un niño en 2004-2005, tres niños en 2005-2006 y 22 niños en 2006-2007 (tabla 2). De las 26 infecciones por S. aureus identificadas, 15 (60%) correspondieron a S. aureus resistente a meticilina (MRSA), 6 a S. aureus sensible a meticilina (MSSA) y 5 a S. aureus con sensibilidad desconocida (tabla 3). No se tomó información acerca de la fecha del cultivo bacteriano, y no se pudo determinar si la coinfección con S. aureus estaba asociada a la comunidad o se había contraído en el hospital.
TABLA 3. Organismos aislados de puntos estériles en los niños con gripe y coinfección bacteriana, Estados Unidos, 2004-2007
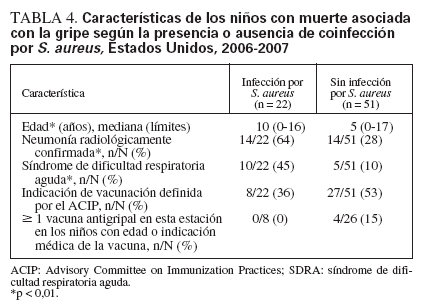
Se evaluaron las características de los niños con y sin coinfección S. aureus-gripe en la estación de 2006-2007 (tabla 4). Los niños con coinfección tuvieron una edad significativamente mayor, y mayor probabilidad de padecer una neumonía o un síndrome de dificultad respiratoria aguda (SDRA) confirmados radiológicamente. La proporción de niños con una situación de alto riesgo definida por el ACIP o que había recibido la vacuna contra la gripe (tabla 4) fue similar, con independencia de la presencia de coinfección por S. aureus.
TABLA 4. Características de los niños con muerte asociada con la gripe según la presencia o ausencia de coinfección por S. aureus,Estados Unidos, 2006-2007
ANÁLISISEste informe describe 166 casos de fallecimientos asociados con la gripe, confirmada por el laboratorio, ocurridos durante las estaciones de la gripe de 20042005, 2005-2006 y 2006-2007 y fueron notificados a los CDC. Destacan varias características de niños que murieron de complicaciones asociadas con la gripe. La gripe fue, a menudo, rápidamente fatal, ya que casi la mitad de los niños fallecieron antes de transcurridas 72 h del inicio de los síntomas y el 75% antes de los siete días; casi la mitad murió en su domicilio o en el servicio de urgencias. El número de coinfecciones bacterianas aumentó sustancialmente en 2006-2007 y la mayoría de las infecciones estuvo causada por S. aureus, principalmente MRSA. Finalmente, muchas muertes correspondieron a niños sin una alteración o edad que les hiciera candidatos a la vacunación. Aun así, de las muertes en niños con indicación para la vacuna contra la gripe, sólo el 21% había sido vacunado durante la estación en que murieron. Este aumento de las muertes pediátricas y de la coinfección bacteriana se produjo en el contexto de las estaciones de una gripe relativamente leve en 20052006 y 2006-2007.
La rápida progresión a la muerte en muchos de los niños de este estudio concuerda con los fallecimientos pediátricos causados por la gripe y notificados en la estación de la gripe de 2003-2004, en los que casi la mitad de las muertes asociadas con la gripe ocurrió fuera del marco hospitalario o en el servicio de urgencias9. En ambos estudios, la mayoría de las muertes se produjo en niños anteriormente sanos sin una alteración médica subyacente, y pocos de los niños con indicación de vacuna contra la gripe estaban vacunados9. Los niños de nuestro estudio experimentaron una amplia gama de complicaciones, similar a los previamente asociados con la gripe grave, incluyendo la neumonía, la coinfección bacteriana, el SDRA, las convulsiones, la encefalopatía y el shock11,12. Los mecanismos de estas muertes asociadas con la gripe son desconocidos, pero algunos podrían consistir en una respuesta inflamatoria anormal del anfitrión a la infección por el virus de la gripe. La gripe y la enfermedad gripal también se han asociado con el síndrome del shock tóxico por S. aureus13. Sin embargo, nuestro estudio no recogió los criterios clínicos del síndrome del shock tóxico por S. aureus para poder determinar su presencia.
Existen varios mecanismos teóricos por los que las infecciones por el virus de la gripe aumentan el riesgo de coinfección bacteriana posterior. El virus de la gripe lesiona la capa de células epiteliales del árbol traqueobronquial, fomentando así la adherencia estafilocócico14,15. El aumento de la adherencia podría estar mediado por la actividad neuraminidasa del virus de la gripe, que aumenta la adherencia bacteriana de 2 a 4 veces en los modelos in vitro que utilizan células alveolares humanas15. El virus de la gripe deprime la respuesta respiratoria en salvas y la función fagocitaria de los neutrófilos y los macrófagos, lo que podría facilitar el desarrollo de una infección bacteriana secundaria15-18.
La proporción de niños con coinfección bacteriana aumentó a más del quíntuplo entre las estaciones de la gripe de 2004-2005 y 2006-2007, debiéndose casi todo el aumento a las coinfecciones por S. aureus. Bhat et al observaron que 24 de los 102 niños con datos y que fallecieron por complicaciones asociadas con la gripe durante la estación de la gripe de 2003-2004 mostraron pruebas de coinfección bacteriana, incluyendo 6 casos con coinfección con MRSA y 5 con MSSA o S. aureus con sensibilidad desconocida9. En el siglo pasado se informó de neumonía y sepsis por S. aureus asociada con la gripe en niños y adultos previamente sanos7,8. Durante la pandemia de 1957 se describió una neumonía por S. aureus asociada con la gripe con antecedente de infección estafilocócica de partes blandas19 (IEPB). Se ha notificado la sepsis fulminante causada por S. aureus en lactantes20 y niños mayores21, y varios estudios han demostrado que el antecedente reciente de IEPB en el paciente o en un miembro de su familia suele predecir a la infección invasora, y se han descrito agrupaciones familiares de infección estafilocócica invasora20,22-25.
Cerca del 30-40% de los niños está colonizado por S. aureus; la prevalencia de la colonización es máxima entre los niños de 6-11 años de edad26-28. Aunque la frecuencia de portador nasal de S. aureus no ha aumentado significativamente, la de portador nasal de MRSA ha aumentado. En 2001, los datos de una revisión de portadores, representativa de la nación, indicó que el 0,8% de la población estadounidense está colonizada26; en 20032004, los datos del mismo estudio señalaron que el 1,5% de la población estadounidense está colonizada29. En 2001, los datos de una gran consulta pediátrica de atención primaria de Tennessee demostraron una tasa de colonización del 0,8%30. En 2005, la repetición de la revisión en la misma consulta pediátrica de atención primaria en Tennessee encontró que la tasa de portador nasal de MRSA superó el 9%30. Se ha informado que la tasa de portador nasal de MRSA llega al 22% en los nuevos ingresos en un hospital pediátrico; el 92% de los niños con MRSA no era portador previamente conocido de MRSA, aunque algunos tenían factores de riesgo de colonización por MSRA28,31-33. Además de la resistencia antibiótica, existen pruebas recientes de que muchos de estos MRSA aislados corresponden a la cepa USA30020,33, que se ha asociado con la toxina leucidina Panton-Valentine (PVL), un importante factor de virulencia relacionado con la neumonía necrosante y las lesiones cutáneas necróticas34. A medida que aumenta la tasa de portador nasal de MRSA, existen posibilidades de crecimiento de la coinfección con MRSA y el virus de la gripe, lo que produce intensa morbilidad y mortalidad en los niños.
La vacuna de la gripe sigue siendo la principal estrategia de prevención de la gripe y sus complicaciones asociadas. En la actualidad, todos los niños de 659 meses de edad y los que padecen determinadas alteraciones crónicas subyacentes deberían recibir una vacuna anual de la gripe. Sin embargo, sólo el 21% de los casos a quienes se había recomendado la vacuna anual había recibido la vacuna contra la gripe. Destaca que el 46% de los casos no cumplió los actuales criterios de vacunación contra la gripe, aunque la vacunación pudiera haber sido indicada en algunos niños por los contactos con personas en alto riesgo de complicaciones de la gripe. Los valores de cobertura de la vacuna contra la gripe en los niños en alto riesgo de complicaciones de la gripe siguen siendo muy bajos. Sólo cerca del 21% de los niños de 6-23 meses de edad estaba totalmente vacunado contra la gripe durante la estación de la gripe de 2005-200635 y los datos del registro de vacunación indican que la cobertura en la estación 2006-2007 fue similar36. Esto indica que se debe realizar grandes esfuerzos para aumentar la cobertura de la vacuna contra la gripe en los grupos objetivo. La vacuna contra la gripe puede disminuir las complicaciones de la gripe, como la otitis media aguda y la neumonía, en los niños pequeños y los adultos37-39. Al disminuir el riesgo de gripe, presumiblemente también disminuyen las infecciones bacterianas invasoras facilitadas por la alteración de las defensas del anfitrión durante la infección por el virus de la gripe.
Varios estudios han demostrado la eficacia del tratamiento antiviral para prevenir las complicaciones secundarias. El tratamiento temprano con el inhibidor de la neuraminidasa oseltamavir disminuyó en un 44% el desarrollo de la otitis media en los niños40, así como el desarrollo de varias complicaciones bacterianas secundarias (sinusitis, bronquitis o neumonía) que necesitan antibióticos en adultos previamente sanos41. Se desconoce el mecanismo por el que los inhibidores de la neuraminidasa disminuyen las complicaciones bacterianas, pero podría estar asociado con la inactivación de la neuraminidasa viral y la eliminación de su capacidad para facilitar la adherencia bacteriana15,42,43. Según los estudios preclínicos, se ha propuesto que incluso el tratamiento tardío con inhibidores de la neuraminidasa podría prevenir las complicaciones asociadas con la gripe, aunque puede no modificar el curso de la infección por el virus de la gripe15,42. Un reciente estudio de la eficacia del tratamiento de los pacientes adultos hospitalizados con oseltamivir consiguió la disminución de las complicaciones y la mortalidad de la gripe, aunque el tratamiento comenzase 2 días después del inicio de la enfermedad44.
Nuestros hallazgos están sujetos a varias posibles limitaciones, que podrían desembocar en una infravaloración de las muertes por gripe y las coinfecciones bacterianas en los niños. La integridad de las notificaciones de la mortalidad pediátrica asociada con la gripe fue variable, y menor en los niños que no habían sido hospitalizados. Es probable la infranotificación de las muertes pediátricas asociadas con la gripe, porque la notificación de la muerte pediátrica asociada con la gripe sólo es obligatoria desde 2004. Las obligaciones estatales de notificación han aumentado durante los tres últimos años, y en la actualidad 42 estados obligan a la declaración. Sin embargo, los aumentos de la notificación afectarían a la cifra total de informes remitidos, pero no a la proporción de casos con coinfección bacteriana. Los bajos valores de estudio de la gripe en los niños también podrían contribuir a la infranotificación. Pese a la disponibilidad y la utilidad de las pruebas de la gripe, aún no se ha incorporado al estudio diagnóstico habitual de la mayoría de los niños visitados en atención primaria o en el servicio de urgencias con una enfermedad gripal45. Además, los médicos pueden no solicitar el estudio diagnóstico de la gripe en los casos graves y los datos clínicos se limitan a los pacientes fallecidos en su domicilio o en un servicio de urgencias. No todos los casos fallecidos fuera del hospital se someten a una exploración postmortem. Incluso de los remitidos a la exploración postmortem, no a todos se realiza el estudio diagnóstico estafilocócico o de la gripe en las muestras necrópsicas46. No recogemos sistemáticamente información sobre las bacterias aisladas de lugares no estériles (como el tubo endotraqueal), lo que podría haber descubierto otros casos de neumonía bacteriana en los niños con infección fatal por el virus de la gripe. Por lo tanto, podemos haber infravalorado la proporción de casos con coinfecciones bacterianas, incluyendo la debida a S. aureus. Además, nuestros hallazgos constituyen una infravaloración del MRSA grave y la gripe porque no incluimos los casos graves no fatales.
La mortalidad pediátrica asociada con la gripe es rara, pero la proporción de casos en los que se identificó S. aureus aumentó al quíntuplo durante las tres últimas estaciones de la gripe. Las crecientes tasas de portadores nasales de MRSA pueden aumentar la posibilidad de coinfección por MRSA y el virus de la gripe, provocando morbilidad grave y mortalidad en los niños. La vacuna contra la gripe sigue siendo la principal estrategia de prevención de la gripe. Aunque los esfuerzos de vacunación deberían centrarse en los niños en máximo riesgo de enfermedad grave y de complicaciones, todo niño que desee (o cuyos padres deseen) disminuir su riesgo de infección gripal debe ser vacunado. También deben vacunarse los niños que conviven con personas en alto riesgo de complicaciones de la gripe. En febrero de 2008, el ACIP recomendó la vacuna anual contra la gripe a todos los niños de 6 meses a 18 años de edad, con implementación gradual durante los dos próximos años47.
CONCLUSIONESLos niños en riesgo de complicaciones de la gripe o los niños sanos con enfermedad respiratoria moderada o grave deben ser estudiados respecto a la gripe y, si están infectados, deben recibir tratamiento con oseltamivir o zanamivir48. Los médicos deben considerar el tratamiento con vancomicina u otro antibiótico de los niños con sospecha de neumonía por S. aureus durante la estación de la gripe para tratar el MRSA si residen en áreas con gran prevalencia de MRSA24 o tienen factores de riesgo de la infección por MRSA (como alteraciones subyacentes, antecedente de colonización o infección por MRSA). Es necesario realizar otros estudios para evaluar los factores de riesgo de coinfección con la gripe y bacterias patógenas, para valorar el aumento de la vacunación antigripal en los niños y determinar el papel de la vacuna contra la gripe y de los agentes antivirales en la prevención de la morbilidad grave y la mortalidad causadas por la gripe entre los niños.
*Los niños con enfermedades de alto riesgo definidas por el ACIP incluyen a los que reciben tratamiento a largo plazo con aspirina, los que tienen una enfermedad pulmonar crónica (incluyendo el asma), cardiovascular (excepto la hipertensión), renal, hepática, hematológica o metabólica (incluyendo la diabetes sacarina), inmunodepresión o cualquier alteración (como la disfunción cognitiva, las lesiones de la médula espinal, los trastornos convulsivos u otros desórdenes neuromusculares) que pueda comprometer la función respiratoria o el manejo de las secreciones respiratorias o que pueda aumentar el riesgo de aspiración.
Correspondencia: Lyn Finelli, DrPH, Centers for Disease Control and Prevention, Influenza Division, 1600 Clifton Rd, NE, MS A-32, Atlanta, GA 30333, Estados Unidos.
Correo electrónico: lfinelli@cdc.gov