En el ser humano, el cinc es un micronutriente esencial para la síntesis de proteínas, el crecimiento y la diferenciación celular1,2. Se ha demostrado que un déficit grave de este oligoelemento se asocia con la detención del crecimiento, hipogonadismo, deterioro de la función inmune, problemas cutáneos, disfunción cognitiva y anorexia2,3.
El déficit dietético de cinc es frecuente en diversas partes del mundo, en particular en los países en desarrollo. Este déficit puede originarse a partir de la ingesta insuficiente de alimentos que contienen cinc (sobre todo de origen animal) o de una falta de absorción debido a su unión a las fibras y fitatos, que, en general, están presentes en los cereales, frutos secos y legumbres4. La absorción insuficiente de este micronutriente también puede ser consecuencia de las anomalías de la mucosa y del compromiso de la integridad intestinal inducidos por una diarrea persistente debida a infecciones gastrointestinales5.
Numerosos estudios han examinado la asociación de la morbilidad infantil y el déficit de este micronutrien-1,6-9. Estos estudios sugieren que las poblaciones con un déficit de cinc corren un mayor riesgo de desarrollar enfermedades diarreicas, infecciones respiratorias, y retraso del crecimiento. Utilizando los datos disponibles, Caulfield y Black estimaron que, en todo el mundo, el déficit de cinc se asocia con un exceso de muertes de casi 800.000 anuales entre niños menores de cinco años de edad, incluidas las debidas a diarrea (176.000), neumonía (406.00), y paludismo10 (207.000). Además, estos autores atribuyeron al déficit de cinc una pérdida global de casi 28 millones de años de vida ajustada a la discapacidad.
La administración de cinc se ha estudiado como instrumento en el tratamiento y prevención de la diarrea, infecciones respiratorias, neumonía e infecciones agudas de las vías respiratorias inferiores (IARI) y el paludismo entre niños11-18. En un metaanálisis se demostró que la adición de cinc a la estrategia terapéutica de niños con diarrea dio lugar a una disminución de la duración y frecuencia de la diarrea persistente, definida como la que persistió más de 14 días19.
Estos estudios han dado lugar a la administración de suplementos de este micronutriente entre niños en una tentativa de tratar y prevenir las infecciones habituales de la infancia. Unos pocos estudios también han examinado su efecto sobre los parámetros del crecimiento20-25. En un metaanálisis publicado en 1999 se demostró que los suplementos continuos de cinc no se asociaron con una disminución de las tasas de diarrea y neumonía infantil26. Desde entonces, se han publicados estudios adicionales a mayor escala y de ámbito más amplio que los incluidos en el metaanálisis previo. Además, dicho metaanálisis incluyó estudios en los que los suplementos se administraron durante períodos tan breves como de 2 semanas. Es probable que los programas de administración suplementos a niños se instauren para duraciones más prolongadas, extendiéndose durante al menos unos pocos meses. Por esta razón, consideramos que el tema merecía un nuevo examen y condujimos un metaanálisis de los estudios publicados que examinaron la eficacia de los suplementos de este micronutriente administrados durante como mínimo 3 meses en la prevención de la diarrea y las enfermedades respiratorias entre niños.
MÉTODOSProtocolo de investigación y revisión de estudioPara identificar los estudios que habían examinado el efecto de los suplementos de cinc sobre la incidencia de diarrea o de infecciones respiratorias, se efectuó una búsqueda en las bases de datos PubMed, Science Citation Index y Cochrane Central Database of Controlled Trials utilizando las palabras clave siguientes: “zinc” (cinc), “supplement” (suplemento), “AND” (Y) “diarrea” (diarrea)” “OR” (O) “respiratory illness” (enfermedades respiratorias) “OR” (O) “pneumonia” (neumonía). Las búsquedas captaron los estudios publicados hasta noviembre de 2005. Dos autores independientes revisaron los resultados de la búsqueda para identificar los ensayos clínicos originales efectuados en seres humanos o de campo. Se excluyeron del análisis los estudios que prestaban atención a los efectos de la administración de cinc en el tratamiento de la diarrea aguda o persistente, o las enfermedades respiratorias. Sin embargo, se consideraron elegibles para la inclusión en el metaanálisis los estudios que reclutaron a niños restablecidos recientemente de una enfermedad diarreica y sometidos a observación para episodios diarreicos recurrentes, ulteriores. Se excluyeron los estudios publicados sobre suplementos de cinc administrados durante menos de 3 meses. Mediante una búsqueda manual de las listas bibliográficas de los estudios identificados originalmente sobre el papel terapéutico y profiláctico del cinc, se identificaron estudios adicionales, al igual que revisiones sobre el tema.
Dos autores (Aggarwal y Sentz) revisaron independientemente cada uno de los estudios identificados para determinar si cumplían los criterios mínimos de calidad, incluida a) la asignación aleatoria de la intervención activa y el placebo, b) la evaluación doble enmascarada de las variables analizadas y c) un seguimiento como mínimo > 90%. Además, identificaron los parámetros sobre los que estuvieron disponibles los datos de estos artículos con el objetivo de usarlos en el diseño de una hoja de extracción de datos. Ambos revisores extrajeron independientemente los datos de cada uno de los estudios seleccionados y cualquier diferencia entre ambos se resolvió a través de una revisión conjunta del manuscrito.
Métodos estadísticosDe los estudios seleccionados, se extrajeron los datos sobre el número de episodios de enfermedades diarreicas y respiratorias en los grupos tratados con suplementos de cinc y placebo. Cuando no se proporcionaban explícitamente dichos datos, se calcularon multiplicando el número medio de episodios de estas enfermedades por niño por el número total de individuos del estudio en cada grupo. A partir del número de episodios de la enfermedad y duración del seguimiento en el grupo que recibió suplementos y placebo, para cada estudio, se calcularon los cocientes de riesgo (CR) ajustados. Además, cuando estuvieron disponibles, se recuperaron los datos sobre las tasas de las formas graves de las enfermedades de interés (diarrea persistente de 14 días o más de duración; diarrea grave, en función de los criterios definidos por el investigador; infección de las vías respiratorias inferiores, neumonía, etc.).
Para el análisis estadístico y el metaanálisis se utilizó el programa estadístico Review Manager versión 4.2.8 (Nordic Cochrane Centre, Cochrane Collaboration, Copenhague). Los errores están-dar del logaritmo del CR se calcularon utilizando métodos estadísticos estándar. Se combinaron los datos de los diferentes estudios utilizando un método genérico de la varianza inversa, y, para cada parámetro, se calcularon un CR combinado y su error están-dar y los intervalos de confianza del 95%. Para cada parámetro, se probó la heterogeneidad entre estudios utilizando el estadístico 2 con sus grados de libertad (gl); además, también se calculó el estadístico I2 que determina el grado de incongruencia de los resultados entre los diversos estudios. Se consideró que estaba presente una heterogeneidad significativa si el valor de p fue inferior a 0,10. Cuando no se identificó una heterogeneidad significativa (p µ 0,10), se utilizó un modelo de efectos fijos para combinar los datos de los diversos estudios; en los casos con una heterogeneidad significativa (p < 0,10), se utilizó un modelo de efectos aleatorios para proporcionar una estimación más conservadora del efecto. En este último caso, los datos se examinaron adicionalmente utilizando análisis de subgrupo para evaluar las posibles causas de la heterogeneidad.
Se examinó el sesgo de publicación utilizando un análisis de gráfico en embudo, y se cuantificó utilizando el método de la correlación del rango de Begg y el método de la intercepción de la regresión de Egger27,28, considerándose significativos valores de p < 0,10. Además, para imputar los estudios omitidos y calcular de nuevo el efecto combinado añadiendo estos estudios omitidos, se utilizó el método de podar y completar de Duvall y Tweedie29,30.
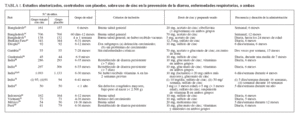
RESULTADOSIdentificación de los estudiosEn la tabla 1 se citan los estudios clínicos o de campo identificados en la búsqueda de los ensayos publicados que evaluaban el papel del cinc en la prevención de la diarrea o las enfermedades respiratorias15,16,23,24,31-43. Por diversas razones, se excluyeron cuatro estudios adicionales21,22,25,44que examinaban el efecto profiláctico de los suplementos de cinc sobre estas enfermedades. De éstos, uno se excluyó porque la asignación de los individuos del estudio al grupo cinc o placebo no fue aleatoria22. Otro estudio se consideró inelegible porque estudiaba la morbilidad entre recién nacidos cuyas madres habían recibido suplementos de cinc durante el embarazo45. Un estudio conducido en Brasil incluía dos grupos diferentes de suplementos de cinc (1 mg/día y 5 mg/día); la asignación al último grupo no fue aleatorizada ni concurrente con la del grupo placebo, por lo que no fue elegible para el metaanálisis21. Los datos del otro grupo de este estudio que recibió suplementos de cinc (1 mg/día) tuvieron que excluirse debido al hecho de que los datos publicados no permitían la extracción de los parámetros usados en el presente análisis. Por último, en un ensayo con un diseño de estudio factorial, se utilizaron el cinc y la “estimación psicosocial” como intervención dirigida a mejorar la interacción madre-hijo asignándose las intervenciones de manera aleatorizada y no aleatorizada, respectivamente. Este estudio tuvo que excluirse porque el artículo publicado no permitía la extracción de datos para los grupos que recibieron cinc y placebo respectivamente, sin la estimulación psicosocial. Así mismo, los datos se presentaban como medianas de grupo lo que impedía el cálculo del número total de episodios de enfermedad.
TABLA 1. Estudios aleatorizados, controlados con placebo, sobre uso de cinc en la prevención de la diarrea, enfermedades respiratorias, o ambas
En el metaanálisis se incluyó un total de 17 estu-15,16,23,24,31-42. De éstos, en un estudio36 hubo 2 grupos de intervención con frecuencias diferentes de administración de los suplementos de cinc (diaria o semanal); para el análisis, cada uno de los grupos de tratamiento se consideró como un estudio separado. El texto que sigue hace referencia a estos ensayos como estudios independientes. En dos estudios publicados se describía la misma población por separado para los resultados de morbilidad diarreica y respiratoria, respectivamente35,43. Se analizaron los datos de los 17 estudios, que incluyeron a 3.819 niños tratados con suplementos de cinc y 3.840 tratados con placebo. En la tabla 2 se citan algunos de los otros estudios excluidos con las razones para su exclusión20,44,46-48.
Prevención de la diarreaDe los 17 estudios elegibles, 15 proporcionaban datos sobre el número de episodios de diarrea entre grupos tratados con un suplemento de cinc o el correspondiente15,16,23,24,31-40.
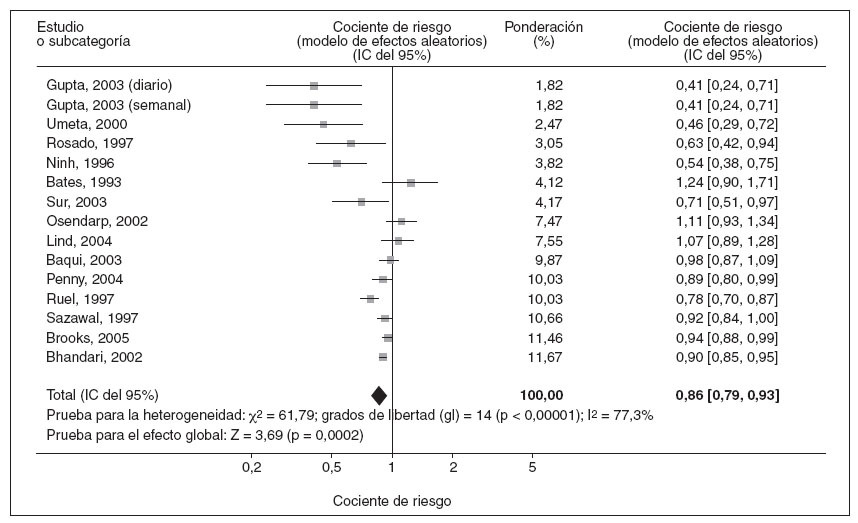
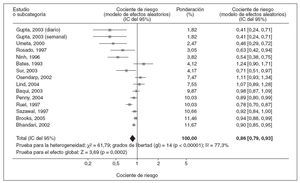
En la figura 1 se muestran los resultados del metaanálisis para la incidencia de diarrea entre niños tratados con suplementos de cinc o el correspondiente placebo. De los 15 estudios, en 3 los cocientes de riesgo superaban 1,0, y en 12, el valor era más bajo. Utilizando un modelo de efectos aleatorios, el análisis del presente estudio reveló que los suplementos de cinc se asociaron con una reducción significativa de la incidencia de episodios de diarrea en un 14% (CR 0,86, IC del 95% = 0,79-0,93).
Fig. 1. Metaanálisis de los cocientes de riesgo de incidencia de episodios de diarrea en niños tratados con suplementos de cinc o placebo. IC: intervalo de confianza.
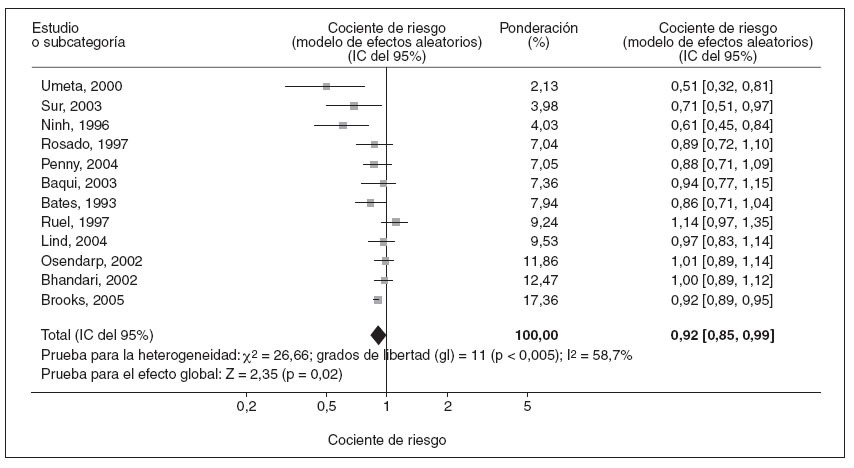
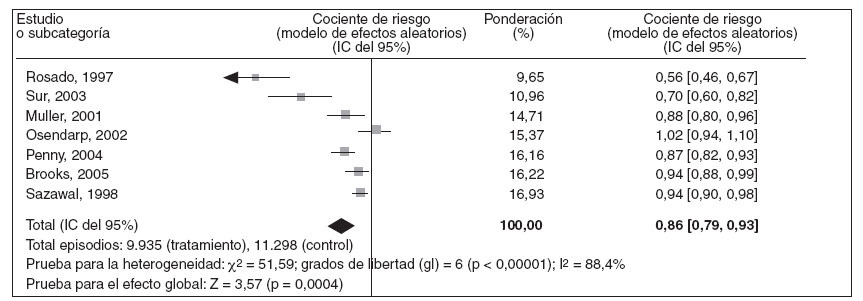
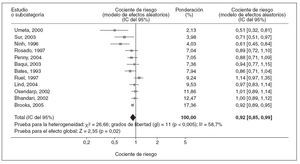
Prevención de las enfermedades respiratoriasEn 12 estudios estuvieron disponibles datos sobre la frecuencia de enfermedades respiratorias, e incluyeron a 2.709 niños tratados con suplementos de cinc y a 2.803 niños tratados con el correspondiente place-15,16,23,24,31-34,37,39,40,43. Los datos combinados revelaron una reducción del 8% en la incidencia de enfermedades respiratorias entre niños tratados con suplementos de cinc con un CR combinado en el modelo de efectos aleatorios de 0,92 (IC del 95% = 0,85-0,99; fig. 2).
TABLA 2.Lista de estudios identificados durante la búsqueda inicial pero excluidos más tarde, junto con las razones de su exclusión
Fig. 2. Metaanálisis de los cocientes de riesgo de incidencia de episodios de enfermedades respiratorias en niños tratados con suplementos de cinc o placebo. IC: intervalo de confianza.
Prevención de las formas graves de enfermedad diarreica
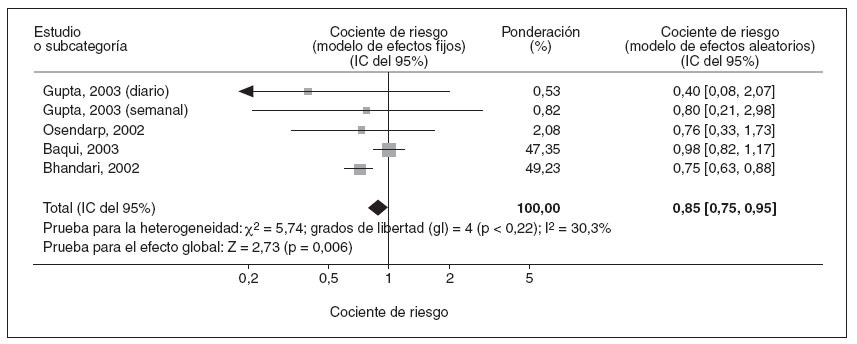
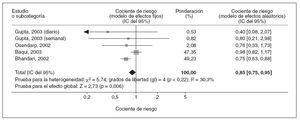
Los datos sobre los cocientes de riesgo de incidencia de enfermedad diarreica grave, incluida la diarrea grave o enfermedad disentérica, estuvieron disponibles en 5 estudios15,31,35,36. Para esta enfermedad en niños tratados con suplementos de cinc comparado con los que recibieron placebo, el cociente de riesgo combinado del modelo de efectos fijos fue de 0,85 (IC del 95% = 0,75-0,95), indicando una reducción significativa de la frecuencia de diarrea grave (fig. 3). Utilizando el modelo de efectos aleatorios, el cociente de riesgo combinado fue de 0,84 (IC del 95% = 0,70-1,01).
Fig. 3. Metaanálisis de los cocientes de riesgo de incidencia de episodios de diarrea grave y/o disentería en niños tratados con suplementos de cinc o placebo. IC: intervalo de confianza.
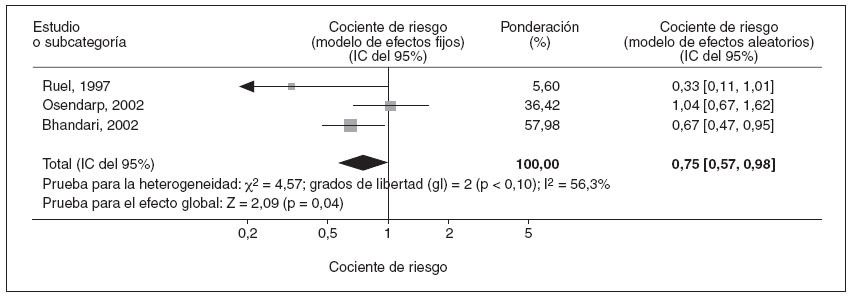
En tres estudios se proporcionaban datos sobre los cocientes de riesgo de la incidencia de episodios de diarrea persistente31,34,35. Un análisis combinado de estos estudios utilizando un modelo de efectos fijos demostró una reducción significativa de estas enfermedades, con un cociente de riesgo combinado de 0,75 (IC del 95% = 0,57-0,98) para la incidencia de diarrea persistente en niños tratados con suplementos de cinc comparado con los que recibieron placebo (fig. 4). No fue posible utilizar el modelo de efectos aleatorios debido al reducido número de estudios disponibles.
Fig. 4. Metaanálisis de los cocientes de riesgo de incidencia de episodios de diarrea persistente en niños tratados con suplementos de cinc o placebo. IC: intervalo de confianza.
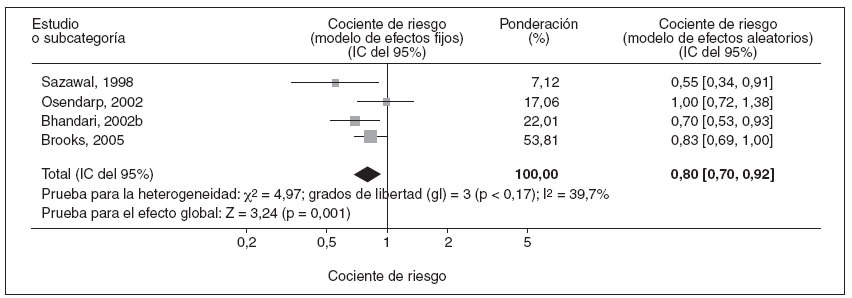
Prevención de la enfermedad respiratoria graveEn 4 estudios se proporcionaban datos para la comparación de las tasas de incidencia de enfermedad respiratoria grave, descrita de forma variable como neumonía o infección de las vías respiratorias inferiores16,31,42,43. Para dichas enfermedades la estimación combinada del cociente de riesgo mediante el modelo de efectos fijos fue de 0,80 (IC del 95% = 0,70-0,92; fig. 5), indicativo de una reducción significativa de la frecuencia de estas enfermedades. Usando el modelo de efectos aleatorios, el cociente de riesgo combinado fue de 0,79 (IC del 95% = 0,65-0,95).
Fig. 5. Metaanálisis de los cocientes de riesgo de incidencia de episodios de infecciones de las vías respiratorias inferiores o neumonía en niños tratados con suplementos de cinc o placebo. IC: intervalo de confianza.
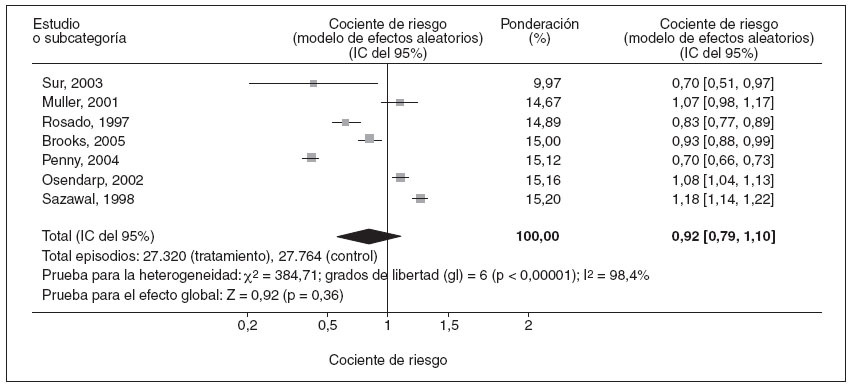
Duración de la diarrea y la enfermedad respiratoriaEn la reducción del número de días con diarrea o enfermedad respiratoria (figs. 6 y 7, respectivamente) la eficacia combinada del cinc fue de 0,86 (IC del 95% = 0,79-0,93) y 0,92 (IC del 95% = 0,78-1,10), respectivamente; de ellas, esta última no fue estadísticamente significativa.
Fig. 6. Metaanálisis de los cocientes de riesgo de número de días con diarrea en niños tratados con suplementos de cinc o placebo. IC: intervalo de confianza.
Fig. 7. Metaanálisis de los cocientes de riesgo de número de días con enfermedad respiratoria en niños tratados con suplementos de cinc o placebo. IC: intervalo de confianza.
Razones de la heterogeneidad entre estudiosLos análisis de subgrupo para el tipo de preparado de cinc utilizado, dosis total de cinc a la semana (70 mg o más comparado con menos de 70 mg) y la frecuencia de administración (diaria o menos) no explicaron la heterogeneidad entre estudios.
Los datos disponibles no permitieron evaluar los efectos de los suplementos de cinc por separado en niños con buen y mal estado nutricional, o de niños con un déficit y sin un déficit de cinc en el momento de la inclusión en el estudio.
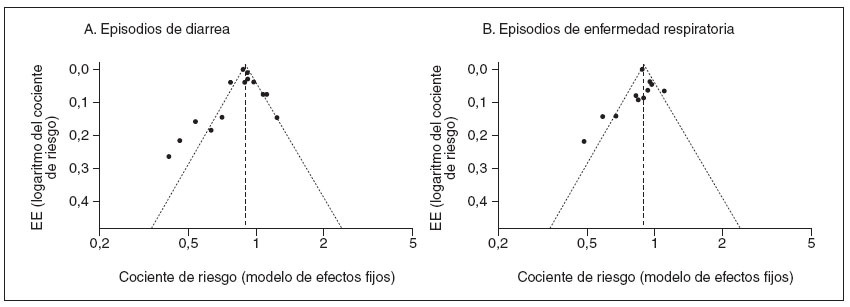
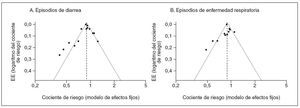
Sesgo de publicaciónPara evaluar si se produjo un sesgo en los estudios publicados en favor de aquellos con resultados positivos, representamos gráficamente el tamaño del efecto de cada ensayo frente a la varianza del efecto de la reducción en el número de episodios de diarrea o enfermedades respiratorias. En ausencia de un sesgo de publicación es predecible que este gráfico tenga una forma semejante a un embudo invertido28. Los gráficos en embudo para ambos parámetros fueron casi idénticos (fig. 8) con un exceso de estudios favorables con una varianza alta y un número en apariencia limitado de estudios publicados de pequeño tamaño y un efecto negativo, lo que indica la existencia de un sesgo de publicación.
Fig. 8. Gráfico en embudo de los estudios sobre suplementos de cinc para la prevención de la diarrea o enfermedades respiratorias para evaluar la persistencia de un sesgo de publicación.
En los estudios efectuados acerca del efecto de los suplementos de cinc sobre la diarrea (p = 0,070) pero no sobre las enfermedades respiratorias (p = 0,340), el método de intercepción de la regresión de Egger indicó la presencia de un sesgo de publicación significativo. En los estudios sobre diarrea (p = 0,138) el método de correlación del rango de Begg no demostró la presencia de un sesgo de publicación significativo pero identificó pruebas de este sesgo en los estudios sobre enfermedad respiratoria (p = 0,029). El análisis de “podar y completar” para los estudios sobre diarrea demostró 3 estudios “omitidos” en la porción inferior derecha; después de la adición de estos estudios, se obtuvo un cociente de riesgo sumario de 0,90 (0,82-0,98). De forma parecida, hubo 3 estudios “omitidos” para las enfermedades respiratorias; tras la adición de éstos, el cociente de riesgo sumario fue de 0,95 (0,87-1,04).
DISCUSIÓNEl presente metaanálisis indica que en niños pequeños los suplementos de cinc dan lugar a una reducción del riesgo de diarrea e infecciones respiratorias en un 14% y 8%, respectivamente. Los suplementos también se asociaron con una reducción de la tasa de formas graves de estas enfermedades y del número de días con diarrea por niño. Sin embargo, no se identificó una reducción significativa del número de días con enfermedad respiratoria. En los estudios publicados se detectó una heterogeneidad significativa en los efectos profilácticos de la administración de cinc, con pruebas de un sesgo de publicación.
El presente metaanálisis prestó atención a la estimación del efecto de los suplementos de cinc sobre la reducción de la morbilidad infantil. En muchos países en desarrollo el déficit de cinc es habitual, y su origen es una ingesta dietética insuficiente o los problemas de absorción4. Se considera que es uno de los 10 principales factores que contribuyen a la carga de enfermedad entre niños procedentes de países en desarrollo49 y ha dado lugar a llamamientos para iniciar programas de suplementos y fortificación de los alimentos. Aunque varios estudios han evaluado la eficacia de los suplementos de cinc entre niños en la prevención de las infecciones, sus resultados han sido variables. El presente metaanálisis ofrece una revisión estructurada que resume los efectos de los suplementos de cinc y proporciona una eficacia cuantificada que contribuye a la formulación de normas relativas a implementar programas a gran escala de administración de suplementos de cinc. Proporciona pruebas de que es probable que estos programas reduzcan la morbilidad debida a diarrea e infecciones respiratorias aunque es posible que la proporción prevenida sea modesta.
Los hallazgos del presente metaanálisis de una reducción de la frecuencia de diarrea y enfermedades respiratorias en niños tratados con suplementos de cinc indican que esta intervención sería útil en países en desarrollo donde el déficit de cinc es habitual y la mortalidad alta. Aunque el efecto de los suplementos sobre la morbilidad debida a infecciones infantiles fue modesto, el número absoluto de episodios de enfermedad prevenido sería amplio dado que la mayor parte de los niños menores de 5 años de edad experimentan como promedio diversos episodios al año. Puesto que se estima que más de 3,5 millones de niños fallecen de diarrea o enfermedad respiratoria49, efectos incluso muy modestos se traducirían en importantes reducciones absolutas de la morbimortalidad infantil49.
Las estimaciones proporcionadas por el presente metaanálisis permiten una mejor estimación de los beneficios de los suplementos de cinc. Se estima que, en todo el mundo, cada año se producen casi 2.000 millones de episodios de diarrea entre niños menores de 5 años de edad50. Utilizando la estimación combinada del presente estudio, sería de esperar que los suplementos de cinc previnieran 280 millones de episodios anuales de diarrea50. Además, los datos del presente metaanálisis son útiles para el cálculo de los cocientes de rentabilidad y coste/beneficio de la administración de suplementos de cinc en países en desarrollo.
El efecto relativamente modesto de los suplementos de cinc observado en el presente metaanálisis implica que esta intervención debe combinarse con otras destinadas a reducir la morbilidad infantil. La facilidad económica y la rentabilidad relativas de estas intervenciones contribuirían a determinar la prioridad de su implementación.
Por otra parte, una combinación de intervenciones sería sinergista, proporcionando la combinación un mayor beneficio que la suma de los beneficios previsibles si estas medidas se aplicaran individualmente, lo que mejoraría aun más su rentabilidad.
El presente metaanálisis se caracteriza por varios puntos fuertes. Sólo se incluyeron los estudios considerados de alta calidad porque cumplieron criterios estrictos de inclusión. Sólo se incluyeron los estudios aleatorizados, controlados con placebo, en los que los autores desconocían la asignación del tratamiento. Una evaluación enmascarada impide el sesgo del observador; esto es de particular importancia en los estudios sobre suplementos de cinc porque los análisis de las variables de estos estudios (es decir, incidencia de diarrea o enfermedad respiratoria y sus formas graves) son de naturaleza subjetiva. En segundo lugar, prestamos atención a excluir los estudios en los que la administración de cinc tuvo una finalidad terapéutica, mientras que en el metaanálisis previo sobre este tema26 se incluyeron dichos estudios, lo que habría dado lugar a una sobreestimación del efecto profiláctico potencial del cinc. Además, el presente metaanálisis incluye los resultados de los estudios a mayor escala sobre el tema, publicados hace poco tiempo. Por otra parte, si evidenciamos una heterogeneidad significativa, utilizamos un modelo más robusto de efectos aleatorios para combinar los resultados de los estudios publicados.
El presente análisis adolece de limitaciones inherentes. No tuvo en cuenta los efectos beneficiosos de los suplementos de cinc sobre el crecimiento lineal, citado con frecuencia como otro beneficio de este micronutriente. Tampoco consideramos el efecto de los suplementos sobre el paludismo. Sólo se ha examinado enunos pocos estudios en África18,33, demasiado limitados comparado con los efectuados sobre diarrea y enfermedades respiratorias. Así mismo, los resultados del presente análisis no serían aplicables a niños con infección por virus de la inmunodeficiencia humana, aunque la diarrea y enfermedades respiratorias son habituales en estos pacientes. Por otra parte, el presente análisis sólo abordó los efectos profilácticos del cinc y no revisó los estudios sobre sus efectos terapéuticos.
Es predecible que los beneficios de un programa de administración de suplementos, incluida la administración de cinc, sean desproporcionadamente mayores en individuos cuyo estado nutricional sea inferior a lo estándar o francamente deficiente. En dos estudios, los niños reclutados inicialmente con niveles séricos bajos de cinc parecieron experimentar las mayores reducciones de las tasas de incidencia y prevalencia de diarrea después de recibir suplementos de cinc comparado con niños cuyos niveles séricos basales eran más altos32,38. Sin embargo, no fue posible analizar los datos sobre diarrea y enfermedades respiratorias para niños con diversos grados de desnutrición dado que en los otros estudios que cumplieron los criterios de inclusión no estuvieron disponibles dichos datos estratificados. De hecho, en los ensayos en los que se administraron suplementos de cinc para el tratamiento de la diarrea, parecieron ser más beneficiosos en niños con un estado nutricional deficiente y niveles séricos bajos de cinc. Sería útil emprender estudios adicionales que pudieran analizar el impacto diferencial del cinc en niños con un déficit para identificar las subpoblaciones que pueden beneficiarse más en un ámbito de recursos limitados. Es de destacar que el diagnóstico del déficit de cinc es difícil y los niveles séricos no necesariamente son precisos con este objetivo. Además, la mayor parte de estudios sobre suplementos de cinc se han realizado en países en desarrollo; por lo tanto, los resultados del presente metaanálisis no se aplican necesariamente a niños procedentes de regiones desarrolladas. Diversos estudios aleatorizados, controlados, a gran escala, emprendidos después del metaanálisis de 1999, han respaldado los resultados del presente metaanálisis16,35,40.
La existencia de una heterogeneidad significativa en los resultados de los diversos estudios publicados puede distraer de las conclusiones del presente análisis. Tuvimos en cuenta la heterogeneidad utilizando técnicas de metaanálisis de modelos de efectos aleatorios para los análisis en los que los estudios demostraron una heterogeneidad significativa. El modelo de efectos fijos sólo se usó para algunos análisis; incluso en éstos, combinamos los datos utilizando también el modelo de efectos aleatorios y pusimos de relieve que los resultados eran en su mayor parte similares.
Por otra parte, el análisis del gráfico en embudo indicó la presencia de un sesgo de publicación. Esta impresión visual se reforzó todavía más mediante los criterios cuantitativos de un sesgo de publicación; la discordancia entre los resultados de los métodos de Begg y Mazumdar27 y de Egger et al28 para determinar el sesgo de publicación se explica por la sensibilidad relativamente baja de estos métodos, por lo que los resultados no significativos de estas pruebas no descartan la presencia de un sesgo. La presencia de heterogeneidad y un sesgo de publicación sugiere la necesidad de emprender estudios aleatorizados, controlados a mayor escala, que examinen los beneficios de los suplementos de cinc. También será importante monitorizar las poblaciones en las que ya se han introducido los suplementos profilácticos de cinc para estudiar las tendencias en la morbilidad de las enfermedades con el objetivo de estimar la eficacia de esta intervención en condiciones de campo.
Los estudios incluidos en el presente metaanálisis utilizaron una dosis de cinc de 15-140 mg/semana. Aunque los análisis de subgrupo no demostraron ningún efecto de la dosis sobre los beneficios identificados con los suplementos en el análisis de subgrupo, esto habría guardado relación con la sensibilidad limitada de estos análisis y el reducido número de estudios que utilizaron diversas dosis. La amplia variación de las dosis usadas en diversos estudios, que en ocasiones superaron la cantidad diaria recomendada para el cinc (11 mg/día para varones y 8 mg/día para mujeres), sugiere la necesidad de emprender estudios adicionales sobre la dosis óptima de los suplementos, en particular, porque dosis altas se han asociado con la inhibición de la absorción de otros micronutrientes51 y con una menor supervivencia en niños con infección por VIH52.
CONCLUSIONESEn conclusión, los datos combinados del presente metaanálisis indican que los suplementos de cinc administrados a niños sanos dan lugar a una reducción significativa aunque modesta de la frecuencia de diarrea y enfermedades respiratorias. Esta intervención también se traduce en una disminución de la frecuencia de diarrea grave e infecciones graves de las vías respiratorias inferiores, y del número de días de diarrea por niño; no obstante, en los datos combinados de los estudios incluidos no se detectó una reducción significativa del número de días con enfermedad respiratoria por niño. Estos datos revisten importancia para la salud pública y respaldan la implementación de los suplementos de cinc en países en desarrollo para mejorar la salud infantil. Además, los resultados del presente análisis hacen hincapié en la necesidad de obtener datos adicionales relativos al cinc a través de estudios a mayor escala, en particular en los que los individuos se estratifiquen por el estado nutricional basal. Dichos datos serán importantes para evaluar las diferencias en las respuestas de niños bien nutridos y desnutridos a los suplementos de cinc, y, por lo tanto, permitirán instaurar una intervención más dirigida.
AGRADECIMIENTOSDurante la presente investigación el Dr. Aggarwal contó con la financiación del Overseas Associateship Program del Department of Biotechnology, gobierno de la India. La presente investigación contó con una financiación parcial del Fogarty International Center, National Institutes of Health y la Bill and Melinda Gates Foundation.
Los autores agradecen a la Dra. Jessica Seidman la revisión crítica del manuscrito y sus sugerencias.
La presente investigación formó parte de una revisión a mayor escala financiada por la Bill and Melinda Gates Foundation y los National Institutes of Health para la prevención de las enfermedades de la infancia. Ninguna de ambas fuentes de financiación desempeñó papel alguno en el diseño del estudio, obtención, y análisis de los datos e interpretación de los resultados; redacción del manuscrito y decisión de presentarlo para su publicación.
Correspondencia: Mark A. Miller, MD, Division of International Epidemiology and Population Studies, Fogarty International Center, National Institutes of Health, 16 Center Dr., Bethesda, MD 20892-6705, Estados Unidos.
Correo electrónico: millemar@nih.gov