La retinopatía del prematuro (ROP) es una enfermedad caracterizada por la neovascularización anormal en la retina que puede llevar a ceguera.
ObjetivoDeterminar la prevalencia de ROP grave.
Material y métodosEstudio retrospectivo, observacional, descriptivo, transversal con revisión de expedientes de prematuros < 34 semanas de gestación y < 1,750g al nacimiento, así como recién nacidos > 34 semanas y > 1,750g que a criterio del médico contaban con factores de riesgo para ROP. Todos los neonatos fueron revisados por un retinólogo del año 2005 al 2014 determinando la prevalencia de ROP por año. La muestra fue consecutiva no probabilística. Se compararon únicamente las prevalencias de ROP severa por ser esta la que requiere tratamiento y por el alto riesgo de ceguera.
ResultadosIncluimos 143 niños, encontrando que 29 (20.2%) presentaron ROP severa. La comparación por año mostró un pico en 2005, con descenso en la prevalencia de ROP en 2014. En los 10 años de evaluación se observó una tendencia a la baja de ROP severa.
ConclusionesLa prevalencia acumulada de ROP severa fue de 20.2%, semejante a la de otros países de Latinoamérica. La prevalencia elevada desde 2005 hasta 2009 es explicada por la evaluación de prematuros externos manejados en instituciones sin tamizaje para ROP y referidos solo para su evaluación oftalmológica. Detectamos un descenso en la prevalencia a partir de 2010, que incluyó únicamente pacientes tratados en nuestra institución. De 2011 a 2014 no se reportaron niños con ceguera por ROP.
Retinophaty of prematurity (ROP) is a disease in which abnormal neovascularization develops in the retina and could be a cause of blindness.
ObjectiveTo determine severe ROP prevalence.
Material and methodsIn this retrospective, observational, descriptive, transverse study, we did a review of the clinical records of premature patients with < 34 weeks of gestation and a birth weight < 1,750g, and neonates with a gestational age >34 weeks and birth weight > 1,750g if they have risk factors for ROP. From 2005 to 2014, all the newborns were examined by a retinologist. ROP prevalence per year was determined, only the prevalence for severe ROP was compared because it requires treatment and has a high risk for blidness.
ResultsOne hundred forty-three newborns were included, 29 (20.2%) had severe ROP. When comparing for years there was a peak during 2005, with a descend in the prevalence of severe ROP in 2014, so in ten years there was a downward trend.
ConclusionsSevere ROP cumulated prevalence was 20.2%, similar to that observed in other latinoamerican countries. The high prevalence observed from 2005 to 2009, is explained because we examined patients refered from other institutions without screening programs for ROP. In 2010 we observed a descend in the prevalence, because only patient from our institution were included. From 2011 to 2014 we report none blind children with ROP.
La retinopatía del prematuro (ROP) es una enfermedad retiniana vasoproliferativa multifactorial, cuya incidencia aumenta de forma inversamente proporcional a la edad gestacional, aproximadamente el 65% de los recién nacidos menores de 1,250g y el 80% de los menores de 1,000g desarrollan algún grado de ROP1,2.
El desarrollo de la red sanguínea del ojo comienza a las 16 semanas, desde la parte central posterior hacia la periferia y culmina a las 40 semanas de gestación (SDG), por consiguiente, cuando nace un prematuro la retina no ha completado aún su desarrollo y la periferia carece de vasos sanguíneos3.
La ROP se origina por una alteración de la vasculogénesis ocasionando vasoconstricción y obliteración del lecho capilar, seguido de falla en la perfusión e hipoxia local, la cual induce a la formación de neovascularización, es decir tejido fibrovascular proliferativo extrarretiniano, que en etapas avanzadas se extiende al humor vítreo provocando hemorragias, exudación, tracción sobre la retina y por último desprendimiento de esta y por consiguiente ceguera4.
Se han determinado varios factores de riesgo que intervienen en el desarrollo de este padecimiento, entre los que se encuentran: prematurez extrema, bajo peso, concentraciones altas de oxígeno, ventilación mecánica, anemia, hiperoxemia, oscilaciones de hipo-hiperoxemia, transfusiones sanguíneas, uso de eritropoyetina tempranamente, raza blanca y sexo masculino entre otras5–7.
La organización mundial de la salud (OMS) define prematurez al recién nacido mayor de 20 semanas y menor de 37 SDG. A nivel internacional el 9% de los nacimientos registrados cada año son prematuros, y el 2% nacen antes de las 32 SDG8. En los países en desarrollo la ROP afecta el 35% de los prematuros con peso menor de 1,500g, de los cuales 6 a 27% requieren tratamiento. En Argentina se reportó una incidencia de 4.3 casos por 1,000 niños nacidos vivos (RN) durante el año 2008. En los EE. UU. en un análisis poblacional nacional durante 9 años, se informó una incidencia global de ROP de 34 millones de RN vivos, lo que representó 1.7 casos por cada 1,000 nacidos vivos. En la unión americana aproximadamente entre 400-600 niños por año pueden quedar ciegos por retinopatía del prematuro, lo que representa el 20% del total de casos de ceguera en preescolares9,10.
En Europa la incidencia de ROP es alrededor del 5 a 7% de los RN vivos, si nos centramos en los casos más severos que necesitarán tratamiento, la cifra se reduce a un 3 a 7%11.
El grupo NEOCOSUR que concentra información de 5 países de América del Sur (Argentina, Chile, Uruguay, Perú y Paraguay) en el periodo de 2001-2011 registró una incidencia de 31% de ROP entre neonatos de edad gestacional de 24 a 31 semanas y menos de 1,500g al nacer12. Sea cual sea la estadística consultada, la incidencia de ROP es de 4 a 5 veces mayor en países en vías de desarrollo (Latinoamérica, Asia, Europa del este), pero también en países desarrollados en los cuales ha mejorado la supervivencia de niños de extremado bajo peso al nacer. La red neonatal de Chile en un periodo de 5 años (2000-2004) en menores de 32 semanas de edad gestacional refiere 90% de niños evaluados con 23% de ROP y 4% tratados13.
La división de neonatología del Instituto Materno Infantil del Estado de México, en el año 2006 reportó estadios graves de 3 o mayores en el 31.5% con una prevalencia de ceguera del 5.2%., se observó que el mayor número de prematuros con algún grado de ROP fue entre las 31 y 32 SDG14.
En el Hospital General Agustín O¿ Horán de los Servicios de Salud de Yucatán, México, en el año 2008 se registraron 1,297 nacimientos anuales, de ellos 10.4% fueron prematuros con peso menor de 1,500g y < 32 SDG, de estos el 30% cursó con algún grado de ROP, el 13.3% con ROP grado I, el 3.3% con ROP grado II y el 1.3% con ROP grado III15.
La importancia de conocer la prevalencia de ROP, consiste en identificar la posibilidad de prevención de ceguera por ROP, ya que esta entidad representa una de las principales causas de ceguera prevenible16.
Actualmente en México, contamos con los protocolos de tamizaje del lineamiento técnico para el manejo de la retinopatía del recién nacido prematuro editado por la Secretaria de Salud, publicado en el año de 2007, actualizado en 2008, en este documento se establecen los siguientes criterios para evaluación de ROP en RN:
- 1.
Todos los recién nacidos pretérminos de < 34 SDG y/o de peso menor a 1,750g de peso al nacimiento.
- 2.
A criterio del médico tratante los recién nacidos pretérminos mayores a 34 SDG y con peso al nacimiento > 1,750g que hayan recibido oxígeno suplementario.
- 3.
A criterio del médico tratante los recién nacidos pretérminos que tengan factores de riesgo17.
Además, en México es obligatoria la revisión de los prematuros para tamizaje de ROP en base a la Ley General de Salud a partir del año 2013, el artículo 61 señala: «La aplicación del tamiz oftalmológico neonatal, a la cuarta semana del nacimiento, para la detección temprana de malformaciones que puedan causar ceguera, y su tratamiento, en todos sus grados»18–21.
El inicio de las revisiones se basa en las recomendaciones de la Asociación Americana de Pediatría para los bebés con una gestación de por lo menos 28 SDG, los exámenes se deben efectuar de 4 a 6 semanas después del nacimiento.
La clasificación internacional de ROP se basa en: localización, severidad, extensión y presencia o ausencia de enfermedad plus.
Localización: según la distancia entre la ora serrata y el disco óptico. Se distinguen 3 zonas.
Zona I: comprende un círculo en torno al disco óptico con un radio del doble de la distancia entre el disco óptico y mácula.
Zona II: desde el borde de la zona I hasta el borde de un círculo con centro en el disco óptico y un radio del disco hasta la ora serrata nasal.
Zona III: desde el borde externo de la zona II hacia la periferia.
Severidad: se consideran 5 etapas.
Grado I: línea de demarcación fina entre la retina vascular y avascular.
Grado II: elevación de la línea de demarcación sobre el plano de la retina formando un cordón o borde.
Grado III: elevación del cordón vascular hacia el vítreo por proliferación fibrovascular con tejido de neoformación que da un aspecto deshilachado.
Grado IV: desprendimiento retinal parcial.
IVa: sin desprendimiento de la mácula.
IVb. Con desprendimiento de la mácula.
Grado V: desprendimiento retinal total.
Extensión: se mide según los 12 husos horarios comprometidos.
Enfermedad plus o «más» (+): es la dilatación vascular progresiva y tortuosidad de vasos retinales posteriores y puede también acompañarse de ingurgitación del iris, rigidez pupilar, opacidad vítrea, hemorragia del vítreo.
Con base en los hallazgos oculares se establece la «enfermedad umbral», que es aquella que en el 50% de los casos puede producir ceguera, afectando 5 husos contiguos u ocho husos horarios alternos de ROP en grado III y enfermedad plus. Si un recién nacido llega al G III (+) las probabilidades de quedar con algún tipo de secuela visual son del 80%, si no sobrepasa el GII (+) las posibilidades de secuelas son del 45%, en ausencia de enfermedad plus las posibilidades de secuelas son bajas22.
El diagnóstico debe realizarse mediante oftalmoscopia indirecta a las 4 semanas de vida. La frecuencia de los controles posteriores va a depender de la decisión del oftalmólogo considerando la localización, etapa y presencia de enfermedad plus. La fotocoagulación con láser es considerada hasta el momento el tratamiento de elección para ROP. El uso de medicamentos inhibidores del VEGF ha mostrado resultados alentadores como tratamiento de la retinopatía en etapa umbral, como monoterapia o bien como coadyuvante23.
El pronóstico visual en la mayoría de los pacientes tratados es excelente. Hasta la etapa II la ceguera es reversible sin mayores secuelas. La mayoría (mayor 80%) de los prematuros extremos (<1,000g) van a desarrollar algún grado de ROP y al menos el 10 a 15% presentan ROP grave. La mayoría de los casos se resolverán sin tratamiento24. La ceguera bilateral es actualmente muy rara con el seguimiento y tratamiento adecuados.
Los niños ciegos ocasionan una carga económica significativa para la familia y la comunidad. En este momento se estima que en el mundo existen 1.4 millones de niños ciegos, y se estima que esta cifra aumenta en 50,000 niños cada año25.
La retinopatía del prematuro es la principal causa de alteraciones visuales y ceguera prevenible en los RN pretérminos, en países desarrollados, sobre todo de los más inmaduros o con peso de 750g a 1,000g26.
América Latina incluido México, se reconoce dentro de las regiones con alto riesgo para desarrollar ceguera por ROP dado el alto índice de nacimientos prematuros y cobertura no equitativa de los servicios avanzados en neonatología27,28.
La prevalencia ha incrementado en los últimos años debido a los grandes avances en la neonatología, el incremento de la terapia intensiva neonatal, el uso de oxígeno generalizado, y el mayor uso de equipos de ventilación asistida que hacen sobrevivir a los niños de muy bajo peso al nacer29.
El Hospital de la Amistad Corea-México (HACM) en el estado de Yucatán, está catalogado como un hospital pediátrico de referencia para otras Unidades que no cuentan con un servicio especializado en Neonatología, recibe y atiende prematuros graves que ameritan terapia intensiva, por lo que son de alto riesgo para padecer ROP GIII o mayor y como consecuencia ceguera. Siendo de importancia conocer los resultados epidemiológicos del trabajo realizado en este hospital.
Algunos de los factores de riesgos descritos forman parte del arsenal terapéutico del neonatólogo para el manejo integral de este tipo de paciente y no se puede prescindir de estos, pero al conocer los riesgos, debe hacerse énfasis en su uso adecuado y evitar abusos tratando de individualizar cada caso, valorando riesgo-beneficio de cada terapéutica.
Debido a la inexistencia de síntomas o signos clínicos precoces que indiquen el desarrollo de la ROP es preciso un estudio precoz y regular, siendo de trascendental importancia realizar un programa de detección temprana que permita identificar la población en riesgo, ofrecer diagnóstico temprano y tratamiento oportuno en búsqueda de reducir el número de casos, sensibilizando a los médicos que tratan a los prematuros, para su adecuada referencia con el oftalmólogo.
Material y métodosEn el HACM se realizó un estudio retrospectivo, observacional, descriptivo, transversal, mediante la revisión de expedientes del año 2005 al 2014 y recabando la información en hojas de captación de datos diseñadas para este fin.
En esta unidad se inició el protocolo de tamizaje para ROP desde el año 2005, de acuerdo a las guías británicas, y a partir del 2008 se basa en los lineamientos técnicos editados por la Secretaria de Salud mexicana. En ese momento el HACM era la única unidad en el Estado de Yucatán en donde se realizaba dicho tamizaje, por lo que del año 2005 hasta el año 2008 en el estudio se incluyeron niños referidos de otras instituciones tales como el IMSS (H. Juárez y T1), el Hospital Agustín O¿ Horán, así como clínicas particulares y pacientes de los estados de Campeche, Quintana Roo y Tabasco, los cuales fueron referidos especialmente para valoración del programa de tamizaje ROP.
La muestra fue consecutiva no probabilística, se incluyeron a los neonatos pretérminos de <34 SDG y/o 1750g o menos de peso al nacimiento; también se incluyeron a los RN pretérmino > 34 SDG y con peso al nacimiento > 1,750g que hubiesen recibido asistencia respiratoria en cualquier modalidad y que a criterio del médico contase con un factor de riesgo para ROP.
Los criterios de exclusión fueron expedientes de recién nacidos de término, expedientes incompletos y expedientes de prematuros que no contaron con documento de valoración oftalmológica.
Como criterios de eliminación se estableció pacientes a quienes se les encontró por hallazgo otra enfermedad retiniana, así como los RN que fallecieron antes de su primera valoración oftalmológica.
ResultadosSe registraron durante los años 2005 a 2014 un total de 752 ingresos al servicio de neonatología, donde 270 fueron prematuros, de los cuales se excluyeron 108 expedientes al no cumplir con los criterios de peso y/o edad gestacional requeridos y se eliminaron 19, ya que el expediente se encontraba incompleto o habían fallecido antes de ser evaluados por primera vez por el oftalmólogo, 143 cumplieron con los criterios de inclusión para este estudio.
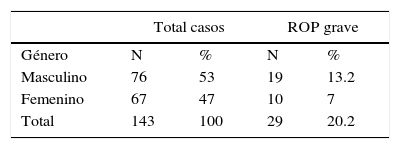
De los 143 prematuros, 83 (58%) no presentaron ROP, 31 (21.6%) presentaron ROP no grave y 29 (20.2%) ROP grave (fig. 1). El género masculino presentó con mayor frecuencia ROP en cualquiera de sus grados (tabla 1). En este estudio los prematuros más pequeños que sobrevivieron no presentaron ROP grave, sin embargo, los prematuros tardíos sí presentaron cuadros más severos (fig. 2). En cuanto al rango de edades gestacionales que sobrevivieron y que presentaron algún grado de ROP, este fue de 28 a 36 SDG. Siendo la mayor frecuencia entre las 32 y 33 SDG (tabla 2).
Distribucion de gravedad de la retinopatía del prematuro (ROP). Por edad gestacional
| Semanas de gestación | Sin ROP | Con ROP no grave | Con ROP grave | Total niños con ROP | Total de prematuros |
|---|---|---|---|---|---|
| 26 | 0 | 1 | 0 | 1 | 1 |
| 27 | 0 | 1 | 0 | 1 | 1 |
| 28 | 1 | 2 | 5 | 7 | 8 |
| 29 | 0 | 3 | 3 | 6 | 6 |
| 30 | 4 | 1 | 5 | 6 | 10 |
| 31 | 6 | 3 | 0 | 3 | 9 |
| 32 | 10 | 7 | 6 | 13 | 23 |
| 33 | 24 | 8 | 5 | 13 | 37 |
| 34 | 21 | 2 | 4 | 6 | 27 |
| 35 | 12 | 1 | 1 | 2 | 14 |
| 36 | 5 | 2 | 0 | 2 | 7 |
| Total | 83 | 31 | 29 | 60 | 143 |
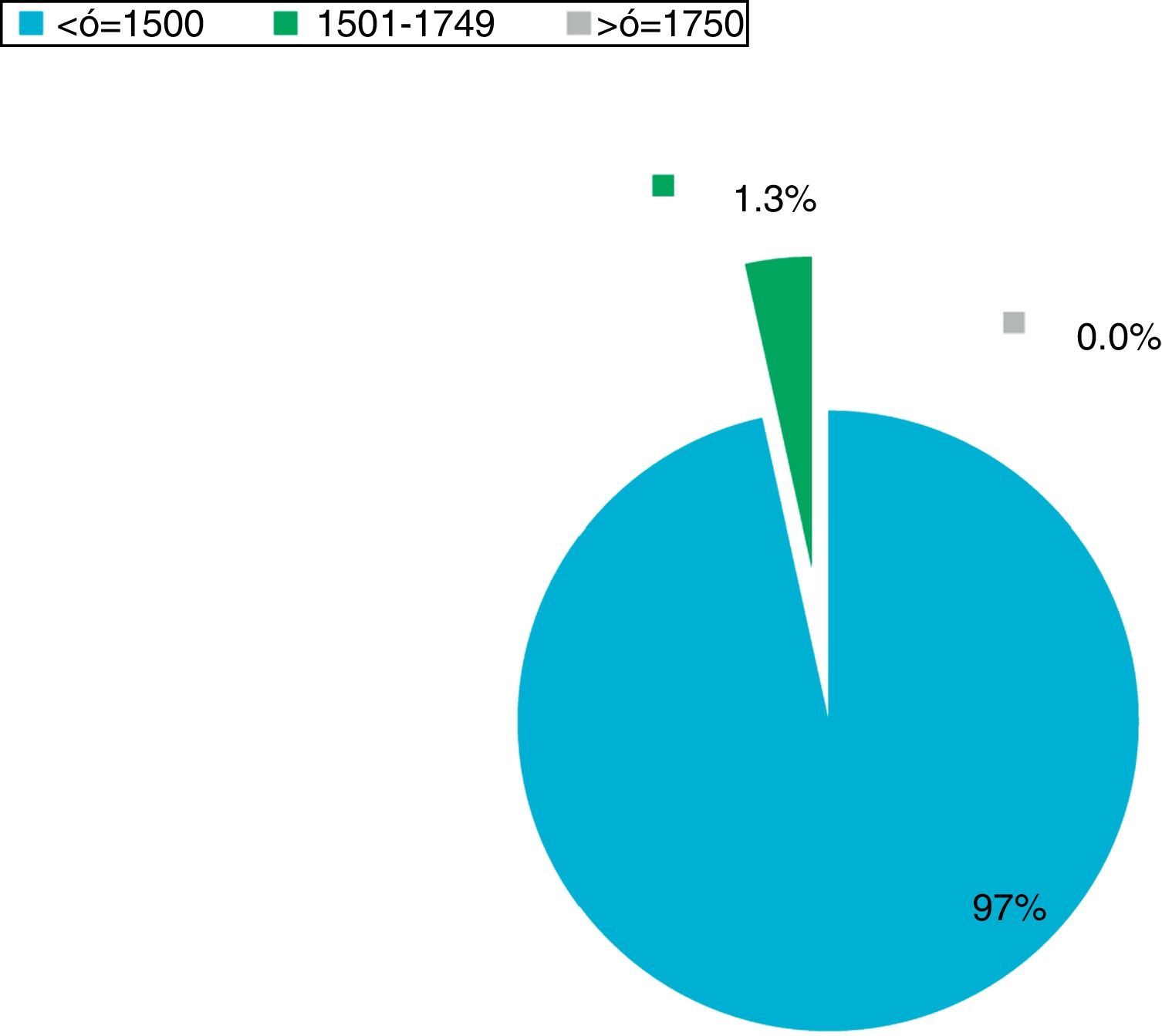
La tendencia de ROP por edades gestacionales presentó su mayor frecuencia entre los prematuros moderados y tardíos. En el factor de riesgo peso para ROP grave, el 97% de los prematuros pesó < 1,500g (intervalo 600g a 1,500), ninguno de los prematuros con ROP grave pesó más de 1,750g. La prevalencia anual de ROP grave desde el 2005 al 2014, mostró una tendencia a disminuir a partir del año 2009. En los primeros 5 años se detectaron en promedio dos niños ciegos por año. Desde 2011 no se han observado nuevos casos de ceguera por ROP. En el último año 2014, la prevalencia descendió a 7%.(fig. 3).
DiscusiónLa retinopatía del prematuro es una vítreo-retinopatía proliferativa que se desarrolla en niños prematuros y que en sus formas más graves puede provocar ceguera. Los niños ciegos ocasionan una carga económica significativa para la familia y la comunidad. En este momento se estima que en el mundo existen 1.4 millones de niños ciegos y entre las causas principales se encuentra la ROP30 y se estiman 50,000 niños cada año.
Actualmente en México contamos con los protocolos de tamizaje oftalmológico tales como el Lineamiento Técnico Mexicano para el manejo de la retinopatía del recién nacido prematuro editado por la Secretaría de Salud y actualizado en 2008 y es el actualmente utilizado en nuestra institución, como la Guía de Práctica Clínica 201531–33.
En nuestro estudio hacemos hincapié en la retinopatía grave, (GIII, GIV, GV) puesto que si un recién nacido llega al G III (+) las probabilidades de permanecer con algún tipo de secuela visual son del 80%, mientras que los otros grados tienen mejor pronóstico.
Es importante mencionar que la prevalencia acumulada de ROP en este estudio fue de 41.8% y la de ROP grave de 20.2%. Lo anterior es similar a las reportadas en otros hospitales de México y en países en desarrollo, como es el caso de Colombia, ya que han reportado casos de ROP grave en niños hasta de 2,000g de peso, por lo que incluyen en sus criterios de tamizaje hasta este peso (Grupo NEOCOSUR)34.
En estudios en el Estado de México reportan estadios graves en el 31.5% con prevalencia de ceguera del 5.2%. En nuestro estudio reportamos en promedio dos niños ciegos por año los primeros 5 años, con una disminución de esta complicación en los siguientes años hasta llegar a cero.
En cuanto al género en nuestro estudio encontramos que la retinopatía del prematuro grave fue más frecuente en el sexo masculino (13.2%) (tabla 1), lo cual es considerado como uno de los factores de riesgo de múltiples patologías, no siendo esta la excepción, además del uso de oxígeno, edad gestacional y raza blanca según la literatura35,36.
El predominio de pesos menores o igual a 1,500g independiente de la edad gestacional fue determinante para la presencia de ROP grave, estando acorde este resultado con estudios relacionados que apoyan que como factores de riesgo se encuentran el bajo peso al nacer, la desnutrición o falta de progresión en el incremento de peso posnatal y la deficiencia del nivel de factor de crecimiento insulinoide descrito en el método WINROP37.
En este estudio presentó una mayor prevalencia de ROP en los prematuros moderados entre 32 y 33 semanas, edades gestacionales muy semejantes a las reportadas de otros países de América Latina y en países en vías de desarrollo, con la misma tendencia descrita por Gilbert, incluso en pretérminos tardíos, atribuible a una mayor sobrevida de pretérminos moderados y tardíos38,39. Por otra parte nuestros resultados difieren con los informes de países desarrollados, como el Reino Unido y la Unión Americana, donde la ROP grave se presenta en edades gestacionales más tempranas probablemente por tener mayor supervivencia40.
La supervivencia de prematuros extremos, menores de 28 semanas aún no está totalmente documentada en México y es considerada como baja, siendo escasos los reportes como describe Montiel, de hospitales en donde se tiene como límite de viabilidad las 26 SDG y 700g de peso al nacimiento, con una sobrevida intacta sin secuelas significativas en 28 SDG y 900g de peso al nacimiento41. A diferencia con los países desarrollados, como Australia, en donde la supervivencia de prematuros extremos es hasta de 24 SDG lo cual condiciona que la ROP grave vaya en aumento42.
La evolución de la prevalencia anual en nuestro estudio desde el año 2005 hasta el año de 2008 fue elevada, atribuyéndose esto a las características de los pacientes que fueron evaluados, puesto que al catalogarse nuestro centro hospitalario como un hospital de referencia y en su momento, único para el tamizaje oftalmológico neonatal, en él se evaluaban no solamente a los prematuros propios, tratados intrahospitalariamente, sino también se atendía como consulta oftalmológica a pacientes prematuros egresados de otras instituciones locales y otros estados del sureste de la República Mexicana, después de que ellos habían concluido tratamiento hospitalario en dichas instituciones.
Posteriormente a partir del año 2010 en el HACM fue notable la disminución de la prevalencia de ROP grave, fenómeno explicado por la creación de programas de tamizaje en los centros de atención neonatal en otras instituciones locales, con lo que disminuyó la referencia de pacientes prematuros al HACM, para valoración de consulta oftalmológica. Sin embargo, los prematuros incluidos a partir de 2009 fueron pacientes referidos para su manejo hospitalario inicial en su primer día o en la primera semana de vida.
Aun cuando no se determinaron en este estudio los factores que favorecen la disminución de la ROP grave, en el transcurrir de los años es un hecho el énfasis para el entrenamiento a personal médico y de enfermería sobre el adecuado uso de oxigenoterapia, de mezcladoras aire-oxígeno, así como la monitorización continua de la oximetría, la disminución del uso de la ventilación mecánica invasiva e incremento del manejo de presión positiva continua a la vía aérea, alimentación enteral, lactancia materna y nutrición parenteral tempranas43.
Al contar con mejoras en los servicios de neonatología, mejora a su vez el pronóstico de los prematuros, y al ser la retinopatía del prematuro tan frecuente en nuestro medio, es importante promover los programas con tamizaje estricto de los prematuros que tengan riesgo, realizarlo en base a lineamientos establecidos y actualizado en nuestro país a partir del año de 2008, así como en la Guía de Práctica Clínica del país. De acuerdo a nuestros resultados, son vigentes los criterios establecidos en México para la población que se atiende en el HACM, tanto en peso como edad gestacional. Aunque cada institución puede valorar los criterios de acuerdo a sus resultados. También se deben fomentar otros estudios de investigación prospectivos multicéntricos para conocer el comportamiento epidemiológico y la incidencia de ROP en la península de Yucatán, determinar los factores de riesgo asociados con ROP en nuestra región, para prevenir y disminuir la incidencia de ceguera por ROP.
Conclusiones- 1.
La ROP presentó una prevalencia acumulada de 41.8% en 9 años.
- 2.
La prevalencia de ROP grave fue del 20.2%.
- 3.
La retinopatía del prematuro grave fue más frecuente en el género masculino.
- 4.
Las edades gestacionales que presentaron ROP grave fueron en el rango de 28 a 35 semanas, con pico de mayor a las 33 semanas.
- 5.
A partir de 2011 y hasta 2014 no hemos encontrado nuevos casos de ceguera por ROP.
Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datosLos autores declaran que en este artículo no aparecen datos de pacientes.
Derecho a la privacidad y consentimiento informadoLos autores declaran que en este artículo no aparecen datos de pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.