INTRODUCCION
Recientemente, han aparecido diversos trabajos en los que se analizan las indicaciones y los resultados de la denominada cirugía altamente agresiva, cirugía de «máximo esfuerzo» o citorreducción quirúrgica «óptima» mediante las técnicas de peritonectomías, en el cáncer de ovario.
Presentamos nuestra propia experiencia de los últimos 3 años en este tipo de cirugía que, aunque limitada a 14 casos, nos permitirá extraer algunas conclusiones sobre las indicaciones, la intensidad de la cirugía practicada, la morbilidad de este tipo de cirugía y los resultados a corto y medio plazo.
Es difícil definir qué se entiende por cirugía ultrarradical (CU), pues en la literatura médica no suele haber uniformidad de criterios en cuanto a los actos quirúrgicos que la caracterizan.
Suele definirse como cirugía radical citorreductora la técnica que, una vez eliminada la masa tumoral, no deja enfermedad residual superior a 1 cm.
Nosotros consideramos que la terminología cirugía «ultrarradical» (CU) define mucho mejor las características de esta intervención, en contraposición al término radical, o citorreducción primaria, que ha sido aplicado con excesiva benevolencia. Ha podido comprobarse1 que solamente el 42-45% de las pacientes tratadas por ginecólogos oncólogos había recibido una óptima citorreducción, a pesar de aceptarse una definición menos estricta de enfermedad residual.
La CU fue perfectamente sistematizada por Sugarbaker en el tratamiento de la carcinomatosis peritoneal de origen tumoral primario gastrointestinal2. Consiste en la práctica secuencial de varios procedimientos quirúrgicos, hasta un total de 6, que permiten abordar las regiones del abdomen, la pelvis y el territorio retroperitoneal que macroscópicamente estén afectadas por el tumor primario o los implantes tumorales, independientemente de que la infiltración tumoral se limite al peritoneo parietal o infiltre las vísceras correspondientes de estas regiones. Los procedimientos se realizan en el mismo acto quirúrgico, y sólo en las regiones en que se detecte una enfermedad tumoral visible. El objetivo de la citorreducción es la erradicación de toda la enfermedad tumoral macroscópica: citorreducción «completa», pero la localización primaria del tumor, la histología y el grado de diferenciación pueden permitir intensidades de la cirugía menor, que en el caso de las neoplasias de ovario corresponderían a residuos de 0,5 cm (citorreducción con «residuo tumoral mínimo»), pero en otro tipo de tumores bien diferenciados sólo admitiría residuos no superiores a 0,25 cm.
El mismo Sugarbaker, y otros grupos3, adaptaron y aplicaron estas técnicas de citorreducción al tratamiento de las neoplasias ginecológicas avanzadas, y más concretamente a los tumores epiteliales de ovario en su tratamiento quirúrgico de inicio (citorreducción «primaria») o en el rescate quirúrgico de las persistencias o recurrencias (citorreducción «secundaria»). En este último caso, los criterios de indicación y de intensidad de la citorreducción son más exigentes.
Con la finalidad de evaluar la respuesta al tratamiento y de facilitar el pronóstico de las pacientes sometidas a este tipo de cirugía, se divide la cavidad abdominopélvica en 13 compartimientos o regiones, que siempre han revisarse quirúrgicamente de forma sistemática, y se puntúan en función del volumen tumoral en cada una de ellas. La puntuación de cada región varía de 0 (ausencia de tumor macroscópico) a 3 (presencia de masa superior a 5 cm). La puntuación de cada una de estas regiones se suman y estarían en rangos mínimos de 0 a un máximo de 39. A este sistema de clasificación del volumen o carga tumoral peritoneal se le denomina índice de cáncer peritoneal (ICP).
También se define un índice de citorreducción tras la cirugía (CC) según el tamaño del tumor residual: CCO, ausencia de tumor residual macroscópico; CC1, tumor residual < 0,25 cm; CC2, 0,25-2,5 cm; CC 3, > 2,5 cm.
Actualmente, hay evidencias de que la supervivencia de las pacientes está en relación con el ICP, y muy especialmente con el grado de CC conseguido con la cirugía. Indudablemente, esta variable también está relacionada con otra variable independiente, que es la respuesta al tratamiento quimioterápico mediante la utilización de los fármacos adecuados.
En una publicación anterior4 describimos nuestra técnica de CU, con alguna variante sobre la primitivamente descrita por Sugarbaker. En síntesis, seguimos los siguientes pasos quirúrgicos:
-- Peritonectomía pélvica o pelviperitonectomía, que incluye la extirpación en bloque, extrafascial y centrípeta de los órganos genitales internos, el peritoneo parietal del hemiabdomen inferior, y el colon rectosigmoide, junto con el mesorrecto, cuando éste está afectado trasmuralmente por el tumor.
En algunas ocasiones, en el 30% de las pacientes de esta serie, este procedimiento se ha tenido que ampliar a causa de una infiltración tumoral del complejo ileocecal o la eliminación de los órganos anteriormente descritos, conjuntamente con las últimas asas ileales y el colon ascendente. Es lo que nosotros hemos denominado como pelviperitonectomía «ampliada».
-- Extirpación de todo el epiplón mayor a raíz de la curvatura mayor gástrica, asociada a esplenectomía, cuando macroscópicamente el territorio ganglionar esplénico, la cápsula o el parénquima esplénico estén afectadas por el tumor.
-- Peritonectomía del cuadrante superior izquierdo del abdomen, incluye la serosa del hemidiafragma izquierdo y el peritoneo posterior de esta región anatómica, dejando al descubierto la fascia de Gerota y la glándula suprarrenal izquierda.
-- Peritonectomía del cuadrante superior derecho del abdomen, destinada a eliminar la serosa del hemidiafragma derecho, conjuntamente con la cápsula hepática de Glisson, cuando estas estructuras estén afectadas tumoralmente.
-- Omentectomía del epiplón menor y colecistectomía
-- Resecciones intestinales, gástricas, vesicales parciales, etc.
Obviamente, las resecciones viscerales dependerán del grado de infiltración tumoral, siempre procurando eliminar de forma subserosa los implantes no infiltrantes, o fulgurar los aislados y de pequeño tamaño. Pero la citorreducción quirúrgica «completa» constituye el fundamento de este tipo de cirugía, por lo que la exéresis multivisceral no puede evitarse en algunos casos de neoplasias de ovario en estadio avanzado.
MATERIAL Y MÉTODOS
Se efectúa una revisión retrospectiva de los casos clínicos patológicos y quirúrgicos de 14 pacientes afectadas de carcinoma de ovario, intervenidas quirúrgicamente mediante una CU. Se realiza una aproximación descriptiva para presentar la evolución de la enfermedad, utilizándose distribuciones de frecuencias y medidas de tendencia central.
RESULTADOS
Desde octubre de 2003 a diciembre 2005 hemos intervenido a 14 pacientes diagnosticadas de neoplasias de ovario en estadio avanzado de la enfermedad. La afección tumoral abdominopélvica fue considerada como voluminosa, y en 4 de ellas asociada además a una enfermedad ganglionar retroperitoneal. En 3 pacientes la indicación de la citorreducción fue «primaria», y una paciente de este subgrupo había recibido previamente quimioterapia neoadyuvante, constatándose en la respuesta objetiva del tumor a la quimioterapia de inicio.
En las restantes 11 pacientes, la CU fue «secundaria» y motivada por una recurrencia peritoneal y retroperitoneal de la enfermedad.
Entre las pruebas diagnósticas preoperatorias, habituales para cualquier presunto carcinoma abdominal, la tomografía computarizada (TC) es indispensable. Permite el diagnóstico diferencial con otras tumoraciones intraabdominales. Así, por ejemplo, en el carcinoma de ovario diseminado se observa una extensión difusa de la enfermedad diferente a la imagen que podría observarse en el seudomixoma peritoneal, que muestra un magma espeso de consistencia similar a la grasa. La paracentesis no suele aportar ninguna ventaja para establecer la estrategia quirúrgica.
La preparación preoperatoria no diferirá en nada a la que se realiza a cualquier paciente que ha de ser sometida a cirugía mayor. Realizamos una preparación intestinal sistemática, una profilaxis con heparina y una profilaxis antibiótica. En todas las pacientes se realiza reserva de hematíes y de plasma. La administración de plasma se determina durante el acto quirúrgico en función de la extensión del tumor peritoneal y el grado de intensidad de la cirugía. Con la administración de plasma se pretende compensar la gran pérdida de proteínas y factores de coagulación que se produce durante una desperitonización masiva del abdomen, así como los efectos de quemadura interna que provoca el uso intensivo del electrobisturí. La paciente se coloca con escasa elevación de las extremidades inferiores. A diferencia de otros grupos de investigación, no utilizamos la cateterización previa de los uréteres.
El volumen tumoral se catalogó en 3 pacientes con un ICP de 1 a 10 (dentro de este subgrupo se incluían las pacientes sometidas a cirugía de intervalo tras quimioterapia neoadyuvante), 6 pacientes con ICP de 11 a 25, y las 5 pacientes restantes con ICP superiores a 26. Por tanto, se trataba de pacientes mayoritariamente afectadas por un elevado volumen o carga tumoral, que afectaban a diversas regiones anatómicas e infiltraban uno o más vísceras.
Cinco de las 14 pacientes presentaban una fijación de las estructuras del hemiabdomen inferior y fueron sometidas a la variante más extensa de pelviperitonectomía: la pelviperitonectomía «ampliada», además, de otros procedimientos de peritonectomía. En 3 pacientes, la CU requirió 3 de los procedimientos, en 6 pacientes 4 o 5 procedimientos, y en 5 pacientes se practicaron las 6 técnicas descritas de peritonectomía.
La citorreducción conseguida se consideró «con mínimo residuo tumoral» (0,5 cm tras la cirugía) en 4 pacientes, mientras que se consiguió erradicar completamente la enfermedad residual macroscópica en las restantes 10 pacientes.
En 13 pacientes se realizaron anastomosis digestivas, en todos los casos como mínimo una anastomosis colorrectal baja, y en 8 pacientes, además, otras anastomosis digestivas, hasta un total de 22 suturas digestivas en la serie.
No hubo mortalidad postoperatoria, ni dehiscencias anastomóticas u otras complicaciones sépticas abdominales. Una paciente del grupo de las CU «secundarias» presentó en el postoperatorio inmediato un cuadro de oclusión intestinal que requirió cirugía resectiva intestinal para la resolución de un proceso retráctil mesentérico.
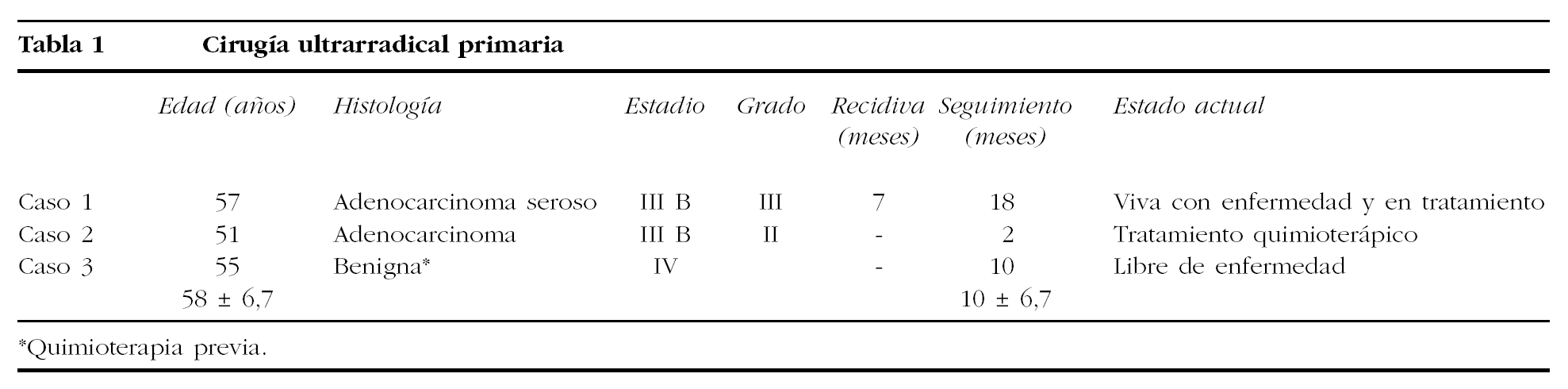
Tan sólo una de las 3 pacientes que fueron sometidas a CU en un primer intento quirúrgico ha recidivado a los 7 meses de la intervención. Las otras 2 pacientes se hallan libres de enfermedad, una recibiendo tratamiento quimioterápico y la otra tras 10 meses de la cirugía. En este grupo no se ha producido ningún fallecimiento, hasta el momento de redactar el presente trabajo (tabla 1).
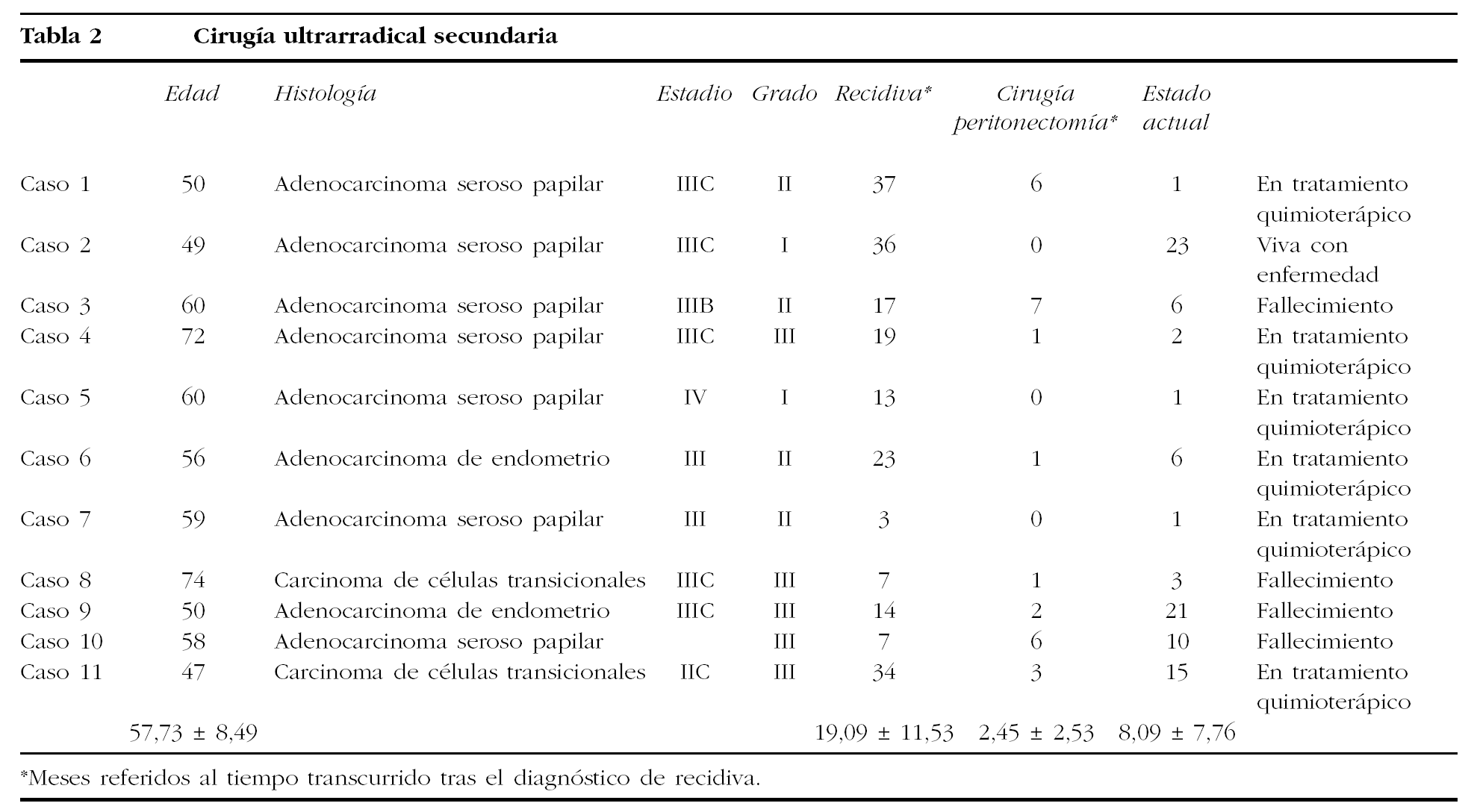
En el segundo grupo, constituido por 11 pacientes cuya edad media fue semejante a la del grupo anterior (57,7 ± 8,5 años), se establecieron los siguientes diagnósticos: 2 adenocarcinomas endometrioides en estadios IIIc y grado 3; 3 adenocarcinomas serosos papilares en estadios IIc, IIIb y uno sin clasificar; otros 3 en estadios IIIc y 2 en estadio IV, y una paciente con carcinoma de células transicionales, en estadio IIc y grado 3.
Todas las pacientes recibieron quimioterapia adyuvante (carboplatino-taxol).
Las recidivas de la primera cirugía, según el diagnóstico mediante TC previa a la intervención, fueron: 2 casos en el epiplón, uno en el espacio perihepático, periesplénico, y otro con lesión pancreática y paraaórtica, 2 ascitis, un caso con metástasis peritoneales, otro en la cúpula vaginal y otro en la vejiga. La paciente afectada de carcinoma de células transicionales fue intervenida por primera vez 5,5 años antes de la CU. Recidivó por primera vez a los 33 meses de la cirugía y quimioterapia. Se realizó cirugía de rescate seguida de quimioterapia. A los 34 meses de la anterior, se efectuó CU por recidiva en el peritoneo. Actualmente, está en tratamiento con inhibidores de la angiogénesis, 15 meses después de la CU, y en aparente remisión completa de la enfermedad.
La mediana de supervivencia libre de enfermedad desde la primera cirugía fue de 19 meses (rango, 3-37). La CU como segundo acto quirúrgico se produjo a los 21,5 meses de la primera intervención. Se han producido 4 fallecimientos, a un tiempo mediano de 8 meses (rango, 6-21) tras la segunda intervención (tabla 2).
DISCUSION
Es evidente que nuestra corta experiencia no permite extraer conclusiones estadísticamente válidas. Pero ante una cirugía que requiere unos conocimientos, unas habilidades y unas aptitudes que no están al alcance de la mayoría de los ginecólogos españoles, con especial dedicación a la ginecología oncológica, debemos plantearnos una serie de consideraciones de orden asistencial y sanitario.
En un reciente artículo5, los autores se cuestionan si la cualidad del cirujano influye en las cifras de supervivencia del cáncer de ovario, y llegan a las siguientes conclusiones:
-- Las pacientes con enfermedad avanzada, operadas por ginecólogos oncólogos, tienen mayores posibilidades de obtener una óptima citorreducción.
-- La supervivencia global es superior en el grupo tratado por ginecólogos oncólogos, pero las cifras se igualan si la citorreducción que se obtiene es similar en uno y otro grupo.
-- En los estadios precoces, la estadificación es mucho más exacta y precisa en el grupo intervenido por ginecólogos oncólogos.
En un reciente trabajo6, multicéntrico, prospectivo y observacional, se valora el impacto de la citorreducción en el intervalo libre de enfermedad, y las variantes internacionales de las técnicas quirúrgicas. Los autores observan que la más completa citorreducción se logra en las pacientes con una enfermedad menos avanzada. En el mismo estudio se hace hincapié en la importancia de la selección de las pacientes, que se someten a una cirugía agresiva citorreductora, que pretenda ser eficaz, priorizando la selección antes que la citorreducción agresiva, indiscriminada.
Otros autores7 defienden un punto de vista similar, aceptando la citorreducción secundaria en las pacientes en que se consiguió una citorreducción primaria óptima, y mantuvieron un largo período libre de enfermedad, especialmente si se trataba de carcinomas endometrioides.
Validar la conveniencia de una cirugía agresiva del carcinoma de ovario es difícil, pues generalmente tiene que recurrirse a trabajos colaborativos, en los que es imposible asegurar la radicalidad de unos y otros cirujanos. Recientemente, varios autores8 pertenecientes a diversos centros y países, llegan a la conclusión de que la linfadenectomía pélvica y aórtica en el carcinoma de ovario mejora el intervalo libre de enfermedad, pero no influye sobre la supervivencia. Se acepta de forma generalizada que el volumen de enfermedad residual es el único factor independiente, predictivo de la supervivencia9.
Ante la acumulación de posiciones contradictorias, los sesgos involuntarios de que adolecen los estudios basados en experiencias quirúrgicas y la muy subjetiva interpretación que los cirujanos tenemos tanto de nuestras técnicas como las de los demás, nos obligan a ser extremadamente cautos en las decisiones que tomemos.
La lucha contra el cáncer de ovario es ardua, desesperante y llena de continuas excepciones, si consideramos la historia natural de la enfermedad. No deja de llamar la atención que en contadísimas ocasiones se tenga en cuenta la calidad de vida de la paciente. No se trata de puntuar sobre un índice de Kafnorsky, sino de conocer el estado real de la mujer sometida a CU: sus cambios psicológicos y su relación con el entorno, aparte de las alteraciones orgánicas y las secuelas del tratamiento.
Es posible que las nuevas medicaciones citostáticas y la quimioterapia intraperitoneal10 ayuden a mejorar la calidad de vida y el pronóstico de nuestras pacientes. Sin embargo, es evidente que cuando el curso de la enfermedad es inexorable, es frecuente el recurrir a terapias agresivas e inútiles. En un reciente editorial11, sus autoras hacen hincapié en la inutilidad de los tratamientos agresivos o falsamente curativos, que tan sólo conducen a un progresivo deterioro del paciente, que suele confundir el término «respuesta» con el de «curación». En el análisis de los factores que condicionan las terapéuticas «fútiles», tal como las denominan Gruenigen et al11, no deben desestimarse las características personales tanto de la paciente como del médico. En éste pueden influir la edad, el sexo y la educación recibida durante la residencia, así como sus creencias y su propia ética profesional.
En nuestro país, que todavía carece de la subespecialización en ginecología oncológica, es imprescindible que se concentrara el tratamiento de las pacientes oncológicas en los hospitales que dispongan de equipos multidisciplinarios capaces de atender a todos los peculiares requerimientos de la paciente oncológica. Las decisiones sobre la estrategia del tratamiento son cruciales y condicionarán el futuro de la paciente. La CU y la cirugía de estadificación del cáncer de ovario sólo deben realizarlas los cirujanos ginecólogos-oncólogos. La mejor conducta «oncológica» que puede adoptar el ginecólogo no habituado en este tipo de cirugía es remitir el caso al centro de referencia, e inhibirse de los tratamientos para cuya aplicación no ha sido convenientemente formado.
Correspondencia:
Dr. S. Dexeus.
Departamento de Obstetricia y Ginecología.
Instituto Universitario Dexeus.
Paseo de la Bonanova, 69. 08017 Barcelona. España.
Correo electrónico: margal@dexeus.com
Fecha de recepción: 9/6/2006. Aceptado para su publicación: 21/11/2006.