INTRODUCCIÓN
La citología en medio líquido (Thin Prep Pap Test [TPPT]) es un método novedoso de preservación y manejo de las muestras citológicas, que puede sustituir al método tradicional (citología convencional [CC]). El TPPT es el primer sistema aprobado por la Food and Drug Administratation (FDA).
El cribado cervical fue originalmente empleado por Georges Papanicolaou para el estudio del estado hormonal en cobayas, y se utilizó en humanos para estudiar los cambios celulares que experimentan las mujeres durante el ciclo celular. Pronto se convirtió en un buen método diagnóstico del cáncer cervical y, con el tiempo, diversas generaciones de patólogos y citólogos hemos ido aprendiendo los cambios diagnósticos relacionados con las lesiones neoplásicas y preneoplásicas1.
Debemos decir que, si bien en el cribado poblacional no se han realizado estudios prospectivos aleatorizados que avalen la eficacia del método, al menos en España, en los últimos años la incidencia de cáncer cervical ha disminuido en un 70% en Estados Unidos y Europa1.
En un metaanálisis de CC, que comprende 62 publicaciones, se indica una sensibilidad del 11-99% y una especificidad del 14-97%. Los autores concluyen que la CC puede ser incapaz de conseguir a la vez una sensibilidad y una especificidad elevadas2. Otro estudio3, que evalúa los diferentes test de cribado, concluye que la CC tiene una sensibilidad global del 67% y una especificidad del 60%.
Como todos sabemos, la CC tiene falsos negativos y falsos positivos, que pueden deberse a errores en el muestreo, en la interpretación o en ambos, pero, según algunos autores, estas lesiones constituyen el 30% de los nuevos casos de cáncer de cérvix4,5.
Diferentes estudios demuestran que el TPPT permite diagnosticar un 30-200% más casos de lesión escamosa intraepitelial de bajo grado (low-grade squamous intraepithelial lesion [LSIL]) y un 25-103% más casos de alto grado (HSIL)6-13, incluso utilizando el método denominado split-sample, que en una misma toma efectúa un extendido convencional y el material sobrante lo disuelve en medio líquido14, si bien no proporciona los mismos resultados. Coste et al15 obtienen peores resultados con TPPT que con CC, y concluyen que el TPPT es menos válido y más susceptible de obtener falsos positivos y falsos negativos que la CC.
Los datos respecto al diagnóstico de células escamosas atípicas de significado incierto (atypical scamous cells of uncertain significance [ASCUS]) son variables. Para algunos autores el TPPT disminuye la cantidad de diagnósticos de ASCUS6 mientras que para otros la aumenta12,13,16. Abulafia et al17 realizan un metaanálisis de los datos publicados en la literatura médica respecto a la comparación entre CC y TPPT, revisando un total de 17 artículos que incluyen 35.592 pacientes. En este metaanálisis se observa un incremento de la sensibilidad y la especificidad del TPPT respecto a la CC, tomando como patrón de referencia la colposcopia y la biopsia. En otro artículo, publicado por Ferris et al18, se concluye que el TPPT aumenta la cantidad de exámenes satisfactorios, ASCUS y SIL de forma no estadísticamente significativa respecto a CC, y muestra una sensibilidad y una especificidad menores que ésta (del 52,6 frente al 63,1%, y del 99,5 frente al 99,7%, respectivamente). El valor predictivo positivo es mayor en el TPPT que en la CC (el 93,8 frente al 87,8%).
El Colegio Americano de Obstetras y Ginecólogos, en sus recomendaciones, basadas en la evidencia científica, indica que el TPPT es tan válido como la CC para el cribado poblacional19.
Si bien no es objeto de este trabajo, debemos comentar también la posibilidad de efectuar distintas pruebas, añadidas al diagnóstico citológico convencional en tomas conservadas con citología líquida Thin Prep de material no utilizado para el diagnóstico. Así, se han aplicado técnicas de reacción en cadena de la polimerasa (PCR), hibridación in situ, captura de híbridos, inmunohistoquímica, p-16, etc.20-23.
MATERIAL Y MÉTODOS
Hemos revisado los diagnósticos citológicos mediante CC y citología líquida (Thin Prep), los primeros entre el 1 de enero de 2001 y el 30 de junio del 2003, y entre el 1 de julio de 2003, en el momento de implantar el nuevo método, hasta el 30 de junio de 2004. En el primer grupo obtuvimos un total de 8.086 casos y en el segundo 3.064. Todas las pacientes procedían del Dispensario de LAC del Servicio de Ginecología y Obstetricia del Hospital del Mar de Barcelona. Por tanto, en ambos grupos las pacientes fueron previamente seleccionadas para acudir al Dispensario de LAC de nuestro Hospital.
Las tomas fueron efectuadas de forma usual en los casos de citología convencional, y fijadas con PreservCyt (Cytyc, Cytyc Corporation, Massachussetts); en los casos de citología líquida Thin Prep la toma se redujo a la zona de transición. El material obtenido fue disuelto en un frasco que contiene medio líquido fijador (PreservCyt).
Las citologías líquidas Thin Prep fueron procesadas en un aparato semiautomático Thin Prep 2000. La obtención de preparaciones se basa en 3 fases: dispersión de la muestra, recolección de ésta en un filtro y transferencia a un portaobjetos. Se utilizan filtros de policarbonato que disgregan los grupos de células y disuelven el moco, y un sistema de vacum a través de filtros que captan las células bajo control por ordenador. La recogida de células se controla para proporcionar el número adecuado de células, y la transferencia de las células captadas a la preparación se realiza por expulsión de aire ayudado con una carga electrostásica. El resultado final es un círculo de 20 mm de diámetro con células distribuidas al azar, en monocapa y bien conservadas.
Tanto las preparaciones de CC como las obtenidas con Thin Prep fueron teñidas con el método de Papanicolaou.
La interpretación fue realizada por una citotécnica, y la revisión la realizó, según los métodos usuales, un patólogo experto.
RESULTADOS
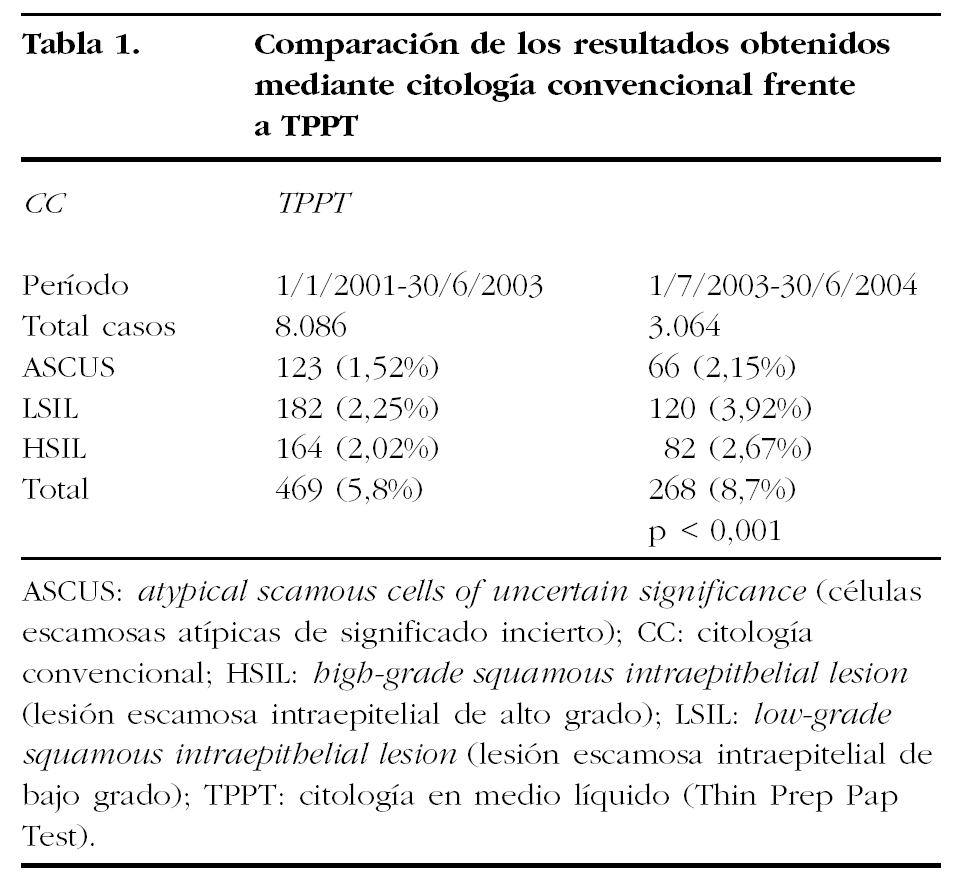
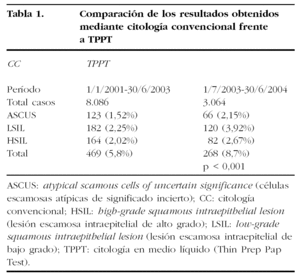
Se observó un incremento de todos los diagnósticos, ASCUS, LSIL y HSIL. El incremento solamente fue estadísticamente significativo si se tomaban los datos en conjunto, pero no lo fue si tomábamos los datos por diagnósticos (tabla 1).
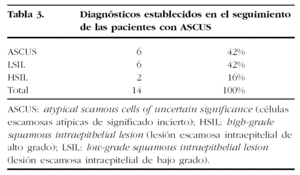
De las 66 pacientes con diagnóstico de ASCUS, solamente fueron seguidas 44, dado que 22 no acudieron a la visita de control. En las 44 pacientes seguidas, observamos la persistencia de la lesión o aparición de LSIL o HSIL en el 32% de los casos, y la negativización en el resto (tabla 2). De los casos que presentaron lesión en el seguimiento, la mayoría correspondieron a ASCUS o LSIL. Solamente el 16% de los casos fueron HSIL (tabla 3).
Las pacientes con diagnóstico de LSIL sumaron un total de 102. En 18 pacientes, por motivos diversos, se repitieron las tomas, por lo que revisamos un total de 120 citologías. De las 102 pacientes, una tenía un carcinoma escamoso de vagina, y 16 pacientes fueron biopsiadas (tabla 4). Se halló lesión en 15 de ellas (93,7%) y ausencia de lesión en una (6,3%).
El resto de las pacientes fueron citadas a los 6 meses para un control citológico; 25 pacientes no acudieron a control; 60 sí lo hicieron y fueron valoradas con citología; de éstas se negativizaron 24 (40%) y mostraron lesión 36 (60%). La distribución de las lesiones de detalla en la tabla 5.
No acudieron 25 de las 82 pacientes con diagnóstico de HSIL que fueron citadas para ser sometidas a una colposcopia y una biopsia. En las 57 restantes no se halló lesión en el 5,3% de los casos. El resto (94,7%) mostraba algún tipo de lesión displásica o cáncer, y las pacientes se distribuyeron de la siguiente forma: displasia leve (8,7%), displasia moderada/grave (84,3%) y carcinoma escamoso (1,7%) (tabla 6).
DISCUSIÓN
Nuestros resultados, por lo que respecta al incremento del diagnóstico, mediante citología Thin Prep, son similares a los casos reportados en la literatura médica, si bien, tomados por separado, no observamos un incremento estadísticamente significativo del diagnóstico.
Para Monsonego et al2, la citología líquida incrementa los diagnósticos de ASCUS, LSIL y HSIL, y en conjunto estos últimos son estadísticamente significativos.
Asimismo, diversos autores6,8,12,17,24-27 describen un incremento notable del diagnóstico de HSIL utilizando citología líquida, que va desde un 28%27 a un 233%21.
Para Abulafia et al17, basándose en un metaanálisis de 17 estudios que incluye a 21.752 pacientes, con correlación citología-biopsia, la citología líquida incrementa la sensibilidad y la especificidad para el diagnóstico de atipia, LSIL y HSIL, respecto a la citología convencional.
Por lo que respecta a los casos de ASCUS, de los que no disponemos de estudio histopatológico, los datos obtenidos en el seguimiento de estas pacientes son similares a los obtenidos por nosotros mismos en una serie previa28. Los datos que ofrece la literatura médica son variables: para algunos autores10,12,16,24,29,30, la citología líquida incrementa el porcentaje de diagnósticos de ASCUS, mientras que para otros6,7,8,13,18,26,27 los disminuye. En un metaanálisis de Berstein et al14, que incluye 154.380 casos de citología Thin Prep y 311.175 casos de CC, se observa un incremento porcentual del diagnóstico de ASCUS de un 3,28% en la CC a un 3,94% en la citología Thin Prep. Este mismo metaanálisis muestra un incremento de muestras satisfactorias en la citología Thin Prep respecto a la CC.
La correlación citología-biopsia en nuestros casos para la LSIL asciende a un 80,9% si consideramos solamente el diagnóstico de LSIL, y a un 93,6% si consideramos el diagnóstico de displasia de cualquier grado.
Para la HSIL, la correlación citología-biopsia en nuestros casos ascendería al 84,3% si consideramos solamente los diagnósticos de displasia moderada y grave, y al 86% si añadimos a las displasias de alto grado el de carcinoma.
Diversos autores6,7,8,12 muestran una correlación media entre citología y biopsia para LSIL del 76% y para HSIL del 90%. Para Weintraub et al16, la citología líquida incrementa la correlación citohistológica de un 41 a un 44% en la LSIL, y de un 82 a un 87% en la HSIL. Para Limaye et al25, la correlación histológica se incrementa con la citología líquida para la LSIL, pero disminuye para la HSIL.
Sin embargo, para Coste et al15, la CC es superior a la citología líquida en todos los aspectos.
Como conclusión, creemos que la citología en medio líquido (Thin Prep Pap Test), incrementa de forma más o menos significativa la detección de lesiones cervicales preneoplásicas y, por tanto, mejora el rendimiento de la citología cervicovaginal.
Correspondencia:
Dr. F. Alameda Quitllet.
Servicios de Anatomía Patológica, Ginecología y Obstetricia. Hospital del Mar. IMAS.
Passeig Marítim, 25-29. 08003 Barcelona. España.
Correo electrónico: 86780@imas.imim.es
Fecha de recepción: 24/11/05. Aceptado para su publicación: 16/1/07.