INTRODUCCION
Aproximadamente el 20% de los pacientes con dolor torácico y prueba de esfuerzo positiva no tienen enfermedad arterial coronaria significativa y se considera que presentan síndrome X cardiológico1. A pesar de la intensa investigación sobre la patogenia en síndrome X cardiológico en los últimos 30 años, aún se desconoce si los mecanismos biológicos de disfunción endotelial y del desequilibrio hemostásico están implicados, como lo están en la enfermedad arterial coronaria2. Los estudios en síndrome X cardiológico han ido perfilando la disfunción endotelial como uno de los mecanismos patogénicos de disfunción microvascular que podrían contribuir a la angina3.
En la enfermedad arterial coronaria, la disfunción endotelial con incremento del factor de Von Willebrand (FvW) activa el proceso de coagulación con incremento del factor tisular (TF), su inhibidor (TFPI-t)4, el fibrinógeno (Fb) y del inhibidor del activador del plasminógeno (PAI-1)5. Este desequilibrio, junto con los factores de riesgo clásicos, puede contribuir a la aterotrombosis y al desarrollo de enfermedad arterial coronaria6.
Recientemente se ha objetivado una asociación entre la disfunción endotelial y el desarrollo de enfermedad arterial coronaria en algunas mujeres con angina sin evidencia angiográfica de enfermedad arterial coronaria7. Sin embargo, los estudios en pacientes con síndrome X cardiológico muestran resultados conflictivos8. Por el contrario, en pacientes con angina vasoespástica, la disfunción endotelial se ha objetivado como la causante de la angina variante9 con riesgo de formación de trombo en presencia de valores elevados de Fb10 respecto de los controles sanos. En pacientes con síndrome X cardiológico, la presencia combinada de los biomarcadores de disfunción endotelial y del desequilibrio hemostásico a modo de «perfil biológico de riesgo»11 podría tener implicación en su fisiopatología. El presente estudio analizó la presencia combinada de los biomarcadores de disfunción endotelial (FvW) y del desequilibrio hemostásico (Fb, TFPI-t y PAI-1) en pacientes con síndrome X cardiológico, y los resultados se compararon con sujetos control y con pacientes estables sin enfermedad arterial coronaria con angina mixta y angina vasoespástica, y pacientes con enfermedad arterial coronaria.
MATERIAL Y MÉTODOS
Diseño del estudio y participantes
Estudio de controles sanos y de pacientes estables de 45 a 65 años reclutados consecutivamente durante 24 meses. Habían ingresado por angina y fueron dados de alta ≥ 6 meses previos a comenzar el estudio. Se seleccionaron cuatro grupos de pacientes, 3 grupos sin evidencia angiográfica significativa de enfermedad arterial coronaria (síndrome X cardiológico, angina mixta, angina vasoespástica) y un grupo con enfermedad arterial coronaria.
En los pacientes con síndrome X cardiológico y angina mixta la prueba de esfuerzo fue positiva y negativa, respectivamente. Ninguno presentó vasospasmo coronario durante la prueba de la ergobasina y la función ventricular izquierda fue normal. Se excluyó a aquellos con hipertrofia ventricular izquierda y con enfermedad cardíaca valvular.
Los pacientes con angina vasoespática presentaron angina de reposo, alteraciones del segmento ST (prueba de esfuerzo positiva), vasospasmo coronario severo durante la prueba de la ergobasina y la función ventricular izquierda fue normal. Se excluyó a aquellos con infarto agudo de miocardio (IAM) previo o con contractilidad miocárdica anormal. Permanecieron estables, con ≤ 1 episodio de angina por semana en promedio. Los pacientes con enfermedad arterial coronaria habían presentado un IAM diagnosticado por dolor torácico, elevación del segmento ST y liberación de enzimas miocárdicas (CK-MB > 10 µg/l) y una fracción de eyección > 50%. Se excluyó a aquellos pacientes con depresión mayor y a aquellos que recibían tratamiento con anticoagulantes o terapia hormonal.
El grupo control estuvo constituido por 20 participantes voluntarios sanos de la plantilla del hospital, de ambos sexos, apareados por edad. Se incluyó a 2 controles sanos por cada paciente con enfermedad arterial coronaria. No tenían antecedentes de enfermedad cardiovascular ni factores de riesgo mayor (diabetes, tabaquismo, hipertensión sistémica o hipercolesterolemia). Se excluyó a las mujeres en período de menopausia que recibían algún tipo de medicación o terapia hormonal.
La historia clínica incluyó los factores de riesgo y las características del dolor torácico. A todos los pacientes con angina y a 6 pacientes con IAM se les realizó una angiografía coronaria durante la fase aguda. El informe angiográfico fue valorado por dos observadores independientes, que no conocían a los pacientes. En los pacientes con angina, se evaluó el número de vasos coronarios epicárdicos con ≥ 50% de estenosis y la respuesta a ergobasina. Se consideró el espasmo coronario cuando el diámetro de la luz de la arteria se redujo > 80% durante la prueba de ergobasina. La fracción de eyección fue valorada con un ventriculograma izquierdo con contraste.
Muestras de sangre y ensayos
Se realizó una extracción de sangre venosa 6 meses postevento en condiciones de ayuno después de 30 min de reposo, entre las 8:30 y 9:30 h, en tubos Vacutainer que contenían citrato sódico y CTAD. El plasma se separó por centrifugación a 3.000 r.p.m a 4 °C y almacenado a 80 °C hasta su análisis. Se tuvo en cuenta las recomendaciones de la European Concerted Action on Thrombosis (ECAT)12.
El tratamiento con nitratos, antagonistas del calcio, bloqueadores beta, inhibidores de la enzima de conversión de angiotensina (ECA), hipolipemiantes o aspirina fue interrumpido al menos durante 4 días previos a la extracción. Sin embargo, la nitroglicerina sublingual fue permitida en episodios de dolor torácico eventual. Ningún paciente experimentó angina durante las 48 h que precedieron a la extracción de sangre. El protocolo fue aprobado por el comité ético del hospital y se obtuvo el consentimiento informado previo al estudio.
Determinaciones
Se determinaron: el FvW antigénico (ELISA, ASSERA CHROM FvW, Diagnostica Stago), el TFPI-t (ELISA, ASSERACHROM® TOTAL TFPI, Diagnostica Stago), el Fb (Von Clauss, Dade Behring, Alemania) y PAI-1 antigénico (ELISA, Tintelize PAI-1, Biopool International). Los coeficientes de variación intra e interensayo de los métodos estuvieron entre el 5 y el 10%.
Análisis estadístico
Los resultados se presentan en medianas (amplitud intercuartílica) y porcentajes. Las diferencias entre casos y controles se valoraron mediante la prueba exacta de Fisher para las variables sexo y factores de riesgo, y la prueba de la U de Mann-Whitney para las variables continuas edad y biomarcadores. Las diferencias entre los casos se valoraron con el estadístico exacto de Fisher para las variables sexo y factores de riesgo, y la prueba de Kruskal-Wallis para las variables continuas edad y biomarcadores. El coeficiente de correlación de Spearman se utilizó para determinar las relaciones entre los biomarcadores en los diferentes grupos de casos. Se usó el paquete estadístico SPSS para Windows (versión 10.0, Chicago, IL, EE.UU.). Un valor de p < 0,05 se consideró estadísticamente significativo para todos los análisis.
RESULTADOS
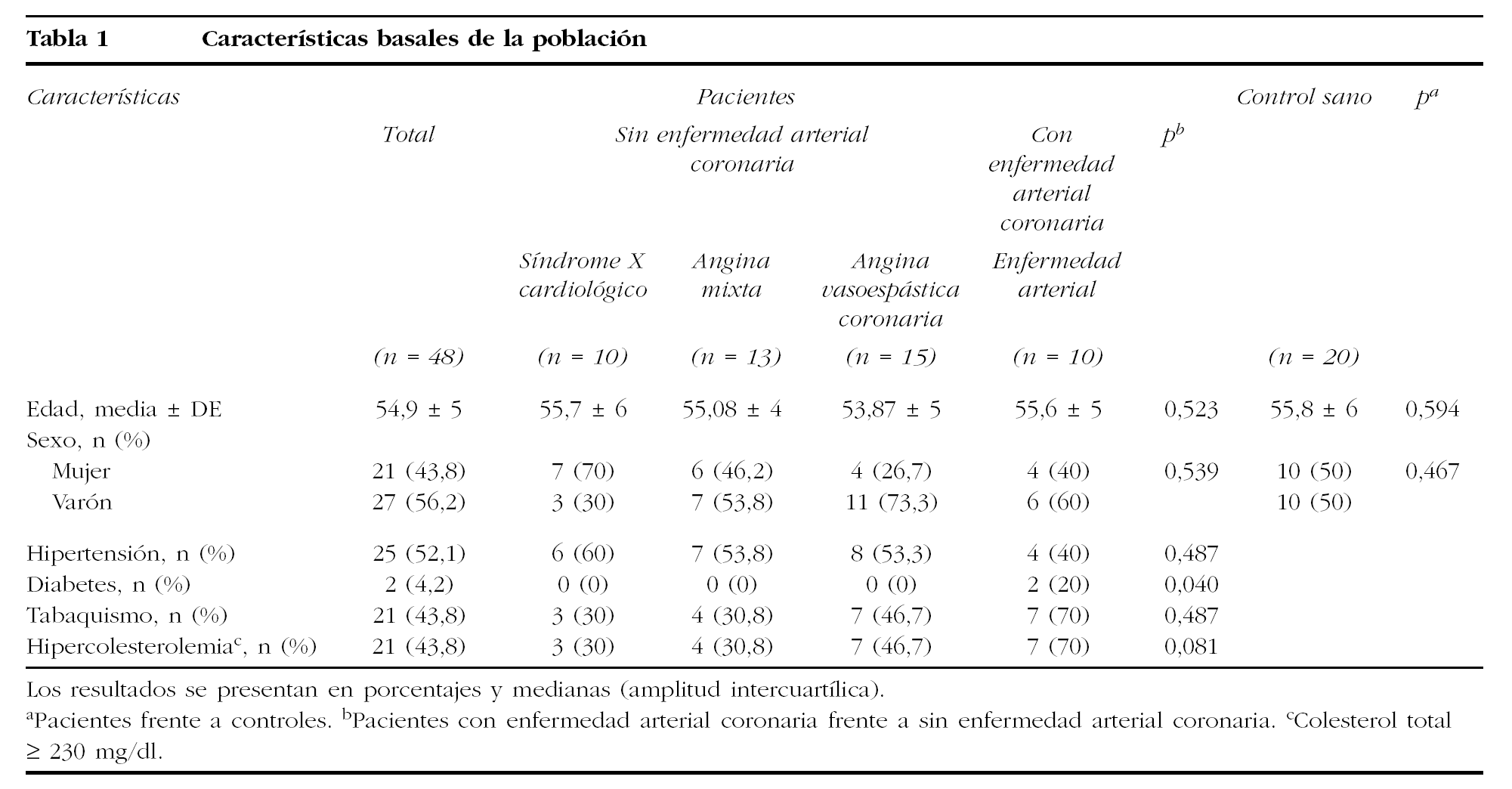
Características basales de la población (tabla 1)
En este estudio se reclutó a 48 pacientes estables, 3 grupos sin enfermedad arterial coronaria (10 con síndrome X cardiológico, 13 con angina mixta y 15 con angina vasoespástica) y un grupo de 10 pacientes con enfermedad arterial coronaria, y 20 controles sanos. La media de edad de los pacientes y controles fue de 54,9 ± 5 y 55,8 ± 6 (el 43,8 frente al 50% mujeres), respectivamente. En los pacientes con síndrome X cardiológico el 70% fueron mujeres y en angina mixta, angina vasoespástica y enfermedad arterial coronaria el 53,8, el 73,3 y el 60% fueron varones, respectivamente. No hubo diferencias significativas en la distribución por edad y sexo en el total de pacientes y controles ni entre pacientes con y sin enfermedad arterial coronaria.
Del total de pacientes, el 52% tenía hipertensión, el 43,8% hipercolesterolemia y eran fumadores activos y un 4% eran diabéticos. Sólo hubo diferencia significativa en la diabetes entre pacientes con y sin enfermedad arterial coronaria. En los pacientes con síndrome X cardiológico, la hipertensión arterial fue más frecuente (60%) mientras que en los pacientes con enfermedad arterial coronaria fueron más frecuentes el tabaquismo (70%) y la hipercolesterolemia (70%).
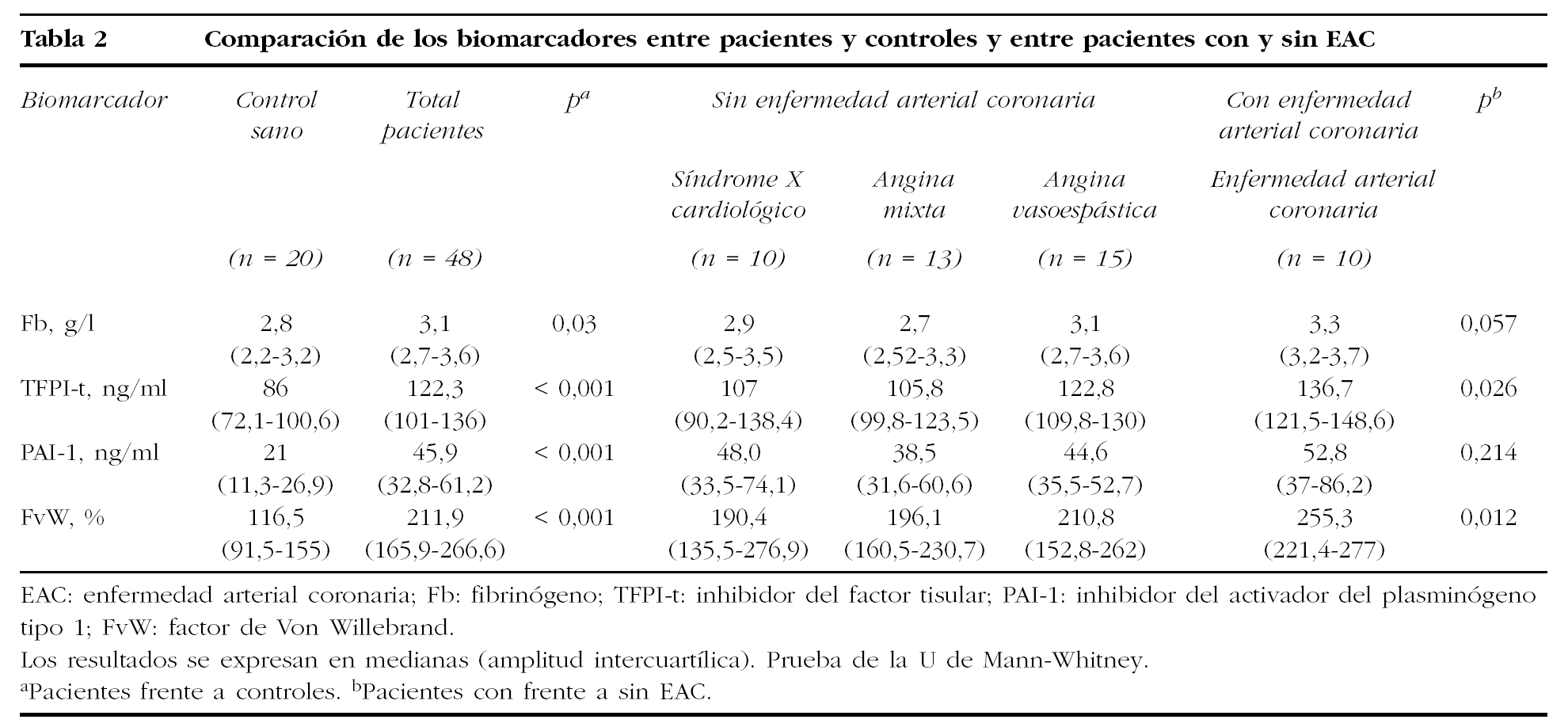
Biomarcadores entre pacientes y controles, y entre pacientes con y sin enfermedad arterial coronaria (tabla 2)
Hubo diferencias significativas en los niveles medios de todos los biomarcadores: Fb (3,1 [2,7-3,6] frente a 2,8 g/l [2,2-3,2]; p - 0,003), FvW (211,9 [165,9-266,6] frente a 116,5% [91,5-155]; p < 0,001), TFPI-t (122,3 [101-136] frente a 86 ng/ml [72,1-100,6]; p < 0,001) y PAI-1 (45,9 [32,8-61,2] frente a 21 ng/ml [11,3-26,9]; p < 0,001) en el total de pacientes respecto del grupo control. Sin embargo, cuando se comparó cada grupo de pacientes con el control también hubo diferencias significativas en todos los biomarcadores: Fb (angina vasoespástica 3,1 [2,7-3,6] [p - 0,04] y enfermedad arterial coronaria 3,3 g/l [3,2-3,7] [p - 0,001), FvW (síndrome X cardiológico 190,4 [135,5-276,9] [p - 0,004]; angina mixta 196,1 [160,5-230,7] [p < 0,001]; angina vasoespástica 210,8 [152,8-262] [p < 0,001] y enfermedad arterial coronaria 2,55% [221,4-277] [p < 0,001]), TFPI-t (síndrome X cardiológico 107 [90,2-138,4] [p - 0,03]; angina mixta 105,8 [99,8-123,5] [p - 0,002]; angina vasoespástica 122,8 [109,8-130] [p < 0,001] y enfermedad arterial coronaria 136,7 ng/ml [121,5-148,6] [p < 0,001]) y PAI-1 (síndrome X cardiológico 48 [33,5-74,1] [p < 0,001]; angina mixta 38,4 [31,6-60,6] [p < 0,001]; angina vasoespástica 44,6 [35,5-52,7] [p < 0,001] y enfermedad arterial coronaria 52,8 ng/ml [37-86,2] [p < 0,001]), excepto en el Fb en el síndrome X cardiológico y la angina mixta (2,9 [2,5-3,5] [p = 0,559] y 2,7 g/l [2,52-3,3] [p - 0,842]), respectivamente.
De la comparación entre el total de pacientes con y sin enfermedad arterial coronaria sólo hubo diferencias significativas en el TFPI-t (136,7 [121,5-148,6] frente a 110,5 ng/ml [100,9-127,5]; p = 0,02) y en el FvW (255,3 [221,4-277] frente a 200,5% [151-249,7]; p = 0,01). No hubo diferencias significativas entre los 4 grupos de pacientes.
Correlación entre biomarcadores de disfunción endotelial y del desequilibrio hemostásico en pacientes (tabla 3)
En el total de pacientes hubo correlación positiva entre TFPI-t y Fb (r - +0,33; p - 0,02) y entre TFPI-t y FvW (r - +0,55; p < 0,01). Sin embargo, en los pacientes sin enfermedad arterial coronaria el FvW se correlacionó positivamente con el TFPI-t (r - +0,4; p - 0,002) y en los pacientes con enfermedad arterial coronaria, el FvW se correlacionó positivamente con Fb (r - +0,7; p = 0,01).
DISCUSION
Los resultados de este estudio dan soporte a la hipótesis de que en pacientes estables con síndrome X cardiológico la disfunción endotelial (FvW) y el desequilibrio hemostásico (Fb, TFPI-t y PAI-1) están implicados. No obstante, el incremento combinado de estos biomarcadores refleja un estatus de actividad biológica aterotrombótica coronaria parecida a la de otros pacientes sin enfermedad arterial coronaria, angina mixta y angina vasoespástica, aunque es menos severa que en la enfermedad arterial coronaria3,7.
En este estudio los diferentes tratamientos suspendidos días previos a la extracción de la muestra no desestabilizaron clínicamente a los pacientes y pensamos que no influyeron en los resultados. De la comparación de los biomarcadores entre el total de pacientes y los sujetos control hallamos un incremento significativo similar en el Fb, FvW, TFPI-t y PAI-1. Los estudios previos muestran resultados contradictorios8,10. El aumento no significativo del Fb hallado en pacientes con síndrome X cardiológico y angina mixta podría reflejar menor severidad en la activación local de la coagulación en ausencia de enfermedad arterial coronaria1,13. Por el contrario, el incremento significativo de Fb en pacientes con angina vasoespástica, similar a los pacientes con enfermedad arterial coronaria, refleja cierta actividad protrombótica10.
Las diferencias significativas halladas entre pacientes con y sin enfermedad arterial coronaria en el FvW y TFPI-t, y las asociaciones significativas halladas entre estos biomarcadores en los pacientes sin enfermedad arterial coronaria y entre FvW y Fb en pacientes con enfermedad arterial coronaria, sugerirían que la disfunción endotelial podría ser el mecanismo común iniciador del desequilibrio hemostásico1,14. El predominio de inhibidores (TFPI-t) sobre activadores de la coagulación (Fb) en pacientes sin enfermedad arterial coronaria reflejaría menor severidad de la activación de la coagulación. Además, la asociación entre FvW y TFPI-t reflejaría estabilidad clínica o incluso ausencia de progresión de la aterotrombosis y de desarrollo de enfermedad arterial coronaria. Lo contrario puede interpretarse de la asociación entre FvW y Fb en la enfermedad arterial coronaria, que en caso de que apareciera de novo en los pacientes sin enfermedad arterial coronaria, sería un signo precoz de progresión de la aterotrombosis y del desarrollo de enfermedad arterial coronaria. También podría interpretarse como un signo de inestabilidad clínica, o un mayor grado de severidad en la activación de la coagulación15,16.
El hecho de que los pacientes con angina sin enfermedad arterial coronaria compartan mecanismos biológicos semejantes entre sí que los diferencian de los pacientes con enfermedad arterial coronaria y de los controles sanos podría significar que representan entidades biológicas semejantes, independientemente del resultado de la prueba de esfuerzo o de la presencia de vasospasmo.
En conclusión, la disfunción endotelial y el desequilibrio hemostásico parecen hallarse implicados en la fisiopatología del síndrome X cardiológico de forma parecida a los pacientes con angina mixta o angina vasoespástica, aunque de un modo menos severo que en enfermedad arterial coronaria.
Limitaciones
A pesar del escaso número de pacientes estudiados, las diferencias halladas permiten apuntar las conclusiones mencionadas, aunque ampliar el número de pacientes permitiría delimitar mejor el alcance de estos hallazgos.
Agradecimientos
Los autores agradecen la colaboración del personal administrativo, técnicos y de enfermería del hospital, a Eduardo Hermosilla por su supervisión en los análisis estadísticos y a la Fundaciò Institut de Recerca de l'Hospital Universitari Vall d'Hebron.
Correspondencia:
Dra. B.E. Meneses Londoño.
Unidad de Menopausia. Servicio de Ginecología Endocrina. Hospital Materno-Infantil Vall d'Hebron.
Pg. Vall d'Hebron, 119-129. 08035 Barcelona. España.
Correo electrónico: bemenese@vhebron.net
Fecha de recepción: 25/2/2005.
Aceptado para su publicación: 10/1/2006.