Conocer el conocimiento de las recomendaciones españolas para el cribado del cáncer de cuello uterino (CCU) y evaluar la utilización por los ginecólogos en España de las pruebas de detección del virus del papiloma humano (VPH).
Sujetos y métodosEncuesta dirigida a ginecólogos de la Sociedad Española de Ginecología y Obstetricia y la Asociación Española de Patología Cervical y Colposcopia. Se recogieron los datos aportados por 141 especialistas.
ResultadosParticipó el 30% de la población objeto de estudio. El 95,6% conocía las recomendaciones. El 93,5% utilizaba habitualmente la técnica de detección del VPH (el 77,7% como cribado de CCU). Los criterios de uso variaron considerablemente entre participantes. El principal motivo para no usar la técnica fue su falta de disponibilidad.
ConclusionesEs necesario reforzar la formación e información sobre las recomendaciones disponibles acerca de las nuevas estrategias de cribado y, en particular, del uso clínico de la determinación del VPH.
To determine knowledge of the Spanish guidelines for cervical cancer screening, and to evaluate the use of tests for the detection of human papilloma virus (HPV) by Spanish gynecologists.
Subjects and methodsThe survey focused on gynecologists who were members of the Spanish Society of Gynecology and Obstetrics and the Spanish Association of Cervical Pathology and Colposcopy. One hundred forty-one specialists completed the questionnaire.
ResultsThirty percent of the target population participated. A total of 95.6% were aware of the recommendations and 93.5% routinely used the test for the detection of the HPV (77.7% for cervical cancer screening). The criteria for the use of the test varied considerably among participants. The main reason for not using the technique was its unavailability.
ConclusionsTraining and information on the available recommendations for the new screening strategies and, particularly, on the clinical use of HPV determination should be reinforced.
La prevalencia de la infección por el virus del papiloma humano (VPH) en España es cercana al 9%. Considerando los genotipos de alto riesgo 16 y 18, la infección afecta al 2,3% de mujeres con citología normal1 y al 70-76% de todos los casos de cáncer de cuello uterino (CCU)2. La infección está relacionada con el patrón de comportamiento sexual de la comunidad y con la edad, siendo más frecuente entre los 15-25 años, con una disminución entre los 25-40 años, para posteriormente estabilizarse. La infección genital por VPH es una de las enfermedades de transmisión sexual más frecuentes en el mundo3,4. Se estima que el 80% de la población mundial, sexualmente activa, será infectada a lo largo de su vida5.
Su evolución natural es hacia la curación espontánea (aclaramiento) en más del 90% de los casos. Actualmente, el CCU se considera el final de una infección por VPH de riesgo alto ni aclarada ni controlada: no se espera que una mujer VPH negativa desarrolle un CCU6–8. Globalmente, el CCU es el tercer cáncer más frecuente en la mujer, con una incidencia estimada de 530.000 nuevos casos en 2008 y una mortalidad del 52%. El 85% de los casos se da en países en vías de desarrollo, donde supone el 13% de los cánceres femeninos9,10. En España, ocupa el undécimo lugar en la población femenina y el segundo en mujeres entre 15 y 44 años11. Con una incidencia, ajustada por edad, de 7,1 casos por cada 100.000 mujeres/año, es una de las más bajas de Europa, aunque la distribución geográfica del tumor dentro del país no es homogénea, oscilando entre 3,36 casos por 100.000 mujeres/año en Cuenca y 12,05 en Mallorca8. Sin embargo, según datos de la International Agency for Research on Cancer (IARC), España es uno de los pocos países europeos en los que la incidencia de cáncer de cérvix está aumentando, probablemente en relación a inmigración procedente de países con alta prevalencia y/o a un ineficaz cribado oportunista8,12,13.
El cribado del CCU tiene como objetivo la detección de las neoplasias intraepiteliales escamosas avanzadas (CIN2 y CIN3), así como el cáncer microinvasivo y el adenocarcinoma in situ (AIS). La citología cervical ha sido la herramienta más utilizada para el cribado del CCU durante los últimos 50 años. Sin embargo, debido a la fuerte asociación entre la infección por VPH y el desarrollo del CCU6,7,14, en los últimos años se ha propuesto la inclusión de técnicas de identificación del VPH, basadas en el análisis de la presencia de secuencias de ADN viral, en programas de cribado de CCU.
El test de VPH es la única prueba de cribado que ha demostrado en un ensayo prospectivo y aleatorizado provocar un impacto decreciente sobre la mortalidad por CCU15. Existe una cierta unanimidad en Europa al establecer propuestas que incluyen como prueba inicial de cribado la determinación de VPH a partir de los 30 años y hasta los 6516.
Si España quiere utilizar adecuadamente los recursos disponibles con un mejor coste/beneficio, debería de considerar este cambio en las técnicas de cribado. Sin embargo, los cambios deben de ir precedidos por una adecuada información a los profesionales y a la población. Con este objetivo, diversas sociedades científicas españolas consensuaron unas recomendaciones para el cribado del CCU, entre las que se incluía la realización de pruebas de detección del VPH17.
El objetivo de este estudio fue conocer el grado de conocimiento de estas recomendaciones y evaluar la utilización por los ginecólogos en España de las diferentes pruebas de detección del VPH.
Sujetos y métodosSe diseñó un estudio descriptivo transversal dirigido a todos los ginecólogos adscritos a la Sociedad Española de Ginecología y Obstetricia (SEGO) y a la Asociación Española de Patología Cervical y Colposcopia (AEPCC). En una primera fase se elaboró un cuestionario (tabla 1) en el que se preguntaba acerca del conocimiento de los encuestados del consenso del 200617 sobre el cribado de patología cervical y las indicaciones para solicitar las pruebas de detección del VPH. Las encuestas fueron respondidas de forma voluntaria, garantizando la confidencialidad de los datos recogidos. La encuesta se respondía a través del acceso a una WEB dedicada exclusivamente a este ejercicio para mantener los datos confidenciales (http://epilymph.org/dev/index2.php?option=com_ckforms&view=ckforms&id=3&Itemid=77). Tras el envío inicial en septiembre de 2009 se enviaron 3 recordatorios, mediante correo electrónico, en el plazo de 6 meses, a todos los profesionales suscritos a dichas sociedades de los que se disponía contacto (n = 467).
Encuesta sobre el uso en España de la prueba para la determinación del virus del papiloma humano (VPH)
| 1.- ¿En qué ámbito sanitario ejerce? | Público/Privado/Ambos |
| 2.- ¿En qué comunidad autónoma? | |
| 3.- ¿Conoce la existencia del nuevo consenso español 2006 de cribado de patología cervical en el que se definen las indicaciones del uso clínico de la prueba de VPH? | No/Sí |
| 4.- ¿Utiliza habitualmente la prueba de VPH para el cribado de cáncer de cuello uterino? | No/Sí |
| 5.- Si no la utiliza (puede marcar más de una respuesta) | |
| 5.1.-¿Podría indicar la razón? | No tengo informaciónNo lo tengo disponibleNo esta contemplado en el protocolo que se sigue en mi medioNo dispongo en mi medio de un laboratorio que lo practiqueLas evidencias que lo aconsejan no me parecen suficientesMe va bien con lo que hago |
| 6.-Si la utiliza (puede marcar más de una respuesta) | |
| 6.1.- ¿Cuál es la técnica de determinación que suele solicitar? | PCR caseraPCR comercial (especificar)PCR tiempo realCaptura de híbridosHibridación in situSecuenciaciónDesconozco la técnica que usa mi laboratorio de referenciaOtras (especificar) |
| 6.2. ¿En qué casos utiliza usted la prueba del VPH? | En cualquier edadA partir de los 30-35 añosEn mujeres de 40 o más años con historia deficiente de cribadoSolo en mujeres que considero de riesgo alto |
| 6.3.- Ante un resultado de prueba de VPH positiva con citología negativa, ¿qué prueba complementaria suele solicitar? | ColposcopiaRepito la citología:A los 3 mesesA los 6 mesesAl añoRepito la prueba de VPH:A los 3 mesesA los 6 mesesAl año |
| 6.4. ¿Usa la prueba para decidir la conducta que debe seguirse frente a los siguientes resultados citológicos? | InflamaciónL-SILASC-USASC-HAGCH-SILCáncer |
| 6.5. ¿Tiene en cuenta la edad a la hora de usar la prueba de VPH en una situación de selección de conducta? | No tengo en cuenta la edadSí tengo en cuenta la edad<20 añosEntre 20 y 30 años<30 años |
| 6.6. ¿Tiene en cuenta el nivel socioeconómico a la hora de usar la prueba de VPH en una situación de triage? | No/Sí |
| 6.7. ¿Tiene en cuenta la capacidad de seguimiento a la hora de usar la prueba de VPH en una situación de triage? | No/Sí |
| 6.8. ¿Utiliza la prueba de determinación de VPH en el estudio de los siguientes resultados histológicos? | Metaplasia escamosaCervicitis crónicaCIN ICIN IICIN IIICarcinoma escamosoAdenocarcinoma |
| 6.8. ¿Utiliza la prueba de determinación de VPH en el seguimiento de pacientes tratadas con cirugía, láser o crioterapia de las siguientes lesiones? | CIN ICIN IICIN IIICáncerOtros (especificar) |
| 6.9.- ¿En qué momento del seguimiento suele solicitar la prueba de determinación del VPH? | Inmediatamente postratamiento1-3 meses4-6 meses7-12 meses13-24 meses |
| 7.- Comentarios | |
AGC: células glandulares atípicas; ASC-H: atipia de células escamosas, no se descarta lesión intraepitelial; ASC-US: atipia de células escamosas de significado indeterminado; CIN: neoplasia intraepitelial cervical; H-SIL: lesión intraepitelial escamosa de grado alto; L-SIL: lesión intraepitelial escamosa de bajo grado; PCR: reacción en cadena de la polimerasa.
En una segunda fase se modificó el cuestionario reduciendo el número de preguntas, pero manteniendo el mismo contenido y se difundió entre los asistentes al XXII Congreso Anual de la AEPCC y en la XXX Reunión Nacional de la Sección de Ginecología Oncológica y Patología Mamaria de la SEGO.
La información se introdujo en una base de datos de Access. Los datos fueron explotados por el Instituto Catalán de Oncología. Se analizaron todas las respuestas obtenidas, ya fuese de manera conjunta para las preguntas incluidas en los dos cuestionarios como las respuestas que únicamente se incluyeron en la primera versión. Se calcularon las frecuencias absolutas y relativas (porcentaje) de las variables incluidas en el cuestionario mediante el programa SPSS versión 13.0.
ResultadosEl cuestionario fue contestado por 141 médicos. Un total de 50 (35,5%) respondieron el primer cuestionario por vía web y 91 (64,5%) rellenaron el cuestionario en los dos congresos anteriormente mencionados. El 54,7% (n = 76) ejercía en el ámbito público, el 19,4% (n = 27) en el ámbito privado, el 25,9% (n = 36) en ambos y 2 participantes no lo indicaron. En el análisis por comunidad autónoma (CC. AA.); la participación más numerosa fue de 37 (26,8%) ginecólogos en Cataluña, seguida de la Comunidad Valenciana con 18 (13%) y de Andalucía con 17 (12,3%).
A la pregunta sobre si conocían la existencia de las recomendaciones de la SEGO de 200617 respondieron 137 ginecólogos y sólo 6 (4,4%) contestaron que no. En cuanto a la pregunta sobre la utilización habitual de la prueba de determinación del VPH, de los 139 especialistas que respondieron, 130 (93,5%) contestaron afirmativamente y 9 (6,5%) indicaron que no la utilizaban. La técnica más utilizada fue la captura de híbridos (44,6%). En la tabla 2 se muestran las frecuencias de las técnicas utilizadas.
Pruebas de detección de VPH usadas por los participantes en la encuesta
| N= 130 | Total | PCR, n (%) | PCR comercial, n (%) | Captura de híbridos, n (%) | Hibridación in situ, n (%) | Secuenciación, n (%) | Desconocida, n (%) |
| Total respuestasa | 135 | 9 (6,9) | 33 (25,4) | 58 (44,6) | 6 (4,6) | 2 (1,5) | 27 (20,8) |
N: número de participantes que contestan a la pregunta; n= número de respuestas; PCR: reacción en cadena de la polimerasa; (%): porcentaje de uso de la técnica respecto del total de participantes.
Entre los ginecólogos que no utilizaban habitualmente las técnicas de detección de VPH, los motivos indicados fueron «falta de disponibilidad» (44,4%), «el protocolo que se sigue en mi medio no lo contempla» (22,2%), y con una frecuencia del 11% cada una reseñaron «falta de información», «las evidencias que lo aconsejan no me parecen suficientes», «no trabajo con patología del tracto genital inferior (PTGI)», «protocolo individualizado» y «el precio».
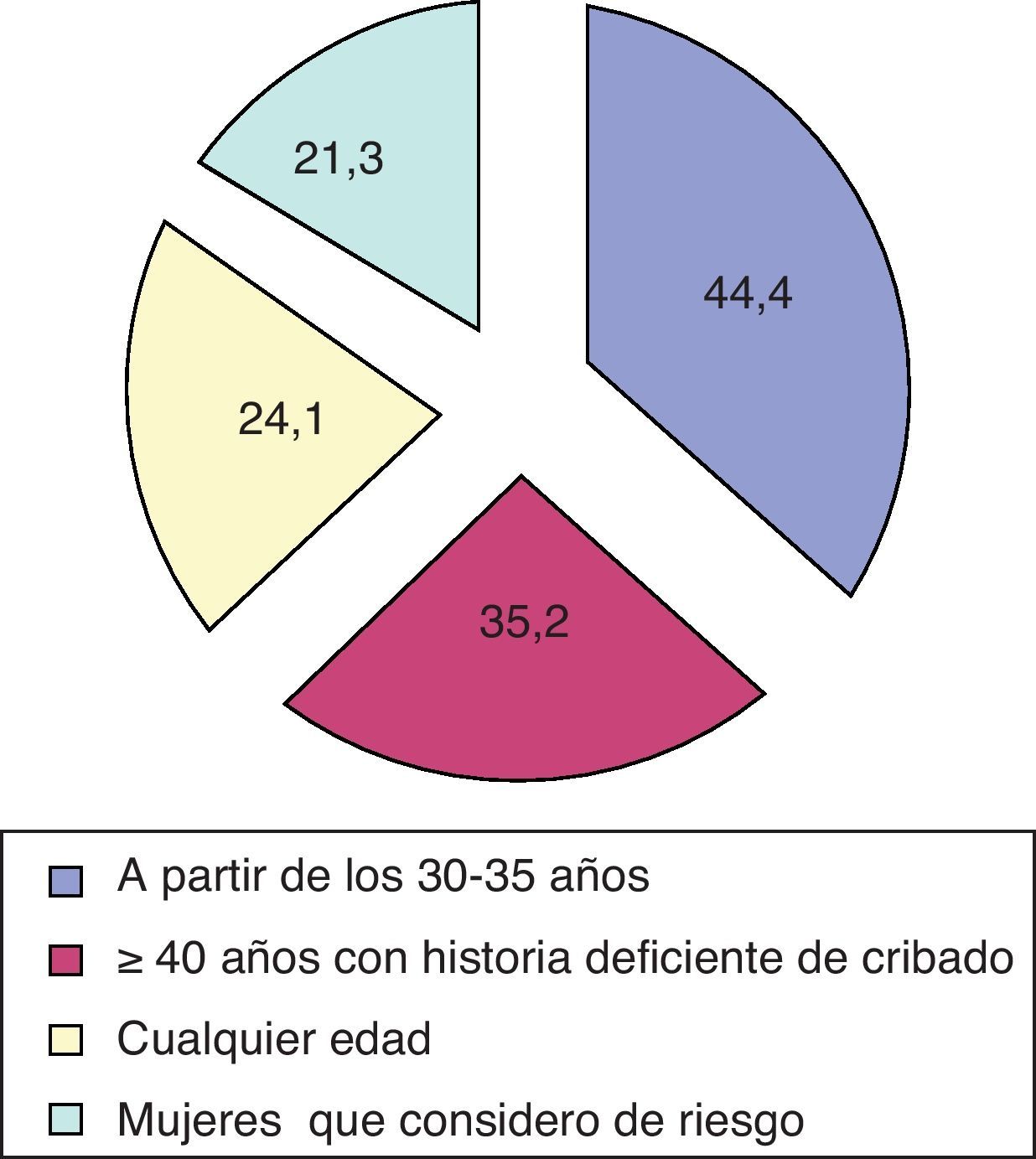
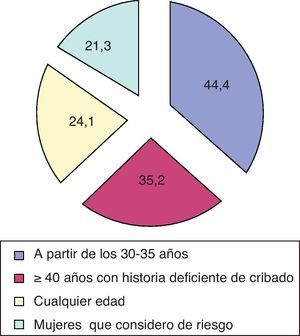
La utilización de las pruebas de detección del VPH para el cribado de CCU fue respondida afirmativamente por 108 encuestados (77,7%) de los 139 que respondieron a la pregunta. En la figura 1 se muestran los motivos indicados para la realización de estas pruebas.
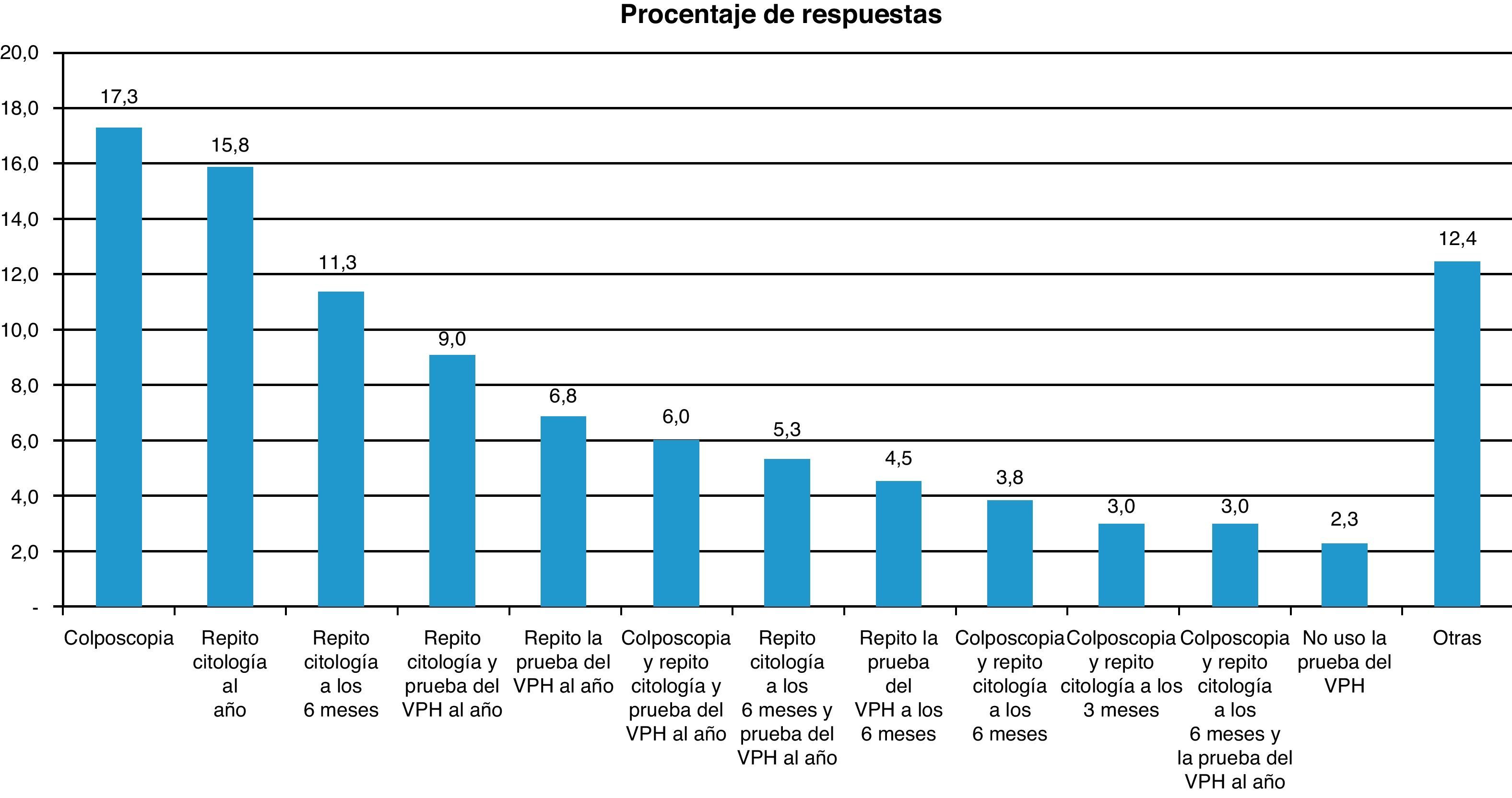
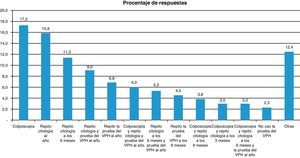
Respecto al tratamiento a seguir ante una citología negativa y una prueba VPH positiva, la mayoría de los encuestados realizarían solamente una colposcopia o repetirían exclusivamente la citología al año (fig. 2) (porcentajes calculados sobre los 133 participantes que han respondido a la pregunta).
Un total de 133 participantes en la encuesta afirmaron usar la detección del VPH en la toma de decisión frente a alguna lesión citológica. El 88,7% de ellos utilizaban la prueba ante un resultado citológico de ASC-US y alrededor del 44% frente al de células escamosas atípicas; no puede excluirse una lesión intraepitelial (ASC-H), células glandulares atípicas (AGC) o ante un resultado de lesión de bajo grado (L-SIL). Su uso disminuía si el resultado citológico era compatible con inflamación (2,3%) o con lesiones de alto grado (H-SIL) (25,6%) y cáncer (14,3%).
El 89,6% de los participantes en la encuesta tenían en cuenta la edad de la mujer, el 10% el nivel socioeconómico y el 51,1% la capacidad de seguimiento al solicitar la prueba de VPH.
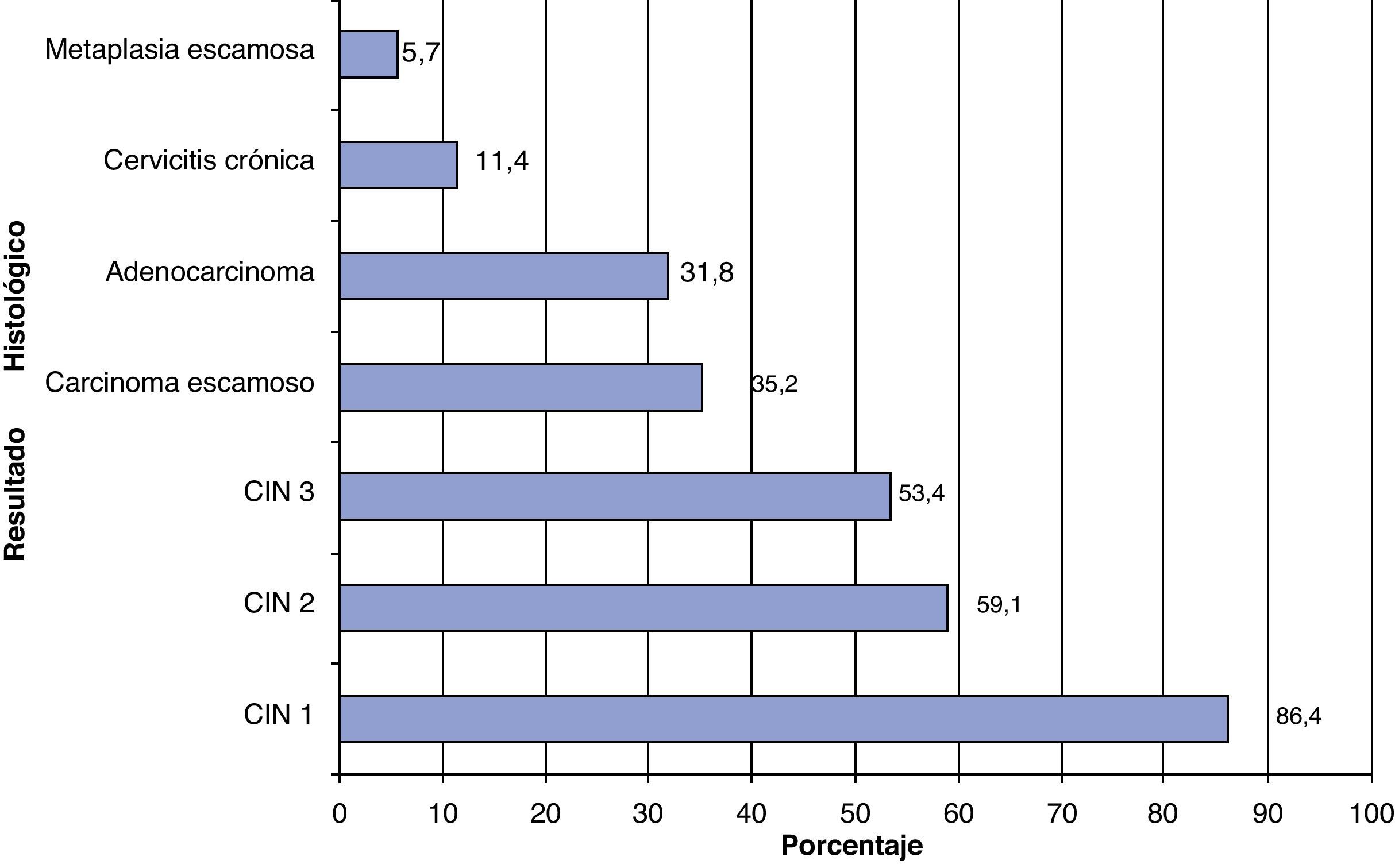
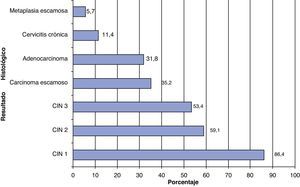
El 33,8% de los encuestados no utilizaban la detección del VPH según el resultado histológico. Entre los que sí la utilizaban la causa más frecuente era el hallazgo de CIN I (fig. 3).
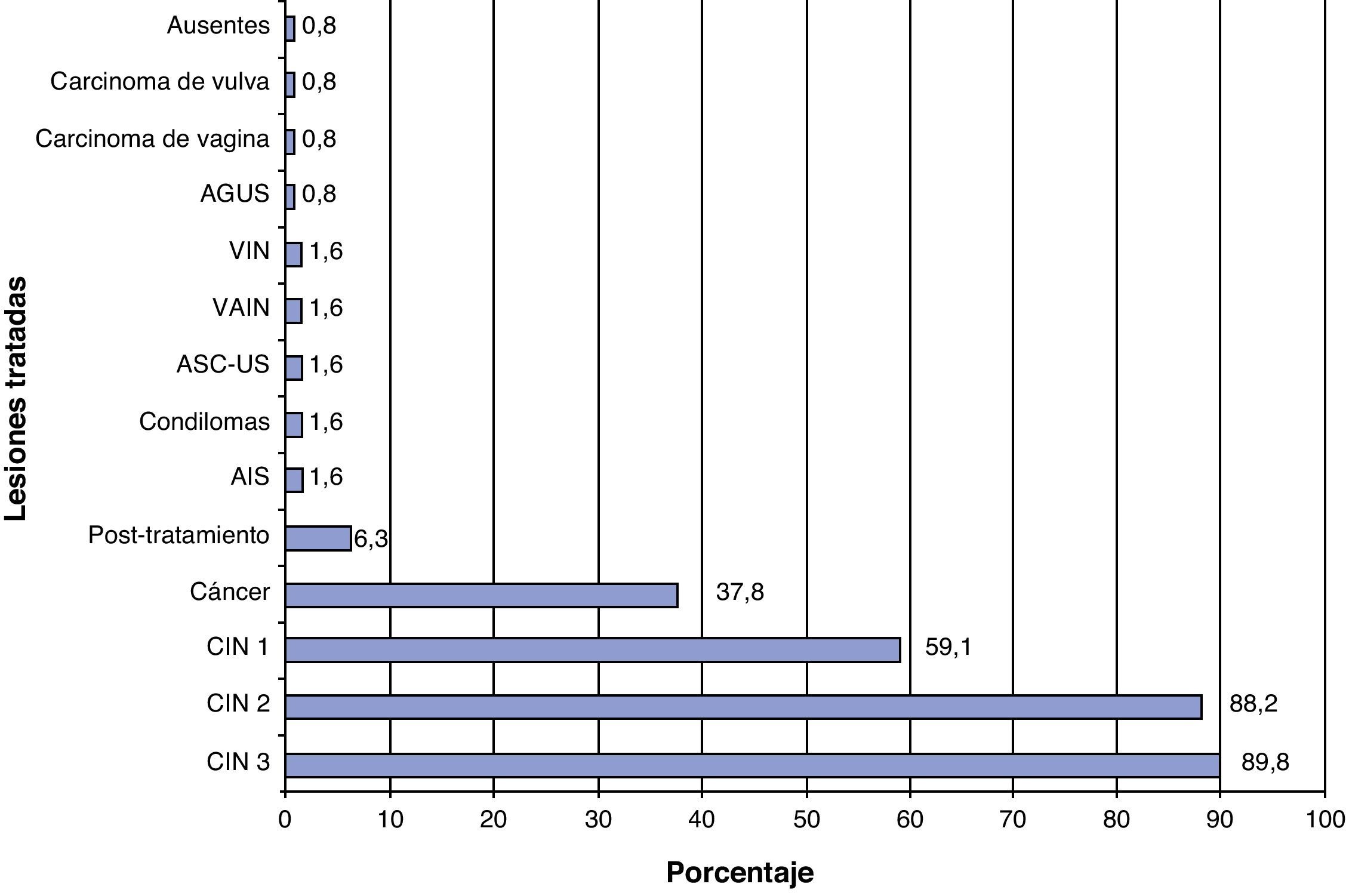
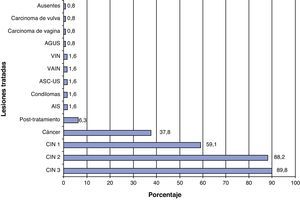
De total de 136 encuestados que responden a la pregunta, el 6,6% no utiliza la determinación de VPH en el seguimiento de pacientes tratadas con cirugía, láser o crioterapia y el 93,4% sí que la utilizan con esa finalidad. Cerca del 90% de estos últimos la solicitaban en el control del CIN 1 y del CIN 2 (fig. 4). El 41,9% de los encuestados solicitaban la prueba de VPH antes de los 6 meses del tratamiento, el 34,6% antes del primer año y el 7,4% inmediatamente después del tratamiento. El 8,8% de los encuestados indicaron que variaban el momento de solicitud de la prueba de VPH en el seguimiento dependiendo de la paciente.
Diagnósticos en los que se cree que la determinación del VPH es útil en el manejo posterior. AGUS: atipias de células glandulares de significado indeterminado; AIS: adenocarcinoma in situ; ASC-US: atipia de células escamosas de significado indeterminado; CIN: neoplasia intraepitelial cervical; VAIN: neoplasia vaginal intraepitelial; VIN: neoplasia vulvar intraepitelial.
Los dos comentarios adicionales más frecuentes fueron «la necesidad de unificar los criterios de actuación entre instituciones, pública y privada, y las CC. AA.» y «la evidencia científica no es suficiente como para incorporar la vacuna frente al VPH a la prevención del CCU».
DiscusiónLa mayoría de los encuestados se muestran conocedores de la existencia de recomendaciones sobre el uso de la prueba de detección del VPH en nuestro medio. También la mayoría asegura utilizar habitualmente dicha prueba. Sin embargo, teniendo en cuenta la población a la que iba dirigida la encuesta, hemos encontrado una baja participación en el estudio (30%), aunque con diferencias notables entre comunidades autónomas. La ausencia de respuesta podría estar relacionada con una falta de información o de concienciación con este tema y la distribución geográfica podría responder a un manejo diferente de los canales de difusión de la información entre comunidades. Sin embargo, utilizamos el correo electrónico como manera principal de difusión de la encuesta para facilitar el acceso de manera equitativa. Aunque son pocos los encuestados que reconocen no utilizar las pruebas de detección del VPH, parece que en su mayoría se debe a la falta de disponibilidad de estas en su medio.
El consenso de 2006 propone 5 recomendaciones para la realización de las pruebas de detección del VPH: prueba inicial de cribado, junto con la citología, en mujeres mayores de 35 años; para la identificación de mujeres con citología de ASC-US que precisan estudio colposcópico; en el seguimiento de pacientes con diagnóstico de CIN I, seleccionadas después de colposcopia; en mujeres posmenopáusicas con citología de L-SIL y para el control de curación después del tratamiento de neoplasias intraepiteliales17. En este estudio se evidencia que la técnica se utiliza casi por el 80% como cribado a partir de los 30-35 años y en mujeres con al menos 40 años con una historia deficiente de cribado. Casi una cuarta parte de los participantes la usan a cualquier edad. Sólo en un 21,3% de los casos se realiza en mujeres de riesgo.
En cuanto a su utilización en segunda línea de cribado, la mayor parte de los encuestados realizan la técnica ante resultados citológicos sospechosos, especialmente ante la presencia de L-SIL. También es habitual la utilización de la prueba de detección del VPH en el seguimiento de pacientes tratadas con cirugía, láser o crioterapia. El consenso de 200617 propone unas pautas de seguimiento en distintas situaciones de citología y test de VPH con el fin de unificar las formas de actuación, actualizadas en 201018. Sin embargo, como se ha visto en este estudio, la actitud de los profesionales ante un resultado positivo de la prueba del VPH con citología negativa es muy diversa (fig. 2), lo que pone en evidencia una falta de uniformidad de criterios debido probablemente a falta de información sobre las recomendaciones disponibles. Las recientes recomendaciones publicadas en 2010 sobre prevención primaria y secundaria, auspiciadas por la SEGO, reconocen esta falta de seguimiento en España y lo achacan a una falta de claridad y potencia en la transmisión del mensaje18.
Las técnicas más utilizadas para la detección del VPH son técnicas basadas en la reacción en cadena de la polimerasa (PCR) y la captura de híbridos (CH). Ambas tienen ventajas e inconvenientes: la primera incluye a un número importante de técnicas de las que no siempre se dispone de estudios de validación. En general, todas las técnicas de determinación de VPH requieren espacios adecuados y personal especializado para su realización. Los problemas de posible contaminación son más importantes cuando se realiza PCR que cuando se hace HC2. La genotipificación propuesta en algunas técnicas permite conocer el tipo específico de virus y las infecciones múltiples, lo que permite especular sobre la posible persistencia de la infección. La HC2 detecta 13 tipos de VPH de riesgo alto y requiere menos especialización del personal, aunque es importante mantener espacios limpios y personal adiestrado en la técnica19. Entre los participantes que utilizan pruebas de detección del VPH se observa un predominio de utilización del método de captura de híbridos, quizás por su facilidad de incorporación en el laboratorio. Ya que hay suficiente evidencia que avala la utilidad de la detección del VPH en la reducción de la incidencia y mortalidad por CCU18, parece necesario enfocar los esfuerzos en el desarrollo de un método rápido, de fácil uso, sensible y específico que permita su aplicación a gran escala y con un costo moderado19.
Los resultados de esta evaluación deben de interpretarse con cautela debido a la baja participación y a que la encuesta no ha sido previamente validada. La concordancia de las respuestas de los profesionales que realizan su actividad en zonas geográficas en las que esta bien estructurada la utilización del VPH, como en Cataluña, va a favor de que la encuesta mide lo que se había planteado al iniciar el estudio. Sin embargo, sería adecuado monitorizar en el tiempo el uso de estas técnicas y el conocimiento que de ellas tienen los profesionales.
ConclusionesDebido a la relativa facilidad para su identificación y abordaje terapéutico, el CCU es uno de los procesos neoplásicos más estudiados y mejor conocidos y quizá el único cáncer potencialmente prevenible en su totalidad20. El estudio presentado demuestra que es importante insistir en la sensibilización sobre la bondad de la prevención secundaria basada en la determinación del VPH. Es necesario reforzar la formación e información sobre las recomendaciones disponibles acerca de las nuevas estrategias de cribado, en general, y en particular sobre el uso clínico de la determinación del VPH.
Conflicto de interesesEsta publicación ha sido patrocinada por Meda, Qiagen y Sanofi Pasteur MSD.
Javier Cortés y José Manuel Ramón y Cajal han recibido becas de viaje y honorarios por asesorías y conferencias de GSK, Qiagen y Sanofi Pasteur MSD.
Silvia de Sanjosé ha recibido becas de viaje de GSK, Qiagen y Sanofi Pasteur MSD.
Jose Godínez ha recibido becas de viaje de Qiagen.
Los autores agradecen a Content Ed Net Madrid su asistencia editorial en la preparación de esta publicación.