El diagnóstico y seguimiento de la preeclampsia requiere de la determinación de proteinuria y la técnica de referencia para esta evaluación es la excreción en orina de 24h. Sin embargo, su recolección es engorrosa para la gestante e implica un retraso en el diagnóstico, por el tiempo que requiere. El objetivo de este estudio es evaluar el rendimiento diagnóstico del índice proteína/creatinina (IPC), calculado en un espécimen aislado, para descartar y predecir una proteinuria significativa (≥ 300mg/24h) en gestantes ambulatorias con sospecha o diagnóstico previo de preeclampsia.
Material y métodosEl IPC fue calculado en 106 especímenes de orina aislada, obtenidas tras la recolección del espécimen de 24h, de 66 gestantes que acudieron de forma ambulatoria a la Unidad de Medicina Materno Fetal de nuestro hospital por hipertensión gestacional. La correlación entre el IPC y la excreción de proteína durante 24h fue calculada. El análisis de curvas ROC fue utilizado para evaluar el rendimiento diagnóstico y establecer el punto de corte adecuado para predecir la ausencia o presencia de proteinuria significativa.
ResultadosSe detectó una proteinuria significativa en 31 orinas de 22 gestantes. La correlación entre el IPC y la excreción en orina de 24h fue significativa (rSpearman=0,658 [p=0,01]). El área bajo la curva ROC para el índice proteína/creatinina fue de 0,838, superior al de la tira reactiva (0,629 [IC del 95%, 0,551-62-0,707]). Ningún punto de corte fue adecuado para excluir y predecir simultáneamente una proteinuria significativa; sin embargo, el uso de la tira reactiva y del IPC, con dos puntos de corte, 120mg/g para descartar proteinuria significativa y 240mg/g para confirmarla, clasificó inicialmente de forma correcta el 44,3% de las orinas e hizo innecesaria la recolección de orina de 24h en el 51% de los casos.
ConclusionesEl IPC, usado conjuntamente con la determinación de proteína urinaria mediante la tira reactiva, es una herramienta útil en la evaluación inicial de gestantes ambulatorias con hipertensión gestacional o preeclampsia para descartar o predecir una proteinuria significativa, pero no debería ser utilizada como alternativa a la excreción de 24h en el rango intermedio de IPC, requiriendo la recolección de un espécimen de 24h para garantizar resultados seguros.
Diagnosis and follow-up of preeclampsia requires measurement of proteinuria and the gold standard for this evaluation is the 24-hour collection. However, this collection is cumbersome, time consuming and delays clinical diagnosis. The purpose of this study is assess the diagnostic performance of the spot urine protein/creatinine (P/C) ratio to predict the absence or presence of significant proteinuria (≥ 300mg per 24hours) among outpatient pregnant women with suspected or previous diagnosis of preeclampsia.
Material and methodsThe P/C ratio was calculated in 106 single voided urine samples, obtained after the completion of the 24-hour collection, from 66 outpatient pregnant women admitted to the Maternal Fetal Care Unit at our Hospital to follow-up of hypertension gestational. Correlation between the spot urine P/C ratio with the 24-hour urine protein excretion was calculated. Receiver operator characteristic (ROC) curves analysis was used to evaluate the diagnostic performance and to determinate the best cutoff to predict the absence or presence of significant proteinuria.
ResultsSignificant proteinuria on 24 hour collection urine was identified in 31 urines from 22 pregnant women. There was a significant correlation between the spot urine P/C and 24-hour urine protein excretion (rSpearman=0,658, p=0,01). ROC curves analysis revealed an area under the curve for spot P/C ratio of 0,838, greater than urine dipstick (0,629). No single P/C ratio cutoff was appropriate to rule-out or predict significant proteinuria; however, use of dipstick and spot urine P/C ratio, with two cutoffs, 120mg/g to predict the absence of significant proteinuria and 240mg/g to confirm it, clasiffied correctly 44,3% of urines and avoided the collection of 24hours urine in 51% of the cases.
ConclusionsSpot urine P/C ratio, in conjunction with dipstick urianalysis, is a useful test in the initial screen for rule-out and predict significant proteinuria in outpatient pregnant women with hypertensive pregnancy or preeclampsia, but it should not be used as an alternative to 24-hour total protein evaluation in midrange P/C ratio, requiring a full 24-hour urine for accurate results.
La preeclampsia, complicación que afecta a un 2-8% de las gestaciones y se asocia a un incremento de la morbimortalidad materno-fetal1, se caracteriza por el desarrollo de hipertensión y proteinuria después de la semana 20 de gestación en una gestante normotensa antes del embarazo. La proteinuria se define por una excreción urinaria igual o superior a 300mg en un espécimen de 24h2,3. Precisamente la necesidad de recolectar una muestra de 24h es la limitación principal de esta determinación, dado que dicha recolección está asociada a un importante error preanalítico y supone un retraso en el diagnóstico y posible manejo de la gestante afectada. Debido a estas desventajas, se ha planteado el uso de métodos alternativos para la detección de proteinuria significativa durante la gestación, como la determinación semicuantitativa con tira reactiva o el cálculo del índice proteína-creatinina (IPC) en un espécimen de orina aislada. El empleo de la tira reactiva es sencillo, barato y proporciona un resultado de forma rápida, pero su utilidad ha sido cuestionada4–7. El IPC es un parámetro ya ampliamente utilizado para la detección de proteinuria, tanto en niños como adultos, cuyo empleo es recomendado en guías internacionales8 y nacionales9,10. Sin embargo, su empleo en el contexto de la gestación sigue siendo controvertido, aunque su uso es recogido por la International Society for the Study of Hypertension in Pregnancy (ISSHP) en sus recomendaciones para el diagnóstico de trastornos hipertensivos durante el embarazo11. Algunos estudios desaconsejan su empleo por su bajo rendimiento diagnóstico12,13, mientras que otros apoyan su uso, fundamentalmente para la exclusión de proteinuria significativa14–18; sin embargo, no existe unanimidad respecto a los puntos de corte que deben ser aplicados en la práctica clínica19 y además la mayoría de los estudios han sido realizados en población gestante hospitalizada20, por lo que los puntos de corte obtenido no serían aplicables a población gestante ambulatoria. El objetivo de este estudio es evaluar el rendimiento del IPC, compararlo con el de la determinación de proteína urinaria mediante tira reactiva y establecer los puntos de corte más adecuados para la exclusión/predicción de proteinuria significativa en una población de mujeres gestantes ambulatorias con enfermedad hipertensiva del embarazo (EHE).
Material y métodosEste estudio prospectivo ha sido realizado en el Hospital Universitario Santa María del Rosell de Cartagena entre abril de 2009 y abril de 2010. Se seleccionó para el estudio a gestantes, en la semana 20 o posterior de gestación, que acudieron de forma ambulatoria a la Unidad de Medicina Materno Fetal de nuestro hospital por EHE y a las que se solicitó la determinación de la excreción urinaria de proteína como parte del protocolo para el diagnóstico y control de la preeclampsia. En todas ellas se solicitó la recolección de una muestra de orina aislada, posterior a la de la orina de 24h, para estudio mediante tira reactiva y cálculo del IPC, así como el consentimiento para la realización de dichas determinaciones. Se definieron los siguientes criterios de exclusión: a) no recolección de la muestra de orina aislada; b) concentración de creatinina en orina aislada inferior a 30mg/dl; c) recolección inadecuada de la orina, valorada mediante encuesta a la gestante; d) alteración del sedimento urinario, valorado mediante microscopía de campo brillante: hematuria (10 o más hematíes por campo de alta resolución) y/o leucocituria (10 o más leucocitos por campo de alta resolución) y/o datos sugerentes de infección urinaria (leucocituria con bacteriuria o positividad a la prueba de nitritos en la tira reactiva), y e) presencia de hipertensión arterial o patología renal conocida previa a la gestación.
MétodosLa concentración urinaria de proteína fue determinada mediante turbidimetría, con adición previa de cloruro de benzetonio, y la de creatinina mediante la reacción cinética de Jaffé o del picrato alcalino, ambas en los autoanalizadores HITACHI 917 y Cobas 6000 (Roche Diagnostics), cuya transferibilidad de resultados fue previamente comprobada. Para la determinación semicuantitativa de la concentración urinaria de proteínas se emplearon las tiras reactivas para urianálisis Combur-test 10, en la que dicha determinación se basa en el error proteico del indicador de pH, con lectura mediante espectroscopia de reflectancia en un analizador Miditrón, expresándose los resultados como: negativo, 1+ (25mg/dl), 2+ (75mg/dl), 3+ (150mg/d) y 4+ (500mg/dl).
Análisis estadísticoPara el análisis estadístico de los datos se emplearon los programas SPSS v 15.0 y EPIDAT 3.1. La asociación entre la excreción de proteína en orina de 24h y la determinación de proteína en orina mediante tira reactiva y el IPC se analizaron mediante el coeficiente de correlación de Spearman. Se evaluó el rendimiento diagnóstico de ambos parámetros mediante el análisis de curvas ROC y se establecieron los puntos de corte con mayor utilidad para excluir/confirmar una proteinuria significativa, definida por una excreción en orina igual o superior a 300mg/24h.
ResultadosTras aplicar los criterios de exclusión, se excluyeron 37 orinas y se incluyeron en el estudio 106 muestras de orina pareadas (de 24h y aisladas) recogidas por 66 gestantes, cuya edad media (desviación estándar) fue de 32,8 (5,3) años (rango: 17-43); 26 gestantes proporcionaron más de un espécimen de orina para el estudio.
Se detectó una proteinuria significativa en 31 orinas de 24h (29,3%) correspondientes a 22 gestantes (20,8%). El rango de proteinuria fue de 70-18.750mg/24h. Sólo 2 gestantes (1,9%) presentaron una proteinuria en el rango de preeclampsia severa (≥ 2g/24h).
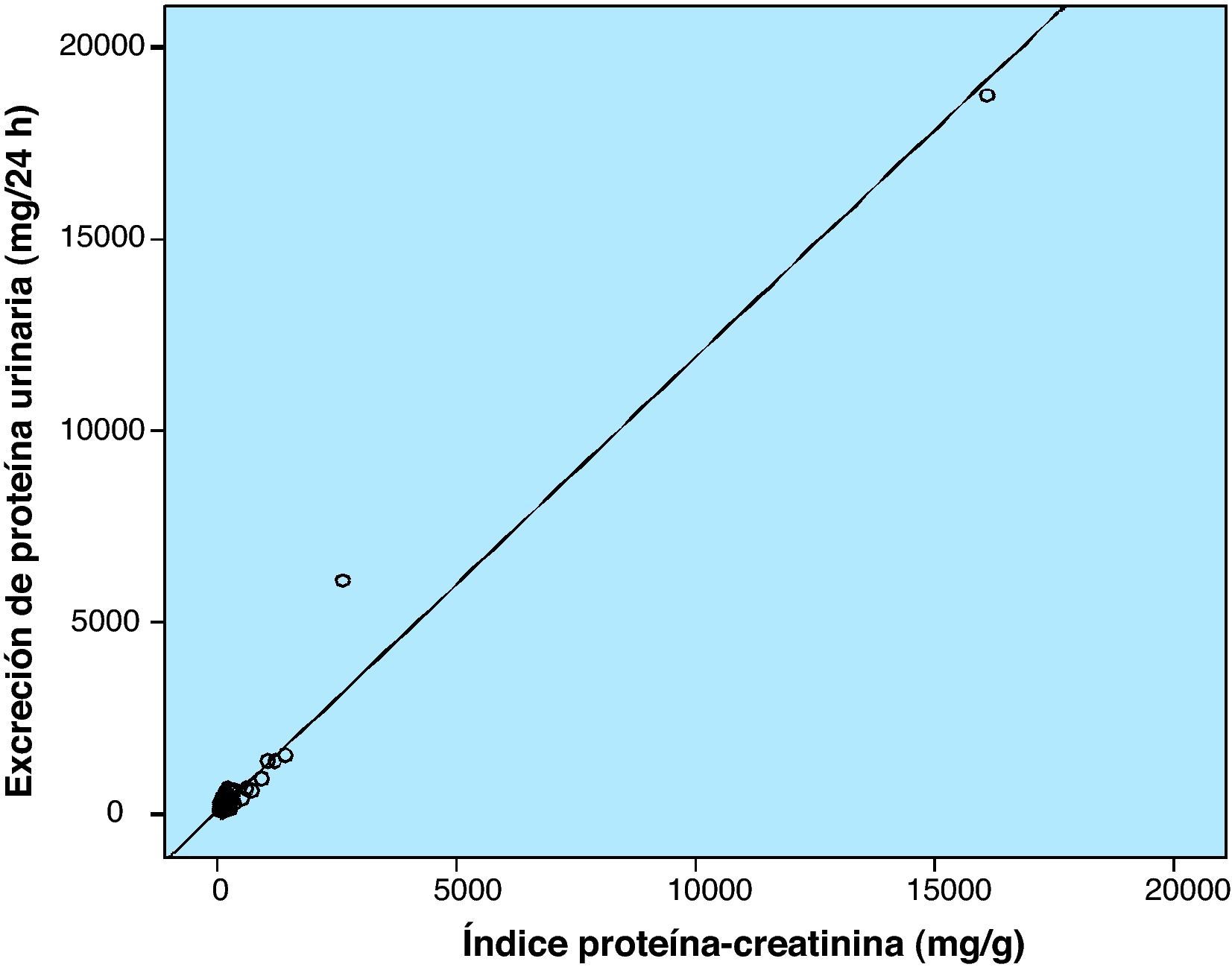
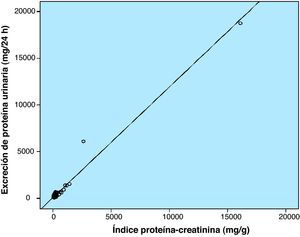
Se correlacionó el IPC con la excreción urinaria de proteína en 24h, obteniéndose un coeficiente de correlación de Spearman de 0,658 (p=0,01) (fig. 1).
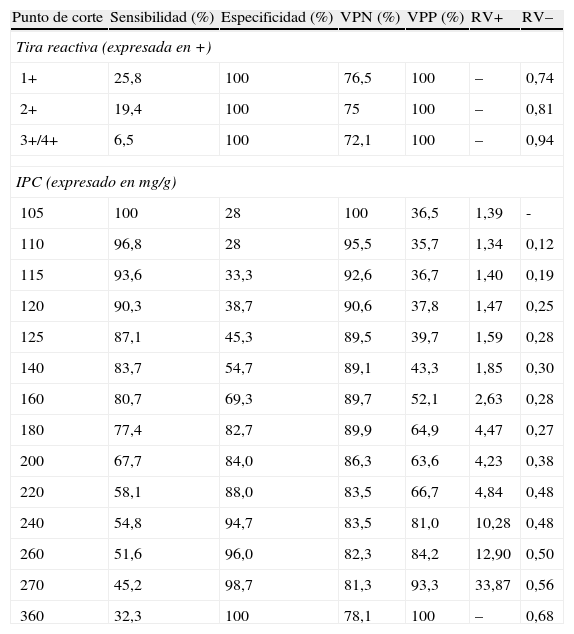
El rendimiento diagnóstico del IPC y de la determinación semicuantitativa de proteína urinaria mediante tira reactiva, expresado en términos de sensibilidad, especificidad, valores predictivos positivo (VPP) y negativo (VPN) y razones de verosimilitud positiva (RV+) y negativa (RV−), se muestra en la tabla 1.
Rendimiento diagnóstico del IPC para predecir una proteinuria ≥ 300mg/24h
| Punto de corte | Sensibilidad (%) | Especificidad (%) | VPN (%) | VPP (%) | RV+ | RV– |
| Tira reactiva (expresada en +) | ||||||
| 1+ | 25,8 | 100 | 76,5 | 100 | – | 0,74 |
| 2+ | 19,4 | 100 | 75 | 100 | – | 0,81 |
| 3+/4+ | 6,5 | 100 | 72,1 | 100 | – | 0,94 |
| IPC (expresado en mg/g) | ||||||
| 105 | 100 | 28 | 100 | 36,5 | 1,39 | - |
| 110 | 96,8 | 28 | 95,5 | 35,7 | 1,34 | 0,12 |
| 115 | 93,6 | 33,3 | 92,6 | 36,7 | 1,40 | 0,19 |
| 120 | 90,3 | 38,7 | 90,6 | 37,8 | 1,47 | 0,25 |
| 125 | 87,1 | 45,3 | 89,5 | 39,7 | 1,59 | 0,28 |
| 140 | 83,7 | 54,7 | 89,1 | 43,3 | 1,85 | 0,30 |
| 160 | 80,7 | 69,3 | 89,7 | 52,1 | 2,63 | 0,28 |
| 180 | 77,4 | 82,7 | 89,9 | 64,9 | 4,47 | 0,27 |
| 200 | 67,7 | 84,0 | 86,3 | 63,6 | 4,23 | 0,38 |
| 220 | 58,1 | 88,0 | 83,5 | 66,7 | 4,84 | 0,48 |
| 240 | 54,8 | 94,7 | 83,5 | 81,0 | 10,28 | 0,48 |
| 260 | 51,6 | 96,0 | 82,3 | 84,2 | 12,90 | 0,50 |
| 270 | 45,2 | 98,7 | 81,3 | 93,3 | 33,87 | 0,56 |
| 360 | 32,3 | 100 | 78,1 | 100 | – | 0,68 |
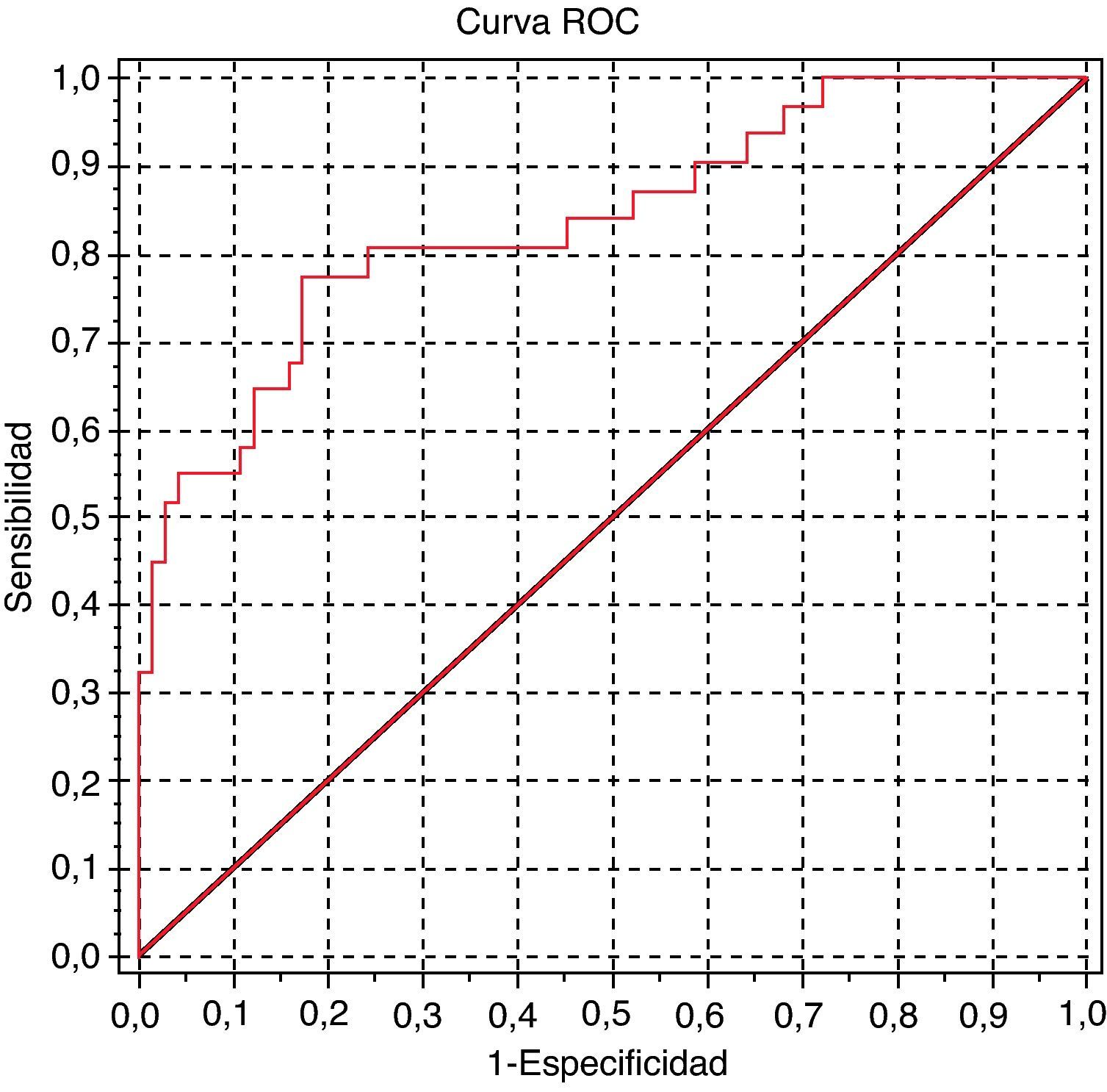
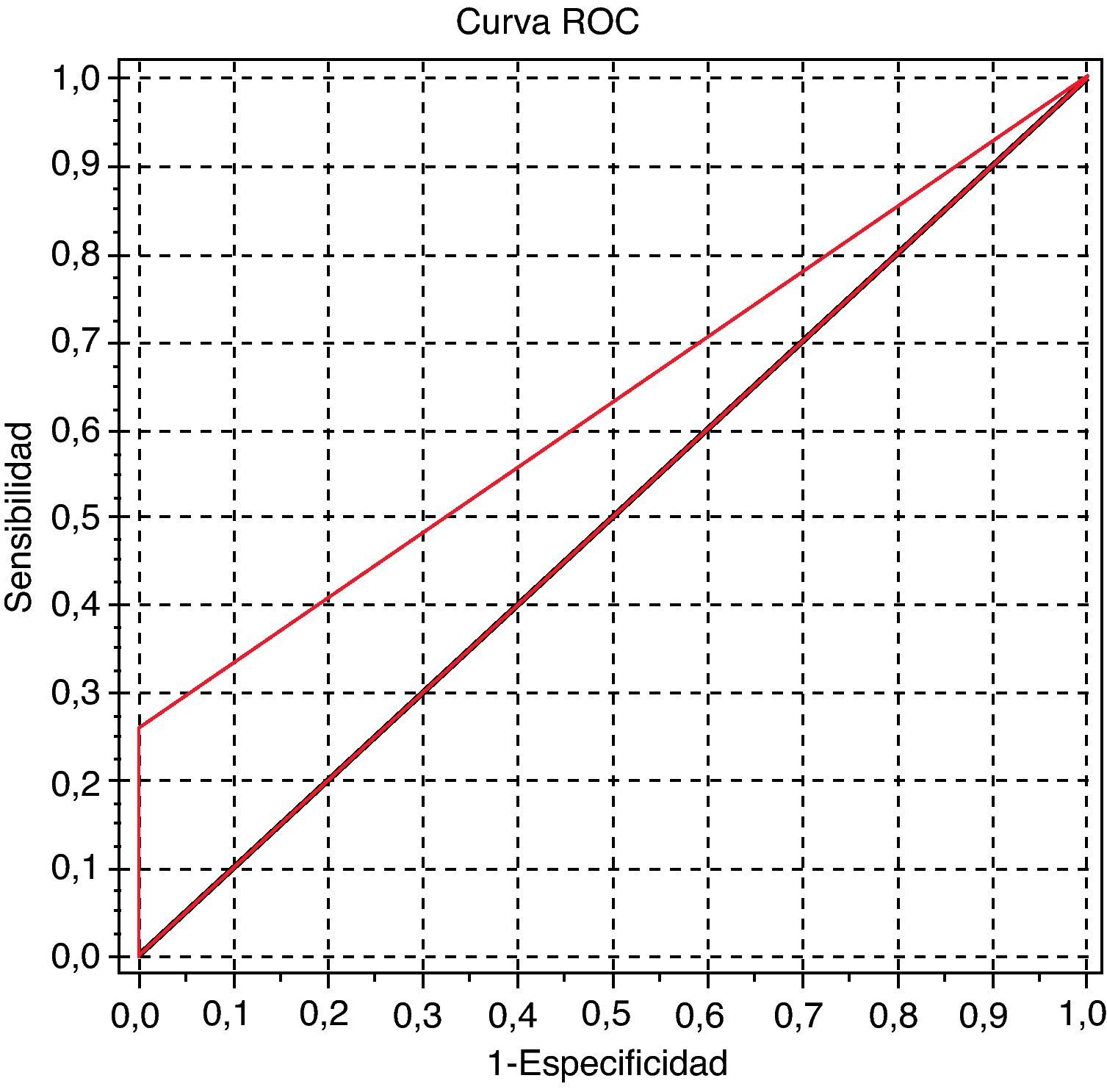
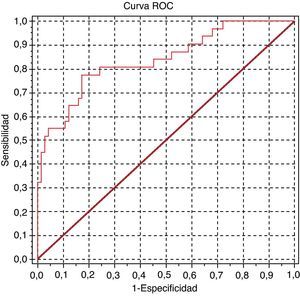
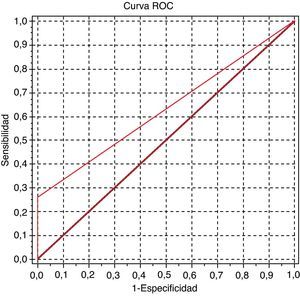
El área bajo la curva ROC fue de 0,838 (IC del 95%, 0,745-0,932; fig. 2) y 0,629 (IC del 95%, 0,551-62-0,707; fig. 3) para el IPC y para la determinación de proteína urinaria mediante tira reactiva, respectivamente.
DiscusiónLa proteinuria constituye el elemento diferenciador entre la hipertensión gestacional y la preeclampsia. La prueba de referencia para la detección de proteinuria significativa es la excreción de proteína en orina de 24h2, cuya determinación está sometida a errores de tipo preanalítico, dada la dificultad de garantizar una recolección completa, y supone un retraso en el diagnóstico o control de la paciente. La necesidad de este tipo de muestra sería consecuencia de la alta variabilidad de la concentración urinaria de proteína durante el día, asociada a factores como la ingesta y excreción de agua, la diuresis, el ejercicio y la dieta, y que además aumenta a consecuencia de cambios patológicos en la presión arterial21. Dicha variabilidad excluiría el uso de un espécimen aislado para la medida de la concentración de proteína urinaria2. Sin embargo, diversos estudios han demostrado una menor variabilidad del IPC, parámetro calculado en una muestra aislada, que de la concentración de proteína medida en diversas muestras tomadas a lo largo de un día22,23, así como una fuerte correlación entre el IPC y la proteinuria de 24h16,18,24. Por ello, la medida del IPC en una muestra aislada sería una alternativa fiable a la excreción en el espécimen de 24h.
Revisiones recientes14,19,21 recomiendan el empleo del IPC como test para descartar una proteinuria igual o superior a 300mg/24h. Además, su uso para el diagnóstico de preeclampsia es recogido por la ISSHP11, que recomienda utilizar como punto de corte un IPC de 30mg/mmol; sin embargo, el empleo en la práctica clínica de esta determinación está poco extendido, probablemente por la falta de consenso respecto al punto de corte a emplear en su manejo rutinario19,21. Además, la mayoría de los estudios han sido realizados en población hospitalizada16,24,25, por lo que los resultados no serían extrapolables al contexto ambulatorio. Así, Rodríguez-Thompson et al24 y Al et al25 recomiendan un IPC de 190mg/g para predecir una proteinuria significativa en población hospitalizada y Saudan et al26 recomiendan un IPC de 30mg/mmol, obtenido en una población formada por gestantes hospitalizadas y ambulatorias. Young et al27 no encontraron un punto de corte adecuado para la detección de proteinuria significativa en gestantes ambulatorias, aunque concluyen que un IPC inferior a 150mg/g excluye dicha proteinuria. Más recientemente, Dwyer et al28, en una población mayoritariamente ambulatoria, recomiendan una estrategia basada en el uso secuencial de la tira reactiva y del IPC, con un punto de corte inferior a 150mg/g para descartar una proteinuria significativa y de 280mg/g para predecirla. Otro factor que contribuiría a las diferencias en los puntos de corte es la variabilidad de los métodos de medida de proteína en orina.
Nuestro estudio demuestra que el IPC es una herramienta útil en el estudio de la proteinuria, como demuestra un área bajo la curva ROC de 0,838, similar al de estudios que abogan por el uso de este parámetro24,28. El punto de corte con mayor rendimiento diagnóstico para la detección de proteinuria significativa fue de 180mg/g, similar al descrito por otros autores24,28. Sin embargo, consideramos, al igual que otros autores18,27,28, que una estrategia basada en este único punto de corte no es útil en la práctica clínica, dado que el empleo de este valor hubiera supuesto una clasificación errónea de 20 orinas (18,9%), correspondientes a 17 gestantes (24,2%).
Respecto a la comparación con la tira reactiva, nuestros resultados son iguales a los de otros estudios28. El IPC es un parámetro con mayor sensibilidad y, por tanto, más útil para descartar una proteinuria significativa, que la determinación de proteína mediante tira reactiva. En nuestro estudio, la positividad de la tira reactiva predijo con una especificidad y valor predictivo positivo máximo una proteinuria significativa.
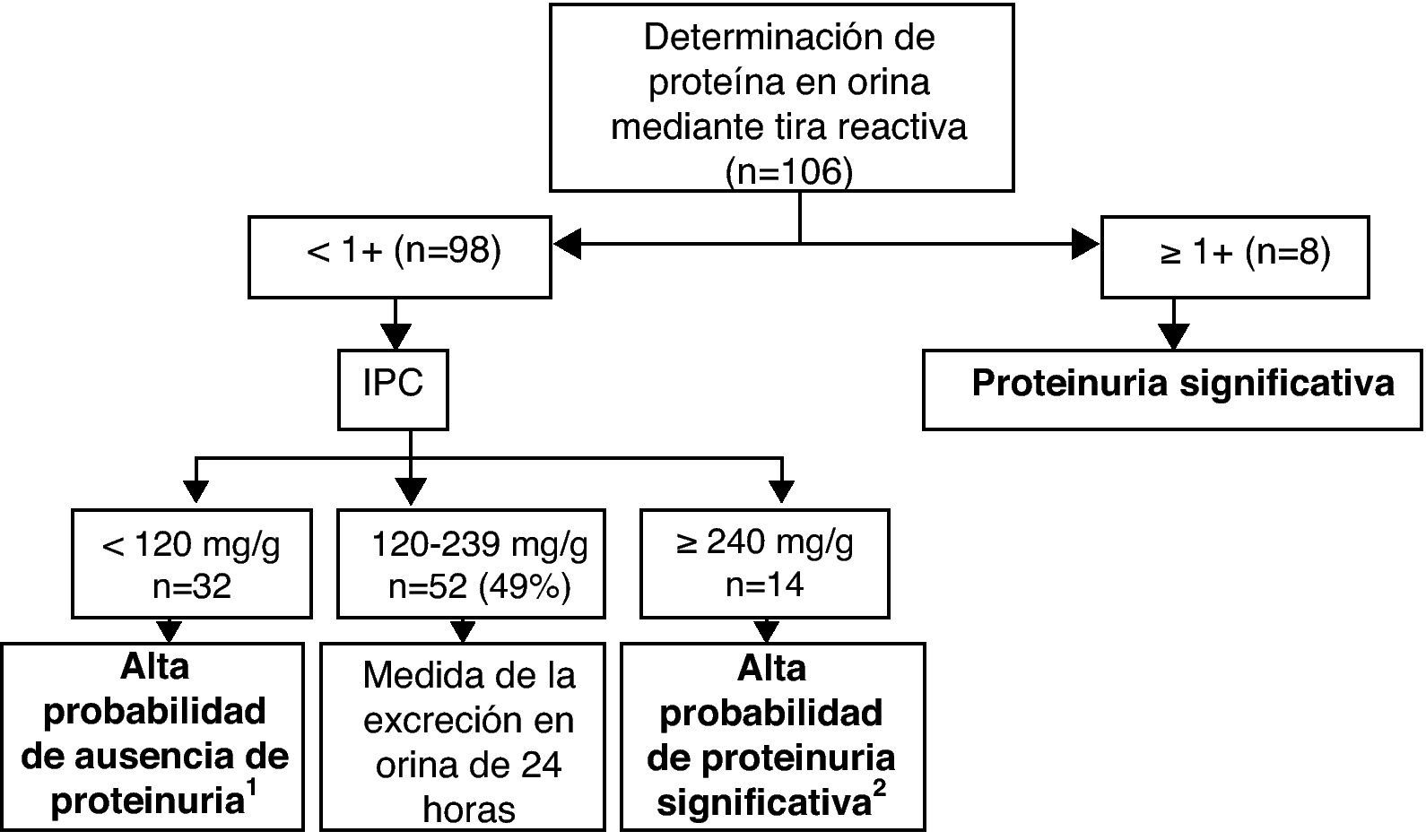
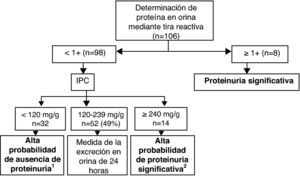
Basado en los datos de rendimiento diagnóstico obtenidos en nuestro estudio para el IPC y para la tira reactiva, proponemos un algoritmo de detección de la proteinuria basado en una estrategia en dos pasos para la identificación rápida de pacientes ambulatorias con sospecha de preeclampsia y seguimiento de la proteinuria en pacientes con diagnóstico previo de preeclampsia (fig. 4). En el primer paso, se determinaría la concentración de proteína urinaria mediante tira reactiva; un valor ≥ 1+ predice una proteinuria significativa. En un segundo paso, en orinas con tira negativa se determina el IPC. Un IPC < 120mg/g excluye con una elevada probabilidad una proteinuria significativa (sensibilidad: 90,3%, VPN: 90,6% y RV–: 0,25), un IPC ≥ 240mg/g predice con una elevada probabilidad una proteinuria significativa (especificidad: 94,7%, VPP: 81% y RV+: 10,28) y valores intermedios (120-239mg/g) requerirían la medida de la excreción urinaria en un espécimen de 24h. El empleo de este algoritmo en nuestra población de estudio hubiera permitido descartar o predecir de forma correcta una proteinuria significativa en 47 orinas (44,3%) y reducir la necesidad de recolectar un espécimen de 24h en más de la mitad de los casos (51%).
Algoritmo para la detección de proteinuria ≥ 300mg/24h basado en la determinación secuencial de la proteinuria mediante tira reactiva y del IPC. 1Con este punto de corte para descartar una proteinuria ≥ 300mg/24h, tres orinas, de la misma gestante, con proteinurias significativas moderadas (306, 414 y 384mg/24h) hubieran sido clasificadas erróneamente como proteinurias no significativas. 2Con este punto de corte para predecir una proteinuria ≥ 300mg/24h, cuatro orinas, de cuatro gestantes, hubieran sido clasificadas erróneamente como proteinurias significativas. Tres de ellas presentaban proteinurias próximas a 300mg/24h (260, 273 y 278mg/24h) y la restante presentaba una excreción de 165mg/24h y un IPC de 359, consecuencia de una baja creatinuria (51mg/dl).
En conclusión, el uso conjunto de la determinación de proteína urinaria mediante la tira reactiva y el IPC es una herramienta útil en la evaluación inicial de la gestante ambulatoria con EHE, evitando los inconvenientes de la recolección de orina de 24h y permitiendo una toma de decisiones más rápida. Sin embargo, la falta de un único punto de corte que maximice el rendimiento para descartar y predecir una proteinuria ≥ 300mg/24h obliga a medir la excreción en un espécimen de 24h, además de para la confirmación del diagnóstico, para valores intermedios del IPC.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.