Analizar el impacto sanitario y económico de la vacunación frente al cáncer de cérvix en España con la vacuna VPH 16/18 adyuvada AS04 (Cervarix®) desde la perspectiva del Sistema Nacional de Salud.
Material y métodosAdaptación al entorno español de un modelo farmacoeconómico que simula el impacto que podría esperarse de los actuales programas de vacunación infantil sobre la carga de las lesiones precursoras y cáncer de cérvix. El modelo emplea datos epidemiológicos nacionales y la eficacia demostrada por la vacuna en ensayos clínicos.
ResultadosConsiderando la cobertura vacunal media en España, el modelo estima que actualmente la vacunación con Cervarix® podría evitar anualmente 45.060 ASCUS, 35.166 lesiones CIN1, 29.549 lesiones CIN2/3 y 1.053 casos de cáncer de cérvix, lo que supondría evitar unos costes sanitarios totales de 89.271.085 euros.
ConclusionesLa vacunación con Cervarix® en España disminuiría los casos de cáncer de cérvix y lesiones precursoras y los consecuentes costes sanitarios asociados a su tratamiento.
To evaluate the healthcare and economic impact of vaccination against cervical cancer with the HPV 16/18 AS04-adjuvanted vaccine (Cervarix®) in Spain from the perspective of the national health system.
Material and methodsA health economics model was adapted to the Spanish environment. The model simulated the impact of current vaccination programs on the burden of precancerous lesions and cervical cancer. National epidemiological data and the vaccine efficacy shown in clinical trials were used.
ResultsConsidering the average vaccination coverage in Spain, the model estimated that vaccination with Cervarix® would prevent 45,060 cases of atypical squamous cells of undetermined significance (ASCUS), 35,166 cases of low-grade squamous intraepithelial lesions (LSIL), 29,549 cases of high-grade squamous intraepithelial lesions (HSIL) and 1,053 cases of cervical cancer. Thus, vaccination would save 89,271,085 € in direct medical costs.
ConclusionsVaccination with Cervarix® in Spain would significantly reduce the number of cases of cervical cancer and precancerous lesions and the associated medical costs.
En octubre de 2007 el Consejo Interterritorial del Sistema Nacional de Salud aprobó la inclusión de la vacunación sistemática frente al virus de papiloma humano (VPH)1 en el Calendario Nacional de Vacunación. Siguiendo las recomendaciones de la Comisión de Salud Pública se acordó la inmunización anual, por parte de las comunidades autónomas, de al menos una cohorte de niñas de entre 11 y 14 años de edad.
Con esta medida se ponía a disposición de la población una intervención que había demostrado ser eficaz, segura y que tenía el potencial de evitar un gran número de casos de cáncer de cérvix y lesiones precursoras causadas por la infección de VPH.
En el momento de la inclusión de la vacunación en el calendario solo estaba autorizada en España una vacuna, Gardasil® (Sanofi-Pasteur), vacuna VPH 6, 11, 16, 18 adyuvada con sulfato de aluminio2. Posteriormente se autorizó la vacuna Cervarix® (GlaxoSmithKline) VPH 16/18 AS04 adyuvada.
Cervarix® es una vacuna indicada para la prevención de lesiones cervicales premalignas y cáncer de cérvix causados por determinados tipos oncogénicos del VPH. La indicación está basada en la demostración de la eficacia en mujeres de 15 a 25 años de edad y de la inmunogenicidad en niñas y mujeres de 10 a 25 años3.
Los resultados finales del ensayo clínico fase III (PATRICIA) llevado a cabo con Cervarix® se han incorporado recientemente en la ficha técnica de la vacuna3,4. Dichos resultados confirman la eficacia de la vacuna en la prevención de lesiones premalignas causadas por los tipos oncogénicos incluidos en la vacuna (16 y 18) y además demuestran una protección adicional en la prevención de lesiones causadas por otros tipos oncogénicos mediante protección cruzada.
Además de esta evidencia clínica, que no existía en el momento de la inclusión de la vacuna en el calendario, se dispone de información epidemiológica actualizada sobre la incidencia del cáncer de cérvix y sus lesiones precursoras en nuestro país5,6.
Por otra parte, el seguimiento que el Ministerio de Sanidad realiza sobre las coberturas de las distintas vacunas en las comunidades autónomas7 proporciona datos reales sobre la cobertura de vacunación alcanzada en los programas de prevención del cáncer de cérvix a nivel nacional.
Partiendo del escenario actual (prevalencia de lesiones precursoras y cáncer de cérvix, cobertura actual de los programas de vacunación y costes de la vacuna y de los tratamientos de dichas pacientes), el presente estudio simula cuál sería el beneficio esperado en la reducción de dichas patologías y de los costes asociados a su tratamiento.
El objetivo del presente estudio es por tanto aportar datos sobre el impacto sanitario y económico de la vacunación frente al cáncer de cérvix en España con la vacuna VPH 16/18 AS04 adyuvada (Cervarix®) desde la perspectiva del Sistema Nacional de Salud.
Material y métodosSe diseñó un modelo de cálculo en Microsoft Excel® para estimar el impacto de la vacunación en la prevención de las distintas patologías causadas por el VPH consideradas en el estudio: ASCUS (atypical squamous cells of undetermined significance), lesiones cervicales intraepiteliales de bajo grado (CIN1) y alto grado (CIN2/3), y cáncer de cérvix.
El modelo recoge la prevalencia de las distintas patologías y los costes sanitarios derivados de su diagnóstico y tratamiento. Sobre estos datos, que definen la carga actual de las distintas enfermedades en estudio, el modelo aplica la eficacia demostrada por la vacuna en ensayos clínicos. Considerando un valor de cobertura de vacunación determinado, el modelo proporciona los resultados en salud que se esperarían si las mujeres que hoy presentan dichas patologías hubiesen sido inmunizadas durante su infancia tal y como se viene realizando en la actualidad con las niñas en edad de calendario. Dichos resultados en salud se miden como casos de las distintas patologías evitados por la vacunación con Cervarix®. Además, esos casos evitados se traducen en unos recursos sanitarios cuyo consumo se evitaría al disminuir los casos de lesiones precursoras y cáncer de cérvix, evitando los costes sanitarios correspondientes. La perspectiva empleada para el análisis de costes fue la del Sistema Nacional de Salud, considerando exclusivamente los costes sanitarios directos.
El modelo estima así el beneficio esperado de la vacunación (en este caso con Cervarix®), medido como número de casos evitados y los costes sanitarios asociados, a través de la inmunización anual de la cohorte de niñas de calendario en España.
Datos de entrada del modeloEl modelo se alimenta básicamente de 3 tipos de datos de entrada o inputs: datos epidemiológicos y de prevalencia de las patologías; datos de costes sanitarios directos, y datos de eficacia de la vacuna.
Datos epidemiológicosLos datos epidemiológicos necesarios para el modelo se obtuvieron de publicaciones recientes (estudios epidemiológicos realizados a nivel nacional) y de la información proporcionada por el Centro de Información del VPH y cáncer de cérvix del Institut Català d’Oncologia/OMS5,6,8,9.
Costes sanitariosLos datos de costes empleados se obtuvieron del consumo de recursos sanitarios asociado a las patologías estudiadas. Para ello se recurrió a un estudio nacional sobre el manejo clínico y recursos asociados a las citologías anormales y el cáncer de cérvix en España10. De esta forma se asignó un coste unitario por episodio de patología para los casos de ASCUS y de lesiones CIN1 y CIN2/3. En el caso del coste por episodio de cáncer de cérvix se calculó una media ponderada por el porcentaje de cáncer según el estadío FIGO11.
El análisis de costes se realizó desde la perspectiva del Sistema Nacional de Salud, y todos los costes se expresaron en euros (€) de 2010. Se cuantificaron los costes directamente relacionados con la utilización de recursos sanitarios (costes directos) y no los que hacen referencia a la pérdida de bienestar, de calidad de vida o de la capacidad productiva debida a cambios en los estados de salud del paciente (costes indirectos).
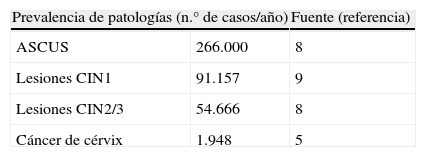
En la tabla 1 se detallan los datos epidemiológicos y de costes sanitarios por episodio empleados en el modelo así como las fuentes empleadas.
Datos epidemiológicos y de costes sanitarios empleados en el modelo
| Prevalencia de patologías (n.° de casos/año) | Fuente (referencia) | |
| ASCUS | 266.000 | 8 |
| Lesiones CIN1 | 91.157 | 9 |
| Lesiones CIN2/3 | 54.666 | 8 |
| Cáncer de cérvix | 1.948 | 5 |
| Coste por episodio (€ 2010) | Fuente (referencia) | |
| ASCUS | 184 € | 10 |
| Lesiones CIN1 | 887 € | |
| Lesiones CIN2/3 | 1.310 € | |
| Cáncer de cérvix | 10.521 € | 10,11 |
CIN: cervical intraepitelial neoplasia.
Los datos de eficacia vacunal empleados se basan en los resultados finales del ensayo clínico PATRICIA, publicados e incorporados recientemente en la ficha técnica de la vacuna3,4,12.
El presente estudio pretende evaluar el beneficio que podría tener la vacunación en la población que actualmente está siendo inmunizada (una cohorte anual de niñas de 11-14 años de edad), por lo que los valores de eficacia empleados en el modelo corresponden al análisis de la cohorte «naïve» de vacunación al ser esta la más semejante a dicha población.
Los valores de eficacia empleados corresponden a la eficacia demostrada por la vacuna independiente del tipo oncogénico encontrado en la lesión.
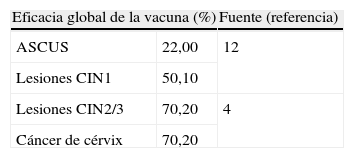
En la tabla 2 se detallan los valores de eficacia de la vacuna utilizados.
Valores de eficacia de la vacuna empleados en el modelo
| Eficacia global de la vacuna (%) | Fuente (referencia) | |
| ASCUS | 22,00 | 12 |
| Lesiones CIN1 | 50,10 | |
| Lesiones CIN2/3 | 70,20 | 4 |
| Cáncer de cérvix | 70,20 | |
| Eficacia frente a los tipos 16/18 (%) | Fuente (referencia) | |
| Lesiones CIN1 | 95,00 | 4 |
| Lesiones CIN2/3 | 95,00 | |
CIN: cervical intraepitelial neoplasia.
El valor de eficacia de la vacuna en cáncer de cérvix tomado para el análisis puede considerarse conservador. Esto se debe a que se ha empleado el mismo dato de eficacia que en lesiones de alto grado CIN2/3 (70,2%) demostrado en el ensayo clínico PATRICIA y reflejado en la ficha técnica de la vacuna. Se estima que la eficacia de la vacuna en cáncer de cérvix podría ser aun mayor debido a que los principales tipos oncogénicos son más prevalentes en los casos de cáncer de cérvix.
Otra variable fundamental en el análisis es la cobertura de vacunación considerada. Si bien el análisis podía haberse realizado desde la asunción de una cobertura ideal máxima semejante a la que se alcanzan por ejemplo con las vacunas pediátricas del calendario vacunal (95%), se consideraron datos reales de cobertura con la vacuna frente al cáncer de cérvix para acercar más los resultados a la situación real. Por ello, se tomó una cobertura media de vacunación del 77% de acuerdo con la información proporcionada por el Ministerio de Sanidad, Política Social e Igualdad para la campaña 2008-20096.
Entre los supuestos establecidos por el modelo hay que señalar la duración de la protección (toda la vida de la mujer vacunada) y el cumplimiento (todas las mujeres reciben el esquema completo de vacunación de 3 dosis).
ResultadosEl modelo proporciona una estimación de los resultados en salud esperados de la vacunación con Cervarix®, medidos como el número de casos de las distintas patologías evitados por la vacunación de las niñas tal y como establece el Calendario Nacional de Vacunación. Dichos casos evitados se traducirían en unos costes sanitarios cuyo consumo se evitaría al disminuir los casos de lesiones precursoras y cáncer de cérvix.
En la tabla 3 se detallan los principales resultados del análisis.
Resumen de resultados. Número de casos de lesiones evitados y costes sanitarios evitados por la vacunación
| Lesión | Número de casos evitados (% reducción) | Costes evitados (€) |
| ASCUS | 45.060 (17%) | 8.291.040 € |
| Lesiones CIN1 | 35.166 (39%) | 31.192.242 € |
| Lesiones CIN2/3 | 29.549 (54%) | 38.709.190 € |
| Cáncer de cérvix | 1.053 (54%) | 11.078.613 € |
| Total costes sanitarios evitados | 89.271.085 € | |
CIN: cervical intraepitelial neoplasia.
Según las estimaciones realizadas, la vacunación con Cervarix® tiene el potencial de prevenir hasta el 54% de las lesiones CIN2/3 y los casos de cáncer de cérvix. Además, la vacunación evitaría hasta el 39% de los episodios de lesiones CIN1 y el consecuente consumo de recursos y costes sanitarios asociados a su diagnóstico y tratamiento.
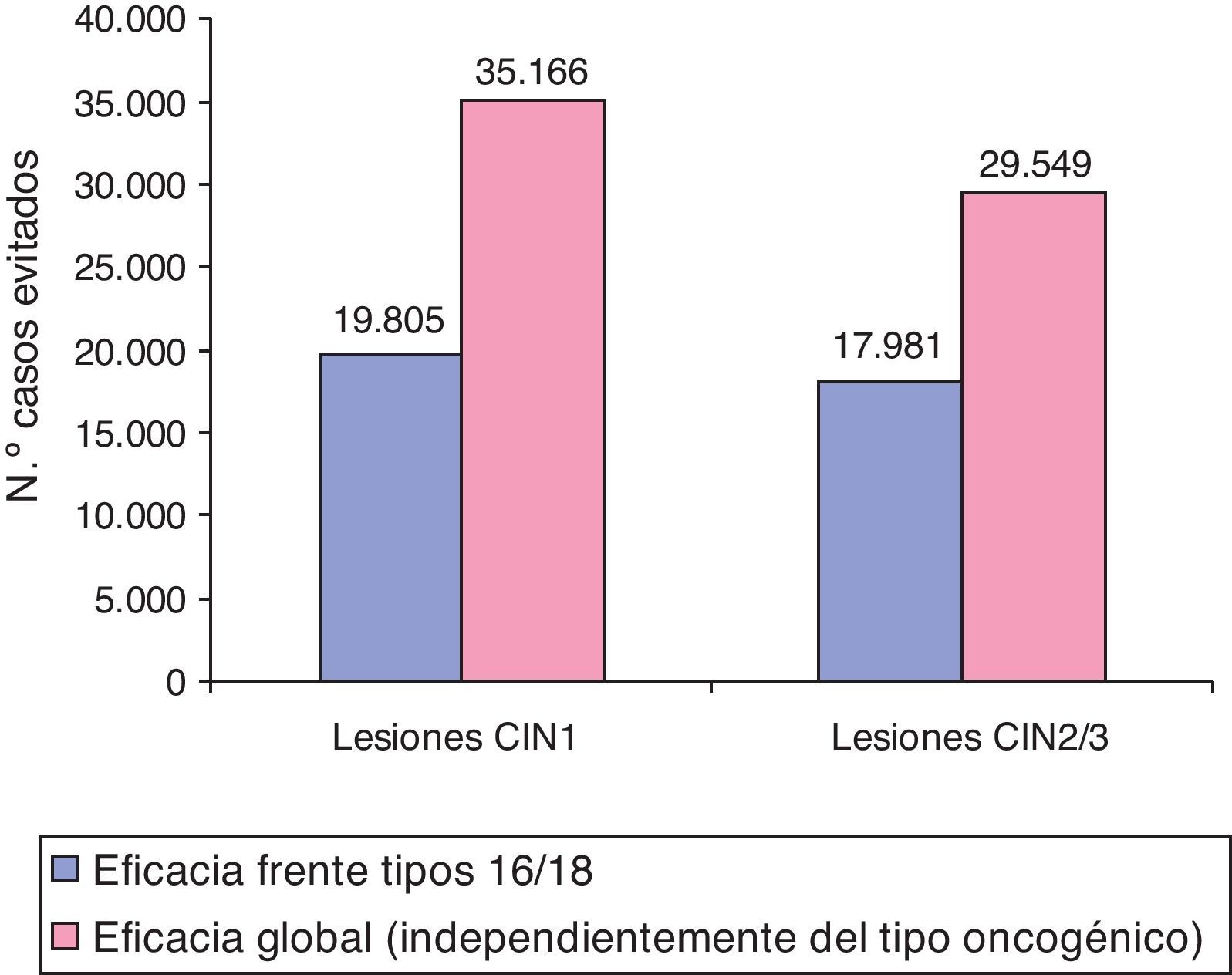
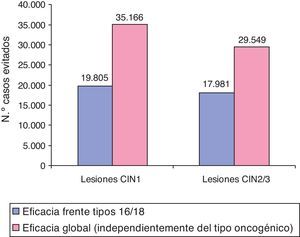
Eficacia global de Cervarix®El presente estudio incluye los últimos datos de eficacia de Cervarix® obtenidos en ensayos clínicos. La herramienta permite así evaluar el significado y la relevancia clínica y económica de los últimos datos de eficacia global (independientemente del tipo oncogénico encontrado en la lesión) demostrada por dicha vacuna.
La figura 1 muestra el beneficio de la vacunación obtenido al considerar la eficacia frente a los tipos oncogénicos presentes en la vacuna (16 y 18) en comparación con la eficacia frente a otros tipos que se incluye como protección global de Cervarix®.
El modelo evidencia que la eficacia global demostrada por Cervarix® le otorga un potencial de protección adicional respecto a la conferida exclusivamente frente a los tipos oncogénicos 16 y 18.
Cobertura de vacunaciónLa cobertura vacunal poblacional es una de las variables más importantes del análisis. El valor medio de cobertura de vacunación tomado en el modelo procede de la información recogida por el Ministerio de Sanidad y es una media de las coberturas de vacunación proporcionadas por las comunidades autónomas.
Para evaluar la influencia de la cobertura de vacunación en los resultados en salud obtenidos, se realizaron diferentes escenarios en los que la única variable que se modificó fue dicha cobertura.
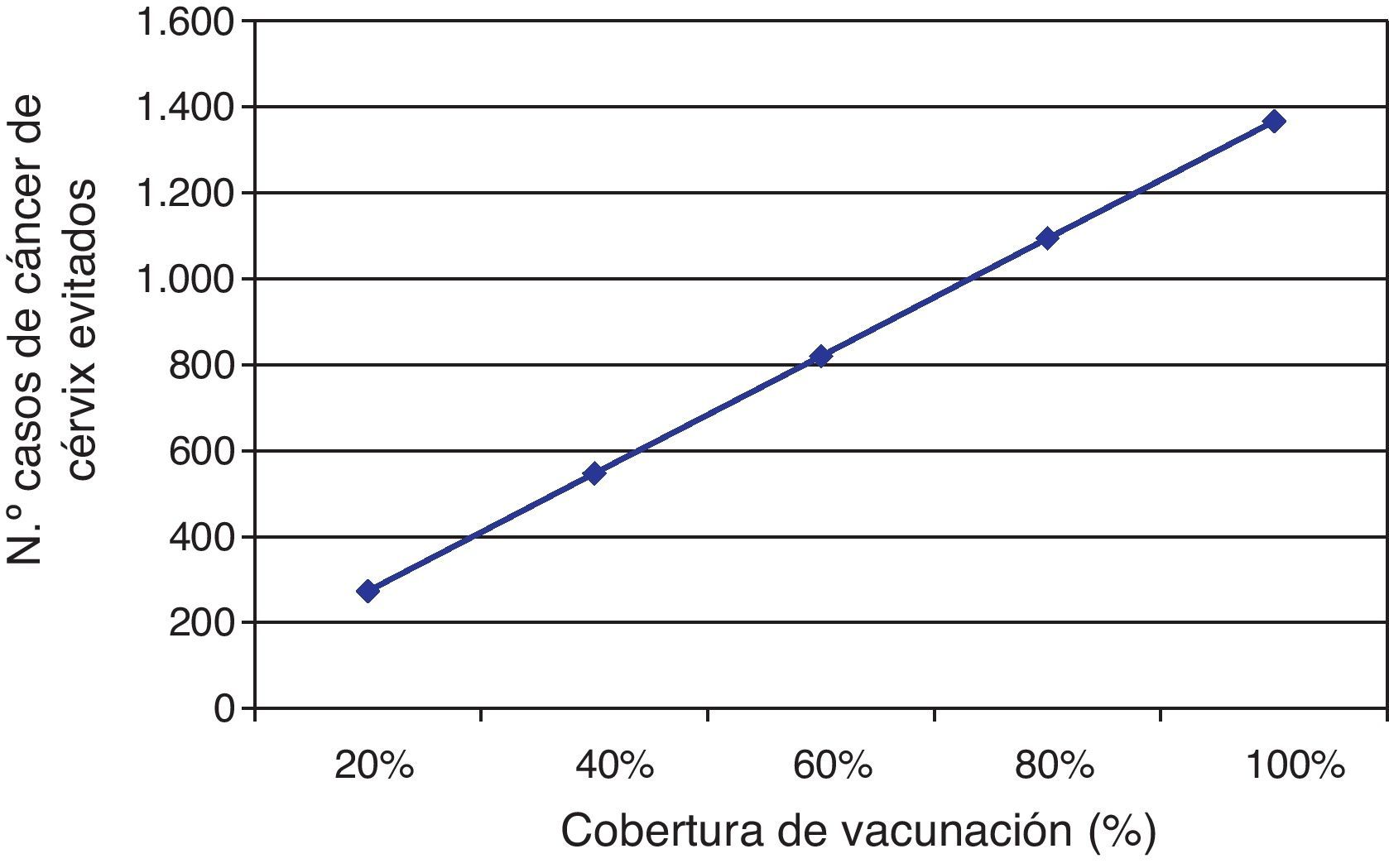
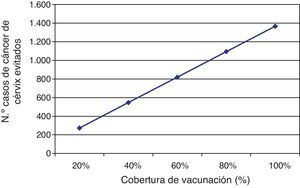
En la figura 2 se detallan los resultados de la vacunación (medidos como número de casos evitados) en relación a la cobertura de vacunación.
Tal y como se observa, disminuir la cobertura de vacunación, por ejemplo, del 80 al 60% significaría dejar de prevenir hasta 400 casos de cáncer de cérvix.
Los datos ponen de manifiesto la gran importancia de conseguir coberturas de vacunación óptimas para obtener el máximo beneficio de los programas de vacunación frente al cáncer de cérvix.
DiscusiónDesde la introducción de la vacunación sistemática frente al cáncer de cérvix en España se han realizado diferentes evaluaciones económicas sobre el beneficio de esta intervención13-17.
No obstante, transcurridos 3 años desde su introducción, se dispone de nueva evidencia epidemiológica sobre la carga de las patologías asociadas al VPH así como de nueva evidencia clínica sobre la eficacia de la vacuna Cervarix®. Se considera pues pertinente aportar nueva evidencia económica que reafirme el valor de la vacunación frente al cáncer de cérvix.
El presente estudio de evaluación económica pretende estimar el potencial impacto de la vacunación (Cervarix®) sobre la carga sanitaria y económica que supone el cáncer de cérvix y las lesiones precursoras en España.
El análisis realizado no escapa a ciertas limitaciones inherentes a la dificultad metodológica que supone evaluar esta intervención sanitaria. Por ejemplo, el análisis supone que la duración de la protección proporcionada por la vacuna es de por vida. En caso contrario debería computarse la revacunación (costes y cobertura). Sin embargo, la estabilidad en el título de anticuerpos a largo plazo y las estimaciones a 20 años hacen muy improbable la necesidad de una dosis de recuerdo18. Por otra parte, el caso base del modelo asume un cumplimiento de la pauta vacunal del 100%, es decir que todas las mujeres reciben las 3 dosis de la vacuna. Finalmente, el presente estudio no tiene en cuenta los cambios o influencias del cribado en la detección precoz de lesiones, los posibles cambios de la epidemiología del VPH a lo largo del tiempo, el coste de adquisición de la vacuna o los costes de la implementación de los programas de vacunación por las comunidades autónomas. Estos supuestos, aunque justificados por la dificultad metodológica del análisis, podrían influir en los resultados obtenidos en el presente estudio. Recientemente se han publicado modelos económicos más complejos que incorporan la mayoría de estas variables y ofrecen una visión más amplia sobre la relación coste-efectividad de las diferentes estrategias de prevención del cáncer de cérvix en España17.
Con todo ello, los resultados del presente estudio ponen de manifiesto la importante carga clínica y económica que suponen no solo los casos de cáncer de cérvix sino las lesiones precursoras del mismo. De este modo, el análisis llevado a cabo permite estimar el impacto sanitario y económico que podría estar ya consiguiéndose gracias a la vacunación sistemática frente al cáncer de cérvix en España. El modelo establece también con claridad que la cobertura de vacunación es uno de los factores que más influye en los resultados esperados de la inmunización frente al cáncer de cérvix.
En el caso concreto de la vacuna 16/18 AS04-adyuvada (Cervarix®), dicho impacto sanitario y económico es aún más importante si se consideran no solo la protección frente a los tipos 16/18 que incluye la vacuna sino también la protección cruzada frente a tipos no incluidos estimada mediante la eficacia global (independientemente del tipo oncogénico) resultado de ensayos clínicos y cuyos datos se han incorporado en la ficha técnica de la vacuna3. Cabe destacar que recientemente se han obtenido nuevos datos de eficacia global de la vacuna 16/18 AS04-adyuvada (Cervarix®) procedentes del análisis final del ensayo PATRICIA que le otorgan una eficacia aún mayor a la considerada en el presente análisis (93,2% en prevención de CIN3+ en la cohorte total de vacunación naïve del estudio)3.
En conclusión, la vacunación frente a las infecciones causadas por el VPH en España disminuiría los casos de cáncer de cérvix y lesiones precursoras del mismo así como los consecuentes costes sanitarios asociados a su diagnóstico y tratamiento. El beneficio sanitario y económico de la inmunización frente al cáncer de cérvix será tanto mayor cuanta más alta cobertura se alcance en los programas de vacunación de las niñas en España.
FinanciaciónEl presente trabajo ha sido financiado por GlaxoSmithKline, S.A. Tres Cantos, Madrid, España.
Conflicto de interesesR. Morano es empleado de GlaxoSmithKline, S.A., empresa comercializadora de la vacuna Cervarix. A. Torné y X. Castelsagué declaran no tener conflicto de intereses.