Analizar las características de las lesiones preneoplásicas del tracto genital inferior (TGI) y los factores asociados a su recidiva.
Material y métodosSe estudió a 376 mujeres tratadas de algún tipo de neoplasia intraepitelial del TGI, en la década de los 90. Las lesiones se agruparon en cervicales y vulvares, y estas en lesiones de alto (CIN II-III o VIN) y de bajo grado (CIN I o atipia vulvar por virus del papiloma humano [AV-VPH]). El tratamiento de las CIN se realizó con asa diatérmica y para las lesiones vulvares fue la resección con bisturí frío y/o láser CO2.
ResultadosLa edad media de las mujeres fue 32 años. La multicentricidad fue identificada en el 57% de las CIN y en el 87% de las lesiones vulvares. Un 10% de las mujeres en ambos grupos presentó algún tipo de inmunosupresión. Se identificó VPH de riesgo alto en el 25% de los casos. Con un seguimiento medio de 21 meses, la recidiva global de la CIN fue del 17% y la acumulada a 5 años del 47%. En las lesiones vulvares fue del 15 y el 54%, respectivamente. En ambos grupos lesionales la recidiva apareció en los primeros 3 años en más del 90% de los casos y se asoció a la inmunosupresión y el genotipo viral de riesgo alto, aunque el único factor de riesgo independiente en el análisis multivariante fue la inmunosupresión. Ninguna paciente progresó a cáncer invasor.
ConclusionesLa inmunosupresión es el factor riesgo predictivo más importante de recurrencia. Las conductas orientadas a estimular la inmunidad podrían ser eficaces en prevención de la recurrencia de la enfermedad por el VPH.
To analyze the characteristics of preneoplastic lesions of the lower genital tract (LGT) and the factors associated with their recurrence.
Material and methodsA total of 376 women treated for some type of intraepithelial neoplasm of the LGT between 1990 and 1999 were studied. The lesions were classified into cervical intraepithelial neoplasms (CIN) and vulvar intraepithelial neoplasms (VIN) and were further classified into high-grade lesions (CIN 2-3 or VIN) and low-grade lesions (CIN 1 or human papillomavirus vulvar atypia [HPV-VA]). Treatment of cervical lesions consisted of CO2 laser and / or loop electrosurgical excision while that of vulvar lesions consisted of cold-knife local excision and / or CO2 laser.
ResultsThe mean age of women was 32 years. Multicentric disease was found in 57% of CIN lesions and in 87% of vulvar lesions. Ten percent of women in both groups had some type of immunosuppression. High-risk HPV was identified in 25% of patients. With a mean follow-up of 21 months, the overall CIN recurrence was 17% and accumulated recurrence rate at 5 years was 47%. In vulvar lesions, these values were 15% and 54%, respectively. In both groups, more than 90% of recurrences occurred in the first 3 years, and relapse was associated with immunosuppression and high-risk viral genotype. In multivariate analysis, the only independent risk factor was immunosuppression. None of the lesions progressed to invasive cancer.
ConclusionsThe most important risk factor predictive of recurrence is immunosuppression. Measures to stimulate immunity could be effective in preventing HPV-related disease.
La evidente implicación demostrada del virus del papiloma humano (VPH) en la génesis de las lesiones preneoplásicas del epitelio cervical y vulvar, y en su evolución a carcinoma invasivo, ha dado lugar a que el concepto y la terminología de este tipo de lesiones hayan evolucionado paralelamente al avance del conocimiento de su biología e historia natural. Hay, por tanto, dos características que definen a las lesiones epiteliales preinvasoras de cérvix y vulva: por un lado, la presencia de atipia celular y, por otro, la posibilidad de progresar a enfermedad invasora.
La prevalencia de la neoplasia intraepitelial cervical (CIN) de alto grado es del 0,5-1% y la de CIN de bajo grado del 3-5% en Reino Unido, con un claro incremento en las últimas décadas y una incidencia máxima en la tercera década de la vida1. En España, en una encuesta realizada por la Sección de Prevención del Cáncer Ginecológico, la tasa de CIN II-III en el año 2000 fue del 0,36% y la de lesiones escamosas de alto grado por citología del 0,42%. Otra encuesta nacional reciente sobre resultados citológicos anormales encontró un 1,2% de lesiones escamosas de bajo grado y un 0,28% de lesiones de alto grado2. El hecho de que este tipo de lesiones sean diagnosticadas en la mayor parte de los casos en mujeres en edad reproductiva hace que debamos ser cautos y no aplicar terapias agresivas que puedan comprometer su capacidad genésica, sin por ello aplicar tratamientos insuficientes que alteren el curso de la enfermedad y dificulten el diagnóstico de persistencia de la lesión; por tanto, este tipo de lesiones provocan un importante impacto social.
Actualmente, las CIN II-III se consideran como verdaderas lesiones precursoras del cáncer de cérvix. Por tanto, para prevenir con eficacia el cáncer cervical invasor se requiere el cumplimiento estricto del protocolo de prevención secundaria, que incluye, además del cribado y el diagnóstico (condicionados por los resultados de la citología, colposcopia, biopsias, análisis del ADN-VPH e información clínica), el tratamiento y posterior seguimiento de estas lesiones precursoras.
La neoplasia intraepitelial vulvar (VIN) se define como una alteración potencialmente maligna del epitelio plano poliestratificado de la vulva. Actualmente, se acepta la clasificación propuesta en 2004 por la Sociedad Internacional para el Estudio de las Enfermedades de la Vulva, en la que la nomenclatura VIN I es sustituida por atipia vulvar por VPH (AV-VPH), englobando el término VIN las lesiones de alto grado (VIN II y III) con verdadero potencial de progresar a carcinoma invasor3. La prevalencia o incidencia de VIN en la población general no se conoce debido a la ausencia de programas organizados para su detección; sin embargo, el número de casos diagnosticados ha experimentado un aumento en las últimas décadas, fundamentalmente en la población joven, menor de 40 años. En la actualidad, la incidencia de VIN se estima entre 1,8 y 2,8 casos por cada 100.000 mujeres4.
La introducción reciente de las vacunas profilácticas frente al VPH ha demostrado su eficacia en la prevención de lesiones preneoplásicas tanto cervicales5,6 como vulvares7, abriendo un nuevo camino en todos los aspectos relacionados con este tipo de lesiones. De momento, aunque no se pueden establecer similitudes entre las VIN y las CIN, en la mayoría de los casos el tratamiento de estas lesiones puede evitar su progresión a carcinoma.
Teniendo en cuenta lo anterior, se plantea un estudio retrospectivo sobre la patología preneoplásica del tracto genital inferior (TGI) cuyos objetivos son: a) analizar las características clínico-patológicas de las lesiones preneoplásicas del TGI; b) estudiar la evolución de estas lesiones tras su tratamiento, y c) valorar su recidiva y progresión.
Material y métodosSe realizó un estudio retrospectivo de 376 mujeres diagnosticadas de algún tipo de neoplasia intraepitelial del TGI: cervical (CIN) y/o vulvo-perineal (VIN); en la Unidad de Patología Vulvo-Cervical (PVC) del Departamento de Obstetricia y Ginecología del Hospital Clínico San Carlos de Madrid durante la década de los noventa.
Las lesiones intraepiteliales cervicales y vulvares se agruparon en lesiones de grado alto (CIN II-III y VIN II-III, respectivamente) y de grado bajo (CIN I1 y VIN I). Siguiendo la actual clasificación de la VIN, se consideró como VIN a la VIN II-III y a la antigua VIN I como AV-VPH. Se consideró multicentricidad en este estudio si aparecían simultáneamente cualquiera estas lesiones, independientemente del grado, en dos o más áreas anatómicas del TGI: cérvix, vagina o vulva.
A todas las mujeres incluidas en el estudio se les hicieron una toma cérvico-vaginal, una colposcopia y una vulvoscopia con ácido acético y toma de biopsia en las zonas sospechosas de lesión8. El tratamiento de las CIN se realizó bien con asa diatérmica, bien con láser de CO2 o bien con la combinación de ambos. El láser usado fue Sharplan de CO2, con una potencia máxima de salida de 60W y manejado con un brazo articulado que se acopla a un colposcopio. Se consideró la conización para aquellas lesiones en las que existía una biopsia cervical con diagnóstico de cualquier grado de lesión y la colposcopia no era satisfactoria, cuando la colposcopia era sospechosa de invasión, cuando existía algún grado de lesión endocervical, cuando había alguna citología con resultado de algún grado de lesión y la colposcopia era negativa, y cuando existía una discrepancia citológico-biópsica con mayor grado en citología. La conización se realizó indistintamente con láser o con asa diatérmica. Completada la conización, se realizó una vaporización con láser del lecho y ectocérvix. La técnica que se empleó para la vaporización cervical fue la de «gorro de vaquero», con una potencia de salida del láser de 50W. En la técnica de conización con láser se realizó con una potencia de 50W y con un punto de disparo enfocado, penetrando hasta 20mm; una vez realizado el cono se procedió a la sección su vértice con tijera. Para la conización con asa de diatermia se emplearon asas de tamaño grande o mediano para escisión del exocérvix y una pequeña para profundizar en el canal endocervical si existía sospecha de lesión endocervical. En este último caso se realizó también un cepillado o legrado endocervical.
El tratamiento de las lesiones vulvares se realizó mediante resección con bisturí frío o láser de CO2 o la combinación de estos: resección de la lesión asociada a vaporización de los bordes y lesiones satélites. Si la biopsia previa vulvar no indicaba invasión, se pudo optar por un tratamiento ablativo con láser de CO2.
La determinación de ADN-VPH se realizó según la técnica de la reacción en cadena de la polimerasa (PCR) en las muestras histológicas obtenidas y se clasificaron los resultados en virus de riesgo alto y bajo según la actual consideración de los genotipos9.
El seguimiento de las pacientes se realizó cada 3-6 meses en la Unidad de PVC mediante citología, vulvo-colposcopia y biopsia dirigida, si era necesario. Se consideró recidiva los casos de pacientes en las que apareció algún grado de lesión durante el seguimiento a nivel cervical o vulvar.
Las pruebas estadísticas utilizadas fueron la prueba exacta de Fisher para las variables cualitativas, y para las cuantitativas la pruebas de la t de Student. La magnitud del riesgo se estimó mediante la odds ratio (OR). Se calcularon los intervalos de confianza al 95% (IC del 95%) de la OR mediante método de Cornfield. El límite de significación estadística se consideró para una p<0,05.
ResultadosSe estudió un total de 345 casos de CIN: 136 (39,4%) de CIN I, 119 (34,5%) de CIN II y 90 (26,1%) de CIN III. Con respecto a la vulva, se estudiaron un total de 228 lesiones vulvares: 207 casos de AV-VPH y 20 de VIN. Del total de casos, 198 (53,7%) fueron multicéntricos: 196 casos con CIN y lesión vulvar, y 2 casos de lesión vulvar y neoplasia intraepitelial vaginal.
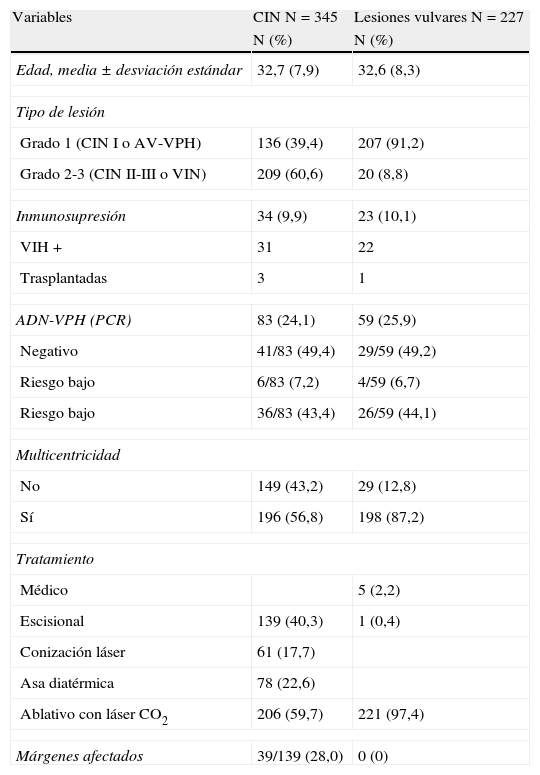
Neoplasia cervical intraepitelialLa descripción de la serie se refleja en la tabla 1. La edad media±desviación estándar de las 345 mujeres con CIN fue de 32,7±7,9 años. Las mujeres con CIN de grado alto o CIN II-III fueron más añosas que las portadoras de CIN I (33,0 frente a 32,3 años), aunque las diferencias no fueron significativas. La CIN II-III fue la lesión más común de la serie con 209 (60,6%) casos; el resto de los casos fueron CIN I (136 casos, 39,9%). En la serie estudiada aparecieron 34 (9,9%) mujeres con inmunosupresión debido a sida (31 casos) y a trasplante renal (3 casos). Se dispuso de determinación de ADN-VPH en 83 (24,1%) casos. Se obtuvo positividad para virus de riesgo alto en 36 (43,4%) de los 83 casos. La multicentricidad fue frecuente entre estas lesiones 196 (56,8%). El tratamiento aplicado fue mayoritariamente ablativo mediante vaporización con láser de CO2 en gorro de vaquero, que se realizó en 206 (59,7%) casos. Los tratamientos escisionales fueron la conización con asa diatérmica en 78 (22,6%) casos y la conización con láser de CO2 en 61 (17,7%) casos, ambos seguidos de vaporización láser en gorro de vaquero. Se observaron bordes afectados en 98 de los 139 casos conizados (28,4%)
Descripción de la serie de los casos de CIN y VIN
| Variables | CIN N=345 | Lesiones vulvares N=227 |
| N (%) | N (%) | |
| Edad, media±desviación estándar | 32,7 (7,9) | 32,6 (8,3) |
| Tipo de lesión | ||
| Grado 1 (CIN I o AV-VPH) | 136 (39,4) | 207 (91,2) |
| Grado 2-3 (CIN II-III o VIN) | 209 (60,6) | 20 (8,8) |
| Inmunosupresión | 34 (9,9) | 23 (10,1) |
| VIH + | 31 | 22 |
| Trasplantadas | 3 | 1 |
| ADN-VPH (PCR) | 83 (24,1) | 59 (25,9) |
| Negativo | 41/83 (49,4) | 29/59 (49,2) |
| Riesgo bajo | 6/83 (7,2) | 4/59 (6,7) |
| Riesgo bajo | 36/83 (43,4) | 26/59 (44,1) |
| Multicentricidad | ||
| No | 149 (43,2) | 29 (12,8) |
| Sí | 196 (56,8) | 198 (87,2) |
| Tratamiento | ||
| Médico | 5 (2,2) | |
| Escisional | 139 (40,3) | 1 (0,4) |
| Conización láser | 61 (17,7) | |
| Asa diatérmica | 78 (22,6) | |
| Ablativo con láser CO2 | 206 (59,7) | 221 (97,4) |
| Márgenes afectados | 39/139 (28,0) | 0 (0) |
AV-VPH: atipia vulvar por virus del papiloma humano; CIN: neoplasia intraepitelial cervical; PCR: reacción en cadena de la polimerasa; VIH: virus de la inmunodeficiencia humana; VIN: neoplasia intraepitelial vulvar.
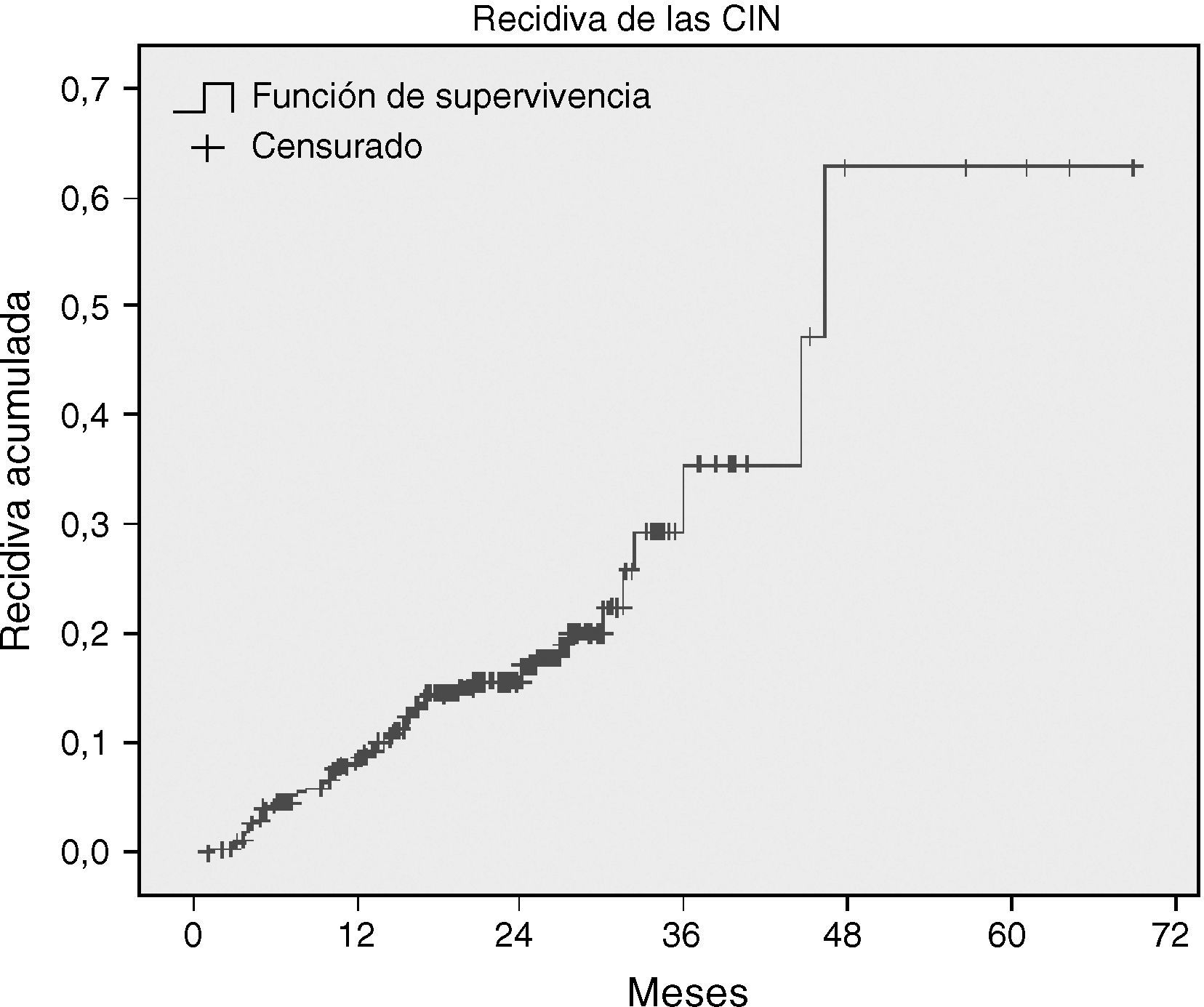
Con una mediana de seguimiento de 21,7 meses, la recidiva global de las lesiones cervicales se observó en el 17% de los casos (58 casos); 3 casos se perdieron durante el seguimiento. En la figura 1 se expone la curva de recidiva acumulada. La recurrencia del CIN apareció fundamentalmente en los primeros 3 años tras el tratamiento (93,1%) y su tasa acumulada fue del 9% el primer año, del 15% el segundo año, del 30% al tercer año y del 47% al cuarto y quinto años.
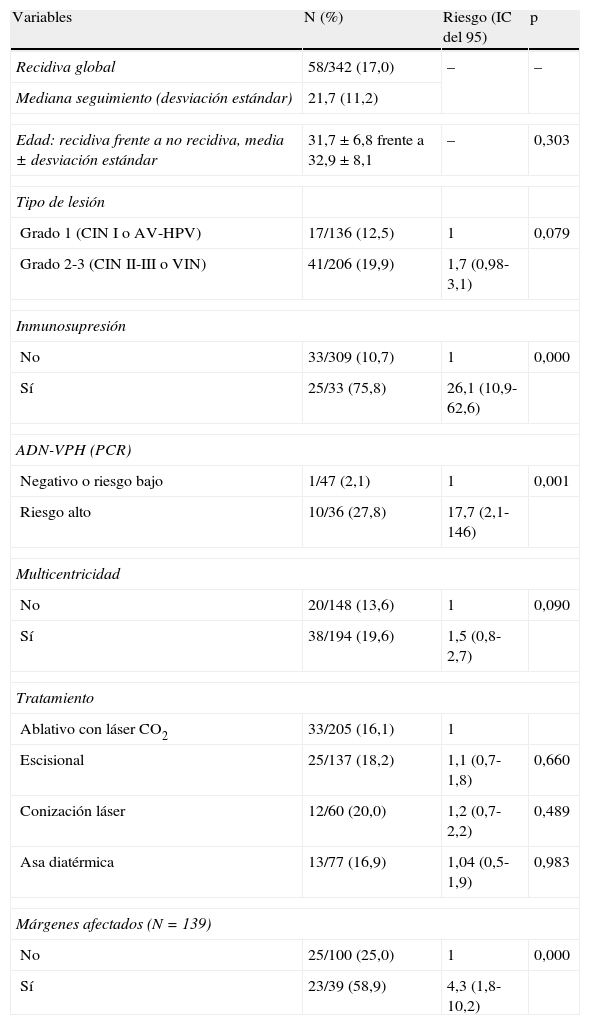
En la tabla 2 se expresa la asociación de las recidivas de CIN respecto a los distintos factores analizados. La recidiva de la CIN se asoció a la inmunosupresión de la paciente, con la presencia de ADN-VPH de riesgo alto y con la afectación de los bordes quirúrgicos. El 75,8% de las lesiones recurrieron en mujeres inmunosuprimidas frente al 10,7% en las inmunocompetentes (riesgo relativo [RR]=26,1 [10,9-62,6]; p=0,000). La recidiva fue del 27,8% en las mujeres con ADN-VPH de riesgo alto frente al 2,1% en las tenían ADN-VPH de riesgo bajo o eran negativas para VPH (RR=17,7 [0,8-2,7]; p=0,001). La recurrencia apareció significativamente más en los casos con bordes afectados frente a los que tenían bordes libres (el 58,9 frente al 25%; RR=4,3 [1,8-10,2]; p=0,000). El grado alto de la lesión (CIN II-III) y la multicentricidad aparecieron más frecuentemente en aquellos casos que recidivaron; sin embargo, las diferencias observadas no fueron estadísticamente significativas, aunque estuvieron cercanas al límite de la significación. El tipo de tratamiento (ablativo o escisional) no influyó en la recurrencia de la lesión. De todos los tratamientos, la conización con láser de CO2 fue la que mayor índice de recurrencia presentó (20%) frente a la conización con asa diatérmica o vaporización con láser de CO2 (el 16 y el 17%, respectivamente).
Recidivas de las lesiones cervicales tras el tratamiento
| Variables | N (%) | Riesgo (IC del 95) | p |
| Recidiva global | 58/342 (17,0) | – | – |
| Mediana seguimiento (desviación estándar) | 21,7 (11,2) | ||
| Edad: recidiva frente a no recidiva, media±desviación estándar | 31,7±6,8 frente a 32,9±8,1 | – | 0,303 |
| Tipo de lesión | |||
| Grado 1 (CIN I o AV-HPV) | 17/136 (12,5) | 1 | 0,079 |
| Grado 2-3 (CIN II-III o VIN) | 41/206 (19,9) | 1,7 (0,98-3,1) | |
| Inmunosupresión | |||
| No | 33/309 (10,7) | 1 | 0,000 |
| Sí | 25/33 (75,8) | 26,1 (10,9-62,6) | |
| ADN-VPH (PCR) | |||
| Negativo o riesgo bajo | 1/47 (2,1) | 1 | 0,001 |
| Riesgo alto | 10/36 (27,8) | 17,7 (2,1-146) | |
| Multicentricidad | |||
| No | 20/148 (13,6) | 1 | 0,090 |
| Sí | 38/194 (19,6) | 1,5 (0,8-2,7) | |
| Tratamiento | |||
| Ablativo con láser CO2 | 33/205 (16,1) | 1 | |
| Escisional | 25/137 (18,2) | 1,1 (0,7-1,8) | 0,660 |
| Conización láser | 12/60 (20,0) | 1,2 (0,7-2,2) | 0,489 |
| Asa diatérmica | 13/77 (16,9) | 1,04 (0,5-1,9) | 0,983 |
| Márgenes afectados (N=139) | |||
| No | 25/100 (25,0) | 1 | 0,000 |
| Sí | 23/39 (58,9) | 4,3 (1,8-10,2) | |
| Variables | Riesgo (IC del 95) | p |
| CIN I | 1 | 0,288 |
| CIN II-III | 0,4 (0,1-1,9) | |
| No inmunosupresión | 1 | 0,000 |
| Inmunosupresión | 14,6 (3,4-61,3) | |
| VPH de riesgo bajo | 1 | 0,067 |
| VPH de riesgo alto | 5,6 (0,6-49,5) | |
| No multicentricidad | 1 | 0,395 |
| Multicentricidad | 1,8 (0,4-8,1) | |
| Márgenes libres | 1 | 0,058 |
| Márgenes afectados | 3,9 (0,9-78,1) | |
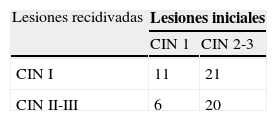
Analizando la histología de las recidivas, del total de lesiones recurrentes 41 (70,7%) casos fueron de grado alto (CIN II-III). La histología de las 58 recidivas cervicales se presenta en la tabla 3. Se produjo recidiva con igual lesión que la inicial en 31 (53,5%) casos, en lesión de grado inferior en 21 (36,2%) casos y en lesión de grado superior en 6 (10,3%) casos. De estos 6 últimos casos, 3 correspondieron a mujeres inmunosuprimidas y en 5 casos se aplicó un tratamiento ablativo con láser de CO2 y en 1 una conización con láser de CO2. No hubo ningún caso de progresión a carcinoma invasor de cérvix.
Cuando se realizó un modelo multivariante según los riesgos proporcionales de Cox, se observó que la única variable independiente predictiva de recidiva fue el estado inmunitario. La inmunosupresión implicó un riesgo de recurrencia de CIN 14,6 veces superior (tabla 4).
Recidiva de las lesiones cervicales. Estudio multivariante de Cox
| Recidivas en 221 lesiones vulvares | |||
| Variables | N (%) | Riesgo relativo (IC del 95) | p |
| Recidiva global | 33/221 (14,9) | – | – |
| Mediana seguimiento±desviación estándar | 20,1 (9,9) | ||
| Edad: recidiva frente a no recidiva, media±desviación estándar | 31,8 (7,5) vs 32,8 (0,6) | – | 0,501 |
| Tipo de lesión | |||
| AV-HPV | 30/204 (14,7) | 1 | 0,724 |
| VIN | 3/17 (17,6) | 1,3 (0,5-3,5) | |
| Inmunosupresión | |||
| No | 21/199 (10,6) | 1 | 0,000 |
| Sí | 12/22 (54,5) | 5,1 (2,9-8,7) | |
| ADN-VPH (PCR) | |||
| Negativo o riesgo bajo | 1/32 (3,1) | 1 | 0,037 |
| Riesgo alto | 6/20 (23,1) | 7,4 (0,94-57,2) | |
| Multicentricidad | |||
| No | 8/29 (27,6) | 1 | 0,051 |
| Sí | 25/192 (13,0) | 0,4 (0,2-0,94) | |
| Tratamiento | |||
| Médico | 0/5 (0) | 0,582 | |
| Ablativo con láser CO2 | 33/215 (15,3) | – | |
| Escisional | 0/1 (0) | ||
AV-VPH: atipia vulvar por virus del papiloma humano; CIN: neoplasia intraepitelial cervical; IC: intervalo de confianza; PCR: reacción en cadena de la polimerasa; VPH: virus del papiloma humano; VIN: neoplasia intraepitelial vulvar.
La descripción de la serie se refleja en la tabla 1. La edad media±desviación estándar de las 227 mujeres con lesiones vulvares por VPH fue de 32,6±8,3 años. Las mujeres con VIN (antiguo VIN 2-3) fueron más añosas que las portadoras de AV-VPH (incluye los cambios por VPH y el VIN 1) (36,1 frente a 32,3 años), aunque las diferencias no fueron estadísticamente significativas. La VIN se presentó en 20 (8,8%) casos y las lesiones con atipia vulvar por VPH fueron las más comunes, con 207 (91,2%) casos. En la serie vulvar estudiada aparecieron 23 (10,1%) mujeres con inmunosupresión debido a sida (22 casos) y a trasplante renal (1 caso). Se dispuso de determinación de ADN-VPH en 59 (25,9%) casos. Se obtuvo positividad para virus de riesgo alto en 26 (44,1%) de los 59 casos. La multicentricidad fue lo más común en estas lesiones: 198 (87,2%). El tratamiento aplicado fue mayoritariamente ablativo mediante vaporización con láser de CO2 de las lesiones vulvares, que se realizó en 221 (97,4%) casos. El tratamiento médico con imiquimod se aplicó en 5 (2,2%) casos.
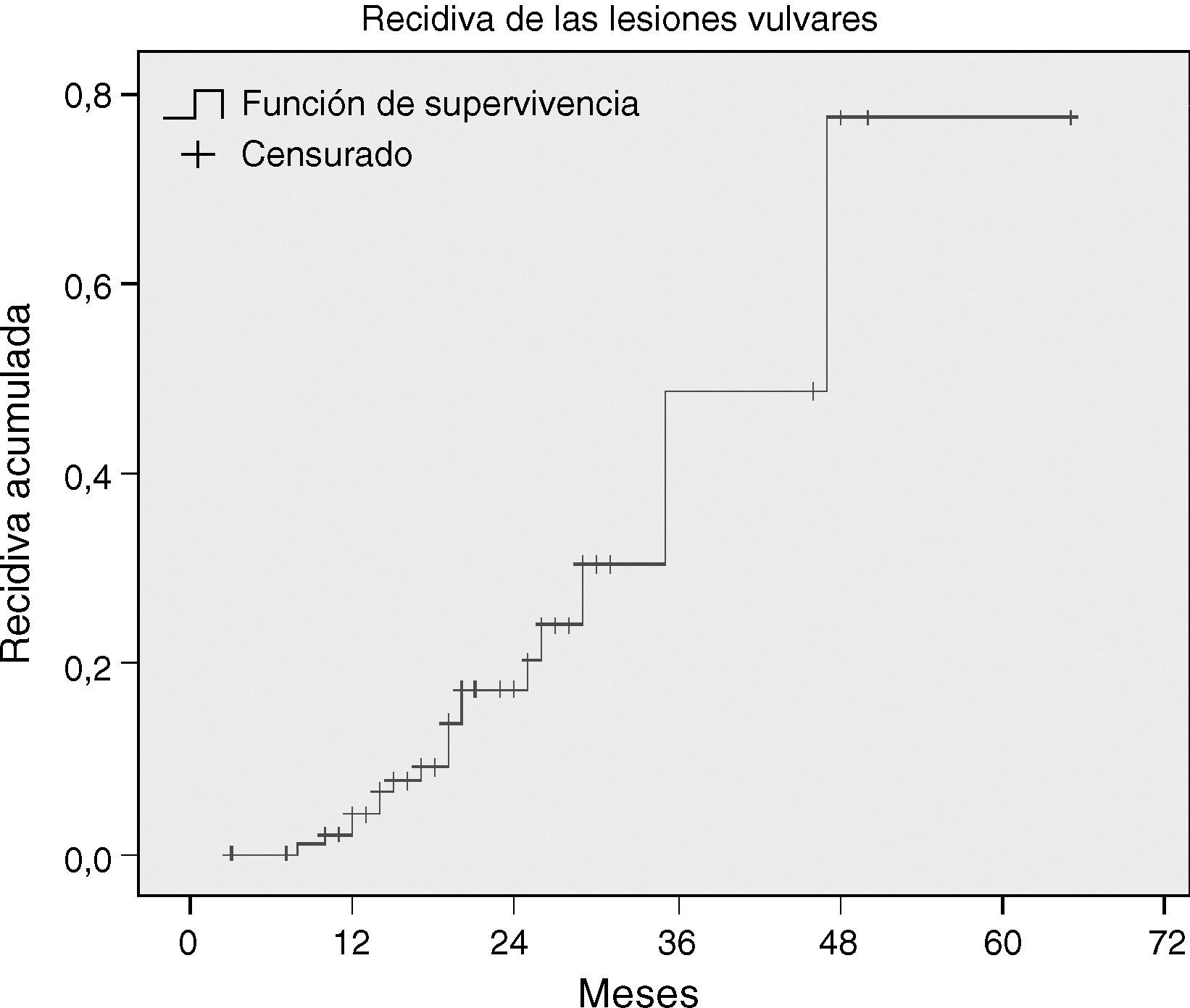
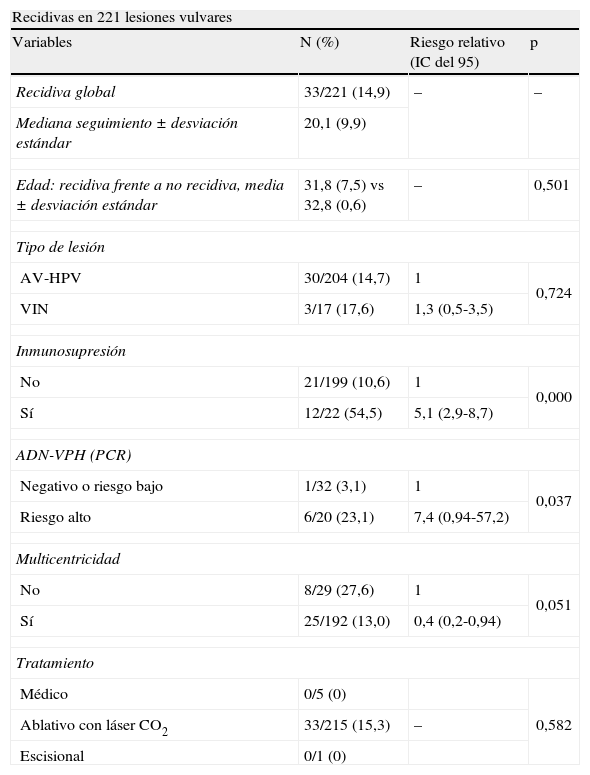
Estudio de las recidivasCon una mediana de seguimiento de 20,1 meses, la recidiva global de las lesiones vulvares se observó en el 14,9% de los casos (33 casos); 6 casos se perdieron durante el seguimiento. En la figura 2 se expone la curva de recidiva acumulada. Como ocurrió en las CIN, la recurrencia de las lesiones vulvares apareció fundamentalmente en los primeros 3 años tras el tratamiento (93,9%) y la tasa acumulada fue del 4% el primer año, del 16% el segundo año, del 39% al tercer año y del 54% al cuarto y quinto años.
En la tabla 2 se presenta la asociación de las recidivas de las lesiones vulvares respecto a los distintos factores analizados. La recidiva de las lesiones vulvares se asoció a la inmunosupresión de la paciente y a la presencia de ADN-VPH de riesgo alto. El 54,5% de las lesiones recurrieron en mujeres inmunosuprimidas frente al 10,6% en las inmunocompetentes (RR=5,1 [2,9-8,7]; p=0,000). La recidiva fue del 23,1% en las mujeres con ADN-VPH de riesgo alto frente al 3,1% en las tenían ADN-VPH de riesgo bajo o eran negativas para VPH (RR=7,4 [0,94-57,2]; p=0,037). La multicentricidad de las lesiones por VPH estuvo al límite de la significación y fue más común las no multicéntricas (27,6%) que en las multicéntricas (13%) (RR=0,4 [0,2-0,94]; p=0,051). El grado de la lesión y el tratamiento aplicado no se asociaron con la recidiva, aunque esta fue más frecuente en las VIN (17,6%) que en las AV-VPH (14,7%). Con respecto al tratamiento, destacó que las 5 lesiones tratadas con imiquimod tuvieron una respuesta favorable sin ninguna recidiva. Todas estas lesiones correspondieron a lesiones de AV-VPH.
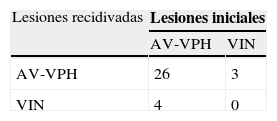
Analizando la histología de las recidivas, del total de lesiones recurrentes, 27 casos (81,8%) fueron AV-VPH y 6 (8,2%) correspondieron a VIN. La histología de las 33 recidivas vulvares se presenta en la tabla 5. Se produjo recidiva con igual lesión que la inicial en 26 (78,8%) casos, en lesión de grado inferior en 3 (9,1%) casos y progresión a grado superior en 4 (12,1%) casos. No hubo ningún caso de progresión a carcinoma invasor de vulva.
No se pudo realizar un modelo multivariante según los riesgos proporcionales de Cox porque no había casos suficientes para el análisis. Usando un modelo de regresión logística lineal e introduciendo las variables inmunosupresión, estatus del ADN-HPV, márgenes quirúrgicos y la multicentricidad, se observó que la única variable independiente predictiva de recidiva vulvar fue el estado inmunitario. La inmunosupresión implicó un riesgo de recurrencia de la lesión vulvar 17,6 veces superior.
DiscusiónLa incidencia de las lesiones preinvasoras de cérvix y de vulva ha tenido un incremento marcado durante las últimas décadas10,11, probablemente como consecuencia de su mayor conocimiento y detección, pero también debido al aumento de las infecciones por VPH, especialmente en la población joven12–14. En este sentido, un estudio demostró un 13% de CIN III en adolescentes sexualmente activas15. La edad media de mujeres con CIN en los distintos estudios publicados oscila entre los 27 y 47 años16. En las VIN, la edad media ha ido disminuyendo de los 50 a los 39 años a partir de los años ochenta17. Hoy existe una sólida evidencia de que el VPH es el causante de CIN18 y de VIN habitual, en donde está presente en cerca del 90% de los casos19. El genotipo 16, tanto para CIN como para VIN, es el más comúnmente implicado20–24. En la serie presentada, tanto las CIN como las VIN presentaron ADN-VPH positivo mediante técnica de PCR en un 50%.
La multicentricidad de las CIN en la serie estudiada fue del 57% y para los VIN del 87%. Estas cifras están de acuerdo con la literatura científica revisada e implican la necesidad de estudiar siempre el TGI ante la presencia de una CIN o una VIN. En un estudio que evaluó la multicentricidad del VPH en el TGI, de 202 mujeres con CIN, el 81% tuvo lesión vulvar concomitante y de 194 pacientes con lesiones vulvares un 85% presentó CIN25. Otros autores describen la multicentricidad en las VIN entre un 32 y un 50%26,27 y se ha sugerido que esta disminuye conforme aumenta la edad de las pacientes28.
La recidiva global de las CIN en la serie estudiada fue del 17%, principalmente durante los primeros 3 años, pero la acumulada durante 5 años fue del 47%. Las cifras de recidiva o persistencia globales se han descrito entre un 5 y un 15%29,30. La mediana de tiempo de las recurrencias es de aproximadamente 9-10 meses, con un rango de 3-23 meses31,32. Van Hamont et al33 revisaron a 1.696 pacientes con CIN II-III tratadas con LLETZ, con una mediana de seguimiento de 6 años y medio. De los casos que presentaron persistencia o recidiva, la mitad se produjo dentro de los primeros 4 meses y el 80% dentro de los 24 meses. El 9,5% de la lesiones recidivaron entre los 3 y 5 años después del tratamiento. El restante 10,2% de las recidivas apareció después de los 5 años de seguimiento con una variación de 62 a 159 meses33.
La edad34,35, la inmunosupresión36,37, los márgenes de resección afectados32,38,39, el compromiso glandular endocervical40, el tamaño de la lesión41 y la presencia de VPH-AR postratamiento35,38,42 han sido identificados en la actualidad como factores de riesgo para recidiva. En esta serie, los factores asociados a la recidiva fueron la inmunosupresión, la afectación de los bordes de resección y la presencia de VPH-AR, pero el único factor predictor independiente en el análisis multivariante fue la inmunosupresión. La inmunodepresión se ha establecido como factor predictivo de la recidiva de CIN, lo que se ha asociado a los valores de linfocitos CD4. Así Fasero et al43 encuentran que la recidiva de las lesiones premalignas de cérvix es mayor en pacientes infectadas por el virus de la inmunodeficiencia humana (VIH) y que ésta se relaciona más con el grado de inmunosupresión que con el tipo histológico de la lesión, sobre todo si los valores de CD4 eran < 200/ml. En otro estudio español32, la presencia de VPH-AR asociada a una carga viral sobre 1.000 RLU implicó tres veces más riesgo de recurrencia. Los autores añaden que la elevada carga viral podría estar relacionada con una mayor extensión de la lesión, lo que determinaría su mayor recurrencia.
Con respecto a la actitud terapéutica, en la serie presentada, el tipo de tratamiento no influyó en el riesgo de recurrencia de las lesiones. En un estudio americano sobre 390 pacientes aleatorizadas para recibir tratamiento mediante asa diatérmica, vaporización con láser o crioterapia; no se encontraron diferencias en relación con la persistencia, recurrencia y complicaciones tras un seguimiento medio de 16 meses29. Nouvo et al44, en una revisión sistemática, tampoco encuentran diferencias entre el cono frío, la ablación con láser, la crioterapia y el asa diatérmica con una mediana de seguimiento de 12 meses.
En la serie estudiada, las CIN II-III representaron la lesión más común, con un 62%. Esto último podría explicar que el 70,7% de las recidivas fueran de alto grado. Estos datos se aproximan a los de una revisión de 3.426 mujeres tratadas con asa diatérmica, el 69% de las cuales fue por CIN II-III. En ese estudio, con una mediana de seguimiento de 35 meses, el 49% de las recidivas fueron lesiones de grado alto y el 0,2% del total durante el seguimiento progreso a cáncer invasor45.
Ningún caso de la serie cervical estudiada progresó a invasión. Es difícil establecer la frecuencia y las tasas exactas de progresión de CIN de alto grado a carcinoma invasor, ya que por razones éticas todas las pacientes reciben tratamiento. En un metaanálisis realizado por Ostor et al46 que incluía 64 estudios con un período de seguimiento de hasta 12 años, el riesgo de progresión de las lesiones de grado alto fue de hasta el 12%. Otros estudios posteriores sitúan algo más elevada la cifra de progresión. Así, Hollowaty et al47 constatan una progresión del 12-25% a los 5 años y Wrigth et al48 del 30-50% a los 12 años. Sin embargo, en algunas series de pacientes tratadas prácticamente no se describe progresión a invasión16. No obstante, la mayoría de estos datos se basan en un seguimiento pequeño, sólo a 2 años. Hoy se sabe que el riesgo de presentar enfermedad invasora en pacientes tratadas aumenta con el tiempo, lo que plantea la necesidad de un seguimiento por al menos 10 años49,50.
De las 3 áreas del TGI que pueden ser afectadas por una neoplasia intraepitelial, el sitio donde más ocurren las recidivas es a nivel vulvar51 y éstas se producen generalmente dentro de los primeros 3 años52. Este dato coincide con los resultados presentados, donde se evidenció que más del 90% de las recidivas de las lesiones vulvares ocurrían en los primeros 3 años. No se conoce una técnica óptima para el tratamiento de las lesiones preneoplásicas de vulva. En general, se recomienda una actitud expectante en las lesiones de grado bajo y se aconseja tratamiento en las de grado alto. No obstante, existe una alta tasa de recurrencia independientemente del tratamiento empleado, que se incrementa con el tiempo y alcanza cifras que rondan el 50%17,53,54. Estos datos están de acuerdo con los de la serie presentada, donde la tasa de recidiva acumulada a los 5 años fue del 54%. Los factores asociados a la recidiva en estas lesiones fueron la multicentricidad, la infección por VPH-AR y la inmunosupresión, que fue la que mejor predijo la recurrencia.
Cuando existe enfermedad multifocal en una VIN de grado alto algunos autores han encontrado recidivas hasta del 50%55,56. Kuppers et al57, en una serie de 102 mujeres con VIN y una media de seguimiento de 3,5 años, observaron que el 36,6% de las pacientes desarrolló recurrencia, la cual se asoció con la multifocalidad y el grado de la lesión. El grado lesional no fue un factor predictor de recidiva en la serie presentada, lo que indica que la gravedad de la lesión puede determinar la progresión de esta, pero no la tendencia a recidivar. Hillemans et al58, en un estudio retrospectivo revisó las distintas modalidades terapéuticas como factor de recurrencia en 93 pacientes con VIN tratadas con vaporización mediante láser de CO2, terapia fotodinámica mediante ácido aminolevulínico (PDT), exéresis de la lesión o vulvectomía. Con una mediana de seguimiento de 53 meses, los autores concluyeron que el tratamiento quirúrgico conservador, la multifocalidad y la infección por VPH de riesgo alto incrementaba el riesgo de recidiva. En una revisión sistemática que agrupó 3.322 casos de VIN 3, la recidiva de las lesiones tampoco dependió del tipo de tratamiento aplicado26. Así, la recurrencia a los 39 meses fue del 18% en las sometidas a vulvectomía, del 22% en las sometidas a exéresis local y del 23% en las vaporizadas con láser. Otros factores se han asociado a la recidiva de las lesiones vulvares como la afectación de bordes quirúrgicos17,56, la edad avanzada, el tabaquismo59 y la sobreexpresión de p5360, pero probablemente la inmunosupresión ha sido uno de los más persistentes en los distintos estudios. Con respecto a esta, un 10% de las mujeres con VIN de la serie presentaban algún grado de inmunosupresión, la mayoría por VIH. Se estima que una paciente seropositiva para VIH tiene 4 veces más riesgo de tener una infección por VPH y, en ellas, la prevalencia de los VIN puede llegar hasta un 37%61. Este antecedente, además de ser un factor de riesgo de VIN, está considerado como uno de los factores más importantes de recurrencia56,62. Esta conclusión se apoya en esta serie, ya que la inmunosupresión resultó ser el único factor de riesgo independiente para recidiva.
La progresión a cáncer de la VIN se establece en un 7-8%53,63. El estudio más reciente y amplio con 405 mujeres afectadas de la VIN encuentra una progresión a carcinoma vulvoperineal de casi el 4%17. Ese estudio además refiere que la progresión a carcinoma aparece en 2,4 años si el tratamiento es incompleto, en 13,5 años en las tratadas correctamente y en 1,1 a 7,3 años (media 3,9 años) en las 10 mujeres no tratadas del estudio. Ninguna paciente en la serie vulvar presentada progresó a invasión; no obstante, el seguimiento medio no llegó a 2 años. La presencia de invasión oculta del estroma, cuando se ha diagnosticado VIN por biopsia, alcanza hasta el 22%53. Este dato debe tenerse en cuenta, ya que es un factor importante en la recurrencia y la progresión. En la serie que se presenta no existió ninguna evidencia de invasión oculta.
En resumen, las lesiones preneoplásicas del TGI aparecen generalmente en la tercera década de la vida de la mujer, son frecuentemente multicéntricas y 1 de cada 6 recidivarán tras el tratamiento. Esta recidiva aumenta con el tiempo y es más común en los primeros 3 años tras la terapia. El grado de la lesión y el tipo de tratamiento aplicado no son factores importantes en la recurrencia lesional. Aunque la presencia de virus de riesgo alto y la afectación de los bordes de resección son factores importantes en la recurrencia de las lesiones, la debilidad del sistema inmunitario aparece como el factor más significativo para predecir la recidiva. Este dato sugiere que las maniobras orientadas a estimular la inmunidad de la paciente podrían reducir el riesgo de recurrencia de las lesiones preneoplásicas del TGI asociadas a la infección por el VPH.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.