Se presenta un caso de adenocarcinoma de endometrio bien diferenciado en una mujer de 30 años, sin hijos, cuya lesión se trató con gestágenos y resección histeroscópica. Tras el tratamiento se consiguió una gestación normal, que se siguió, durante 18 meses, de una anticoncepción con un dispositivo intrauterino (DIU) de levonorgestrel. Tras retirar el DIU se consiguió otra gestación normal. Finalmente, completados los deseos reproductivos, se practicó una histerectomía total con doble anexectomía.
Se comentan los aspectos éticos, diagnósticos y terapéuticos, así como las incertidumbres que tuvimos que afrontar, incluida la posibilidad de progresión de las lesiones y defunción de la paciente.
We present the case of a 30-year-old childless woman who was diagnosed with a well-differentiated endometrial adenocarcinoma. The patient chose conservative treatment consisting of megestrol and hysteroscopic resection. After this treatment, a normal pregnancy ensued, followed by contraception with an intrauterine device (IUD) delivering levonorgestrel for 18 months. After removal of the IUD, a second normal pregnancy occurred. After the second pregnancy, the patient had no desire for more children and a total hysterectomy with bilateral salpingo-oophorectomy was performed. We discuss the ethical, diagnostic and therapeutic dilemmas posed by this case, including the possibility of progression and patient death.
El adenocarcinoma de endometrio es el cáncer pélvico ginecológico más frecuente1. Es propio de mujeres posmenopáusicas; apenas un 15% ocurre antes de la menopausia, pero menos del 4% en mujeres de menos de 40 años2,3.
Los adenocarcinomas de endometrio en mujeres jóvenes suelen presentarse en un entorno de hiperestronismo mantenido, asociado a formas de anovulación crónica y de obesidad4. En el momento de su diagnóstico su estado evolutivo difiere poco del existente en mujeres más mayores5, pero su pronóstico final suele ser más favorable2,3,5, con una tasa de tumores sincrónicos en el ovario elevada6,7.
Las formas histológicas más frecuentes en estas pacientes son las endometrioides, bien diferenciadas, sobre la base de hiperplasias atípicas2,3,5.
La indicación terapéutica es la quirúrgica usual, con lavados peritoneales para citología, histerectomía total con doble anexectomía y biopsias linfáticas extensas de los ganglios pélvicos y paraaórticos, que es además el procedimiento que permite el establecer el estadio evolutivo de la enfermedad, planificar tratamientos adyuvantes y definir el pronóstico, aunque este tratamiento conlleva la pérdida de la fertilidad, en estas mujeres jóvenes, la mayoría sin hijos8.
Alrededor de un 75 % de las formas endometrioides bien diferenciadas pueden responder al tratamiento con progestágenos9, por lo que, para mantener la fertilidad, en casos seleccionados, en mujeres muy motivadas, se han ensayado los tratamientos con gestágenos generales, tamoxifeno, agonistas de la GnRH, con frecuencia acompañados de legrados reiterados para comprobar la erradicación de la enfermedad y la respuesta al tratamiento10,11.
El primer caso de fertilidad posterior tras el tratamiento conservador de un adenocarcinoma de endometrio fue descrito en 1959 por Kistner12 y los últimos han sido publicados en 2007; en total, unas 45 mujeres han conseguido ser madres tras estas terapéuticas. La mayoría de las publicaciones son descripciones de casos aislados12-39, pero es relevante el artículo de Godlieb et al34 que reúne 9 casos, los de Randal y Kurman22 y Niwa et al37 con 5 y los de Jadoul y Donnez35 y Elizur et al39 con 4.
El tratamiento conservador del adenocarcinoma de endometrio en la mujer joven, con deseos reproductivos, presenta muchas dudas y conlleva riesgos, que vamos a analizar en la discusión de nuestro caso, cuyo tratamiento iniciamos en julio de 2001, en el que se consiguieron dos gestaciones, separadas por un intervalo de anticoncepción con un DIU liberador de levonorgestrel, que finalizaron, al completar los deseos reproductivos en 2006, en una histerectomía total con ooforectomia bilateral.
CASO CLÍNICOPaciente que nació en octubre de 1970. Tuvo la menarquia a los 12 años y después mantuvo ciclos regulares 4-5/21-30, con dismenorrea, que fue tratada con anovulatorios orales en dosis baja o con ibuprofeno. Fumaba unos 20 cigarrillos diarios. Su peso eran 70kg y su talla 169cm. Sus antecedentes familiares eran irrelevantes, pero refirió que a su madre le habían realizado un legrado por pólipos endometriales, y tres tías, dos paternas y una materna, habían sido histerectomizadas, sin conocer la causa.
En septiembre del 2000 comenzó con reglas abundantes, de unos 20 días de duración, por lo que consultó a su ginecóloga en noviembre, quien observó, en la ecografía transvaginal, una imagen endometrial hiperecoica de 17 × 16mm, por lo que la remitió al hospital para diagnóstico y tratamiento mediante histeroscopia.
En enero del 2001, la ecografía vaginal, ampliada con hidrosonografía, sugirió una «hiperplasia polipoidea», por lo que se realizaron varias tomas ciegas de biopsia. El patólogo informa de «endometrio proliferativo» pero observó un pequeño fragmento de «adenocarcinoma endometrioide», que podría deberse a contaminación de la muestra, por lo que pidió que se repitiera la biopsia.
En marzo se repitió la biopsia, que se informó de «hiperplasia compleja sin atipias, con marcada metaplasia escamosa de tipo modular»; los patólogos comentaron que, en ocasiones, estos hallazgos van unidos a la existencia en profundidad de un adenomioma o adenosarcoma, por lo que recomendaban un control meticuloso.
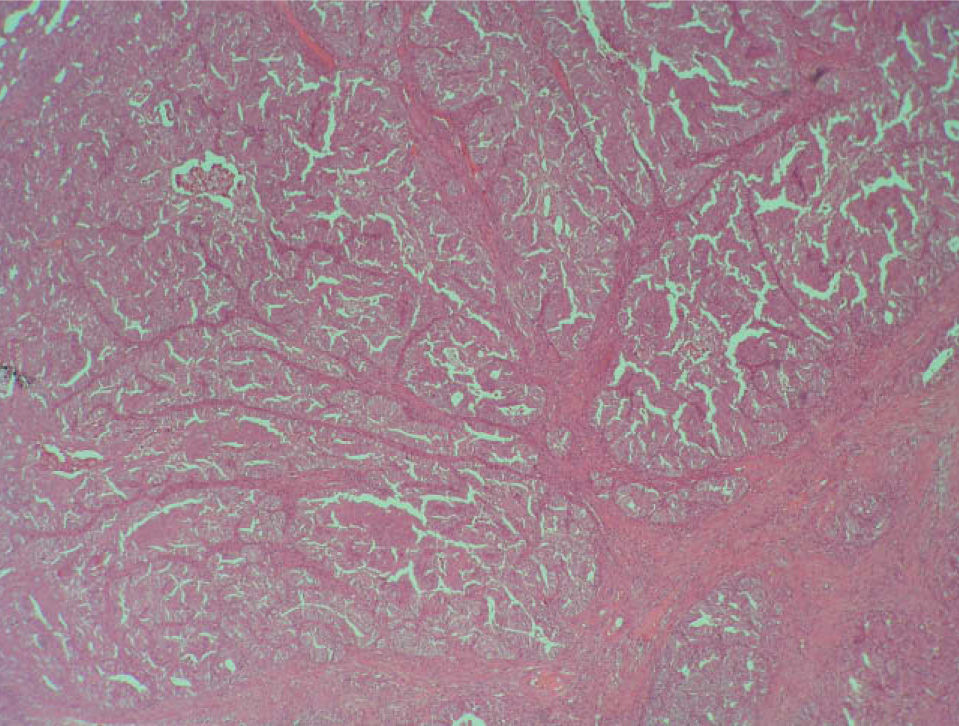
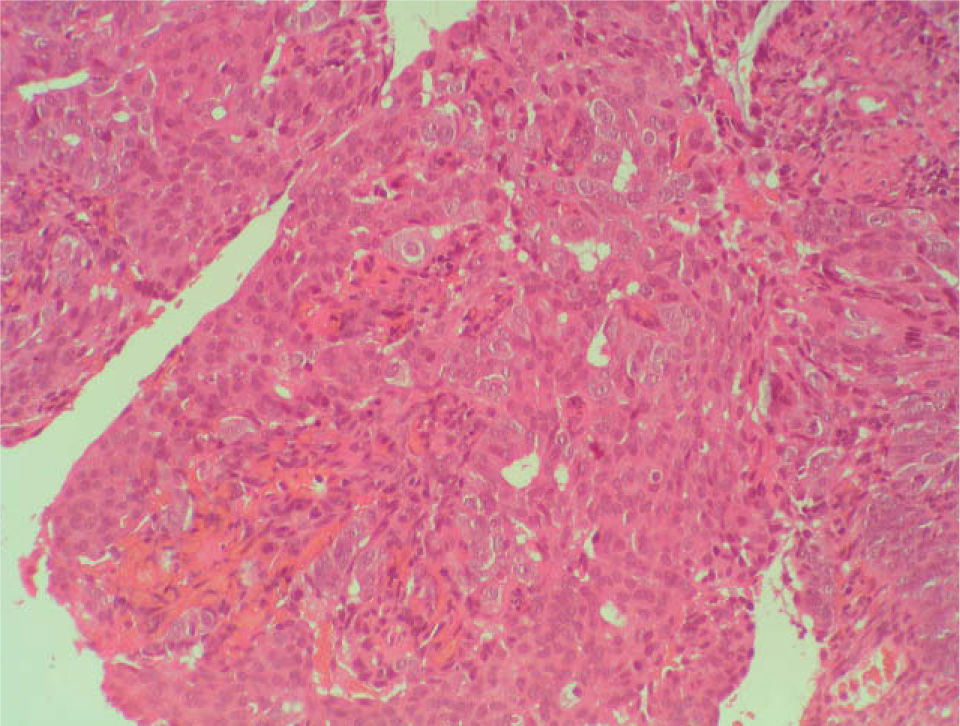
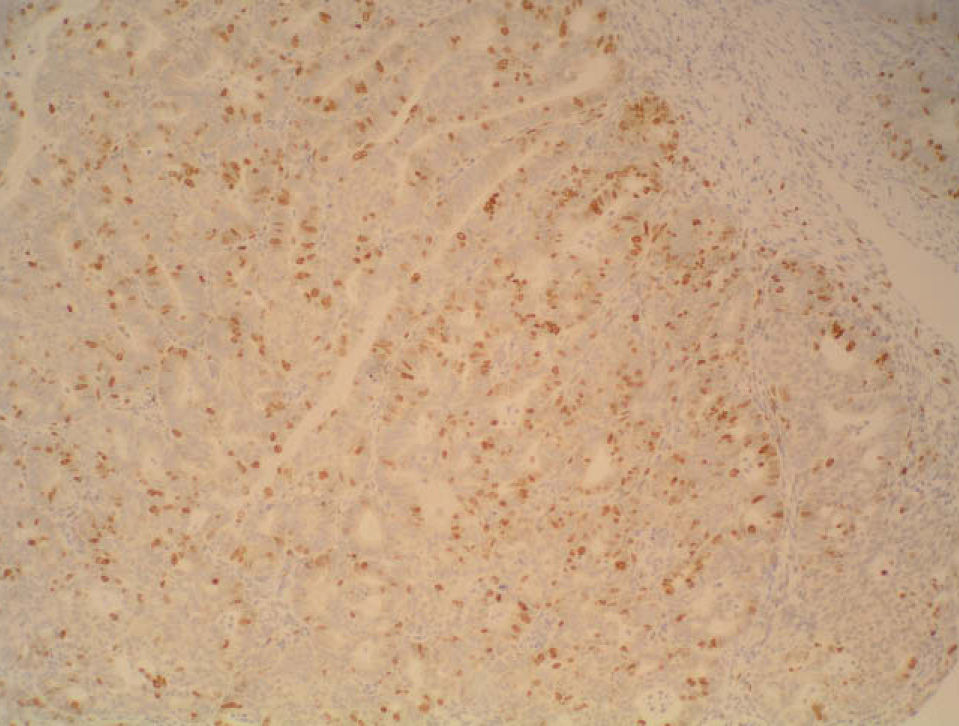
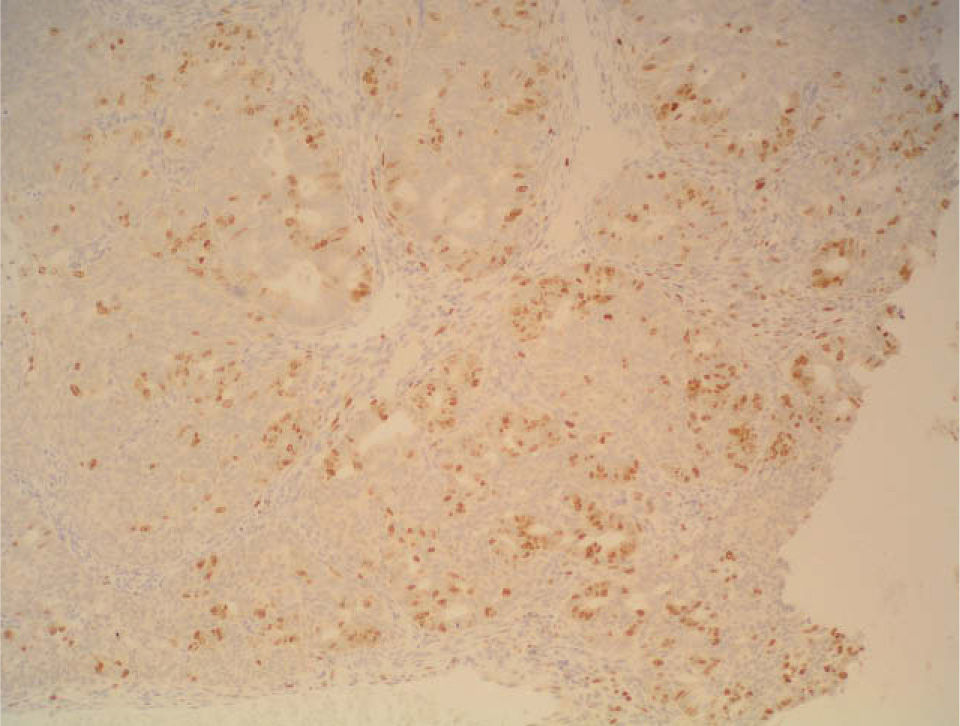
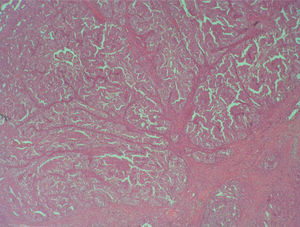
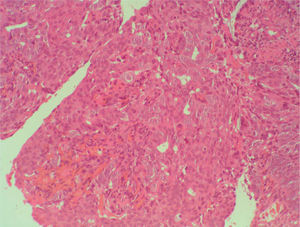
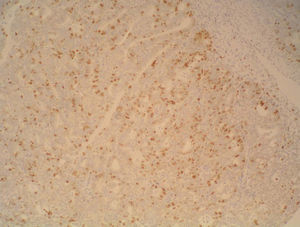
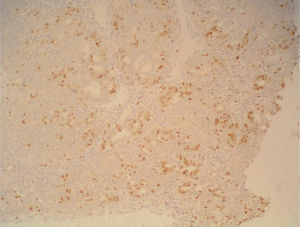
Se planificó una histeroscopia con legrado completo de cavidad y, mientras tanto, se inició un tratamiento con acetato de norestisterona 10mg del día 11 al 25 de cada ciclo. En junio se realizó la histeroscopia, en la que se observó, en la cara lateral derecha, el fondo y el cuerno izquierdo, una estructura adenomatosa que se resecó con el asa de diatermia, y se completó con un legrado completo de la cavidad. El informe del patólogo fue de «adenocarcinoma endometrioide bien diferenciado sobre hiperplasia endometrial compleja con atipias y metaplasia morular» (figs.1-4).
Ante este diagnóstico se plantearon a la paciente dos opciones terapéuticas: cirugía estándar y hormonoterapia.
Durante la fase de información previa al consentimiento informado, se completó una nueva ecografía vaginal con hidrosonografía, Doppler color y velocimetría de los vasos uterinos; se encontró un endometrio engrosado irregular, pero no se ven signos de invasión, ni un mapa vascular alterado ni unas resistencias disminuidas en los vasos uterinos. La resonancia magnética (RM) pélvica fue normal y la evaluación analítica general, que incluye el CA125, también fue normal.
Con un diagnóstico probable de adenocarcinoma de endometrio estadio Ia G1, se inició tratamiento conservador, elegido por la paciente, con 160mg/día de acetato de megestrol.
Se planificaron controles mensuales y, si la respuesta no era adecuada o se detectaban signos de progresión de la enfermedad, se recomendaría cirugía estándar a los 6 meses. A los 2 días de inicio del megestrol, la paciente tuvo una metrorragia de 5 días y no presentó después más hemorragias.
En agosto, un mes después de iniciado el tratamiento, la ecografía transvaginal demostró un endometrio de 7mm, irregular, y un mioma submucoso de 16 × 22mm. La biopsia endometrial que se realizó mostró un endometrio atrófico.
Los posteriores controles con ecografía/Doppler transvaginal, histeroscopia, biopsias, CA125 y RM son negativos, resecándose mediante histeroscopia, en febrero de 2002, lesiones residuales que se diagnostican de pólipo hiperplásico complejo, sin atipias, sobre endometrio secretor avanzado con decidualización iatrogénica y focos de atrofia glandular.
Después de la resección histeroscópica, se suspendió el tratamiento con megestrol y se autorizó a la paciente a quedarse embarazada, continuándose los controles. La presencia de una protrusión polipoidea de 5mm en la hidrosonografía 6 semanas después de suspender el tratamiento llevó a una nueva resección con histeroscopia, que se informó de hiperplasia polipoide compleja con atipia focal. No se realizaron más controles, pues la prueba de embarazo fue positiva a mediados de mayo.
Durante la gestación hubo un episodio de amenaza de aborto, de 10 días; se observó un pequeño hematoma retroplacentario y apareció una diabetes gestacional, tratada con dieta. En enero de 2003 se programó una inducción electiva a la 39 semana, que finalizó con un parto normal, de una niña de 2.960g y una puntuación en la prueba de Apgar de 10/10. Tras la expulsión placentaria se completó un legrado de cavidad; no se encontraron lesiones residuales en el material del legrado ni en la placenta.
A las 6 semanas del parto se examinó la cavidad endometrial mediante histeroscopia; se observaron imágenes endometriales proliferativas, que la biopsia informó de endometrio proliferativo, y se insertó un DIU liberador de levonorgestrel (Mirena®). Los controles endometriales posteriores planificados fueron mediante ecografía transvaginal, biopsia endometrial y CA125 trimestrales, e histeroscopia y RM anuales; es reseñable la presencia frecuente de quistes de ovario funcionales y un informe equívoco de la RM, que fue ignorado ante la normalidad clínica y de las restantes exploraciones.
En junio de 2004, la paciente decidió intentar un nuevo embarazo, por lo que se retiró el DIU, pero se siguieron los controles. El 14 de diciembre de 2004 tuvo una menstruación normal y a finales de enero del 2005 la prueba de embarazo resultó positiva. Esta segunda gestación cursó sin incidentes. El 20 de septiembre de 2005 se produjo el parto espontáneo de una niña de 3.260g y una puntuación en la prueba de Apgar de 10/10.
La paciente refirió que había completado sus deseos reproductivos y, tras el análisis de la posibilidad de recidiva y de la mayor frecuencia de lesiones ováricas, decidió la realización de una histerectomía con ooforectomia. En marzo de 2006 se practicó la intervención y ni en la citología de lavado peritoneal, ni el estudio de los ovarios, trompas o útero se encontraron lesiones. En la actualidad, lleva un tratamiento hormonal sustitutivo con estradiol transdérmico.
DISCUSIÓNLas particularidades relacionadas con el diagnóstico, el estadio evolutivo, las respuestas al tratamiento, la contracepción y las patologías asociadas hacen de este caso un buen ejemplo para comentar la multitud de incertidumbres que presidieron la conducción, advirtiendo que su brillante resultado no hace extrapolable este tipo de conducción a otros casos semejantes.
La primera incertidumbre fue si el diagnóstico anatomopatológico era auténtico, dadas las dificultades que tienen los patólogos para diferenciar entre los adenocarcinomas endometrioides y las hiperplasias complejas con atipias, diferencias que son también difíciles de establecer a nivel molecular40, mientras que se trata de dos lesiones de una agresividad biológica diferente pero que, con gran frecuencia, coinciden. Esta paciente tenía muy pocas probabilidades de presentar un adenocarcinoma de endometrio, ya que no tenía ninguno de los caracteres de riesgo1,2,4-6: era joven, su constitución normal, la historia menstrual era compatible con ciclos ovulatorios, ya que eran ciclos regulares y con dismenorrea. Además, tenía otros elementos que disminuían el riesgo, pues era fumadora y había sido tratada intermitentemente con anovulatorios orales por su dismenorrea1. Los 3 patólogos que analizaron las muestras coincidieron en el diagnóstico de adenocarcinoma endometrioide bien diferenciado.
La segunda incertidumbre era si se daban todas las condiciones para un tratamiento conservador, es decir, si era un tumor limitado al propio endometrio (estadio Ia), con buena diferenciación (G1), con elementos que hicieran previsible una respuesta a la hormonoterapia (presencia de receptores de progesterona), que no existiera ninguna patología asociada (en especial tumores sincrónicos de ovario) y que la paciente estuviera de acuerdo con los riesgos asociados a un tratamiento conservador, ya que en estas condiciones la cirugía consigue prácticamente el 100% de curaciones8.
La certeza de estar ante un estadio Ia sólo se podía conseguir con la cirugía, y las aproximaciones realizadas, mediante la ecografía, con mapa vascular y velocimetría Doppler, y la RM, aunque son valiosas, no permiten conclusiones categóricas. La mejor ayuda es la RM, que permite analizar el útero, los anexos y los linfáticos pélvicos; su precisión está próxima al 90%41, pero para establecer el grado de invasión miometrial, que se relaciona directamente con la afectación linfática, y la morfología ovárica, la ecografía transvaginal con Doppler puede tener una precisión semejante41. La tomografía de emisión de positrones (PET) con glucosa no aporta ventajas; sería mejor la PET con F18 17β-estradiol, al menos si son tumores que poseen receptores de estrógenos42.
También el grado de diferenciación histológico no es, con frecuencia, acorde cuando se parte de muestras obtenidas mediante biopsia, pues existe la posibilidad de que en otras zonas la diferenciación fuera menor. El diagnóstico en este caso se estableció tras la ablación completa de las lesiones bajo control histeroscópico, por lo que se disponía, para la valoración, de casi toda la lesión.
Sólo conocimos que había receptores de estrógenos, no de progesterona, que son los que con mayor claridad se asocian a una respuesta previsible a la hormonoterapia, por lo que esta posibilidad se infirió de las características histológicas, de la presencia de receptores de estrógenos y por la inmediata respuesta terapéutica.
La frecuencia de tumoraciones sincrónicas en los ovarios es más elevada en estas pacientes jóvenes, y en algunas series alcanza hasta el 25%. La exclusión de éstas estuvo basada en técnicas de precisión limitada, en especial si las lesiones son pequeñas, la ecografía transvaginal, la RM pélvica y los marcadores tumorales, el CA125, y se han descrito casos de progresión de lesiones de ovario no diagnosticadas28,36,43.
La condición más clara y necesaria para un tratamiento conservador es la firme determinación de la paciente de ser madre y, para ello, de asumir los riesgos, conociendo todas nuestras incertidumbres y, en nuestra paciente, esta determinación fue muy clara y vehemente, incluso ante un entorno familiar que presionaba para que se efectuara el tratamiento quirúrgico habitual. La respuesta real de estos tumores a los gestágenos no la conocemos, pues hay que contar con un sesgo en las publicaciones; así, muchos casos esporádicos en que el tratamiento fracasó no deben de haber sido publicados. Las series publicadas en aquellos momentos eran pequeñas y una revisión reciente la sitúa en casi un 80%9.
La tercera incertidumbre era qué repercusión sobre el pronóstico podría suponer demorar la cirugía si el tratamiento conservador fracasaba, pues aunque las demoras durante tiempos limitados de 4 a 6 meses no parecen tener una gran influencia, seguramente por factores de confusión que llevan a que los casos de mayor riesgo sean tratados con menores retrasos44, en nuestro caso la demora, desde que se inició la clínica hasta que se instauró el diagnóstico, era ya de 10 meses, a los que había que añadir otros 6 de prueba. Afortunadamente, la rápida respuesta al tratamiento ayudó a apaciguar esta duda, pero hay descritos casos de progresión y metástasis28,43 e incluso la muerte36.
La cuarta incertidumbre respecto de la elección del tratamiento; en ese momento, nos pareció que el acetato de megestrol había sido más utilizado, pero revisiones posteriores muestran que el acetato de medroxiprogesterona ha sido empleado con una frecuencia algo mayor9-11. El acetato de megestrol tiene una potencia unas 30 veces superior a la propia progesterona, mediante su más persistente fijación al receptor de progesterona, lo que provoca una repuesta dicotómica del tumor.
En el estroma acompañante, que es normal, se producen un estímulo mitogénico y una maduración decidual, semejantes a los cambios de la fase lútea.
En la célula epitelial tumoral el efecto es antimitogénico, con promoción de la apoptosis celular. El efecto antimitogénico está mediado por su acción antiestrogénica, mientras que la apoptosis es promocionada por la supresión de la proteína antiapoptótica bcl-2 y por el aumento de la actividad del sistema Fas-FasL, con la activación de la vía de las caspasas. Mientras los hallazgos no son uniformes, otras vías, como la supresión de la metaloproteinasas, podrían estar involucradas45.
En los casos de buena respuesta a los gestágenos, se origina un epitelio endometrial inactivo, sin mitosis, con un estroma decidualizado y una vascularización poco desarrollada, pero algunas glándulas mantienen alteraciones arquitectónicas.
En la anticoncepción posterior se prefirió el DIU liberador de levonorgestrel, ya ensayado en pacientes con estos tumores y malas condiciones de operabilidad, pues los anovulatorios orales, utilizados para el tratamiento de la dismenorrea en esta paciente, no mostraron sus efectos protectores. El DIU fue bien tolerado, permitió el seguimiento del endometrio pero introdujo un factor de confusión, con la presencia frecuente de quistes ováricos funcionales, en una situación en la que la frecuencia de lesiones neoplásicas ováricas es mayor. Los caracteres ecográficos de estos quistes y la normalidad del CA125 permitieron conducir esta circunstancia. Otra alternativa hubiera sido una anticoncepción con solo gestágenos.
Completados los deseos reproductivos, la histerectomía profiláctica estuvo justificada por la elevada frecuencia de recidivas, que intuimos mayor en esta paciente, ya que sugería poseer una predisposición genética, pendiente de estudio, ya que el adenocarcinoma había surgido sin hiperestronismo, sin anovulación crónica y sin obesidad. La frecuencia de neoplasias ováricas descrita en estos casos6,7 llevó a que la paciente también decidiera la ooforectomia profiláctica, ya que un tratamiento hormonal sustitutivo con estrógenos transdérmicos evitaría los efectos del hipoestronismo, con un menor aumento de los riesgos de cáncer de mama.