El objetivo es informar de nuestro estudio multicéntrico de seguridad y eficacia acerca de la angioplastia con stent recuperable en el vasoespasmo secundario a la hemorragia subaracnoidea por aneurisma (HSAa).
MétodosRealizamos un análisis retrospectivo de una base de datos prospectiva de pacientes consecutivos sometidos a tratamiento endovascular mediante angioplastia con stent recuperable para el vasoespasmo relacionado con la HSAa en cuatro departamentos de neurorradiología intervencionista, entre enero de 2018 y julio de 2019. Incluimos a pacientes consecutivos mayores de 18 años con vasoespasmo mayor del 50% de la arteria carótida interna (ACI), la arteria cerebral anterior (ACA) y/o las arterias cerebrales medias (ACM) secundario a HSAa, tratado endovascularmente mediante angioplastia con stent recuperable. Las complicaciones del procedimiento y las complicaciones clínicas se registraron como variables de seguridad. Las variables de eficacia radiológica del procedimiento se definieron como la mejora en el porcentaje de estenosis después del tratamiento endovascular y la mejora o normalización del tiempo de circulación cerebral (TCC).
ResultadosIncluimos 16 procedimientos de angioplastia con stent recuperable en 13 pacientes, con 33 segmentos arteriales tratados (10 ACI, 15 ACM y 8 ACA). No encontramos complicaciones de procedimiento en ningún paciente, ni complicaciones clínicas en pacientes no intubados. Todos los pacientes con TCC retrasado al principio del procedimiento, excepto uno, mostraron una mejora en el TCC. La mejora en el porcentaje de estenosis en la ACI fue de 18± 11,65 (media±DE), 30,67±18,45 en la ACM y 28,38±15,49 en la ACA. No encontramos ninguna asociación estadísticamente significativa entre las variables de tratamiento endovascular y la mejora en el porcentaje de estenosis.
ConclusiónLa angioplastia con stent recuperable como tratamiento del vasoespasmo secundario a la HSAa es un procedimiento seguro y eficaz que mejora el TCC y la estenosis del vaso después del tratamiento.
To determine the safety and efficacy of angioplasty with a retrievable stent in treating vasospasm secondary to subarachnoid hemorrhage (SAH) due to an aneurysm.
MethodsWe retrospectively analyzed prospectively collected data from consecutive patients undergoing endovascular angioplasty with a retrievable stent to treat vasospasm related to SAH due to an aneurysm in four neurointerventional radiology departments between January 2018 and July 2019. We included patients aged>18 years with vasospasm>50% of the internal carotid artery (ICA), anterior cerebral artery (ACA), and / or middle cerebral artery (MCA) secondary to SAH due to an aneurysm treated with endovascular angioplasty with a retrievable stent. The variables used to measure safety were complications of the procedure and clinical complications. The variables used to measure radiological efficacy were improvement in the degree of stenosis after endovascular treatment and improvement or normalization of cerebral circulation time CTT).
ResultsWe included 16 angioplasty procedures with retrievable stents in 13 patients, in which 33 arterial segments were treated (10 ICA, 15 MCA, and 8 ACA). We observed no complications of the procedure in any patients and no clinical complications in patients who were not intubated. All but one of the patients who had delayed CTT at the beginning of the procedure showed improvements in CTT. The mean improvement in the degree of stenosis was 18%±11.65% in the ICA, 30.67%±18.45% in the MCA, and 28.38%±15.49% in the ACA. No statistically significant associations were observed between endovascular treatment variables and the degree of improvement in stenosis.
ConclusionAngioplasty with a retrievable stent is a safe and efficacious treatment for vasospasm secondary to SAH due to an aneurysm, improving CTT and stenosis.
La hemorragia subaracnoidea por aneurisma (HSAa) es un subtipo grave de accidente cerebrovascular con consecuencias de morbilidad y mortalidad elevadas después de la fase aguda de la enfermedad1. El vasoespasmo cerebral es la complicación más importante de la HSAa en la fase subaguda (5-14 días), es la causa principal de la isquemia cerebral tardía grave, que es el principal motivo del resultado clínico desfavorable2. La causa exacta de la isquemia cerebral tardía no se comprende por completo; sin embargo, la prevención o el tratamiento temprano del vasoespasmo cerebral parece mejorar el resultado del paciente3. El tratamiento endovascular del vasoespasmo es controvertido. Existen diferentes enfoques, como la infusión de vasodilatadores arteriales o la angioplastia intracraneal, en función de las diferentes instituciones y preferencias personales. El objetivo del estudio es informar de nuestro estudio multicéntrico de seguridad y eficacia acerca de la angioplastia con stent recuperable en el vasoespasmo secundario a la HSAa. Un objetivo secundario es evaluar las variables del procedimiento endovascular que pueden asociarse con la mejora del porcentaje de estenosis del vaso.
Materiales y métodosDiseño de estudio, pacientes y recopilación de datosRealizamos un análisis retrospectivo de una base de datos prospectiva de pacientes consecutivos sometidos a tratamiento endovascular mediante angioplastia con stent recuperable para el vasoespasmo relacionado con la HSAa en cuatro departamentos de neurorradiología intervencionista de gran volumen, entre enero de 2018 y julio de 2019. Se obtuvo el consentimiento informado de todos los pacientes para el procedimiento endovascular; no se nos exigió presentar información adicional para la autorización institucional debido a la naturaleza retrospectiva del estudio.
Incluimos a pacientes consecutivos mayores de 18 años con vasoespasmo en más del 50% de la arteria carótida interna (ACI), la arteria cerebral anterior (ACA) y/o la arteria cerebral media (ACM) secundario a HSAa, tratados endovascularmente mediante angioplastia con stent recuperable. Se excluyeron los pacientes con tortuosidad pronunciada de la anatomía u oclusión arterial que impidiera el despliegue del dispositivo.
Variables demográficas, clínicas y radiológicas en la presentación hemorrágicaSe registraron variables demográficas (edad y sexo) y variables de factores de riesgo cardiovascular (hipertensión arterial, diabetes mellitus, tabaquismo, antecedentes familiares de aneurisma cerebral, displasia fibromuscular y enfermedad poliquística). La situación clínica de los pacientes se evaluó en el momento del ingreso con dos escalas neurológicas: escala de Hunt y Hess y escala de coma de Glasgow.
Se revisaron las tomografías computarizadas (TC) sin contraste para evaluar la intensidad de la HSAa empleando la escala de TC de Fischer modificada y la presencia de hematoma intraparenquimatoso. Un neurorradiólogo intervencionista analizó la angiografía por sustracción digital (ASD) para determinar el número de aneurismas, la forma (sacular o fusiforme), el tamaño (tamaño máximo en milímetros), la ubicación (arteria comunicante anterior, arteria comunicante posterior, ACM, arteria coroidal anterior, bifurcación de la ACI, segmento oftálmico de la ACI, bifurcación de la arteria basilar, otras localizaciones) y el lado (izquierdo o derecho) del aneurisma sangrante.
Variables clínicas y radiológicas relacionadas con el vasoespasmoDurante el episodio de vasoespasmo se registraron el período de tiempo desde el sangrado (días después de la hemorragia), la intubación del paciente (sí o no) y el déficit neurológico principal.
La ASD fue analizada por un neurorradiólogo intervencionista para determinar su ubicación (ACI, ACA y/o AC) y el lado (izquierdo o derecho) del vasoespasmo, el porcentaje de estenosis previo al tratamiento (comparado con la ASD realizada durante el tratamiento endovascular de un aneurisma sangrante) y el tiempo de circulación cerebral (TCC) (normal o retardado, definido como más de 8 segundos desde la aparición del contraste en la ACI hasta el drenaje venoso).
Variables del tratamiento endovascularTodos los procedimientos se llevaron a cabo con heparinización sistémica de acuerdo con el protocolo local y con un método de desenvainado, a diferencia del método de arrastre utilizado en la trombectomía mecánica, a fin de evitar el daño endotelial y el vasoespasmo iatrogénico. En cuanto a las variables del tratamiento endovascular, se registraron la ubicación (ACI, segmento de la ACA A1 y/o segmento de la ACM M1) y la duración de la colocación del dispositivo (minutos), el lado (izquierdo o derecho) del tratamiento, el tipo de dispositivo (Trevo [Stryker, Mountain View, CA, EE.?UU.], Solitaire [Covidien, Dublín, Irlanda], Vesalio NeVa-VS [Vesalio, Nashville, TN, EE.?UU.], Catch/Catch-Mini [Balt, Montmorency, Francia], dispositivo Aperio [Acandis, Pforzheim, Alemania], dispositivo Preset [Phenox, Bochum, Alemania]) y el tamaño del dispositivo.
También se registró el uso de fármacos vasodilatadores, el tipo y el catéter desde el que se administró el fármaco (microcatéter, catéter guía, otros). Al final del procedimiento se registró el porcentaje de estenosis postratamiento y la mejora del TCC.
Las complicaciones del procedimiento (hematoma inguinal, perforación, disección, vasoespasmo, otros) y las complicaciones clínicas como un nuevo déficit neurológico o el empeoramiento de un déficit neurológico previo se registraron como variables de seguridad durante el tratamiento endovascular. Las variables de eficacia radiológica del procedimiento se definieron como la mejora en el porcentaje de estenosis después del tratamiento endovascular y la mejora o normalización del TCC. Se definieron las variables de eficacia clínica como la mejora de un déficit neurológico anterior.
Análisis estadísticoEl análisis descriptivo incluyó frecuencias y porcentajes para las variables categóricas y la media (desviación estándar [DE]) o la mediana (intervalo intercuartílico [IIC]) para las variables continuas. El tamaño del stent recuperable y la duración de la colocación del dispositivo se dicotomizaron en 4mm y 5 minutos, respectivamente, con el fin de detectar cualquier asociación con la mejora del porcentaje de estenosis del vaso. Se realizó un análisis monofactorial utilizando la prueba U Mann-Whitney para las variables continuas y la prueba de χ2 o la prueba exacta de Fisher para las variables categóricas. Los análisis estadísticos se realizaron utilizando el paquete estadístico para procesar datos en ciencias sociales, versión 20.0 (SPSS, por sus siglas en inglés, Chicago, Illinois, EE.?UU.). Un valor de p <0,05 se consideró significativo.
ResultadosPoblación de pacientesIncluimos 16 procedimientos de angioplastia con stent recuperable en 13 pacientes, sin excluir a ningún paciente por la imposibilidad de desplegar el dispositivo debido a tortuosidad u oclusión arterial. La edad media fue de 52,46±6,9 (media±DE) años y 10 (76,92%) pacientes eran mujeres. Las variables clínicas y radiológicas se resumen en la tabla 1. No hubo pacientes con antecedentes familiares de aneurisma cerebral, displasia fibromuscular o enfermedad poliquística. Ocho pacientes (61,5%) tuvieron un solo aneurisma; 5 (38,5%) pacientes tuvieron más de un aneurisma (2 pacientes tuvieron dos aneurismas, 1 paciente tuvo tres aneurismas y 2 pacientes tuvieron cuatro aneurismas). Todos los aneurismas sangrantes sospechosos eran saculares, excepto uno que era un aneurisma disecante. Todas las demás características de los aneurismas se resumen en la tabla 1.
Variables clínicas y radiológicas relacionadas con la HSAa
| n (%) | |
|---|---|
| Factores de riesgo cardiovascular | |
| Hipertensión | 5 (38,46) |
| Diabetes | 0 (0) |
| Tabaquismo | 1 (7,69) |
| Escala de Hunt y Hess | |
| 1 | 1 (8,3) |
| 2 | 5 (41,7) |
| 3 | 2 (16,7) |
| 4 | 3 (25) |
| 5 | 1 (8,3) |
| Escala de coma de Glasgow | |
| 13-15 | 6 (46,16) |
| 7-12 | 5 (38,46) |
| 3-6 | 2 (15,38) |
| Escala modificada de Fisher | |
| I | 1 (7,69) |
| II | 0 (0) |
| III | 0 (0) |
| IV | 12 (92,31) |
| Hematoma intraparenquimatoso | 1 (7,69) |
| Ubicación del aneurisma sangrante sospechoso | |
| Arteria comunicante anterior | 4 (30,79) |
| Arteria comunicante posterior | 2 (15,38) |
| Arteria cerebral media | 2 (15,38) |
| Arteria coroidal anterior | 1 (7,69) |
| Bifurcación de la arteria carótida interna | 1 (7,69) |
| Segmento oftálmico de la arteria carótida interna | 1 (7,69) |
| Bifurcación de la arteria basilar | 1 (7,69) |
| Otras ubicaciones | 1 (7,69) |
| Lado del aneurisma sangrante sospechoso | |
| Derecho | 6 (46,15) |
| Izquierdo | 6 (46,15) |
| Tamaño del aneurisma sangrante sospechoso (media±DE) | 7,33±3,66 |
Los episodios de vasoespasmo se presentaron en el día 9,2±3,6 (media±DE) después del HSAa. Seis pacientes (37,5%) se encontraban bajo anestesia general cuando se realizó el tratamiento endovascular, por lo que no fue posible realizar una evaluación clínica de los mismos. En esos pacientes, la indicación del tratamiento endovascular se basó en el Doppler transcraneal (DTC) o en la ASD del vasoespasmo, con más del 50% de estenosis de la ACI, la ACM y/o la ACA.
En los 10 pacientes restantes sin anestesia general, el examen neurológico mostró déficit motor en 8 (80%) pacientes, bradipsiquia o fluctuación del nivel de conciencia en 6 (60%) pacientes y afasia en 1 (10%) paciente. Se observó TCC retrasado en 11 (68,75%) pacientes.
Se utilizaron fármacos vasodilatadores en todos los pacientes, en 9 (56,3%) el fármaco vasodilatador se infundió a través del catéter guía y en 7 (43,8%) pacientes se infundió a través del microcatéter antes o después de la angioplastia con stent recuperable. El fármaco vasodilatador utilizado fue verapamilo en 3 (18,8%) pacientes, nimodipino en 3 (18,8%) pacientes, verapamilo más nimodipino en 4 (25%) pacientes, nimodipino más milrinona en 4 (25%) pacientes, verapamilo más nitroglicerina en 1 (6,3%) paciente y verapamilo más nitroglicerina más nimodipino en 1 (6,3%) paciente. La pauta posológica de los vasodilatadores se resume en la tabla 2.
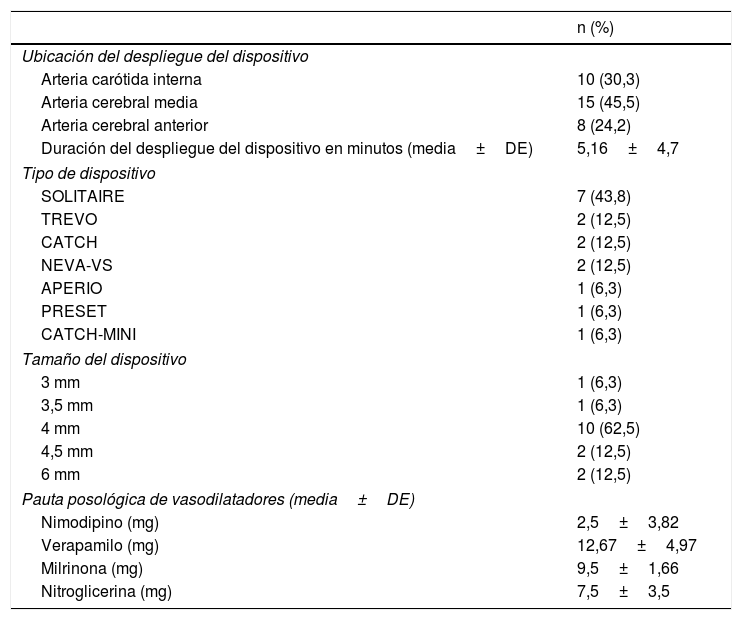
Variables del tratamiento endovascular
| n (%) | |
|---|---|
| Ubicación del despliegue del dispositivo | |
| Arteria carótida interna | 10 (30,3) |
| Arteria cerebral media | 15 (45,5) |
| Arteria cerebral anterior | 8 (24,2) |
| Duración del despliegue del dispositivo en minutos (media±DE) | 5,16±4,7 |
| Tipo de dispositivo | |
| SOLITAIRE | 7 (43,8) |
| TREVO | 2 (12,5) |
| CATCH | 2 (12,5) |
| NEVA-VS | 2 (12,5) |
| APERIO | 1 (6,3) |
| PRESET | 1 (6,3) |
| CATCH-MINI | 1 (6,3) |
| Tamaño del dispositivo | |
| 3 mm | 1 (6,3) |
| 3,5 mm | 1 (6,3) |
| 4 mm | 10 (62,5) |
| 4,5 mm | 2 (12,5) |
| 6 mm | 2 (12,5) |
| Pauta posológica de vasodilatadores (media±DE) | |
| Nimodipino (mg) | 2,5±3,82 |
| Verapamilo (mg) | 12,67±4,97 |
| Milrinona (mg) | 9,5±1,66 |
| Nitroglicerina (mg) | 7,5±3,5 |
No detectamos complicaciones del procedimiento en ningún paciente, ni complicaciones clínicas en pacientes no intubados, como el empeoramiento de un déficit neurológico anterior o la aparición de un nuevo déficit neurológico. De los 13 pacientes, cuatro fueron retratados. Tres de ellos recibieron tratamiento endovascular dos veces en un plazo de 10 a 12 horas, en el contexto del protocolo local para vasoespasmos endovasculares, sin empeoramiento clínico ni de los vasoespasmos, y el paciente restante recibió tratamiento endovascular con fármacos vasodilatadores, debido a la aparición de hemiparesia izquierda. El paciente había sido tratado previamente por hemiparesia derecha días antes, y se consideró como un nuevo episodio de vasoespasmo sintomático. Ninguno de los otros 9 pacientes volvió a ser tratado en el mismo lado del tratamiento de angioplastia con stent recuperable.
Todos los pacientes con TCC retrasado al principio del procedimiento, excepto uno, mostraron una mejora en el TCC (10 de 11 pacientes; 90,91%); no obstante, ninguno volvió a los valores normales. En los pacientes no intubados, se observó la mejora de un déficit neurológico previo en 5 de 8 (62,5%) pacientes en los que se pudo evaluar al paciente.
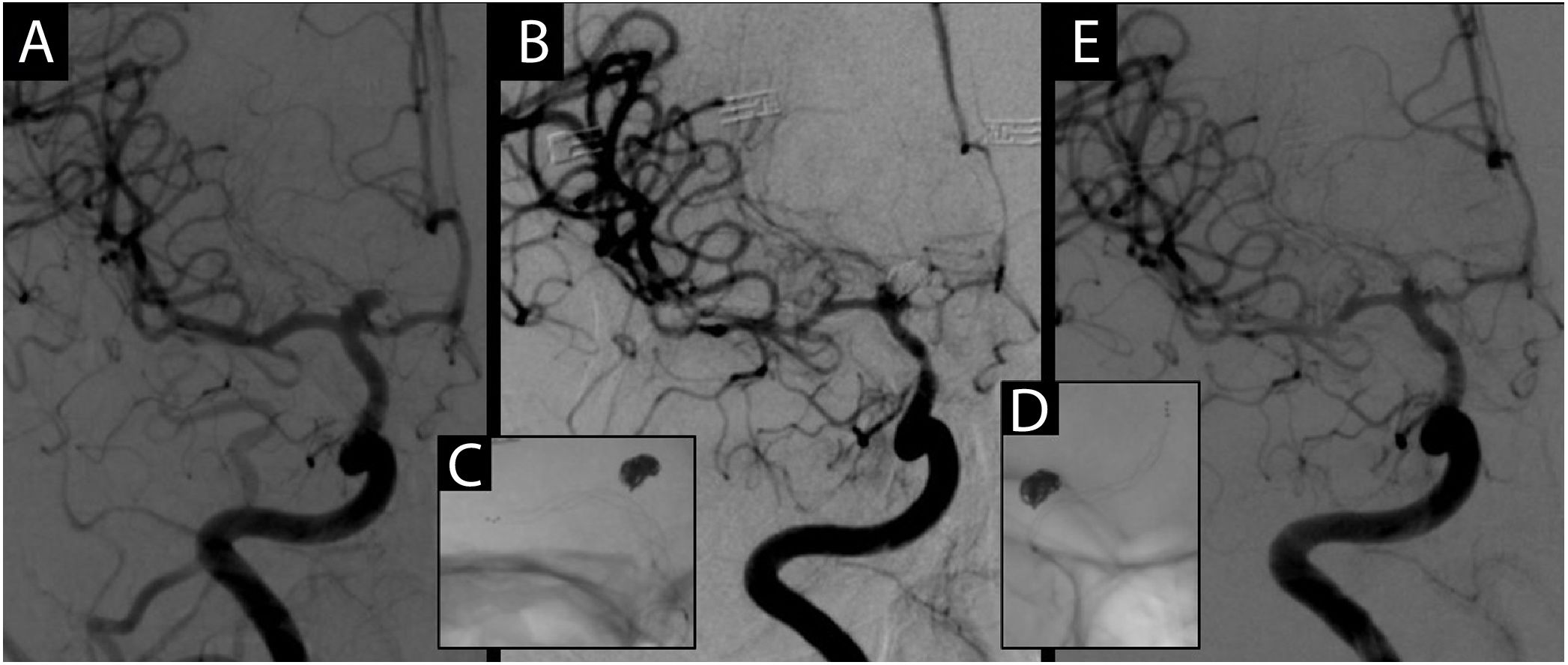
En cuanto a las variables de tratamiento endovascular, 33 segmentos fueron tratados mediante angioplastia con stent recuperable (fig. 1). El resto de las variables se resumen en la tabla 2. El porcentaje de estenosis previa y posterior al tratamiento y la mejora de esta se resumen en la tabla 3. La relación entre las variables del tratamiento endovascular y la mejora del porcentaje de estenosis se resumen en la tabla 4. No pudo realizarse el análisis de la ACI y de los segmentos de la ACA debido al pequeño tamaño de la muestra.
La angiografía en el ingreso (A) mostró un calibre normal de vaso intracraneal y un aneurisma carotídeo interno terminal. Ocho días después, la angiografía previa al tratamiento (B) mostró espasmo del vaso intracraneal en la arteria carótida interna, la arteria cerebral anterior y la arteria cerebral media. Después de la angioplastia con stent en la arteria cerebral media y la arteria carótida interna (C) y en la arteria cerebral anterior (D), la angiografía posterior al tratamiento (E) mostró una mejora en el calibre de los tres vasos.
Variables de eficacia del tratamiento endovascular relacionadas con la estenosis arterial
| Porcentaje de estenosis antes del tratamiento (media±DE) | Porcentaje de estenosis después del tratamiento (media±DE) | Mejora en el porcentaje de estenosis (media±DE) | |
|---|---|---|---|
| Arteria carótida interna | 34,6±14,43 | 16,6±11,31 | 18±11,65 |
| Arteria cerebral media | 52,13±16,34 | 21,47±12,7 | 30,67±18,45 |
| Arteria cerebral anterior | 58,88±20 | 28±24 | 28,38±15,49 |
Relación entre las variables de tratamiento endovascular y la mejora en el porcentaje de estenosis. Mediana (intervalo intercuartílico)
| Colocación del dispositivo <5 min | Colocación del dispositivo ≥ 5 min | p | |
|---|---|---|---|
| Todos los segmentos | 20 (15-25) | 32 (12-45) | 0,503 |
| ACM | 20 (20-30) | 39 (16,5-49) | 0,731 |
| Tamaño del dispositivo ≤ 4 mm | Tamaño del dispositivo> 4 mm | p | |
| Todos los segmentos | 20 (15-30) | 39 (11-45) | 0,33 |
| ACM | 20 (20-30) | 42 (15,75-51) | 0,412 |
| Vasodilatador mediante catéter guía | Vasodilatador mediante microcatéter | p | |
| Todos los segmentos | 28 (12,5-45) | 20 (15-25) | 0,19 |
| ACM | 39 (16,5-49) | 20 (20-30) | 0,328 |
El presente estudio multicéntrico demostró que la angioplastia con stent recuperable como tratamiento del vasoespasmo secundario a la HSAa es un procedimiento muy eficaz en cuanto a la mejora del TCC (90,91%) y el porcentaje de estenosis de los vasos (hasta un 30% de mejora media del diámetro de los vasos en la ACM y cerca de un 20% de mejora media del diámetro de los vasos en la ACI), con una tasa muy baja de complicaciones del procedimiento y clínicas. No descubrimos pacientes que necesitaran un nuevo tratamiento endovascular secundario a la recurrencia de los síntomas o al vasoespasmo en el mismo lado del tratamiento. No encontramos ninguna asociación estadísticamente significativa entre las variables de tratamiento endovascular y la mejora en el porcentaje de estenosis.
Nuestros datos coinciden con la literatura ya publicada. En 2017, Bhobal et al.4 publicaron un artículo de prueba de concepto que presentaba una serie retrospectiva de 4 pacientes; todos ellos fueron tratados con un stent recuperable para un vasoespasmo por HSAa. No tuvieron ninguna complicación, pero 2 (50%) pacientes sufrieron un vasoespasmo recurrente, sin que se especificara si necesitaban o no un tratamiento endovascular secundario.
Kwon et al.5 publicaron en 2018 una experiencia retrospectiva unicéntrica, de 12 pacientes con vasoespasmo debido a HSAa que fueron tratados con stent recuperable, que se desplegaron en 53 segmentos. El despliegue del recuperado de stents fue técnicamente factible en todos los casos. Dividieron a todos los pacientes en dos grupos: 5 pacientes fueron tratados en primer lugar con vasodilatadores intraarteriales y después con el despliegue de stent recuperable (VD-primero) y 7 pacientes fueron tratados primero con el despliegue del stent recuperable y vasodilatadores intraarteriales justo a continuación (RS-primero). Se produjo vasodilatación en el 71,4% de los segmentos en el grupo de VD-primero y en el 82,1% de los segmentos en el grupo de RS-primero. No se detectó ningún vasoespasmo recurrente en el grupo de RS-primero; sin embargo, se detectó vasoespasmo recurrente en 3 (60%) pacientes del grupo de VD-primero.
En este artículo publicado recientemente5 se produjeron tres complicaciones del procedimiento, lo que suponía el 25% de los pacientes. Se observaron dos complicaciones tromboembólicas en los segmentos M2 y M3, ambas completamente resueltas con 1mg y 0,5mg de tirofibán, respectivamente. En un caso, la perforación fue causada por la punta de un microcable durante la navegación del microcatéter; la rotura del vaso se resolvió con la oclusión de la rama con bobinas sin consecuencias clínicas para el paciente. No se observaron secuelas clínicas permanentes ni mortalidad en esos 3 pacientes debido a complicaciones del procedimiento.
Nuestros resultados son comparables a los publicados anteriormente, con un alto índice de eficacia y un bajo índice de complicaciones clínicas. Sin embargo, nuestro estudio mostró un menor índice de complicaciones del procedimiento que el informe anterior. Nuestra hipótesis es que estos resultados podrían deberse parcialmente a la administración continua de un vasodilatador a través del catéter guía en la mayoría de los casos, y al despliegue del stent recuperable solo en los segmentos intracraneales proximales (ACI, ACM, ACA). Estos resultados también podrían estar relacionados con la experiencia de los neurointervencionistas con los stents recuperables, gracias a la trombectomía en el ictus isquémico agudo, lo que hace que este procedimiento sea cada vez más seguro.
Las principales limitaciones de este estudio son el pequeño tamaño de la muestra y el diseño retrospectivo, así como la variabilidad de los dispositivos y vasodilatadores utilizados, lo que limita la validación externa de nuestros resultados. Otra posible limitación es que no comparamos nuestra muestra con otros tipos de tratamiento, como la angioplastia con balón o el uso exclusivo de vasodilatadores intraarteriales. Los estudios futuros deberían tener por objetivo replicar estos resultados en una cohorte multicéntrica más amplia y comparar los dos principales métodos de angioplastia (stent recuperable y balón) dirigidos a la estenosis de vasos grandes, a fin de determinar el mejor perfil de seguridad y eficacia. Es importante tener en cuenta la diferencia de coste del stent recuperable en comparación con el balón de angioplastia, que en algunos países es tres veces mayor, lo que hace que sea un aspecto importante para ampliar su uso en el ámbito clínico.
La principal fortaleza es el diseño multicéntrico en cuatro hospitales de nivel terciario de gran volumen con resultados similares, obteniéndose una baja tasa de complicaciones del procedimiento con una eficacia suficientemente adecuada, al utilizarse como primer paso en el tratamiento endovascular del vasoespasmo secundario a HSAa. El carácter multicéntrico del estudio también incluye diferentes protocolos de tratamiento endovascular (p. ej., diferentes dispositivos, tamaños y tiempo de despliegue de estos), que permiten su evaluación para determinar el mayor efecto de la angioplastia con stent recuperable. En cuanto a las variables del tratamiento endovascular, existe una diferencia no significativa a favor de los dispositivos de más de 4mm y de la colocación durante más de 5 minutos, así como la administración de vasodilatadores a través del catéter guía. No hay datos disponibles en otros trabajos ya publicados, por lo que este es un tema importante para futuras investigaciones, con el objetivo de optimizar la angioplastia con stent recuperable.
Hasta la fecha, la angioplastia con balón y los vasodilatadores intraarteriales son las modalidades de tratamiento endovascular más utilizadas en el vasoespasmo resistente debido a HSAa. En la mayoría de los casos, esas modalidades se utilizan de forma combinada debido a que se supone que la angioplastia con balón es más útil en la estenosis proximal y los fármacos vasodilatadores, en la estenosis distal. De hecho, la discrepancia entre el resultado clínico y el tratamiento de la estenosis de vasos grandes sugiere que el tratamiento de la estenosis distal es igualmente importante para mejorar el resultado clínico6.
La angioplastia con balón es el tratamiento endovascular más eficaz disponible hasta la fecha. En una revisión reciente publicada por Hoh et al.7, hasta el 62% (328 de 530) de los pacientes tratados con angioplastia con balón mejoraron clínicamente. Tanto la mejora del calibre del vaso como la prevención de las lesiones isquémicas se han observado en varios estudios después de la angioplastia con balón8,9. Pero la angioplastia con balón no está exenta de complicaciones; Hoh et al.7 notificaron complicaciones importantes en el 5% de los pacientes, y de rotura de vasos en el 1,1% de los pacientes tratados.
En un artículo recientemente publicado3, el tratamiento endovascular agresivo y precoz en una cohorte demostró un mejor resultado clínico en comparación con una cohorte con una selección más restrictiva para el tratamiento endovascular en términos de isquemia cerebral retardada (20,8% frente a 29%, p=0,0001) y resultado desfavorable (44% frente a 50,6%, p=0,04), respectivamente. Una implicación clínica importante es que probablemente tengamos que tratar a más pacientes de manera temprana, para prevenir la isquemia cerebral retardada y los resultados desfavorables.
Debido a la naturaleza multifactorial de la patogenia de la isquemia cerebral tardía2,10,11 y a la falta de una sólida relación causal entre el vasoespasmo y el resultado funcional12,13, es necesario escalonar el tratamiento endovascular en el vasoespasmo de la HSAa desde el menos efectivo y con menos complicaciones hasta el más efectivo pero con la mayor tasa de complicaciones. Al mismo tiempo, un tratamiento endovascular en pacientes despiertos con vasoespasmo sintomático permite realizar una evaluación clínica del paciente durante el tratamiento, con el fin de establecer una correlación causa-efecto de los síntomas y determinar la eficacia del tratamiento.
Por estos motivos, proponemos un enfoque en dos pasos en que el tratamiento de primera línea sea una angioplastia con stent recuperable en pacientes despiertos. El fármaco vasodilatador se infunde a través del catéter guía durante el despliegue del stent recuperable en el vaso, a fin de potenciar el efecto de ambas estrategias terapéuticas, abordando la estenosis proximal y la distal al mismo tiempo. También recomendamos el uso de la técnica “push and fluff” durante el despliegue del stent recuperable para aumentar la fuerza radial del dispositivo contra la pared del vaso. Tras este abordaje de primera línea, si los síntomas clínicos y/o el vasoespasmo no mejoraban o se normalizaban, consideramos realizar el tratamiento de segunda línea con angioplastia con balón de los segmentos proximales (ACI y/o ACM) con anestesia general para mejorar la seguridad del procedimiento. Con este enfoque en dos pasos, escalonamos el tratamiento endovascular en el vasoespasmo debido a HSAa, permitiendo la evaluación clínica de los pacientes despiertos como primera línea de tratamiento y optando por la seguridad y la eficacia como objetivos principales.
En conclusión, la angioplastia con stent recuperable como tratamiento del vasoespasmo secundario a la HSAa es un procedimiento seguro y eficaz que mejora el TCC y la estenosis del vaso después del tratamiento. Se necesitan más datos para optimizar el rendimiento de la angioplastia con stent recuperable como tratamiento del vasoespasmo secundario a la HSAa.
Autoría- 1.
Responsable de la integridad del estudio: ALR, AV, OC, MW y AT.
- 2.
Concepción del estudio: ALR, AV, CP, OC, MW, LA, SR y AT.
- 3.
Diseño del estudio: ALR, OC, MW y AT.
- 4.
Obtención de los datos: AV, CP, OC y MW.
- 5.
Análisis e interpretación de los datos: ALR, AV, CP, OC, MW, LA, SR y AT.
- 6.
Tratamiento estadístico: ALR, AV, OC y MW.
- 7.
Búsqueda bibliográfica: ALR, AV, CP, OC, MW, LA, SR y AT.
- 8.
Redacción del trabajo: ALR, AV, CP, OC y MW.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: ALR, AV, CP, OC, MW, LA, SR y AT.
- 10.
Aprobación de la versión final: ALR, AV, CP, OC, MW, LA, SR y AT.
Los autores declaran no tener ningún conflicto de intereses.