Para llevar a cabo estudios de optimización de dosis, el fantoma de imagenología debe ser adecuado para evaluar la calidad de la imagen. El coste de los fantomas de gama alta suele ser prohibitivo, por lo que es necesario hallar un método de construcción asequible que emplee sustitutos tisulares que sean razonablemente fáciles de obtener.
Materiales y métodosSe realizaron cálculos teóricos de las características radiológicas de cada uno de los pulmones, el hueso cortical y los tejidos blandos con el fin de elegir el sustituto adecuado; para ello, se eligieron el corcho, el cloruro de polivinilo (PVC) y el agua, respectivamente. La validación consistió, en primer lugar, en la medición de las unidades Hounsfield (UH) de tomografía computarizada (TC) de los tejidos de un paciente real y su posterior comparación con las anatomías correspondientes en el fantoma construido. En segundo lugar, se obtuvieron los valores de relación señal/ruido (S/R) y de relación contraste/ruido (C/R) para evaluar la calidad de las imágenes generadas a partir del fantoma construido y comparar sus tendencias con un fantoma válido utilizando diferentes parámetros de exposición (valores pico de kilovoltaje [kVp] y miliamperios por segundo [mAs]).
ResultadosPartiendo de los cálculos teóricos, las diferencias porcentuales exhibieron una precisión elevada en los sustitutos tisulares al simular los tejidos de un paciente real; con PVC fue de ≥ 5,78%, con corcho ≥ 4,46% y con agua ≥ 5%. La diferencia porcentual (UH de TC) entre el pulmón y el hueso cortical y sus sustitutos tisulares equivalentes fue de 10,44% y de 0,53 a 3,17%, respectivamente. Se encontraron fuertes correlaciones positivas para la S/R al variar tanto los valores de kVp (0,79) como de mAs (0,65). Por el contrario, se halló que la fuerza de correlación de los valores de la C/R era moderada al cambiar los valores de kVp (0,58) y mAs (0,53).
ConclusionesSe ha constatado mediante las UH de TC que los materiales de nuestro fantoma asequible son una réplica de las características radiológicas de un paciente pediátrico de un año de edad, mientras que las correlaciones de la S/R y la C/R confirmaron su aplicabilidad en estudios mediante imágenes y de optimización.
In order to perform chest dose optimisation studies, the imaging phantom should be adequate for image quality evaluation. Since high-end phantoms are cost prohibitive, there is a need for a low-cost construction method with fairly available tissue substitutes.
Materials and MethodsTheoretical calculations of radiological characteristics were performed for each of lung, cortical bone and soft tissues in order to choose appropriate substitute, then, cork, P.V.C. (Polyvinyl Chloride) and water were chosen, respectively. Validation included, firstly, measuring CT Hounsfield Units (HU) of a real patient's tissues then compared against their corresponding anatomies in the constructed phantom. Secondly, Signal-to-noise ratio (SNR) and contrast-to-noise ratio (CNR) values were acquired in this study to evaluate the quality of images generated from the constructed phantom, then, compare their trends with a valid phantom under different exposure parameters (kVp and mAs).
ResultsFrom theoretical calculations, the percentage differences showed high accuracy of tissue substitutes when simulating real patient tissues; P.V.C. was ≥ 5.78%, cork was ≥ 4.46% and water ≥ 5%. The percentage difference (CT HU) between lung and cortical bone and their equivalent tissue substitutes were 10.44% and 0.53%-3.17%, respectively. Strong positive correlations were found for SNR when changing both kVp (0.79) and mAs (0.65). While the correlation strength of CNR values were found to be moderate when changing both kVp (0.58) and mAs (0.53).
ConclusionsOur low-cost phantom approved through CT HU that their materials replicate the radiological characteristics of real one-year-old child while SNR and SNR correlations confirmed its applicability in imaging and optimisation studies.
Se considera que los fantomas de imagenología antropomórficos son la mejor opción para llevar a cabo los estudios de radiología diagnóstica, ya que ofrecen una buena aproximación de la anatomía del paciente y presentan una excelente fidelidad radiológica1. Existen fantomas pediátricos de dosimetría (fantomas de dosimetría ATOM) que simulan tres edades pediátricas: neonatal, uno y cinco años2. Sin embargo, presentan numerosas limitaciones, puesto que han sido diseñados exclusivamente para fines de dosimetría y quizá no sean aptos para realizar evaluaciones de calidad de imagen, ya que no ofrecen un grado de realismo suficiente a la hora de representar la anatomía humana, sobre todo en cuanto a la región torácica3. Además, dichos fantomas de dosimetría se fabrican en forma de conjunto de secciones axiales que generan sombras en las imágenes radiográficas debido a los espacios existentes entre los cortes del fantoma. Por otra parte, los fantomas de dosimetría ATOM se construyen de un modo que no permite al investigador introducir ninguna lesión en el interior del pulmón. Esta fue una de las razones que nos llevaron a excluir este tipo de fantoma del presente trabajo.
Existe una escasez de fantomas pediátricos antropomórficos comerciales y, que los autores sepan, solo se dispone de dos fantomas que simulan el tórax pediátrico. Uno de ellos es el Lungman de Kyoto Kagaku4 (LUNGBOY PH-1C Multipurpose Pediatric Chest Phantom; Kyoto Kagaku Company Ltd, Japón), diseñado para simular un paciente pediátrico de cinco años de edad; el otro es el Gammex RMI© 6105. Sin embargo, el primer fantoma es costoso y no puede adquirirse localmente. El segundo ha sido diseñado como fantoma torácico neonatal. La edad pediátrica se divide en grupos de cero, uno, cinco, 10 y 15 años de edad, respectivamente. Para realizar una optimización de dosis, debe disponerse de fantomas de radiología de cada uno de estos grupos de edad2. Por esta razón, existen escasos fantomas de imagenología radiológica que abarquen todo el rango de edades pediátricas, sin mencionar su coste. Otro motivo es que se ha previsto introducir lesiones en el interior del pulmón que rigen el análisis de la visibilidad de las lesiones en la radiografía pediátrica de tórax. Los fantomas de dosimetría ATOM, por su parte, presentan limitaciones a la hora de evaluar la calidad de imagen debido a los cortes axiales que tienen a lo largo del tronco y que aparecen como líneas negras, lo cual altera la apariencia de la anatomía torácica y afecta también a las lesiones introducidas en el fantoma6. Además, estos fantomas no permiten introducir una lesión en los pulmones a fin de llevar a cabo un análisis de visibilidad de las lesiones.
El proceso de construir un fantoma de imagenología radiológica exige una valoración minuciosa de varios criterios importantes: en primer lugar, la selección de los materiales (sustitutos radiológicos) debe tener una respuesta próxima a la exposición a la radiación, al rango de energía de generación de imágenes, semejante a la de un paciente real; en segundo lugar, la capacidad de dar forma a los sustitutos tisulares para imitar las partes internas y externas del cuerpo humano2,7; por último, la cobertura de los tamaños pediátricos es importante en la construcción del fantoma, ya que la mayoría de los fantomas comerciales representan pacientes neonatos o adultos, por lo que existe una necesidad acuciante de fantomas que cubran las edades que van del primer año a los 158.
En numerosas publicaciones se ha intentado utilizar diferentes tipos de fantomas para simular el tórax pediátrico. Sin embargo, su eficacia es escasa porque no representan al paciente real desde el punto de vista anatómico ni radiológico. Esto significa que en las evaluaciones de calidad de imagen no se tienen en cuenta la forma anatómica ni el ruido9-13.
La simulación de la anatomía torácica exige que los sustitutos equivalentes a los tejidos tengan las mismas características radiológicas que la anatomía humana, además de estar disponibles y ser asequibles. En algunos estudios se han utilizado materiales económicos para construir fantomas de imagenología de la pelvis, como el yeso blanco para simular los huesos y el polimetilmetacrilato (PMMA) para los tejidos blandos8. Sin embargo, este método plantea dificultades para introducir los pulmones y las lesiones en el interior del PMMA, sin mencionar los cortes propios de este método de construcción. En otro estudio se usó gel de agar para simular los tejidos blandos con el propósito de construir un fantoma de imagenología neonatal antropomórfico14. Lamentablemente, el gel de agar puede dar resultados imprecisos debido a que su composición elemental es incierta, además de volverse inestable con el paso de periodos de tiempo relativamente largos15. Otros métodos de construcción recurren a materiales basados en resinas16-19. Pese a su elevada precisión, el proceso de construcción sigue siendo complejo y el coste de los materiales es considerable.
Por todo lo anterior, cabe afirmar que los fantomas de imagenología pediátricos correspondientes al rango de edades de los cero a los 15 años, y en especial aquellos que representan la región torácica, son costosos y escasos, sobre todo en lo referido al estudio de la detección de lesiones en los pulmones. El propósito de este estudio es diseñar y validar un fantoma torácico pediátrico destinado a estudios de optimización de dosis y detección de lesiones.
Materiales y métodosMétodo de diseño del fantomaPara realizar este estudio se ha construido un fantoma torácico pediátrico que facilite la evaluación de los factores que afectan a la optimización de dosis, la detección de lesiones y la calidad de imagen. Un requisito imprescindible del fantoma es que debe ofrecer un grado aceptable de simulación de la región torácica de un paciente pediátrico. La primera fase de la construcción del fantoma (equivalencia anatómica) consistió en determinar la morfología y las dimensiones físicas del fantoma. Durante la segunda fase (equivalencia radiológica) se buscaron sustitutos equivalentes radiológicos de los tejidos correspondientes a huesos, pulmón y tejidos blandos que después se modelaron en función de la forma de los órganos que se determinó en la primera fase.
Equivalencia anatómicaSe ha aplicado una metodología propia para diseñar y construir un fantoma destinado a estudios de optimización que tuviera una forma y dimensiones anatómicas próximas a las de un paciente real. El método propuesto también permitirá construir el conjunto de fantomas necesario para representar diferentes edades y tamaños.
En la primera fase del proceso de construcción se determinaron la morfología y las dimensiones físicas del fantoma. Ello incluyó la altura, anchura y profundidad total, así como el tamaño de las estructuras anatómicas internas. Con este fin se tomaron las medidas de un fantoma de dosimetría ATOM de tamaño estándar que representaba a un paciente de un año de edad empleando los datos de una exploración mediante tomografía computarizada (TC) (120 valores pico de kilovoltaje [kVp] y un grosor de corte reconstruido de 1 mm). A continuación, los datos de TC se usaron para obtener las medidas dimensionales con RadiAnt DICOM Viewer. El motivo que llevó a elegir un fantoma de dosimetría ATOM para medir la morfología y las dimensiones físicas fue evitar la variabilidad en tamaños presente en los datos de las TC clínicas de la misma edad, así como el uso de datos de una TC clínica de un paciente que podría no tener las medidas habituales de esa edad concreta. Por regla general, un fantoma de dosimetría ATOM representa las dimensiones medias correspondientes a su grupo de edad.
Las medidas tomadas correspondieron al pulmón, la columna vertebral, las costillas, el esternón y la clavícula. Todas ellas se indican en las figuras 1 a 6 del apéndice. En lo referente al pulmón, la profundidad y la anchura se determinaron a partir de reconstrucciones sagitales y coronales, tal como se muestra en las figuras 1 y 2 del apéndice, respectivamente. Sus valores correspondientes fueron iguales a 9,2 cm y 5,0 cm, respectivamente. La forma tridimensional global del pulmón se estimó mediante el tratamiento de imágenes 3 D, como puede verse en la figura 3 del apéndice. El tamaño y la forma del pulmón son diferentes en las superficies anterior y posterior; también se tuvieron en cuenta las diferencias entre el pulmón derecho y el izquierdo.
En lo referente a la columna vertebral, se tuvieron en cuenta tanto la médula espinal como las vértebras. La profundidad de la columna, la médula espinal y las vértebras, junto con la longitud de estas últimas, se calcularon a partir de reconstrucciones sagitales. Se obtuvieron valores de 28 mm, 10 mm, 10 mm y 2 mm, respectivamente (tal como se muestra en la figura 4 a) del apéndice). La anchura de la columna se determinó a partir de las reconstrucciones coronales (tal como se muestra en la figura 4 b) del apéndice). La construcción se simplificó aún más calculando los valores de anchura medios en todos los segmentos visibles de la columna (21 mm).
El esternón se formó a partir de seis segmentos completamente diferentes en profundidad y tamaño. La profundidad del esternón se midió mediante reconstrucciones sagitales. La anchura se midió a través de una representación tridimensional del volumen óseo, como se aprecia en la figura 4 a) y la figura 5 del apéndice, respectivamente.
El grosor de las costillas se determinó utilizando cortes axiales de TC. En general, es de unos 4 mm, como se muestra en la figura 6 a) del apéndice. Su anchura se midió utilizando nuevamente una representación tridimensional del volumen óseo. Por norma general, es de unos 8 mm en todas, como se observa en la figura 5 del apéndice. Por último, las dimensiones de la clavícula se obtuvieron empleando los cortes axiales que se muestran en la figura 6 b) del apéndice.
El fantoma se diseñó intencionadamente de un modo que permitiera extraer sus cuatro componentes (pulmón, columna, caja torácica y cartílago). El pulmón se construyó de manera que fuera posible introducir las lesiones permitidas. Además, se pintó el pulmón con un aerosol impermeable para impedir que absorbiera el agua (que es un sustituto equivalente del tejido blando) del entorno. En la tabla 1 se indican los valores de medición totales de la estructura anatómica interna y su sustituto equivalente.
Dimensiones y sustitutos equivalentes de las estructuras anatómicas internas del fantoma
| Tejido | Dimensiones | Sustituto | |
|---|---|---|---|
| Anchura (mm) | Profundidad (mm) | ||
| Pulmón | 5 | 9,2 | Corcho compuesto |
| Costillas | 8 | 4 | PVC |
| Columna vertebral | 21 | 28 | PVC |
| Médula espinal | 1 | 10 | Agua |
| Vértebras | 21 | 10 | Agua |
| Clavícula | Variable | 6 | PVC |
| Cartílago | Variable | 8 | PMMA |
| Tejido blando | Variable | Variable | Agua |
PMMA: polimetilmetacrilato; PVC: cloruro de polivinilo.
La figura 1 a) y b) muestra el diseño del fantoma y su radiografía resultante, respectivamente. Representa el primer prototipo de fantoma que simula la región torácica de un paciente de un año de edad. Aunque se construyó para que tuviera en cuenta los aspectos anatómicos y radiológicos, es posible observar ciertas limitaciones en el prototipo. En primer lugar, la geometría de la clavícula no refleja fielmente la forma de la clavícula del paciente real; en segundo lugar, los bordes del pulmón son muy agudos, en lugar de curvos, como serían los de un pulmón real; en tercer lugar, el manejo del fantoma es difícil. Todas sus partes son desmontables y, sobre todo en el caso de los fantomas de cinco y 10 años de edad, el gran tamaño del pulmón y de las otras partes puede complicar su manipulación.
Equivalencia radiológicaEn la segunda fase, los materiales de sustitución tisular utilizados en este estudio se eligieron para satisfacer cuatro criterios: primero, que ofrecieran coeficientes de atenuación similares a los de los tejidos de un paciente real; segundo, que ofrecieran opciones más sencillas y reproducibles para la construcción de fantomas; tercero, que los materiales pudieran adquirirse comercialmente y fueran relativamente económicos; y cuarto, que pudieran modelarse fácilmente para adoptar la forma de los órganos del tórax.
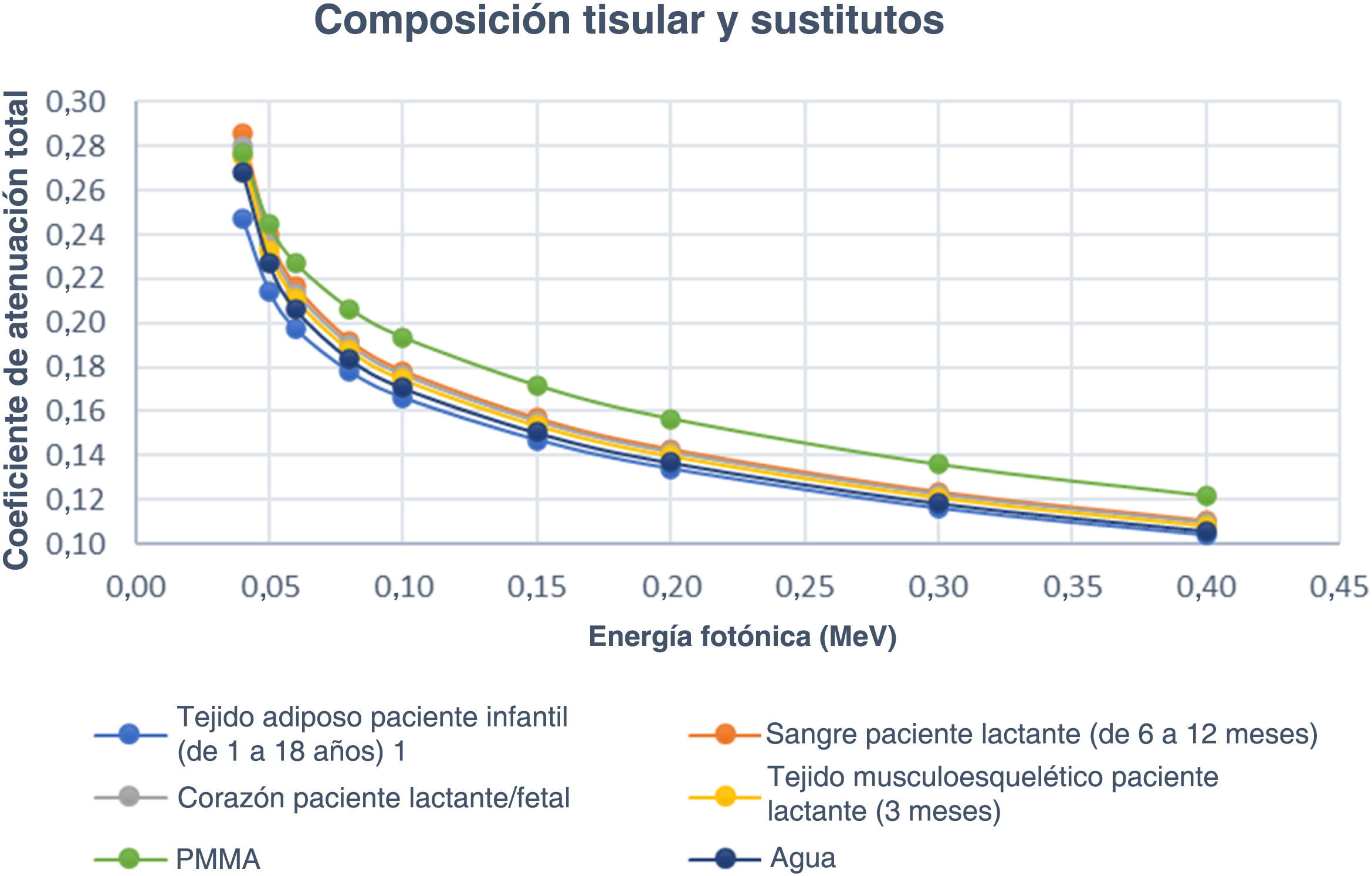
En el presente estudio se ha calculado el coeficiente de atenuación total de cada uno de los tejidos de un paciente neonato (incluidos el tejido adiposo, la sangre, el corazón y el tejido musculoesquelético), el hueso cortical y el pulmón, junto con sus sustitutos tisulares, con el software XCOM20. Puede accederse a este programa por medio de la base de datos web del National Institute of Standards and Technology (NIST). Con él es posible calcular las secciones transversales de fotones para determinar la absorción fotoeléctrica, la dispersión y la producción de pares, además del coeficiente de atenuación total. Dichos cálculos son válidos para cualquier elemento, mezcla o compuesto con un número atómico Z ≤ 100 y cubre el rango de energía que va de 1 keV a 100 GeV20. Asimismo, la composición elemental de los materiales de sustitución tisular que se usa en este software se obtuvo de White et al.23 y, por comparación, se han comunicado estos datos para el cuerpo humano22. Se han hallado semejanzas en la composición orgánica de los tejidos blandos, el hueso cortical y los pulmones entre la edad fetal, neonatal, lactante y pediátrica23. Por consiguiente, se espera que los coeficientes de atenuación totales de cada tipo de tejidos de estas edades sean aproximados.
En este estudio se han utilizado tres tipos distintos de sustitutos tisulares equivalentes (cloruro de polivinilo [PVC], corcho y agua) con el fin de simular el hueso, el pulmón y los tejidos blandos, respectivamente. Se trata de materiales fáciles de obtener y asequibles, pero que, sobre todo, ofrecen propiedades excelentes a la hora de simular las características radiológicas de los tejidos humanos. El primero de ellos es el PVC, considerado un sustituto tisular capaz de simular el hueso humano21. El corcho, por su parte, se considera uno de los mejores sustitutos del pulmón humano debido a que sus propiedades físicas se asemejan a las de este órgano24. El informe n.° 44 de la International Commission on Radiation Units & Measurements (ICRU) coincide igualmente en que podría ser un sustituto tisular de los pulmones humanos. Por último, en diversas ocasiones se ha notificado que el agua es un buen sustituto de los tejidos blandos21.
Método de validación del fantomaJunto con el cálculo teórico del coeficiente de atenuación lineal (que se considera una validación teórica) descrito ya en el apartado «Equivalencia radiológica», en el estudio se han empleado dos métodos diferentes de validación del fantoma construido: el primero consiste en la medición de las unidades de Hounsfield (UH) mediante una exploración de TC de las diferentes regiones de interés (RDI); el segundo, en la comparación de la respuesta (correlación) del fantoma con un fantoma de referencia (Gammex RMI© 610) empleando las medidas físicas de la relación señal/ruido (S/R) y la relación contraste/ruido (C/R) de una radiografía digital al variar diferentes parámetros radiográficos (kVp y miliamperios por segundo [mAs]).
Validación mediante UH de TCCada material presenta unas características de atenuación radiográficas diferentes, que se representan con el número de UH de TC y varían en función de la densidad del tejido del paciente o su sustituto equivalente. Se considera que la medición de los valores de UH de las exploraciones de TC es un método fiable para determinar y comparar la composición y densidad de los tejidos con la de sus materiales equivalentes radiológicos25,26. Por consiguiente, se tuvo en cuenta dicha medición para llevar a cabo la validación experimental del fantoma. Para ello, se realizó una medición del pulmón, la columna vertebral y las costillas de un paciente real y se comparó con las estructuras anatómicas correspondientes del fantoma construido.
Validación mediante el valor del píxelEl valor de cada píxel de una imagen radiográfica digital depende de la magnitud de la atenuación de los rayos X cuando atraviesan la parte correspondiente del organismo27. La información que contiene una radiografía digital viene determinada por el número de píxeles que contiene28. La S/R es un método que se utiliza habitualmente para estimar la información de visibilidad global que aparece en la radiografía29. Ofrece una medida física de la calidad de imagen y se utiliza frecuentemente en estudios de optimización30. Se han utilizado las medidas físicas de calidad de imagen (S/R y C/R) para comparar tendencias en la calidad de imagen y validar las imágenes del fantoma8. Por consiguiente, se midieron los valores de relación S/R y C/R para evaluar la calidad de las imágenes generadas a partir del fantoma construido y, a continuación, comparar sus tendencias con un fantoma válido (Gammex RMI© 610) utilizando diferentes parámetros de exposición (kVp y mAs).
ResultadosCaracterísticas radiológicas de los sustitutos tisulares de hueso, pulmón y tejidos blandosLos valores del coeficiente de atenuación lineal de todos los tejidos blandos y sus sustitutos se enumeran en la tabla 2. Como puede verse en la tabla 3, la diferencia porcentual entre el coeficiente de atenuación lineal del hueso cortical de un paciente pediátrico de un año de edad y su sustituto tisular (PVC) varía entre 0,13 y 18,6%. Dada la energía máxima utilizada durante la obtención de imágenes torácicas de un paciente pediátrico de un año (≥ 80 kVp), la diferencia porcentual efectiva sería de 5,78% y posteriormente se reduciría a medida que aumenta la energía (tabla 3). En el caso del sustituto tisular pulmonar (el corcho), la diferencia porcentual osciló entre 0,13 y 4,46% a lo largo del rango de 50 keV a 150 keV (excepto por 8,78% a 40 keV, que escapa al rango de energía utilizado habitualmente en este proceso), como se muestra en la tabla 4. Por último, se ha demostrado que el agua es una elección adecuada para esta aplicación, ya que su coeficiente de atenuación lineal es muy similar al de los tejidos blandos de un paciente neonato (tejido adiposo, sangre, corazón y tejido musculoesquelético), como se refleja en la tabla 5, mientras que todas las diferencias porcentuales fueron ≥ 5% dentro de un rango de energía de 60 a 150 con todos los tipos de tejido blando. Salvo con los valores de energía más bajos, las diferencias porcentuales superaron el 5% en el caso del tejido adiposo y la sangre. En pocas palabras: estas diferencias porcentuales reflejaron una elevada precisión en la simulación de tejidos de pacientes reales en términos de sus características radiológicas. Por tanto, es posible utilizar agua en fantomas pediátricos para simular los tejidos blandos (tejido adiposo, sangre, corazón y tejido musculoesquelético), corcho para simular los pulmones y PVC para simular el hueso cortical.
Coeficiente de atenuación lineal (cm-1) de diferentes tejidos blandos en la región torácica y sus sustitutos equivalentes a lo largo del rango de energía de rayos X con fines diagnósticos (40-150 KeV)
| Energía (KeV) | Tejido adiposo del paciente | Sangre (lactante) | Corazón (neonatal) | Musculoesquelético (lactante) | Mezcla de gel de agar (4% agar y 96% agua) | PMMA |
|---|---|---|---|---|---|---|
| 40 | 0,2471 | 0,2855 | 0,2801 | 0,2754 | 0,2672 | 0,2773 |
| 50 | 0,2142 | 0,2396 | 0,2360 | 0,2325 | 0,2262 | 0,2447 |
| 60 | 0,1970 | 0,2163 | 0,2137 | 0,2107 | 0,2053 | 0,2270 |
| 80 | 0,1779 | 0,1922 | 0,1902 | 0,1878 | 0,1833 | 0,2066 |
| 100 | 0,1661 | 0,1783 | 0,1767 | 0,1745 | 0,1704 | 0,1936 |
| 150 | 0,1471 | 0,1570 | 0,1557 | 0,1538 | 0,1503 | 0,1718 |
PMMA: polimetilmetacrilato.
Diferencia porcentual absoluta entre el coeficiente de atenuación lineal del hueso cortical de un paciente pediátrico de un año y el PVC
| Hueso cortical (paciente de 1 año) | PVC | ||
|---|---|---|---|
| Energía de rayos X (KeV) | Coeficiente de atenuación lineal (cm-1) | Coeficiente de atenuación lineal (cm-1) | Diferencia porcentual absoluta |
| 40 | 0,6049 | 0,7297 | 18,70% |
| 50 | 0,394 | 0,4557 | 14,52% |
| 60 | 0,2981 | 0,3323 | 10,85% |
| 80 | 0,2168 | 0,2297 | 5,78% |
| 100 | 0,1831 | 0,1886 | 2,96% |
| 150 | 0,1483 | 0,1485 | 0,13% |
PVC: cloruro de polivinilo.
Diferencia porcentual absoluta entre el coeficiente de atenuación lineal del pulmón de un paciente pediátrico neonato y el corcho
| Pulmón (neonato) | Corcho | Diferencia porcentual | |
|---|---|---|---|
| Energía (KeV) | Coeficiente de atenuación lineal (cm-1) | Coeficiente de atenuación lineal (cm-1) | Diferencia porcentual absoluta |
| 40 | 0,0698 | 0,0639 | 8,78% |
| 50 | 0,0589 | 0,0563 | 4,46% |
| 60 | 0,0534 | 0,0522 | 2,20% |
| 80 | 0,0475 | 0,0475 | 0,13% |
| 100 | 0,0442 | 0,0445 | 0,67% |
| 150 | 0,0389 | 0,0395 | 1,41% |
Diferencia porcentual absoluta entre el coeficiente de atenuación lineal de los tejidos blandos y el agua a lo largo del rango de energía de rayos X con fines de diagnóstico (40-150 KeV)
| Energía (KeV) | Tejido adiposo vs. agua | Sangre vs. agua | Corazón vs. agua | Tejido musculoesquelético vs. agua |
|---|---|---|---|---|
| 40 | 8,24% | 6,21% | 4,29% | 2,62% |
| 50 | 5,75% | 5,45% | 3,92% | 2,43% |
| 60 | 4,43% | 4,93% | 3,73% | 2,32% |
| 80 | 3,22% | 4,50% | 3,49% | 2,19% |
| 100 | 2,73% | 4,35% | 3,45% | 2,19% |
| 150 | 2,29% | 4,21% | 3,39% | 2,16% |
Aparte de la precisión de la simulación en cuanto a las características radiológicas, la comparación de la interacción de los rayos X en el hueso cortical de un paciente de un año de edad con el PVC ofreció un comportamiento coherente al incrementar la energía de los rayos X (fig. 2). En comparación con el aluminio (Al), el PVC presentó unos valores de coeficiente de atenuación lineal más próximos a los del hueso cortical de un paciente de un año (fig. 2). Se observaron las mismas pautas de coherencia en el corcho en comparación con el tejido pulmonar de un paciente neonato (fig. 3) y en el agua en comparación con diferentes tejidos blandos del mismo paciente (tejido adiposo, sangre, corazón y tejido musculoesquelético [fig. 4]) al aumentar la energía de los rayos X. Asimismo, la similitud en las características de radiación de los pulmones humanos reales es igualmente notable.
En este estudio se emplearon dos métodos diferentes de validación del fantoma recién construido: el primero consistió en la medición de las UH mediante una exploración de TC de las diferentes RDI; el segundo, en la comparación de la respuesta (correlación) del fantoma con un fantoma de referencia (Gammex RMI© 610) empleando las medidas físicas (S/R y C/R) de una radiografía digital al variar diferentes parámetros radiográficos (kVp y mAs).
Validación mediante UH de TCEn lo referido a UH, se midieron los valores de tres RDI diferentes (columna vertebral, costillas y pulmón) en el fantoma torácico recién construido y el paciente pediátrico de un año. A continuación, se compararon los resultados entre sí, como se refleja en la tabla 6. Tanto el fantoma de imagenología como el paciente fueron sometidos a una TC helicoidal utilizando 80 kVp y un grosor de corte reconstruido de 0,6 mm. Se midió el número de UH de TC; el corcho (-454 UH) y el pulmón del paciente (-504 UH) obtuvieron valores próximos (diferencia porcentual de 10,44%). Este resultado también demuestra que el corcho comercial utilizado en este fantoma coincide con los cálculos teóricos empleados para hallar sustitutos tisulares equivalentes. La diferencia porcentual en los valores de UH entre el PVC y el hueso cortical del paciente de un año de edad fue de 3,17% en la columna vertebral y de 0,53% en las costillas. No fue necesario medir el agua (tejidos blandos), ya que las UH de TC se calibran utilizando agua, por lo que los cálculos de la atenuación lineal (μ) deberían ser correctos, puesto que no se espera que el uso de agua genere ningún tipo de impureza.
Comparación de los valores de UH de diferentes RDI del fantoma y el paciente
| Tejido | Unidad Hounsfield (UH) | Diferencia porcentual absoluta | |||
|---|---|---|---|---|---|
| Nuevo fantoma de imagenología | DE | Paciente | DE | ||
| Pulmón | -454 | 247 | -504 | 129 | 10,44% |
| Columna vertebral | 544 | 304 | 527 | 33 | 3,17% |
| Costillas | 940 | 286 | 945 | 132 | 0,53% |
DE: desviación estándar; RDI: regiones de interés.
Los resultados de los valores de UH de TC enumerados en la tabla 6 demuestran que existe una excelente concordancia entre las UH de las diferentes RDI de un paciente real y las del fantoma.
Validación mediante el valor del píxelSe ha usado el valor del coeficiente de determinación (R2) para examinar el grado de correlación entre las tendencias de los valores de S/R y C/R del fantoma construido en comparación con los del fantoma Gammex RMI© 610 y sus valores. En lo que se refiere a los valores de S/R y C/R al cambiar el valor de kVp, la tabla 7 refleja que, cuando se cambia el valor de kVp, la correlación media de S/R y C/R es de 0,79 y 0,58, respectivamente, mientras que al cambiar los valores de mAs (tabla 8), la correlación media de S/R y C/R es de 0,65 y 0,53. Se halló que la fuerza de dichas correlaciones era claramente positiva para los valores de S/R cuando se variaban tanto el valor de kVp como el de mAs (tablas 7 y 8). Por su parte, la fuerza de la correlación de los valores de C/R era moderada cuando se variaban ambos valores kVp y mAs (tablas 7 y 8).
Valores de correlación (R2) entre la S/R y la C/R del fantoma comparados con los valores del fantoma Gammex RMI© 610 en diferentes RDI al cambiar los valores de kVp (de 50 a 110 en incrementos de 5)
| Valores de mAs | Valores R2 de correlación de S/R | Valores R2 de correlación de C/R | ||||||
|---|---|---|---|---|---|---|---|---|
| N.° RDI | N.° RDI | |||||||
| 1 | 2 | 3 | 4 | 1 | 2 | 3 | 4 | |
| 1 | 0,81 | 0,80 | 0,83 | 0,82 | 0,65 | 0,81 | 0,79 | 0,47 |
| 2 | 0,76 | 0,79 | 0,78 | 0,77 | 0,56 | 0,76 | 0,75 | 0,64 |
| 3,2 | 0,73 | 0,80 | 0,79 | 0,77 | 0,35 | 0,74 | 0,69 | 0,40 |
| 4 | 0,61 | 0,76 | 0,72 | 0,66 | 0,00 | 0,56 | 0,72 | 0,19 |
| 5 | 0,88 | 0,94 | 0,89 | 0,89 | 0,74 | 0,87 | 0,88 | 0,01 |
| Media | 0,79 | 0,58 | ||||||
C/R: contraste/ruido; kVp: valores pico de kilovoltaje; mAs: miliamperios por segundo; RDI: regiones de interés, S/R: señal/ruido.
Valores de correlación (R2) entre la S/R y la C/R del fantoma comparados con los valores del fantoma Gammex RMI© 610 en diferentes RDI al cambiar los valores de mAs (de 1 a 5 en incrementos de 1)
| Valores de kVp | Valores R2 de correlación de S/R | Valores R2 de correlación de C/R | ||||||
|---|---|---|---|---|---|---|---|---|
| N.° RDI | N.° RDI | |||||||
| 1 | 2 | 3 | 4 | 1 | 2 | 3 | 4 | |
| 50 | 0,63 | 0,80 | 0,63 | 0,64 | 0,25 | 0,52 | 0,67 | 0,29 |
| 70 | 0,57 | 0,57 | 0,57 | 0,59 | 0,53 | 0,57 | 0,58 | 0,64 |
| 90 | 0,69 | 0,70 | 0,69 | 0,69 | 0,66 | 0,75 | 0,77 | 0,10 |
| Media | 0,65 | 0,53 | ||||||
C/R: contraste/ruido; kVp: valores pico de kilovoltaje; mAs: miliamperios por segundo; RDI: regiones de interés, S/R: señal/ruido.
En cuanto a los resultados de las características radiológicas tisulares (hueso, pulmón y tejidos blandos), parece existir una concordancia considerable entre el hueso cortical de un paciente de un año de edad y su sustituto tisular (PVC) (tabla 3). Esta concordancia (diferencia porcentual) refleja la capacidad de simulación de este material como sustituto equivalente radiológico teórico. Asimismo, la concordancia entre el pulmón neonatal y el corcho (tabla 4) confirmó la idoneidad del corcho como sustituto radiológico de dicho órgano en neonatos. Por último, la concordancia porcentual en la simulación radiológica entre el agua y todos los tejidos blandos (tabla 5) demuestra que el agua puede ser un sustituto fiable de los tejidos blandos en el fantoma de imagenología pese a que este presente menor solidez debido al uso de este elemento. No obstante, es un problema que puede controlarse empleando un recipiente sólido hecho de PMMA, que es otro sustituto de los tejidos blandos y, por tanto, no afectaría a la imagen radiográfica del fantoma.
Método de validación del fantomaValidación mediante UH de TCLos valores de UH de la TC (en la tabla 6) indican una elevada concordancia entre los materiales del fantoma construido y los tejidos de un paciente real. El grado de concordancia de estos valores guarda relación con el coeficiente de atenuación de los rayos X, y significa que los materiales utilizados en el fantoma ofrecen una validez experimental elevada31. Los valores de las diferencias porcentuales de la tabla 6 entre la columna vertebral y las costillas del paciente y sus sustitutos tisulares (de PVC) registrados fueron > 5%. Por consiguiente, queda demostrado que el PVC, en el marco del sistema de clasificación tisular21,32, es un sustituto de clase A incluido en un rango de error de 5%21,32,33. Entre tanto, la diferencia porcentual al comparar el pulmón neonatal y el corcho fue de 10,44%, por lo que se considera un sustituto de clase B32. Dicha precisión puede justificarse como consecuencia de la naturaleza de la medición del pulmón, que no dispone de un bloque de tejidos medible, ya que está formado por tejido con espacios de aire, por lo que la medición de UH registra una mayor variación.
Validación mediante el valor del píxelSe halló una elevada correlación entre los dos fantomas con respecto a las medidas físicas de calidad de imagen (tablas 7 y 8), donde se observaron correlaciones moderadas y fuertes teniendo en cuenta la diferencia de tamaño entre el fantoma de cero años de edad (Gammex RMI© 610) y el fantoma de un año de edad (el fantoma construido). Dado que la S/R es una medida fiable de la calidad física de imagen y se utiliza frecuentemente en estudios de optimización30, dicha fuerza de correlación puede ser una prueba de la validez del fantoma, así como del elevado grado de simulación estructural y material que este ofrece debido a la semejanza en la respuesta cuando se modifican los factores de exposición (kVp y mAs). Así pues, resulta viable producir imágenes radiográficas posteriores representativas de cada edad empleando el fantoma construido.
ConclusiónSe aplicaron diversos métodos de validación para evaluar la capacidad del fantoma construido de generar radiografías fiables en estudios de optimización. El estudio de las interacciones radiológicas de los diferentes sustitutos tisulares obtuvo diferencias porcentuales relativamente bajas, lo que llevó a la conclusión de que los materiales más adecuados serían el PVC, el corcho y el agua como sustitutos del hueso cortical, el pulmón y los tejidos blandos, respectivamente. En cuanto al método de validación mediante TC, el resultado de las diferencias porcentuales mostró una correlación elevada, lo cual significa que los materiales empleados para la construcción del fantoma replicarían las características radiológicas del tórax de un paciente de un año de edad. Por otro lado, la validación mediante el valor del píxel demostró que existía una correlación elevada y moderada entre la tendencia en la calidad física de la imagen de un fantoma válido comercial y las imágenes obtenidas con nuestro fantoma al aplicar diferentes factores de exposición. Los resultados de los experimentos prueban que el fantoma torácico de un paciente de un año de edad es apto para su uso en estudios de optimización y radiológicos en general. En términos de disponibilidad, los materiales radiológicos equivalentes que se usaron en el fantoma torácico son fáciles de adquirir con un coste relativamente asequible, lo que simplifica en gran medida el proceso de fabricación. Además, existen abundantes datos sobre TC en humanos y los conocimientos necesarios para su uso son sencillos. A modo de resumen de las conclusiones, cabe afirmar que el fantoma es válido para realizar estudios de optimización y puede construirse de un modo bastante simple a partir de materiales asequibles y fáciles de adquirir. Se espera que estos materiales y el método de construcción sean de utilidad en todo el mundo en aquellos lugares donde se carece de medios económicos y no es posible disponer de fantomas antropomórficos comerciales de gama alta.
No obstante, este trabajo presenta algunas limitaciones relativas al proceso de fabricación del fantoma en su conjunto. Así, por ejemplo, algunos sustitutos tisulares están clasificados para fines industriales confidenciales y no suele ser posible adquirirlos34,26. Otra limitación es la preparación y modelado geométrico de los materiales de sustitución tisular durante la construcción32, que hace necesario utilizar otras tecnologías para la inclusión de nódulos pulmonares con su forma anatómica real junto con el resto del tejido pulmonar, que resulta difícil, como la impresión 3 D, que aún se encuentra en proceso de desarrollo35,36. Sin embargo, esta limitación no afecta especialmente al fantoma cuando se utiliza en estudios de optimización y visibilidad de las lesiones, ya que existen esferas equivalentes a las lesiones que pueden introducirse en el corcho para representar la visibilidad de una lesión o nódulo (como una esfera de pequeño tamaño). Por otro lado, el fantoma construido exhibe algunas limitaciones pese a haber sido creado buscando la precisión anatómica y radiológica. En primer lugar, la geometría de la clavícula no refleja exactamente la forma del paciente real. En segundo lugar, manipular el fantoma no es sencillo, puesto que todas sus partes son extraíbles y deben colocarse en la zona anatómica en cuestión. En tercer lugar, sería útil simular específicamente los puntos del tórax a los que está destinado el material, como los componentes óseos (incluyendo vértebras, arcos costales, esternón y clavículas) y los tejidos blandos del interior de ambos pulmones. Sin embargo, la relativa proximidad de sus características de radiación sugiere que su efecto sobre la calidad de imagen será insignificante en los estudios de optimización de dosis. En el futuro será posible mejorar de forma significativa el fantoma empleando equipos avanzados, como los equipos de corte en tres dimensiones, que permitirán superar las limitaciones descritas. Debemos aclarar, por último, que, al emplear el método de construcción expuesto en este artículo, es necesario llevar a cabo otros estudios destinados a la construcción de fantomas para otras edades pediátricas (cinco, 10 y 15 años de edad).
FinanciaciónNo se ha recibido ninguna financiación para este estudio.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.
El autor desea expresar su agradecimiento a la Universidad Femenina Alzahra de Kerbala (Irak).