La neuroftalmología es la parte de la neurología y la oftalmología que se encarga del estudio de las enfermedades que afectan al sistema visual y a los mecanismos que controlan la motilidad ocular y la función pupilar. Las pruebas de imagen permiten realizar una adecuada valoración anatómica y patológica de las estructuras que conforman la vía visual, los nervios que controlan la motilidad ocular y pupilar, y las propias estructuras orbitarias. Este artículo se divide en tres apartados (recuerdo anatómico, técnicas de imagen apropiadas y valoración patológica en función de la sintomatología clínica) con el propósito de proporcionar herramientas útiles que permitan al radiólogo elegir en cada momento la técnica de imagen más adecuada para el correcto diagnóstico de las enfermedades y un ajustado diagnóstico diferencial.
Neuro-ophthalmology is a field combining neurology and ophthalmology that studies diseases that affect the visual system and the mechanisms that control eye movement and pupil function. Imaging tests make it possible to thoroughly assess the relevant anatomy and disease of the structures that make up the visual pathway, the nerves that control eye and pupil movement, and the orbital structures themselves. This article is divided into three sections (review of the anatomy, appropriate imaging techniques, and evaluation of disease according to clinical symptoms), with the aim of providing useful tools that will enable radiologists to choose the best imaging technique for the differential diagnosis of patients’ problems to reach the correct diagnosis of their disease.
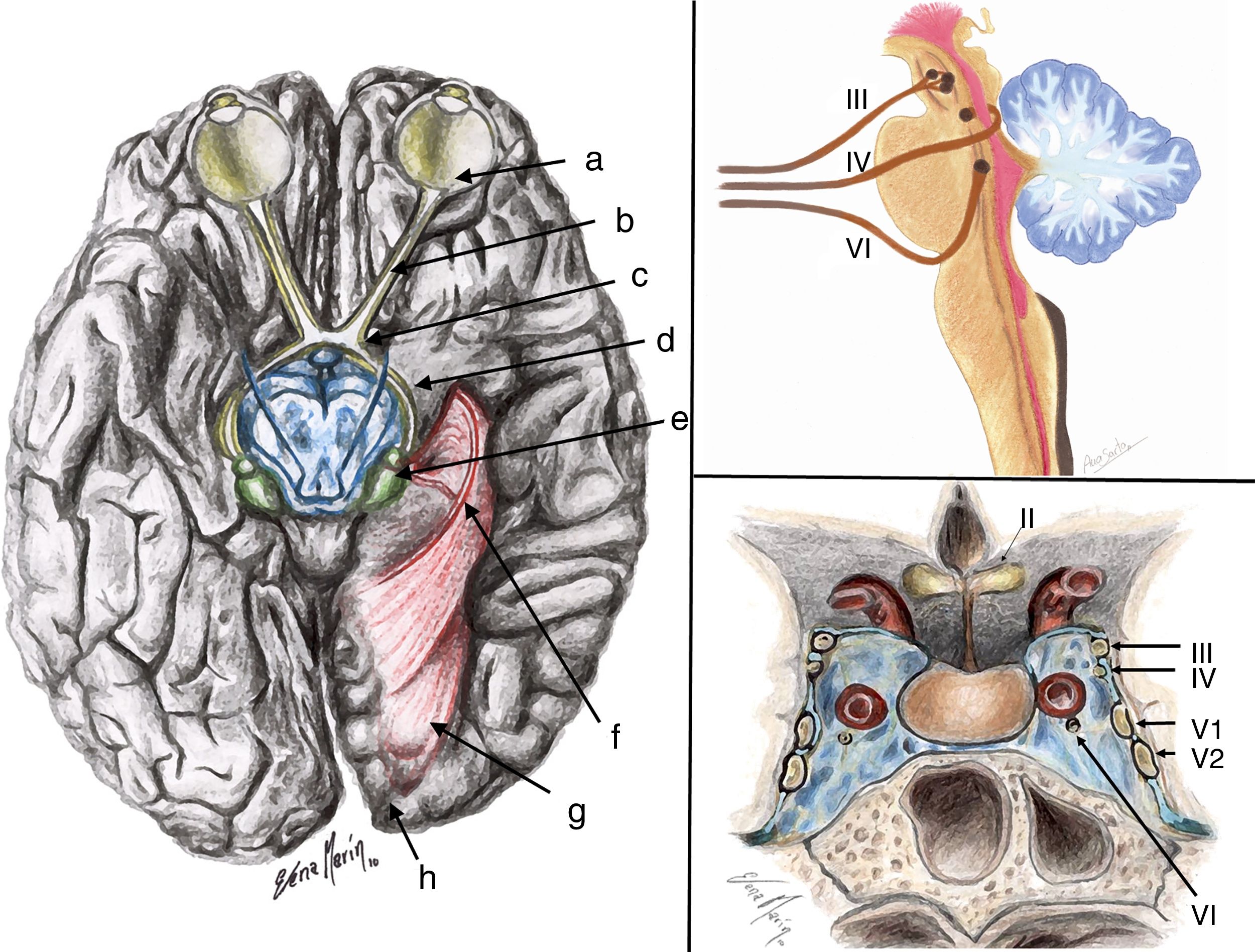
La patología de las vías ópticas y de las estructuras orbitarias es muy variada, pero con escasa incidencia global, por lo que su estudio y valoración representa un pequeño volumen en la práctica habitual del radiólogo, lo que hace que sea poco conocida y, en ocasiones, de difícil manejo. Por ello, resulta de utilidad repasar la anatomía (fig. 1), exponer las técnicas de imagen apropiadas para su evaluación y realizar un adecuado diagnóstico diferencial en función de la sintomatología.
a) Dibujo representativo del trayecto de las vías ópticas. b) Dibujo que muestra la localización de los núcleos de los pares craneales oculomotores y su relación con el mesencéfalo y la protuberancia. c) Dibujo esquemático de las relaciones de los pares craneales con el seno cavernoso y la arteria carótida interna intracavernosa. a: retina; b: nervio óptico; c: quiasma óptico; d: cintilla óptica; e: ganglio geniculado lateral; f: tractos geniculocalcarinos inferiores o asa de Meyer; g: tractos geniculocalcarinos superiores; h: corteza occipital; II: nervio óptico; III: nervio motor ocular común; IV: nervio troclear; VI: nervio patético; V1: primera rama del nervio trigémino; V2: segunda rama del nervio trigémino.
En la retina se encuentran los fotorreceptores, conos y bastones, que realizan sinapsis con las primeras neuronas o células bipolares, y estas hacen una segunda sinapsis con las células ganglionares, cuyos axones forman las fibras del nervio óptico1. La hemirretina nasal recibe información del campo visual temporal, y la temporal la recibe del campo visual nasal. También se produce un cruce superior-inferior, de forma que la información del campo visual superior es recogida por las hemirretinas inferiores, y viceversa1,2. El nervio óptico recorre la órbita y entra en el cráneo por el agujero óptico. Está rodeado de capas meníngeas en continuidad con las meninges intracraneales y por líquido cefalorraquídeo.
Los segmentos intracraneales de ambos nervios ópticos convergen formando el quiasma óptico. Las fibras temporales de cada retina (campos visuales nasales) permanecen en el mismo lado (homolaterales), y las mediales (campos visuales temporales) se decusan hacia el lado contralateral. Solo la mitad de las fibras maculares se decusan; el resto permanecen en el lado homónimo1,3.
Del quiasma parten las cintillas ópticas, que rodeando el mesencéfalo llegan al cuerpo geniculado lateral, núcleo talámico localizado detrás del núcleo pulvinar.
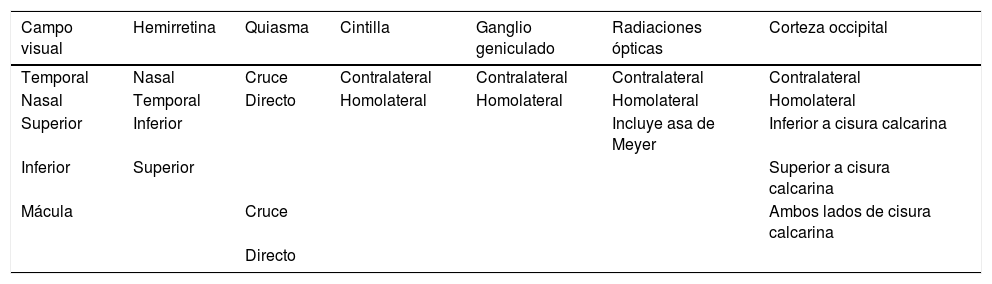
Los tractos geniculocalcarinos (radiaciones ópticas) conectan los núcleos geniculados laterales con la corteza visual. Los axones superiores llevan información de los campos visuales inferiores, transcurren laterales al atrio y el cuerno posterior del ventrículo lateral, atraviesan la sustancia blanca parietal y terminan en la corteza occipital sobre el surco calcarino. Las fibras inferiores, con información de los campos visuales superiores, se curvan anterolateralmente, pasan a través de la porción caudal de la cápsula interna, se continúan por la sustancia blanca temporal (asa de Meyer) rodeando el asta temporal del ventrículo, y se dirigen posteriormente hacia la corteza occipital localizada por debajo del surco calcarino3,4 (tabla 1).
Esquema-resumen de la dirección de las vías ópticas
| Campo visual | Hemirretina | Quiasma | Cintilla | Ganglio geniculado | Radiaciones ópticas | Corteza occipital |
|---|---|---|---|---|---|---|
| Temporal | Nasal | Cruce | Contralateral | Contralateral | Contralateral | Contralateral |
| Nasal | Temporal | Directo | Homolateral | Homolateral | Homolateral | Homolateral |
| Superior | Inferior | Incluye asa de Meyer | Inferior a cisura calcarina | |||
| Inferior | Superior | Superior a cisura calcarina | ||||
| Mácula | Cruce | Ambos lados de cisura calcarina | ||||
| Directo |
Los núcleos del nervio motor ocular común o III nervio craneal (NC) se localizan en la región periacueductal del mesencéfalo a la altura de los tubérculos cuadrigéminos superiores. Un único núcleo central inerva ambos músculos elevadores del párpado, los músculos rectos medial e inferior y oblicuo menor son inervados desde los núcleos homolaterales, y los rectos superiores desde los contralaterales. El nervio sale del mesencéfalo por la cisterna interpeduncular, pasa entre las arterias cerebelosa superior y cerebral posterior, y atraviesa la pared dural del seno cavernoso, situándose en su borde superior3–6.
El núcleo del IV NC (troclear) se encuentra en el mesencéfalo, inferior al núcleo del III NC, por detrás del fascículo longitudinal medial (FLM). Sus fibras se decusan en el mesencéfalo e inervan al músculo oblicuo superior contralateral. El nervio emerge al espacio subaracnoideo a la altura de los tubérculos cuadrigéminos inferiores, dirigiéndose anteriormente a través de la cisterna ambiens entre el mesencéfalo y el tentorio. Atraviesa la pared dural del seno cavernoso inferiormente al III NC3–6.
El núcleo del VI NC (patético) está en la región dorsal de la protuberancia, por delante del suelo del IV ventrículo, adyacente al FLM. La mayoría de sus fibras inervan al músculo recto lateral homolateral, pero un pequeño grupo de axones se dirige, vía FLM, al núcleo contralateral, ofreciendo también inervación al recto lateral del otro lado. El nervio emerge por la parte inferior de la protuberancia y asciende por detrás del clivus para introducirse en el seno cavernoso, viajando en el interior de los plexos venosos3–6. Tras salir del seno cavernoso alcanzan la órbita a través de la hendidura esfenoidal. La primera y la segunda ramas del trigémino también atraviesan la pared dural del seno cavernoso4.
El FLM discurre a lo largo de la cara anterior del acueducto del mesencéfalo hasta el cordón anterior de la médula espinal. Está compuesto por fibras de asociación que conectan los núcleos motores de los NC III, IV, VI y XI homolaterales y cada VI NC con el III NC contralateral. Esta estructura resulta fundamental en la coordinación de la mirada conjugada horizontal3,6,7. En la coordinación de la mirada vertical intervienen el FLM, el núcleo intersticial de Cajal y los NC III y IV6,7.
Vías simpática y parasimpáticaEl núcleo parasimpático de Edinger-Westphal se ubica posterior al núcleo del III NC. Está compuesto de neuronas parasimpáticas preganglionares cuyos axones se unen a las fibras del III NC en su camino hacia la órbita. Estas fibras se encuentran en la periferia del nervio. En el interior de la órbita se dirigen hacia el ganglio ciliar, del que salen las fibras posganglionares para inervar el músculo constrictor de la pupila y el músculo de los cuerpos ciliares3,4,6,7.
La vía simpática está compuesta por tres grupos de neuronas. La primera neurona está ubicada en el hipotálamo y sus axones descienden hasta los niveles C8-D2 de la médula espinal, donde se encuentra la segunda neurona. Desde aquí, la vía simpática asciende hacia el ganglio cervical superior, próximo a la bifurcación carotídea. La tercera neurona está en este ganglio y sus axones ascienden, junto con la adventicia de la arteria carótida interna, hacia el seno cavernoso, uniéndose con la primera rama del trigémino para dirigirse hasta la órbita3,4,6–8.
Técnicas de imagenRadiografía simple de cráneoLa única indicación de la radiografía de cráneo en la actualidad es para demostrar la existencia de cuerpos extraños ferromagnéticos intraorbitarios o intracraneales, cuya presencia puede contraindicar la realización de una resonancia magnética (RM) por el riesgo de movilización.
Ecografía orbitariaLa ecografía realizada con transductores de alta frecuencia, 7 mHz o más, es la técnica de elección para valorar el globo ocular9–12. El globo es explorado correctamente con oftalmoscopia, pero cuando existen cataratas, hemorragias vítreas, etc., que impiden ver a su través, la ecografía puede ser de gran ayuda11,13. Es especialmente útil en pediatría, ya que no requiere sedación y puede utilizarse en el control evolutivo de la respuesta al tratamiento de algunos tumores11,13.
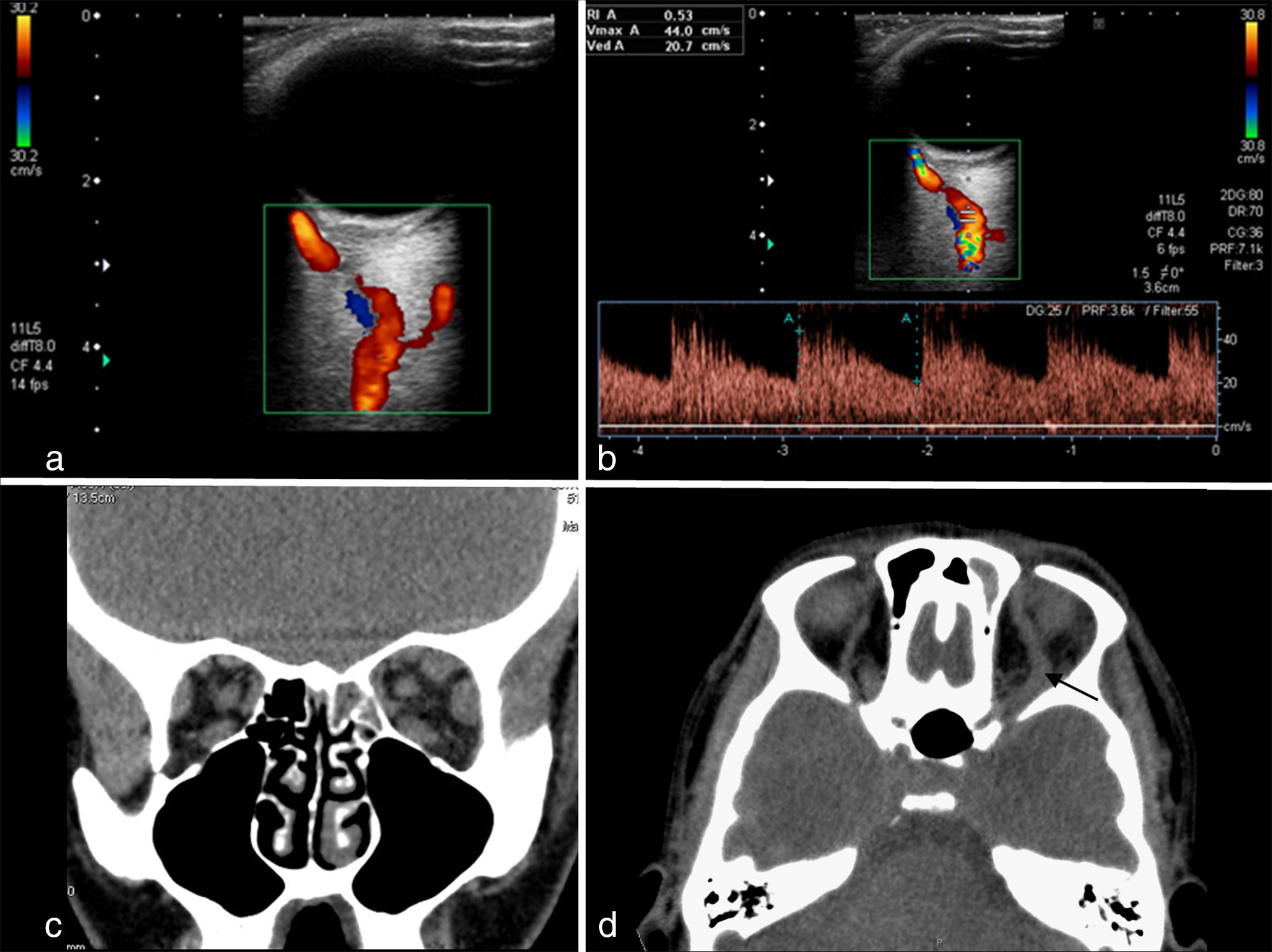
El Doppler es útil en la evaluación de las alteraciones de la dinámica de flujo y permite caracterizar algunas lesiones vasculares. Puede utilizarse en la valoración no invasiva de fístulas carotidocavernosas, en las que se observa un engrosamiento de la vena oftálmica con inversión de la dirección del flujo y arterialización del mismo (fig. 2); es útil tanto para el diagnóstico previo a la arteriografía como para el seguimiento de aquellas de bajo flujo en las que se decide no intervenir14.
Fístula carotidocavernosa. Mujer de 48 años que tras sufrir una caída por las escaleras presenta exoftalmos izquierdo progresivo y edema palpebral. Ecografía Doppler color (a y b) que muestra engrosamiento de la vena oftálmica superior con flujo arterializado. Cortes coronal (c) y axial (d) de TC orbitaria sin contraste en los que se aprecia un engrosamiento de los músculos extraoculares izquierdos debido a edema congestivo y engrosamiento de la vena oftálmica superior (flecha); compárese con la contralateral. Se realizó confirmación arteriográfica y tratamiento mediante embolización sin éxito, y posterior cierre de carótida por encima y debajo de la fístula.
Son las principales técnicas de imagen para el estudio orbitario e intracraneal.
La tomografía computarizada (TC) aporta mayor información sobre las paredes óseas de la órbita, visualiza claramente las calcificaciones y es de elección cuando hay cuerpos extraños ferromagnéticos intraorbitarios que contraindican la realización de RM15. Por su rapidez y mayor disponibilidad, es la técnica indicada en el ámbito de la urgencia. El estudio secuencial de cráneo aporta la información necesaria en casos de patología urgente encefálica vascular y traumática16. La adquisición en equipos de TC multicorte con reformateo en los planos coronal y sagital permite una exhaustiva valoración de las lesiones traumáticas faciales y orbitarias.
La RM ofrece mayor resolución anatómica y mejor caracterización tisular, valorando bien las diferencias de señal entre diferentes tejidos, por lo que es de elección en el estudio orbitario17. Si resulta imposible su realización puede ser sustituida por la TC con suficientes garantías diagnósticas en la mayoría de las ocasiones. Puede realizarse con antenas de cráneo o de superficie17; estas últimas ofrecen mayor relación señal/ruido, permitiendo explorar con excelente detalle anatómico el globo ocular, pero son insuficientes para valorar el ápex orbitario y la extensión intracraneal de las lesiones.
La correcta valoración de la región hipotálamo-hipofisaria debe realizarse mediante RM, así como el estudio de las estructuras cerebrales. Los protocolos dependerán de la zona anatómica a estudiar18.
La angiografía por TC o por RM craneal está indicada ante la sospecha de aneurismas o de malformaciones vasculares.
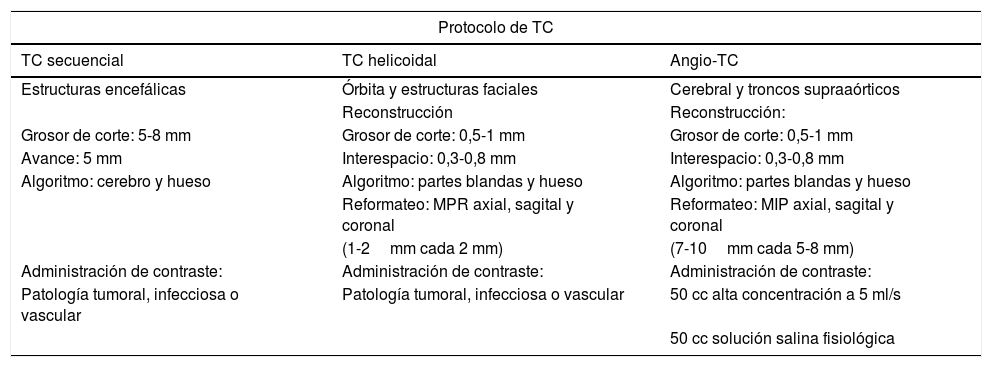
La tabla 2 muestra los protocolos de estudio de TC y RM empleados en nuestro centro.
Protocolos de TC y RM en neuroftalmología del Hospital Universitario Miguel Servet (Zaragoza)
| Protocolo de TC | ||
|---|---|---|
| TC secuencial | TC helicoidal | Angio-TC |
| Estructuras encefálicas | Órbita y estructuras faciales | Cerebral y troncos supraaórticos |
| Reconstrucción | Reconstrucción: | |
| Grosor de corte: 5-8 mm | Grosor de corte: 0,5-1 mm | Grosor de corte: 0,5-1 mm |
| Avance: 5 mm | Interespacio: 0,3-0,8 mm | Interespacio: 0,3-0,8 mm |
| Algoritmo: cerebro y hueso | Algoritmo: partes blandas y hueso | Algoritmo: partes blandas y hueso |
| Reformateo: MPR axial, sagital y coronal | Reformateo: MIP axial, sagital y coronal | |
| (1-2mm cada 2 mm) | (7-10mm cada 5-8 mm) | |
| Administración de contraste: | Administración de contraste: | Administración de contraste: |
| Patología tumoral, infecciosa o vascular | Patología tumoral, infecciosa o vascular | 50 cc alta concentración a 5 ml/s |
| 50 cc solución salina fisiológica | ||
| Protocolo de RM | ||
|---|---|---|
| RM craneal | RM orbitaria | RM hipofisaria |
| Antena de cráneo (órbita) o superficie (globo) | ||
| T1 | T1 axial | T1 sagital y coronal |
| FLAIR T2 | T2FS axial | T1 sagital y coronal con gadolinio |
| Difusión (factor B:1000) | STIR coronal | T2 coronal |
| Eco de gradiente: T2*, SWI | T1FS con gadolinio (axial, coronal, sagital) | |
| Grosor de corte: 2-3 mm | Grosor de corte: 2-3 mm | |
| Matriz: 256 × 256; 512 × 512 | Matriz: 256 × 256 | |
| Secuencias complementarias: | Secuencias complementarias: | Secuencias complementarias: |
| 3D SS coherente: pares craneales | Fast SPGR FS dinámico: | 3DT1 con gadolinio |
| Angio-RM 3D TOF: aneurismas | Tumores y lesiones vasculares | T2 sagital |
| 3DT1 con gadolinio | Difusión SE, EPI, T2* Calcificaciones | |
Equipo de TC: Toshiba Aquilion 64. Toshiba Medical Systems.
Equipo de RM: Signa Excite 1,5. General Electric Healthcare. Milwakee. Wisconsin, USA.
EPI: echo-planar imaging; Fast SPGR: fast spoiled gradient; FS: fat sat (saturación grasa); MIP: proyección de máxima intensidad; MPR: reformateo multiplanar; SE: spin eco; SS coherente: steady state coherent; STIR: short tau inversion recovery; SWI: susceptibility-weighted imaging; T2*: eco de gradiente potenciado en T2; TOF: time of flight.
La arteriografía mantiene su indicación en casos seleccionados de aneurismas, fístulas carotidocavernosas, varices o malformaciones vasculares que requieran confirmación diagnóstica y procedimientos terapéuticos19. En tumores orbitarios e intracraneales muy vascularizados puede resultar beneficiosa su embolización parcial previa a la intervención quirúrgica.
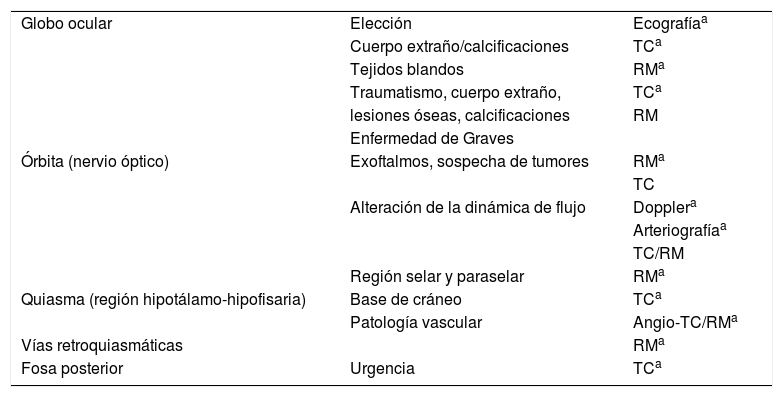
Indicaciones clínicas de las pruebas de imagenEl primer objetivo neuroftalmológico es la localización clínica de la lesión. La diferente sintomatología permite localizar el origen de la patología en cada región anatómica y elegir la técnica de imagen adecuada; puede hacerse una división genérica en globo ocular, órbita, región paraselar, fosa craneal media y fosa craneal posterior. La tabla 3 indica las pruebas de imagen más apropiadas para cada región. En muchas ocasiones, la realización de una técnica no excluye a las demás, y con frecuencia los hallazgos se complementan para llegar al diagnóstico.
Indicaciones de las técnicas de imagen en neuroftalmología según las áreas anatómicas y la patología
| Globo ocular | Elección | Ecografíaa |
| Cuerpo extraño/calcificaciones | TCa | |
| Tejidos blandos | RMa | |
| Traumatismo, cuerpo extraño, | TCa | |
| lesiones óseas, calcificaciones | RM | |
| Enfermedad de Graves | ||
| Órbita (nervio óptico) | Exoftalmos, sospecha de tumores | RMa |
| TC | ||
| Alteración de la dinámica de flujo | Dopplera | |
| Arteriografíaa | ||
| TC/RM | ||
| Región selar y paraselar | RMa | |
| Quiasma (región hipotálamo-hipofisaria) | Base de cráneo | TCa |
| Patología vascular | Angio-TC/RMa | |
| Vías retroquiasmáticas | RMa | |
| Fosa posterior | Urgencia | TCa |
La ecografía con Doppler es la mejor técnica de cribado de la patología del globo ocular, indicada para diferenciar desprendimientos de retina de hemorragias vítreas, a veces difícilmente valorables por oftalmoscopia11,20. Es sencilla y fácil de manejar en casos de búsqueda de cuerpos extraños, aunque hay que ser sumamente cauto cuando se sospecha rotura del globo ocular, ya que la presión sobre el mismo con el transductor podría provocar la extrusión de su contenido. En estos casos es mejor realizar una TC10,12,20, que además permite valorar con alta sensibilidad los cuerpos extraños de diferentes materiales y el estado del resto de las estructuras orbitarias20.
La ecografía proporciona mayor resolución espacial que la RM en la búsqueda de pequeños tumores oculares, pero para la valoración de la infiltración de la esclerótica y la extensión retrobulbar de los tumores la RM es más precisa12,21.
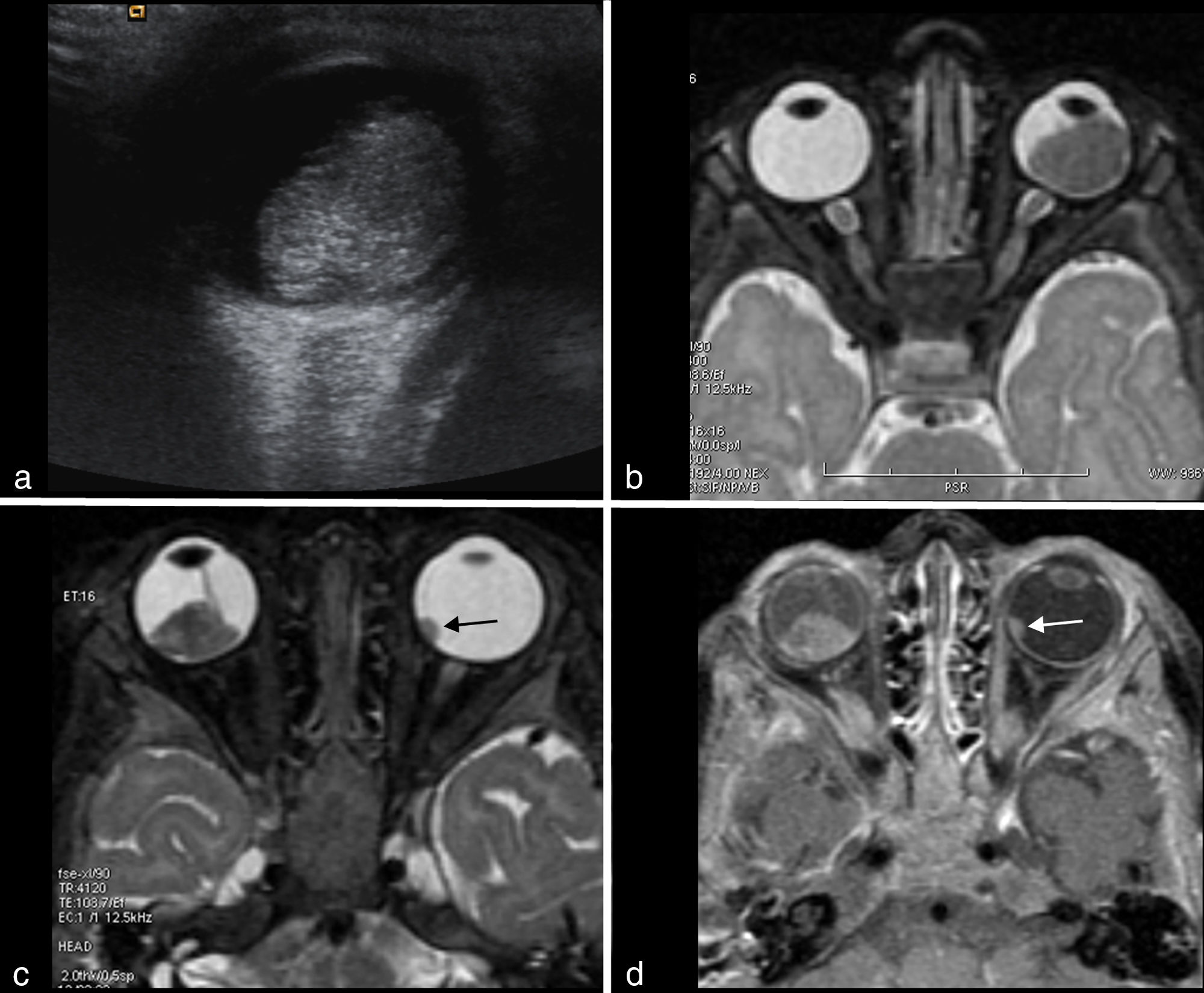
El tumor intraocular más frecuente en la edad pediátrica es el retinoblastoma (fig. 3), cuyo signo clínico característico es la leucocoria. Hasta en el 90-95% de los retinoblastomas aparecen calcificaciones13,22,23, en general en la porción posterior del globo. La ecografía y la TC son altamente sensibles para su detección, identificando calcificaciones desde 2mm de grosor. Sin embargo, la RM muestra mejor las características del tumor, la infiltración retrobulbar y la extensión hacia el sistema nervioso central, así como la presencia de retinoblastomas pineales o supraselares asociados22,24. En la actualidad, a pesar de su alta sensibilidad, no debe realizarse TC orbitaria teniendo en cuenta la alta radiación que supondría para la órbita de los pacientes pediátricos24. Hay estudios que demuestran que la combinación de oftalmoscopia, ecografía y RM consigue detectar calcificaciones en el mismo porcentaje que la TC23. La secuencia de RM más sensible para la detección de calcificaciones es la T2*23. Recientes trabajos avalan la utilidad de la secuencia de difusión en el diagnóstico de los retinoblastomas, ya que muestran mayor restricción a la difusión que otras lesiones oculares, además de posibilitar la monitorización de la respuesta al tratamiento diferenciando tejido tumoral viable de tejido necrótico25,26.
Retinoblastoma. Ecografía ocular (a) y corte axial en T2 con saturación grasa (b) en un lactante de 2 meses con leucocoria. Ecográficamente se objetiva una masa lobulada y heterogénea, con imágenes hiperrefringentes sugestivas de calcificaciones. En T2 la imagen es altamente hipointensa. En ambas técnicas se descarta invasión retrobulbar. Retinoblastoma bilateral. Cortes axiales T2 con saturación grasa (c) y T1 con saturación grasa con gadolinio (d) en un lactante de 9 meses con leucocoria derecha. Lesión intraocular derecha hipointensa en T2 con realce homogéneo tras la administración de gadolinio, que produce desprendimiento de retina sin invasión de las estructuras retrobulbares. En el globo ocular izquierdo se aprecia una pequeña imagen de similares características en la región nasal (flecha).
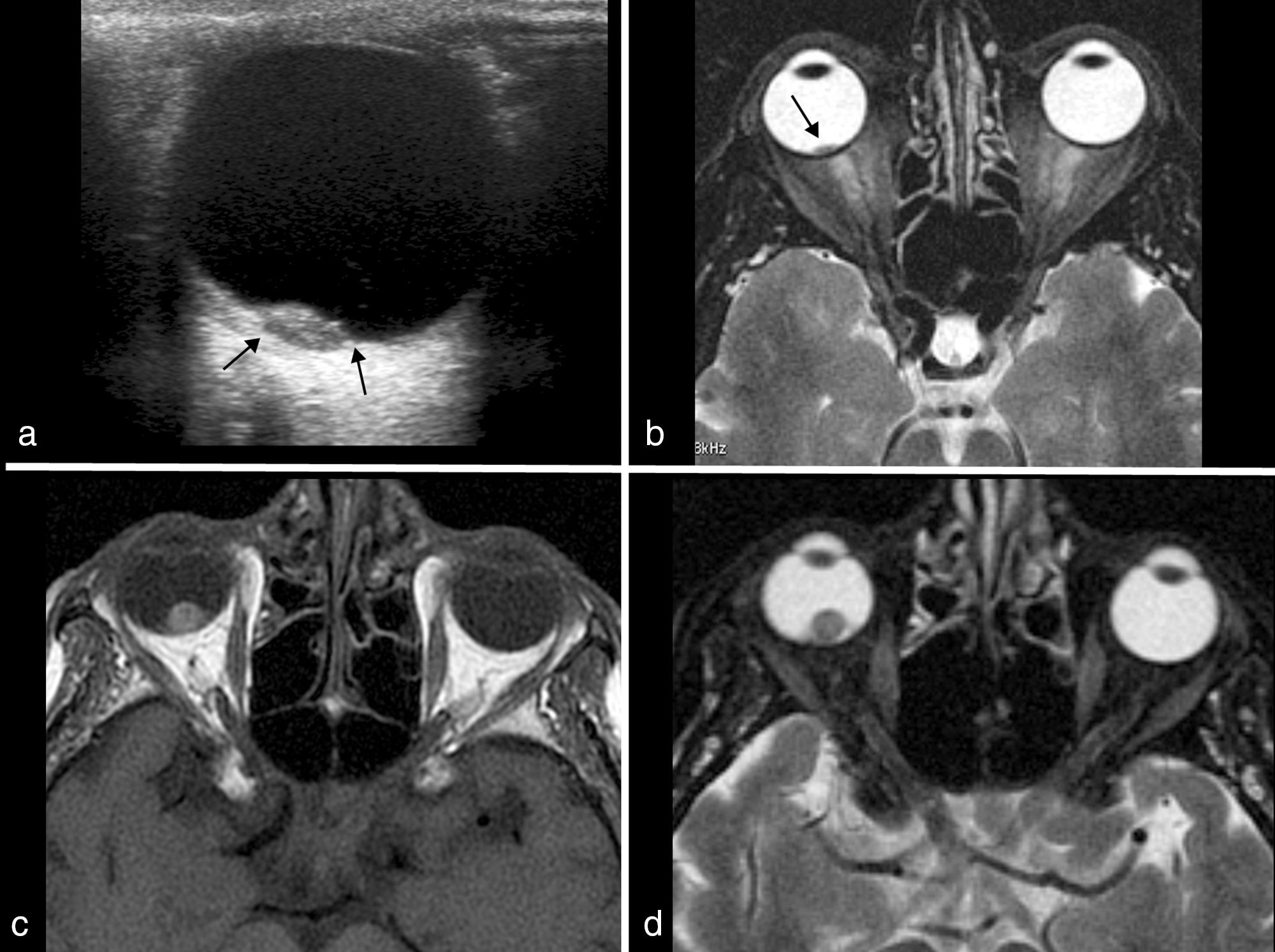
El melanoma coroideo como tumor primario (fig. 4) y las metástasis (mama y pulmón, principalmente) son los tumores oculares más frecuentes en los adultos10,11,27,28, pero pueden aparecer otras lesiones, como hemangiomas, hemangioblastomas o lesiones granulomatosas. La ecografía es muy sensible en la detección de pequeños tumores, pero la RM es la técnica de elección para su estudio, ya que aporta algunos detalles característicos y permite valorar si hay extensión extraocular.
Melanoma. Ecografía ocular (a) y corte axial T2 con saturación grasa (b) en un varón de 58 años que acudió a urgencias por visión borrosa, objetivándose en la oftalmoscopia una masa peripapilar sobreelevada ligeramente pigmentada. En la ecografía se aprecia una pequeña masa lenticular con signo de la excavación coroidea (flechas), y en el corte T2 de RM se visualiza la lesión hipointensa adyacente a la papila. Melanoma. Cortes axiales T1 (c) y T2 con saturación grasa (d) de un paciente de 73 años con una masa prominente en los cuadrantes inferiores vista por oftalmoscopia. En la RM, la lesión muestra las características típicas de los melanomas, hiperintensa en T1 e hipointensa en T2.
Ecográficamente los melanomas son hipoecogénicos y con el signo de la excavación coroidea, característico (aunque no siempre presente) e indicativo de invasión local. Aplicando Doppler muestran una alta vascularización10,27. Las metástasis son hiperecogénicas, con mayor vascularización en el estudio Doppler, y pueden ser múltiples. La característica más significativa de los melanomas en la RM es la hiperintensidad en T1 y la hipointensidad en T2, debido a su contenido en melanina: a mayor contenido en melanina, mayor intensidad de señal en T1, y según algunos autores esto implica peor pronóstico17. Los melanomas amelanóticos no muestran hiperintensidad en T1, lo que dificulta su diagnóstico diferencial con otros tumores29. Las metástasis no se visualizan hiperintensas en T1, a no ser que haya componente hemorrágico o alto contenido mucoide en su interior27. Los trabajos realizados con difusión muestran una gran restricción a la difusión, con coeficiente de difusión aparente disminuido en los melanomas respecto a otras lesiones. Ya que en la actualidad el tratamiento de elección es la radiocirugía, la monitorización del coeficiente de difusión aparente en estudios seriados permite valorar la respuesta al tratamiento30.
La presencia de drusas en la cabeza del nervio óptico puede producir elevación de la papila y borramiento de sus márgenes, pudiendo confundirse por oftalmoscopia con edema de papila. Tanto en la ecografía como en la TC pueden observarse nódulos calcificados unilaterales o bilaterales asiméticos11,12,20.
Neuritis ópticaLa neuritis óptica es un diagnóstico clínico y conlleva pérdida de visión unilateral, dolor, defecto pupilar aferente y defecto campimétrico7. Deben realizarse pruebas de imagen del nervio óptico si existen indicios de neuritis óptica no explicable por glaucoma, isquemia o causas tóxicas, metabólicas, infecciosas o hereditarias31.
Ya que la neuritis óptica puede ser la manifestación inicial en el 15-25% de los pacientes con esclerosis múltiple, y hasta el 75% de estos pacientes tendrán al menos un episodio de neuritis óptica, se recomienda RM craneal en pacientes jóvenes con neuritis óptica retrobulbar aguda que no presenten los factores etiológicos antes expuestos, buscando lesiones típicas de enfermedad desmielinizante31. La RM cerebral es la mejor prueba aislada para valorar el riesgo de esclerosis múltiple futura y para ayudar en la decisión de prescribir terapia inmunomoduladora32,33.
El riesgo de desarrollar la enfermedad es de hasta el 38% a los 10 años y del 50% a los 15 años en pacientes con lesiones hiperintensas en la RM31,33,34. El riesgo de desarrollar la enfermedad con una RM normal es mucho menor, del 22% a los 10 años32,34.
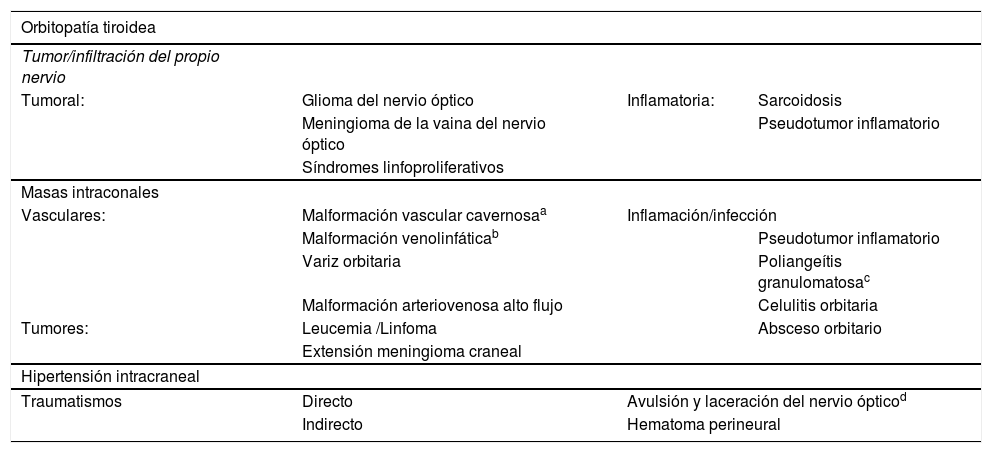
Neuropatía óptica de causa compresivaSuele manifestarse con pérdida de visión lenta y progresiva. Puede deberse a oftalmopatía tiroidea por compromiso del espacio intraorbitario, a compresión de las fibras del nervio óptico por causa tumoral o infiltrativa del propio nervio, o a lesiones ocupantes de espacio intraconales4,7,35,36 (tabla 4).
Causas de neuropatía óptica compresiva (órbita)
| Orbitopatía tiroidea | |||
|---|---|---|---|
| Tumor/infiltración del propio nervio | |||
| Tumoral: | Glioma del nervio óptico | Inflamatoria: | Sarcoidosis |
| Meningioma de la vaina del nervio óptico | Pseudotumor inflamatorio | ||
| Síndromes linfoproliferativos | |||
| Masas intraconales | |||
| Vasculares: | Malformación vascular cavernosaa | Inflamación/infección | |
| Malformación venolinfáticab | Pseudotumor inflamatorio | ||
| Variz orbitaria | Poliangeítis granulomatosac | ||
| Malformación arteriovenosa alto flujo | Celulitis orbitaria | ||
| Tumores: | Leucemia /Linfoma | Absceso orbitario | |
| Extensión meningioma craneal | |||
| Hipertensión intracraneal | |||
| Traumatismos | Directo | Avulsión y laceración del nervio ópticod | |
| Indirecto | Hematoma perineural | ||
El incremento de la presión intracraneal, sea tumoral o idiopática, produce un aumento del líquido cefalorraquídeo en la vaina de los nervios ópticos y la compresión de sus fibras, con alteraciones de la visión37,38.
La afectación es generalmente unilateral, con pérdida del campo visual monocular, excepto en la oftalmopatía tiroidea y la hipertensión craneal, en las que suele ser bilateral35.
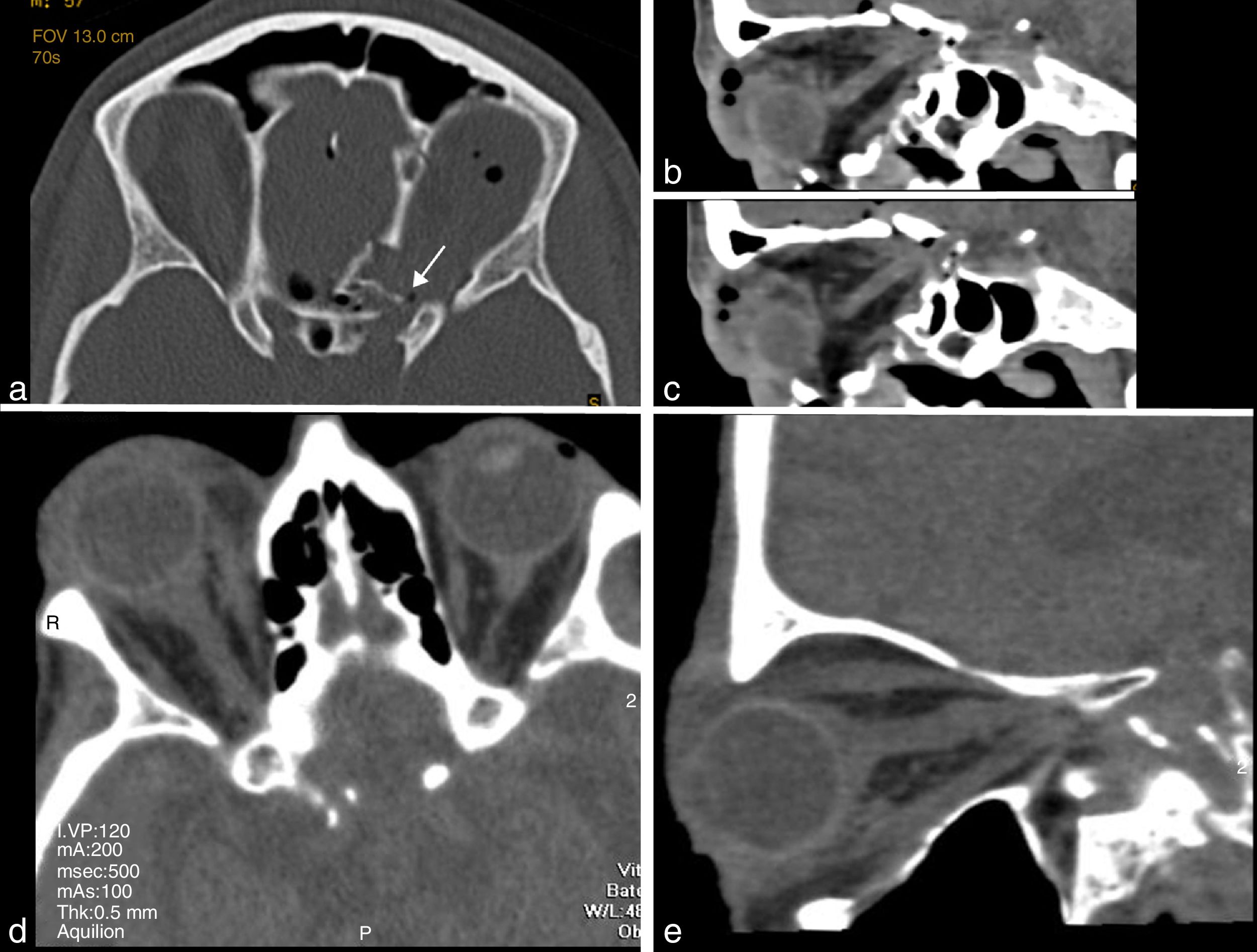
Los traumatismos pueden producir disminución aguda de la visión debido a una lesión del nervio óptico de causa directa, por avulsión del propio nervio o laceración por fragmentos óseos, o de causa compresiva propiamente dicha, por hematomas intraorbitarios o en la vaina del nervio39 (fig. 5). También las contusiones encefálicas en los lóbulos frontales pueden lesionar los nervios ópticos en su trayecto intracraneal35.
Traumatismo orbitario. Corte axial con ventana ósea (a) y reformateo sagital con algoritmo de partes blandas (b y c) en una mujer de 26 años con traumatismo facial tras un accidente de tráfico. Presentó múltiples fracturas del seno maxilar y de la órbita izquierdos, con fractura multifragmentada del techo orbitario, objetivando un fragmento (flecha) en el agujero óptico, lo que produjo una lesión irreversible del nervio óptico a pesar del tratamiento urgente. Traumatismo orbitario. Cortes axial (d) y reformateo sagital (e) de TC realizada a una anciana de 80 años tras una caída por las escaleras, con hematoma periorbitario y limitación de la motilidad ocular. Engrosamiento y desflecamiento de la grasa retrobulbar y perineural compatible con hematoma, que fue drenado con carácter urgente.
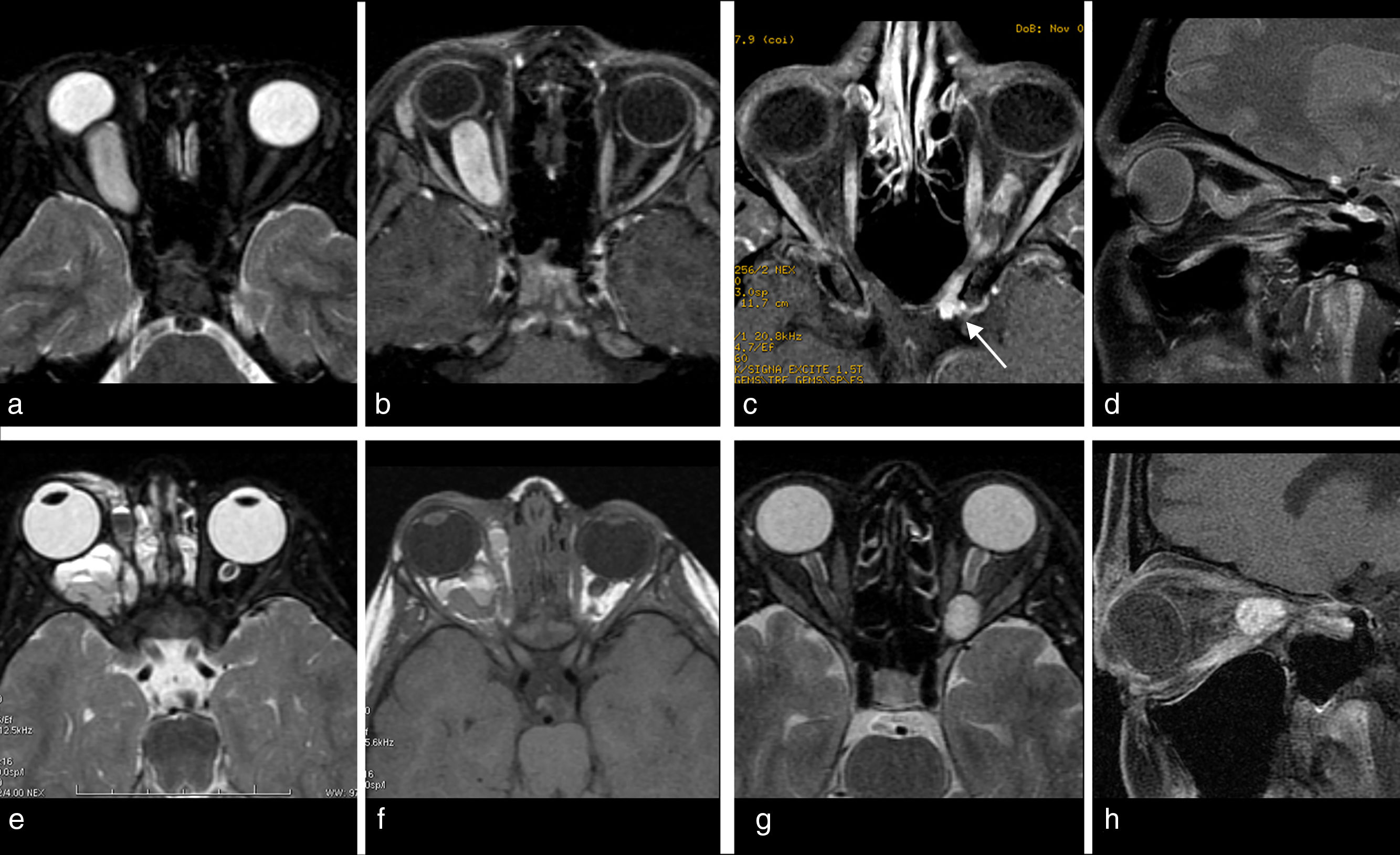
La RM es la técnica de elección para valorar la órbita, por su mayor capacidad de discriminación entre los tejidos de partes blandas17,40. La secuencia T1 es fundamental, ya que la mayoría de las lesiones orbitarias son hipointensas respecto a la grasa, lo que permite valorar adecuadamente sus límites. Las secuencias T2 y T1 con gadolinio, con o sin supresión grasa, aportan datos diferenciadores de algunos tumores (fig. 6).
Glioma del nervio óptico. Cortes axiales T2 con saturación grasa (a) y T1 con saturación grasa con gadolinio (b) en un paciente con disminución de la agudeza visual y edema de papila. Engrosamiento fusiforme del nervio óptico derecho que impronta sobre la papila, hiperintenso en T2 y con realce homogéneo tras la administración de contraste. Meningioma de la vaina del nervio óptico. Corte axial T1 con saturación grasa (c) con gadolinio y sagital T1 con saturación grasa (d) en un hombre joven con pérdida de visión lenta y progresiva y signos de neuropatía izquierda grave en potenciales evocados. Engrosamiento tubular de la vaina del nervio óptico izquierdo que rodea y constriñe al nervio y se realza intensamente con gadolinio, con extensión a través del agujero orbitario a la fosa craneal media (flecha). Malformación venolinfática. Cortes axiales T2 con saturación grasa (e) y T1 (f) en una niña de 2 años con proptosis ocular derecha. Masa orbitaria derecha con componente intraconal y extraconal, con imágenes quísticas y niveles líquido/líquido debido al componente hemorrágico de los quistes. Malformación vascular cavernosa. Cortes axial T2 con saturación grasa (g) y sagital T1 con saturación grasa con gadolinio (h) en un paciente de 60 años con disminución de la agudeza visual del ojo izquierdo. Masa redondeada y bien delimitada en el ápex orbitario, hiperintensa en T2 e intensamente realzada en el corte con contraste, que comprime el nervio óptico.
Las secuencias de difusión pueden ayudar en la diferenciación de algunos tumores orbitarios. Algunos trabajos han demostrado que los gliomas del nervio óptico presentan valores de coeficiente de difusión aparente significativamente menores que los meningiomas17. Igualmente, las enfermedades linfoproliferativas (linfoma) producen mayor restricción a la difusión que las inflamatorias (pseudotumor inflamatorio)41,42.
La TC es más útil para valorar las alteraciones óseas, siendo la técnica de elección en los traumatismos orbitarios y para la detección de calcificaciones (presentes hasta en el 33% de los meningiomas de la vaina del nervio)17 o de flebolitos en los hemangiomas cavernosos y los linfangiomas.
La presencia de papiledema bilateral requiere una TC urgente en busca de masa intracraneal o de hidrocefalia como causas de hipertensión craneal. Ante la ausencia de hallazgos, la angio-TC puede estar indicada para descartar trombosis de seno venoso7,43.
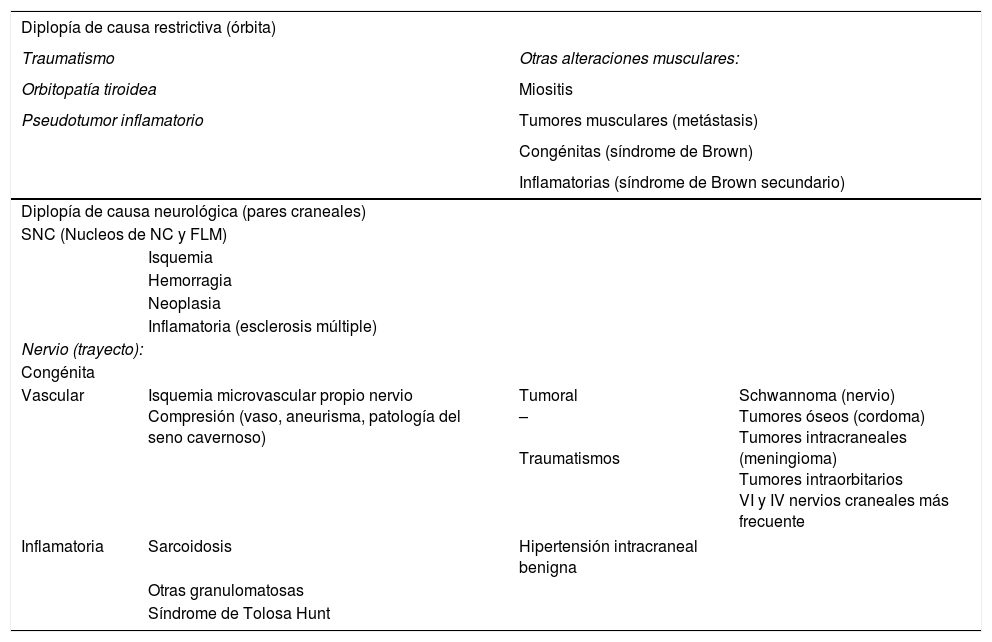
DiplopíaLa diplopía binocular se produce por desalineación de los ejes visuales, de forma que las imágenes procedentes de cada ojo no se fusionan en el cerebro para originar la visión doble. Puede ser de causa restrictiva y entonces la lesión se localiza en la órbita, o de causa nerviosa con la lesión en los núcleos de los NC o en su trayecto, bien por patología intrínseca del propio nervio o por compresión a su paso a través de las cisternas de la base44,45 (tabla 5).
Causas de diplopía
| Diplopía de causa restrictiva (órbita) | |||
|---|---|---|---|
| Traumatismo | Otras alteraciones musculares: | ||
| Orbitopatía tiroidea | Miositis | ||
| Pseudotumor inflamatorio | Tumores musculares (metástasis) | ||
| Congénitas (síndrome de Brown) | |||
| Inflamatorias (síndrome de Brown secundario) | |||
| Diplopía de causa neurológica (pares craneales) | |||
| SNC (Nucleos de NC y FLM) | |||
| Isquemia | |||
| Hemorragia | |||
| Neoplasia | |||
| Inflamatoria (esclerosis múltiple) | |||
| Nervio (trayecto): | |||
| Congénita | |||
| Vascular | Isquemia microvascular propio nervio Compresión (vaso, aneurisma, patología del seno cavernoso) | Tumoral – Traumatismos | Schwannoma (nervio) Tumores óseos (cordoma) Tumores intracraneales (meningioma) Tumores intraorbitarios VI y IV nervios craneales más frecuente |
| Inflamatoria | Sarcoidosis | Hipertensión intracraneal benigna | |
| Otras granulomatosas | |||
| Síndrome de Tolosa Hunt | |||
SNC: Sistema Nervioso Central. FLM: Fascículo longitudinal medial. EM: Esclerosis Multiple. ppio. N.: Propio Nervio.
La oftalmopatía tiroidea y los traumatismos son las causas más frecuentes de diplopía restrictiva.
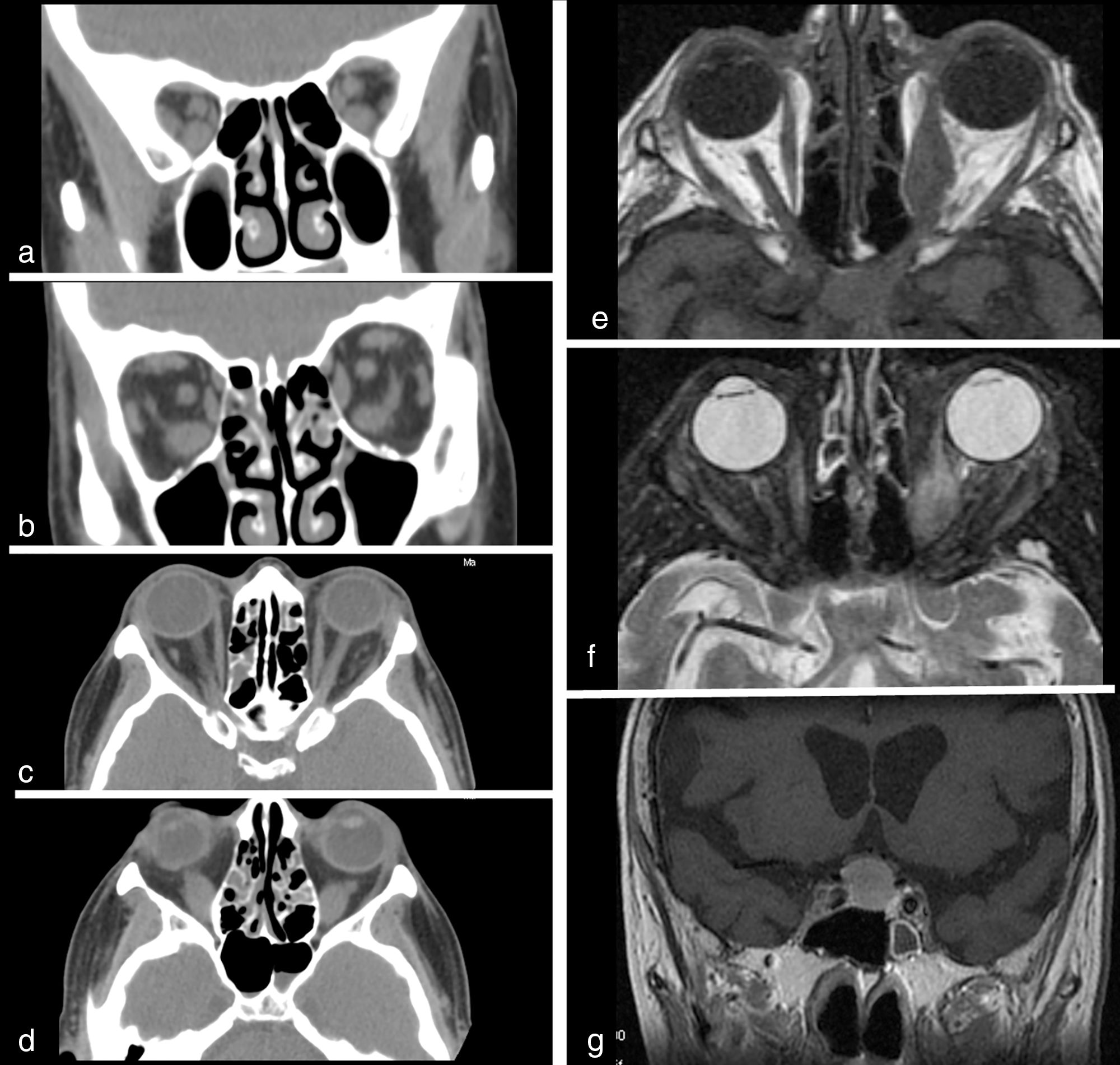
La oftalmopatía tiroidea (fig. 7) se manifiesta con un agrandamiento de los músculos extraoculares, habitualmente bilateral, pero asimétrico. Los músculos más afectados son el recto interno e inferior, y el más raramente engrosado es el recto lateral36,45.
Orbitopatía tiroidea. Cortes coronales (a y b) y axiales (c y d) de estudio de TC sin contraste en una mujer de 43 años con hipertiroidismo. Engrosamiento fusiforme de los músculos extraoculares bilateral y asimétrico, especialmente de los rectos inferiores y en menor medida del recto medial izquierdo y lateral derecho. También se aprecia infiltración inflamatoria de la grasa intraconal. Cortes axiales T1 y T2 con saturación grasa (e y f) de órbitas y coronal T1 con gadolinio de hipófisis (g) en un paciente con hipertiroidismo. Engrosamiento fusiforme del músculo recto interno izquierdo con hiperseñal en la secuencia T2 con saturación grasa, hiperseñal que también se objetiva en el recto medial derecho, indicando fase aguda de la enfermedad. Como hallazgo incidental, macroadenoma hipofisario que desplaza superiormente el quiasma.
La TC orbitaria se incluye en la mayoría de los protocolos diagnósticos de oftalmopatía tiroidea36,46. Los cortes axiales valoran el grado de exoftalmos y el aumento de la grasa orbitaria; los coronales son fundamentales para comparar el volumen de los músculos homónimos de ambos ojos y sus variaciones de tamaño en controles seriados, así como para monitorizar la respuesta al tratamiento. La TC valora adecuadamente las paredes orbitarias antes de planificar la cirugía descompresiva36,40,46. La administración de contraste yodado no es útil y debería evitarse16,47.
La RM permite diferenciar las fases aguda y crónica de la enfermedad. En la fase aguda, el edema muscular produce hiperseñal en las secuencias T2 con supresión grasa y STIR, y en la fase de fibrosis los músculos son hipointensos en T1 y T2, con focos hiperintensos en T1 que representan infiltración grasa40,46. Se ha descrito una buena correlación entre el patrón de señal en T2 y la reversibilidad de la diplopía, al observar cómo los casos con hiperseñal homogénea presentan mejor respuesta al tratamiento que cuando la señal es hipointensa y heterogénea48.
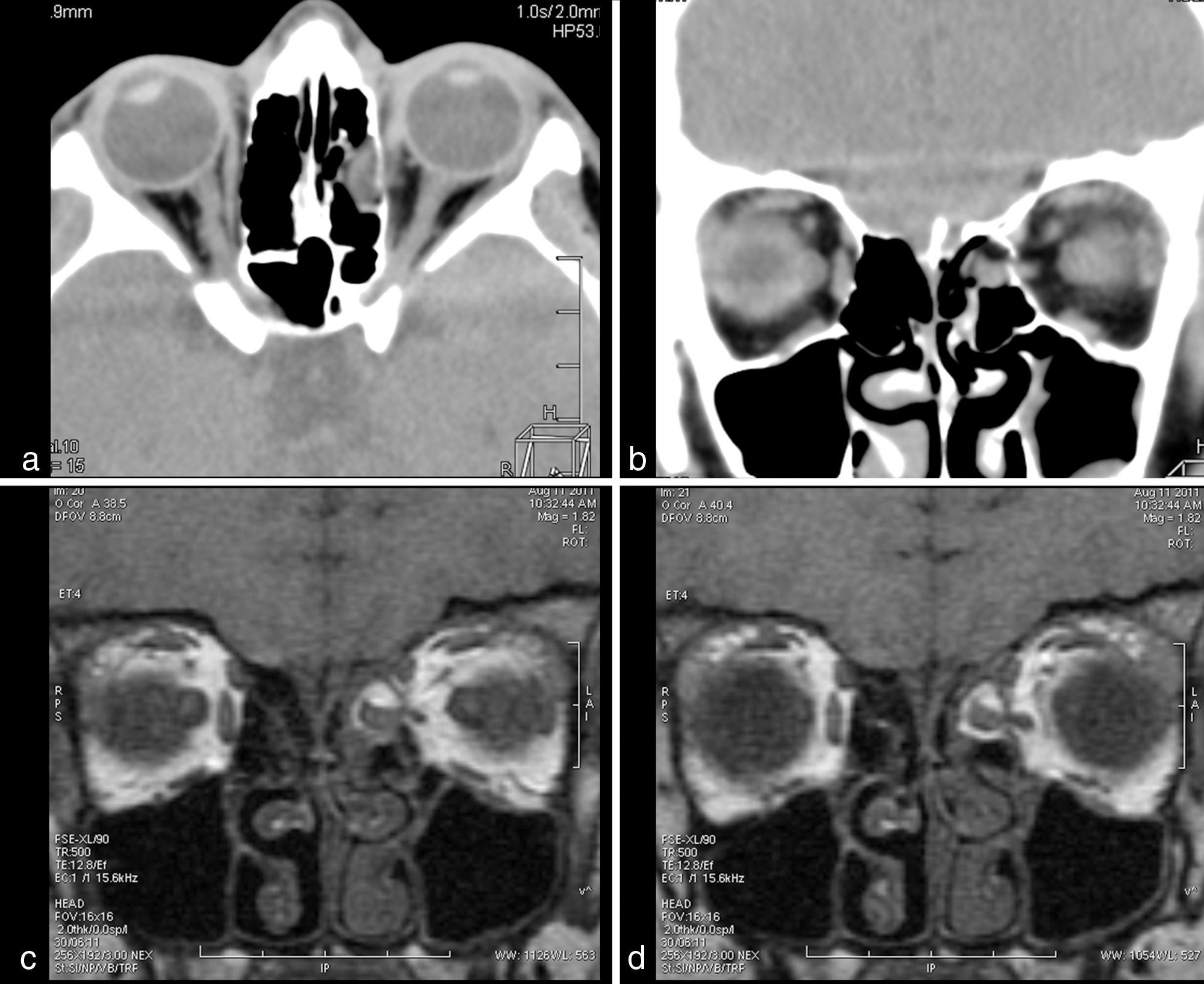
Las fracturas de las paredes orbitarias, especialmente las del suelo orbitario o la lámina papirácea (blow-out), pueden producir restricción a los movimientos oculares, y por tanto diplopía debido a edema o hemorragia en la grasa orbitaria que tracciona del músculo, edema del propio músculo o herniación del vientre muscular a través de la fractura (en general del recto inferior). Por ello, es fundamental valorar el estado de los músculos extraoculares en los estudios de TC de pacientes con traumatismos faciales49. El plano coronal aporta más información en la detección de las herniaciones musculares (fig. 8) y resulta fundamental en la toma de decisión sobre cirugía urgente o diferida50,51.
Fractura blow-out de lámina papirácea con herniación muscular. Cortes de TC axial (a) y coronal (b), y cortes coronales T1 (c y d) en una niña de 13 años que, tras sufrir un traumatismo craneoencefálico por atropello, presenta déficit completo de aducción y parcial de abducción del ojo izquierdo, con diplopía. Los cortes de TC muestran la línea de fractura en la lámina papirácea, ocupación de la celdilla etmoidal media y morfología irregular del músculo recto interno en el lado izquierdo. En los cortes de RM se visualiza más claramente el cambio en la forma y la orientación del músculo recto interno respecto al contralateral, con morfología «en pajarita» debido a la herniación del vientre muscular en la celdilla etmoidal.
Otras afecciones de los músculos extraoculares pueden producir restricción a los movimientos y diplopía. La diferenciación se basa fundamentalmente en la valoración morfológica de las lesiones40.
Diplopía de causa nerviosaLa diplopía causada por parálisis de un NC puede deberse a isquemia en la vasculatura del propio nervio o a pequeños infartos en los núcleos mesencefálicos, por traumatismos, aneurismas en las arterias del polígono de Willis o neoplasias que pueden comprimir los nervios a lo largo de su trayecto45,52–54.
Parálisis aisladas de algún NC en pacientes mayores de 50 años con antecedentes de diabetes, hipertensión arterial o enfermedades vasculares suelen ser de origen microvascular y no precisan estudios de imagen43,53,55–57. Suelen resolverse por completo en menos de 3 meses. Si no se resuelven, o si se trata de un paciente joven sin factores de riesgo vascular, las pruebas neurorradiológicas están indicadas, siendo de elección la RM58 (fig. 9 a-c). En tal caso, la administración de contraste sería conveniente43.
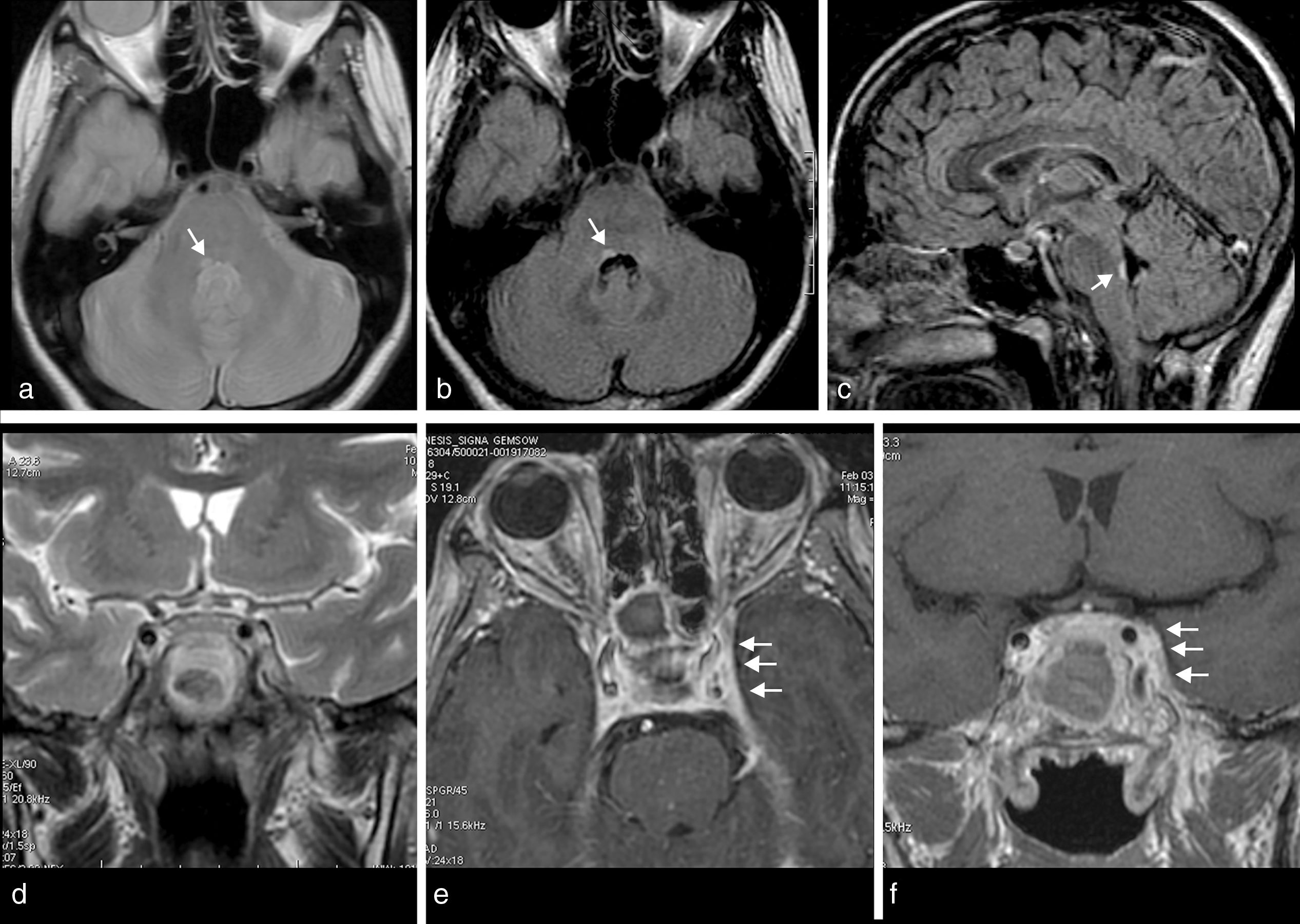
Paciente con esclerosis Múltiple. Cortes axiales DP (a), FLAIR (b) y sagital FLAIR (c) en una mujer de 27 años con paresia del VI nervio craneal derecho. Los cortes de RM muestran una placa de desmielinización hiperintensa adyacente al suelo del cuarto ventrículo en la localización del núcleo del VI nervio craneal. El estudio completo mostraba lesiones desmielinizantes típicas periventriculares y yuxtacorticales. Síndrome de Tolosa Hunt. Cortes coronal T2 (d), axial (e) y coronal (f) con gadolinio de paciente con cefalea, ptosis palpebral izquierda y paresia de III y IV nervios craneales izquierdos. El tratamiento con corticoides produjo una rápida mejoría clínica. Los cortes de RM muestran un engrosamiento del seno cavernoso izquierdo, con intenso realce, que se extiende hacia el ápex orbitario.
El IV NC, por su longitud, y el VI NC, por su trayecto ascendente posterior al clivus, son vulnerables a los traumatismos craneoencefálicos43,45,54. La afectación bilateral del VI NC puede ser secundaria a hipertensión craneal o a compresión de causa tumoral43,53. La prueba de imagen inicial es la TC, ya que generalmente estos pacientes son evaluados con carácter urgente.
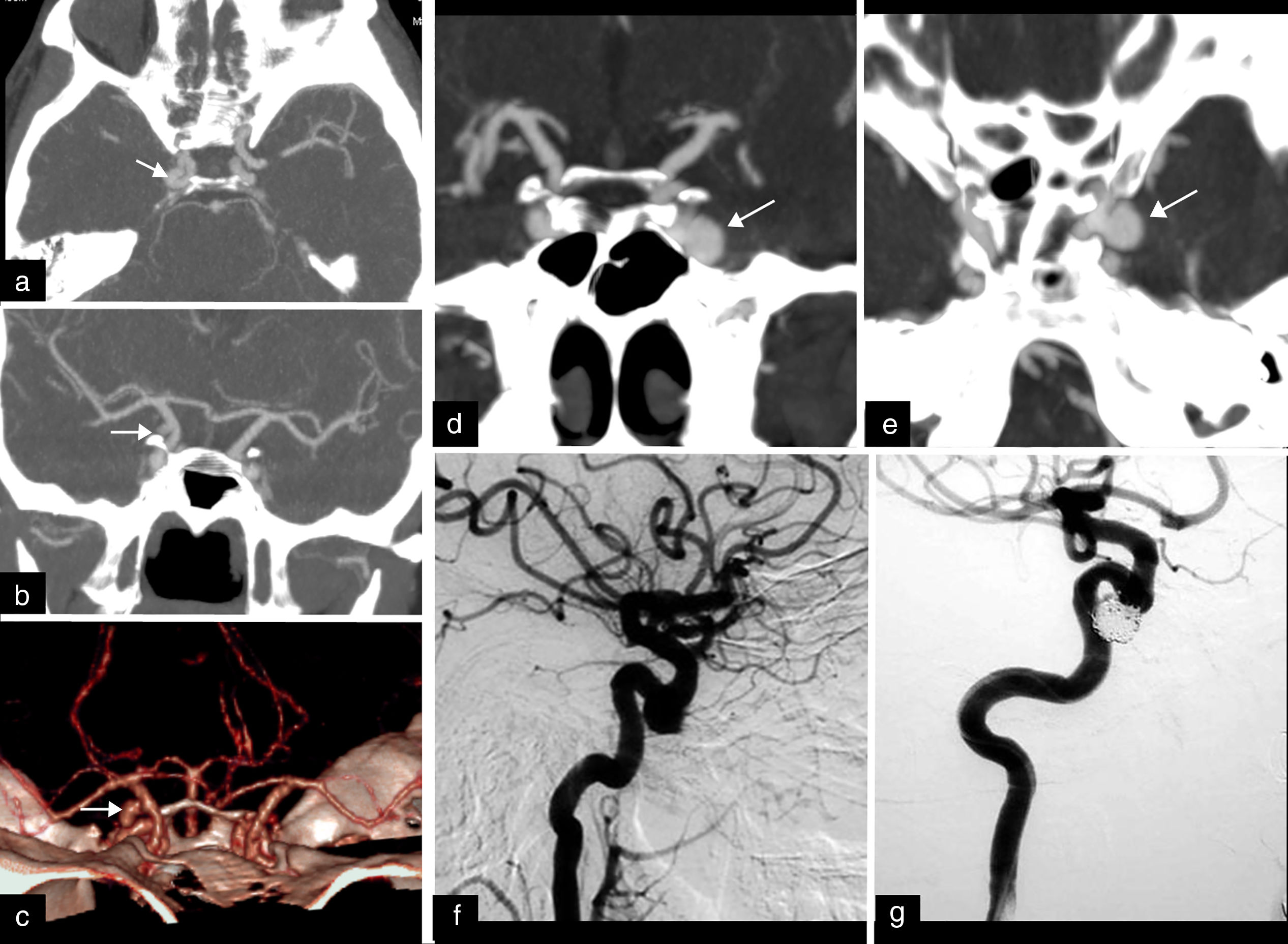
La parálisis completa del III NC asociada a disfunción pupilar, o la parálisis incompleta con o sin afectación pupilar, requieren la realización de angio-TC o angio-RM urgente para descartar un aneurisma, habitualmente localizado en la unión de la arteria comunicante posterior con la arteria carótida interna55,56,59. La Angio-TC, por su mayor disponibilidad en el ámbito de la urgencia, es la técnica más usada (fig. 10). El aneurisma de arteria carótida interna intracavernosa produce con mayor frecuencia parálisis del VI NC, debido a su proximidad dentro del seno cavernoso60.
Aneurismas. Reformateo de proyección de máxima intensidad axial (a), coronal (b) y 3D (c) de angio-TC en una mujer de 50 años que tras presentar cefalea progresiva de varias semanas de evolución acude a urgencias con parálisis completa de III nervio craneal derecho y pupila midriática. Pequeño aneurisma en la unión entre la arteria carótida interna y la comunicante posterior derechas en contacto con el III nervio craneal. Reformateo MIP axial (d) y coronal (e) de angio-TC e imágenes de arteriografía diagnóstica (f) y tras tratamiento (g) de un paciente de 48 años que acudió a urgencias con cefalea intensa de 2 días de evolución con vómitos y paresia del VI nervio craneal izquierdo. Se objetiva un aneurisma en la arteria carótida interna intracavernosa, justificando la compresión del VI nervio craneal. Se confirma mediante arteriografía y se observa el cierre completo del aneurisma tras la embolización.
Neoplasias, traumatismos craneoencefálicos graves o aneurismas de gran tamaño pueden producir afectación de varios NC54. La realización de TC o RM dependerá de la disponibilidad de cada una de ellas en el contexto clínico del paciente.
La patología del seno cavernoso (fístula carotidocavernosa, fístula dural, trombosis) puede producir afectación de varios NC o del VI NC junto con la vía simpática, por su cercanía a la arteria carótida interna3,5,45. La RM es la técnica más adecuada para su estudio. El síndrome de Tolosa-Hunt (fig. 9 d-f) es un diagnóstico clínico, consistente en dolor orbitario con oftalmoplejía homolateral (con mayor frecuencia III NC, seguido de los NC IV y VI), que afecta al seno cavernoso y puede extenderse al ápex orbitario60,61. En la RM se aprecian engrosamiento del seno cavernoso, abombamiento de su borde lateral e intenso realce tras la administración de gadolinio. El tratamiento con corticoides produce mejoría clínica y radiológica. En ocasiones los hallazgos pueden ser sutiles. Para asegurar su diagnóstico es preciso descartar otras causas de afectación del seno cavernoso62.
La oftalmoplejía internuclear consiste en la pérdida o la limitación de la aducción en un ojo y nistagmo horizontal durante la abducción del otro6. La RM muestra las lesiones en la localización del FLM, siendo las causas más frecuentes la esclerosis múltiple en las personas jóvenes y la isquemia en los ancianos4,6.
Defectos campimétricos bitemporalesLos defectos campimétricos bitemporales sitúan la patología en la región quiasmática, donde se produce la decusación de las fibras nasales que corresponden a las hemirretinas temporales.
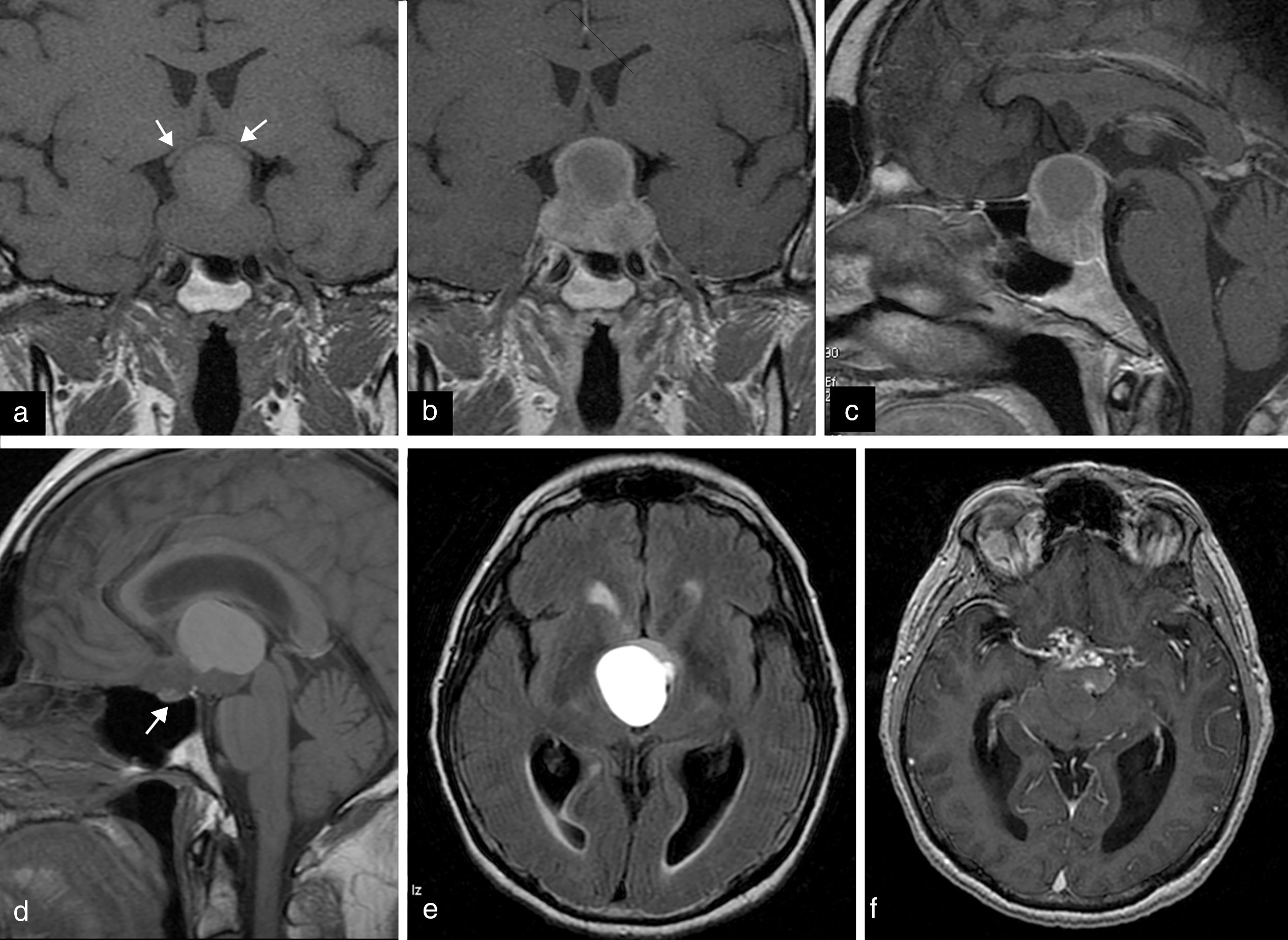
Tumores en la región selar y paraselar (fig. 11), entre ellos el más frecuente el adenoma hipofisario, pueden comprimir el quiasma óptico (tabla 6). Los propios gliomas del quiasma pueden ocasionar defectos campimétricos bitemporales asimétricos según las fibras afectadas. Las lesiones intraselares afectan a los campos temporales superiores, y las lesiones hipotalámicas o de la región del tercer ventrículo afectan a los inferiores3.
Macroadenoma hipofisario. Cortes coronal T1 (a), y coronal (b) y sagital T1 (c) con gadolinio, en un paciente de 59 años con hemianopsia bitemporal. Masa hipofisaria con componente intraselar y supraselar, con morfología en «muñeco de nieve», que comprime el quiasma óptico (flechas). El macroadenoma presenta un componente quístico hiperintenso en T1 que no se realza, a diferencia del resto de la lesión. Craneofaringioma. Cortes sagital T1 (d) y axiales FLAIR (e) y SPGRT1 (T1 spoiled gradient) con gadolinio (f), en un paciente de 61 años con afectación del campo visual derecho y temporal izquierdo. Masa supraselar con lesión quística y componente sólido que se realza con gadolinio. Obsérvese que, a diferencia del macroadenoma, la lesión comprime el quiasma desde arriba, y la hipófisis se encuentra comprimida en el fondo de la silla turca (flecha).
Causas de hemianopsia
| Hemianopsia bitemporal (región quiasmática) | |
|---|---|
| Adenoma hipofisario | Metástasis |
| Craneofaringioma | Pituicitoma |
| Meningioma | Cordoma de clivus |
| Glioma del quiasma | Linfoma |
| Aneurismas | Histiocitosis X |
| Disgerminoma | |
| Hemianopsia homónima (vías retroquiasmáticas y corteza occipital) | ||
|---|---|---|
| Vascular | Infarto | |
| Hematoma | Cintillas ópticas | |
| Tumoral | Núcleo geniculado lateral | |
| Inflamatoria | Enfermedad desmielinizante | Lóbulo occipital |
| Traumática | Lóbulo temporal | |
La técnica de elección para su valoración es la RM centrada en la región hipotálamo-hipofisaria18.
Hemianopsia homónimaLos defectos homónimos del campo visual implican lesiones de la vía visual retroquiasmática3 (tabla 6). Si la hemianopsia es congruente, la lesión se encontrará en la corteza occipital o próxima a ella, y si es incongruente, la lesión debe buscarse en las cintillas, el ganglio geniculado lateral o el asa de Meyer7.
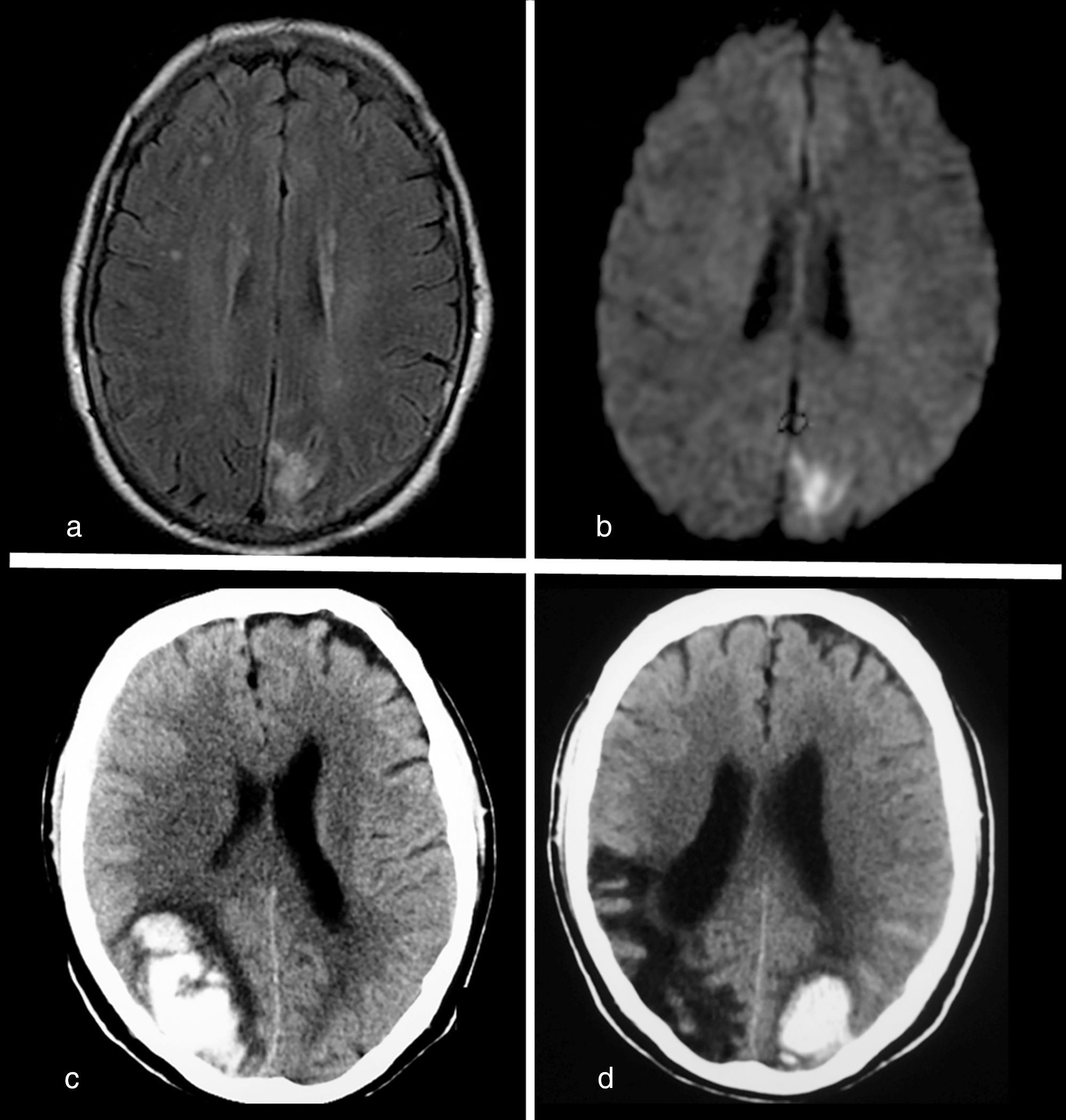
Los accidentes vasculares cerebrales son la causa más frecuente de hemianopsias homónimas aisladas63 (fig. 12). Estos defectos siempre deben ser estudiados radiológicamente, salvo que estén asociados claramente a un accidente vascular cerebral antiguo. Dado que los accidentes vasculares cerebrales producen clínica de instauración aguda, la TC craneal es la técnica inicial para valorar estos casos, especialmente si se sospecha hemorragia. Cuando la causa no se presupone vascular (tumores, enfermedad desmielinizante, etc.), la RM craneal aporta más información para llegar al diagnóstico correcto.
Infarto occipital agudo. Cortes axiales FLAIR (a) y en difusión (b) en un paciente que presenta alteración brusca de la visión, constatándose cuadrantanopsia homónima inferior derecha. Lesión hiperintensa en la corteza occipital izquierda que brilla en difusión. La lesión se encontraba por encima de la cisura calcarina. Hemorragias occipitales agudas. Corte axial de TC (c) en un paciente de 75 años que acude a urgencias con cefalea, vómitos y hemianopsia homónima izquierda, y corte axial de TC (d) del mismo paciente que acude un año más tarde con ceguera completa. En el primer estudio se visualiza el hematoma agudo occipital derecho que justifica la hemianopsia izquierda. En el estudio posterior se aprecian el área de encefalomalacia occipital derecha residual al hematoma previo y un nuevo hematoma occipital izquierdo que, al ocasionar la hemianopsia derecha, produce ceguera completa.
La afectación de la vía simpática cursa con leve ptosis, miosis y, en ocasiones, anhidrosis3,4. Si se sospecha afectación de primera neurona con síntomas cerebrales, deben realizarse RM y angio-RM cerebral, y si no hay síntomas cerebrales, la RM cervical es la elección. En el primer caso podríamos encontrar lesiones isquémicas, inflamatorias o tumorales en la región hipotalámica, y si la afectación es medular, siringohidromielia o neoplasias medulares. Para el estudio de la patología que afecta a la neurona preganglionar, la TC de cuello, incluyendo la encrucijada cervicotorácica, es más adecuada, ya que pueden encontrarse tumores del ápex pulmonar, bocio endotorácico, schwannomas o tumores neuroblásticos, y si hay afectación de neurona posganglionar debe realizarse TC o RM incluyendo secuencias vasculares con el fin de descartar patología arterial, como disección carotídea o lesiones en la región selar y paraselar8,64.
ConclusionesEl conocimiento de la anatomía de las vías ópticas, los NC y las vías autónomas implicados en la motilidad y una correcta información clínica son cruciales para la selección y la planificación de las exploraciones radiológicas. La clasificación de la patología según el signo o síntoma clínico más relevante en cada caso permite seleccionar la técnica de imagen adecuada teniendo en cuenta los diagnósticos diferenciales más habituales en cada grupo de pacientes.
Autoría- 1.
Responsable de la integridad del estudio: ACVM.
- 2.
Concepción del estudio: ACVM.
- 3.
Diseño del estudio: ACVM.
- 4.
Obtención de los datos: ACVM, PSM, CBL y BIH.
- 5.
Análisis e interpretación de los datos: ACVM, PSM, CBL y BIH.
- 6.
Tratamiento estadístico: no procede.
- 7.
Búsqueda bibliográfica: ACVM, PSM, CBL y BIH.
- 8.
Redacción del trabajo: ACVM.
- 9.
Revisión crítica del manuscrito con aportaciones intelectualmente relevantes: ACVM, PSM, CBL y BIH
- 10.
Aprobación de la versión final: ACVM, PSM, CBL y BIH.
Los autores declaran no tener ningún conflicto de intereses.
A Elena Marín y Ana Sarto, por la elaboración de los dibujos que aparecen en este trabajo.