En los últimos 25 años, la investigación científica ha cambiado drásticamente el concepto y el manejo clínico de la lumbalgia. La mayoría de los hallazgos por la imagen, incluyendo los degenerativos, reflejan peculiaridades anatómicas o propias del envejecimiento normal, y resultan clínicamente irrelevantes; las pruebas de imagen sólo han demostrado ser útiles cuando se sospecha enfermedad sistémica o existe indicación quirúrgica por compresión medular o radicular persistente. El informe radiológico debe indicar los puntos clave de la compresión neural, soslayando otros hallazgos intrascendentes. Muchos tratamientos han demostrado ser ineficaces, y algunos contraproducentes, pero existen incentivos económicos y demandas asistenciales para seguir prescribiéndolos. Aplicar las pautas de manejo clínico comprobadamente efectivas mejora los resultados clínicos, disminuye la iatrogenia y reduce el derroche injustificado de gastos sanitarios.
In the last 25 years, scientific research has brought about drastic changes in the concept of low back pain and its management. Most imaging findings, including degenerative changes, reflect anatomic peculiarities or the normal aging process and turn out to be clinically irrelevant; imaging tests have proven useful only when systemic disease is suspected or when surgery is indicated for persistent spinal cord or nerve root compression. The radiologic report should indicate the key points of nerve compression, bypassing inconsequential findings.
Many treatments have proven inefficacious, and some have proven counterproductive, but they continue to be prescribed because patients want them and there are financial incentives for doing them. Following the guidelines that have proven effective for clinical management improves clinical outcomes, reduces iatrogenic complications, and decreases unjustified and wasteful healthcare expenditures.
La lumbalgia mecánica se define como el dolor localizado entre las costillas y el límite inferior de las nalgas, habitualmente acompañado de limitación dolorosa del movimiento y en ocasiones de dolor referido o irradiado a los miembros inferiores (sea uno o ambos), originado en estructuras de la columna vertebral (vértebras, discos, músculos o ligamentos) y no causado por traumatismos directos, fracturas ni enfermedades sistémicas (infecciosas, endocrinológicas, metabólicas, renales, vasculares, digestivas ni ginecológicas)1.
Prevalencia y epidemiologíaLa lumbalgia es la principal causa de incapacidad en el mundo y uno de los principales motivos de gasto sanitario2. Su prevalencia vital entre la población general supera el 80%, pero la mayoría de los episodios («agudos») tienden a mejorar de manera espontánea y duran menos de 14 días3; si superan esta duración («subagudos»), aumenta la probabilidad de que se conviertan en crónicos (>90 días)4. El 20% de los pacientes crónicos generan más del 80% de los costes globales3.
EtiologíaAntiguamente se asumía que la lumbalgia se debía a sobreesfuerzos o a la existencia de alteraciones estructurales del raquis, tales como degeneración del disco, articulación facetaria o afectación de los cuerpos vertebrales. Las imágenes degenerativas observadas en los pacientes con dolor crónico no son más frecuentes ni más avanzadas que las que se ven en personas sanas sin lumbalgia5–8. Todo apunta a que la degeneración del disco y la vértebra es propia del envejecimiento normal, y suele resultar irrelevante y asintomática5,6. Sólo cuando excepcionalmente causa compresión nerviosa persistente puede requerir cirugía (p. ej., en casos de estenosis espinal sintomática por osteofitos o degeneración facetaria avanzada, con o sin espondilolistesis). Sin embargo, incluso en esos casos, lo patológico es la compresión y no la existencia de la degeneración en sí misma.
Los demás hallazgos radiológicos que se consideraban «enfermedades» (escoliosis, espondilólisis, espondilolistesis e incluso estenosis espinal o protrusión/hernia discal en ausencia de signos y síntomas de irritación o compresión nerviosa) no se asocian con la existencia de dolor ni modifican el tratamiento ni el pronóstico6–10.
El dolor lumbar se debe a una enfermedad sistémica en aproximadamente el 1% de los casos, a una compresión nerviosa causada por una protrusión/hernia discal o una estenosis espinal en el 4%, y en el 95% restante a un «síndrome inespecífico»1,8 en el cual el dolor nace de las partes blandas. En los casos inespecíficos, ninguna prueba de imagen permite localizar el origen anatómico exacto del dolor1,5,8, que se desencadena y persiste a causa de mecanismos funcionales indetectables mediante estas pruebas (disfunciones de la coordinación entre distintos grupos musculares, contractura, mecanismos neuroquímicos, etc.).
Si el dolor dura más de 14 días, se activan mecanismos neurofisiológicos que tienden a perpetuarlo, y que a partir de los 90 días pueden mantenerlo, aunque desaparezca la causa que inicialmente lo desencadenó4,11,12. Ciertos genes pueden influir en la facilidad con que se activan esos mecanismos, así como en el ritmo de degeneración de las estructuras raquídeas11,12, pero esto último no ha demostrado tener ninguna trascendencia clínica5,8. En el riesgo de cronificación también influye la falta de potencia o de coordinación de la musculatura13,14.
Presentación clínicaEl síntoma fundamental es el dolor raquídeo de características mecánicas (influido por posturas, movimientos y esfuerzos), en ocasiones asociado a dolor referido o irradiado. La anamnesis identifica los casos de claudicación neurógena típica de la estenosis espinal (dolor irradiado a las nalgas o las piernas, tanto a una como a ambas, que aparece progresivamente con la deambulación, hasta impedirla, y desaparece rápido en sedestación). La exploración física permite detectar los signos de afectación radicular (dolor irradiado, a veces con hipoestesia, anestesia o parestesia a lo largo del dermatomo correspondiente, paresia, hiporreflexia o arreflexia en el miotomo correspondiente, y signos exploratorios característicos –Lasègue < 60°, Bragard, Brudzinsky–) que distinguen entre los casos debidos a compresión radicular por protrusión o hernia discal y los síndromes inespecíficos.
En la repercusión psicológica del dolor puede influir la personalidad del paciente, pero también la información proporcionada15,16; transmitir que un hallazgo degenerativo es una «lesión irreversible que sólo puede empeorar» (sin explicar su irrelevancia, salvo que cause compresión nerviosa), hace que la persona se sienta peor15,16.
Diagnóstico y diagnóstico diferencialEl proceso diagnóstico se basa en la anamnesis y la exploración física1,5,8. Su objetivo no es identificar el origen anatómico o histológico exacto del dolor, que no tiene relevancia pronóstica1,7–10, sino clasificar a cada paciente en uno de los tres grupos que determinan su orientación clínica óptima: a) pacientes en quienes el dolor puede deberse a una enfermedad sistémica, b) pacientes con compresión nerviosa (medular o radicular) subsidiaria de cirugía (urgente o electiva) y c) pacientes con «síndromes inespecíficos» cuyo dolor no se debe a enfermedad sistémica ni a compresión nerviosa. En este último caso, prescribir una prueba complementaria constituye una mala práctica clínica, pues no contribuye al diagnóstico, al tratamiento ni al pronóstico, y genera riesgos y perjuicios innecesarios, tales como cirugía inapropiada, exposición a dosis innecesarias de radiación, costes superfluos (para el paciente –en la sanidad privada– o para los contribuyentes –en la pública–) y empeoramiento injustificado de la sensación de bienestar17,18.
Técnicas de imagen: en qué casos están indicadasLegalmente, la responsabilidad de la adecuación de las pruebas diagnósticas por imagen recae en los radiólogos19. Por lo tanto, estos no deben prestarse a realizar técnicas ineficaces y peligrosas, como la discografía20, ni técnicas efectivas en casos inapropiados16–18. Hasta el 80% de las prescripciones de resonancia magnética (RM) por dolor lumbar que se hacen en nuestro país son inapropiadas21, y un 27% son absolutamente injustificables18. Sin contar el efecto de los demás factores (clínicos, etc.), la probabilidad de que una RM lumbar sea inapropiada es un 250% mayor en la sanidad privada que en la pública18.
En la lumbalgia, ninguna prueba de imagen es inocua. La radiografía y la tomografía computarizada (TC) irradian significativamente; el aumento de las TC realizadas entre 1980 y 2006ha incrementado un 600% la dosis media anual de radiación, y causará el 2% de los futuros cánceres22. Dadas sus múltiples ventajas, debe usarse la RM. Sin embargo, esta detecta muchos hallazgos irrelevantes que se interpretan de manera errónea como patológicos y llevan a tratamientos inapropiados; así, una RM mal indicada aumenta un 200-800% el riesgo de que el paciente sea innecesariamente operado17.
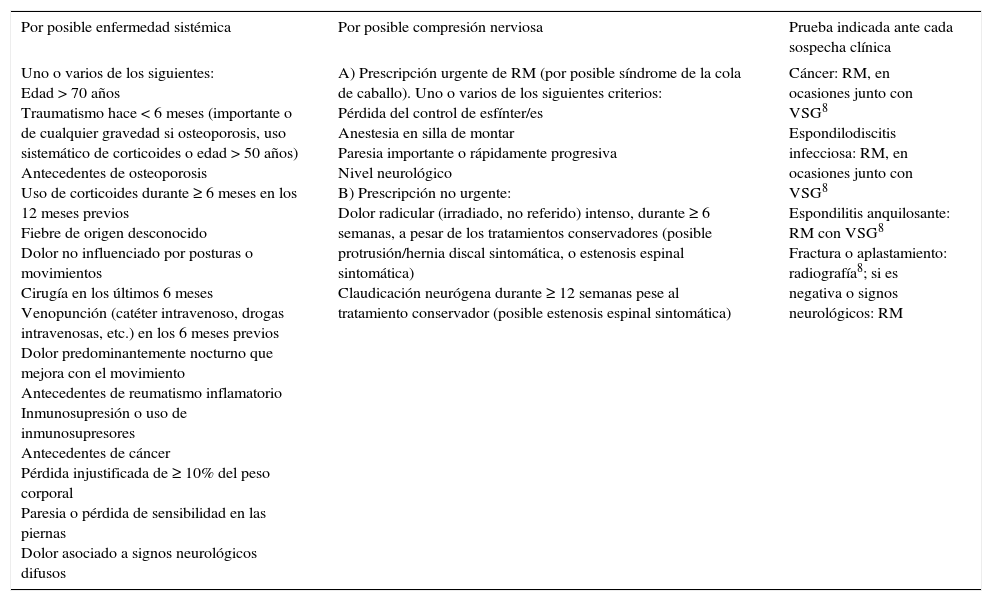
Todas las guías de práctica clínica basadas en el conocimiento científico recomiendan prescribir la RM sólo en dos casos: cuando existen signos de que puede deberse a una enfermedad sistémica o cuando está indicada la cirugía (tabla 1)7,9.
Criterios para valorar la prescripción de pruebas complementarias en pacientes con lumbalgia
| Por posible enfermedad sistémica | Por posible compresión nerviosa | Prueba indicada ante cada sospecha clínica |
|---|---|---|
| Uno o varios de los siguientes: Edad > 70 años Traumatismo hace < 6 meses (importante o de cualquier gravedad si osteoporosis, uso sistemático de corticoides o edad > 50 años) Antecedentes de osteoporosis Uso de corticoides durante ≥ 6 meses en los 12 meses previos Fiebre de origen desconocido Dolor no influenciado por posturas o movimientos Cirugía en los últimos 6 meses Venopunción (catéter intravenoso, drogas intravenosas, etc.) en los 6 meses previos Dolor predominantemente nocturno que mejora con el movimiento Antecedentes de reumatismo inflamatorio Inmunosupresión o uso de inmunosupresores Antecedentes de cáncer Pérdida injustificada de ≥ 10% del peso corporal Paresia o pérdida de sensibilidad en las piernas Dolor asociado a signos neurológicos difusos | A) Prescripción urgente de RM (por posible síndrome de la cola de caballo). Uno o varios de los siguientes criterios: Pérdida del control de esfínter/es Anestesia en silla de montar Paresia importante o rápidamente progresiva Nivel neurológico B) Prescripción no urgente: Dolor radicular (irradiado, no referido) intenso, durante ≥ 6 semanas, a pesar de los tratamientos conservadores (posible protrusión/hernia discal sintomática, o estenosis espinal sintomática) Claudicación neurógena durante ≥ 12 semanas pese al tratamiento conservador (posible estenosis espinal sintomática) | Cáncer: RM, en ocasiones junto con VSG8 Espondilodiscitis infecciosa: RM, en ocasiones junto con VSG8 Espondilitis anquilosante: RM con VSG8 Fractura o aplastamiento: radiografía8; si es negativa o signos neurológicos: RM |
RM: resonancia magnética; VSG: velocidad de sedimentación globular.
Los signos y síntomas que sugieren una enfermedad sistémica son muy sensibles, pero muy poco específicos; si un paciente no presenta ninguno, puede descartarse ese riesgo con total certeza y resulta un error prescribir una prueba diagnóstica1,7,8,18,23. A la inversa, en los pacientes que muestran uno o varios no tiene sentido prescribir sistemáticamente una prueba diagnóstica, sino sólo valorar si está indicada23. La prueba más apropiada depende de la sospecha clínica (tabla 1).
En los pacientes con signos clínicos de indicación quirúrgica, la RM debe ser urgente únicamente si se sospecha «síndrome de la cola de caballo», lo que sucede en siete de cada 100.000 que presentan paresia muy importante, bilateral o rápidamente progresiva, anestesia en silla de montar o pérdida súbita de control de los esfínteres o de la erección1,7,8,23. Las demás indicaciones quirúrgicas no son urgentes, por lo que tampoco lo es la RM24,25. En estos casos, el principal objetivo de la RM es contribuir a planificar la cirugía, por lo que salvo excepciones o motivos organizativos (listas de espera) no está indicada prescribirla antes de 6-12 semanas en caso de compresión radicular por hernia discal ni en 3-6 meses en caso de compresión radicular por estenosis espinal18,25.
Protocolo de imagenEn el estudio de RM debe explorarse desde el cono medular hasta el sacro, en un equipo con antena de múltiples elementos específica. Para mostrar mejor el edema puede usarse una secuencia potenciada en T2 con saturación grasa o STIR. Los planos axiales deben orientarse al plano discal y abarcar toda la extensión craneocaudal de la anomalía. En la (tabla 1, online) se propone un protocolo de los varios existentes.
Qué debe informarse en el estudio de imagenSólo hay que reseñar aquello que contribuya a optimizar el tratamiento (tabla 2), básicamente hallazgos que causen compresión con desplazamiento de estructuras neurales26 (fig. 1). Las alteraciones discales deben informarse de forma normalizada, y en caso de hernia discal, se indicará si el disco está secuestrado o no27,28. Los niveles deben situarse con respecto al plano sagital (fig. 2) y hay que informar siempre las variedades anatómicas a tener en cuenta en la cirugía (p. ej., vértebras supernumerarias)29. En este último caso existen variaciones numéricas entre cuatro y seis vértebras lumbares30, y debemos decir el número de las vértebras con morfología lumbar, situar la anomalía de imagen en el aparente nivel (p. ej., hernia central posterior en L5L6) y recomendar el recuento anatómico de todo el raquis30. Los últimos estudios indican que las anomalías de transición son igual de frecuentes en los pacientes sintomáticos que en la población general31, aunque su papel como etiología de los síntomas es debatido, y para una clasificación académica con fines de investigación se prefiere la de Castellvi30,31.
Elementos imprescindibles en el informe de la patología degenerativa de la columna lumbar
| • Variante anatómica que condicione una posible cirugía (p. ej., vértebra supernumeraria). |
| • Desplazamiento discal, quiste interfacetario o cualquier estructura que comprima una estructura neural26,44. |
| • Alteraciones discales según clasificación normalizada27,28. |
| • Estenosis >1/3 del conducto espinal central o recesos radiculares, siempre indicando su correlación con la historia clínica30. |
| • Espondilolistesis que se asocie a estenosis neuroforaminal32,44. |
| • Edema o transformación de médula ósea indicativos de espondilitis inflamatoria o infecciosa. |
| • Cualquier fractura aguda o crónica, aunque no esté mencionada en la hipótesis diagnóstica. |
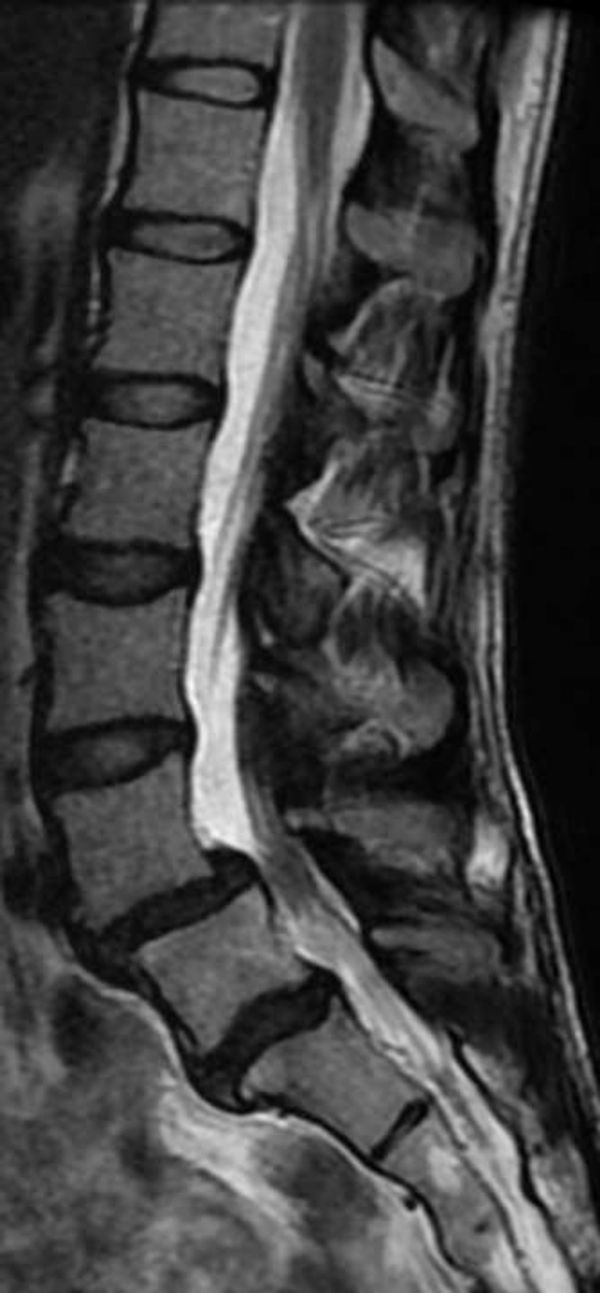
Imagen sagital potenciada en T2. Paciente asintomática a quien se realizó una resonancia magnética de columna dorsal y lumbar por un traumatismo torácico superior. Espondilolistesis de grado I en L4L5 con estenosis moderada (> 1/3) del conducto espinal. Signos involutivos en L5S1.
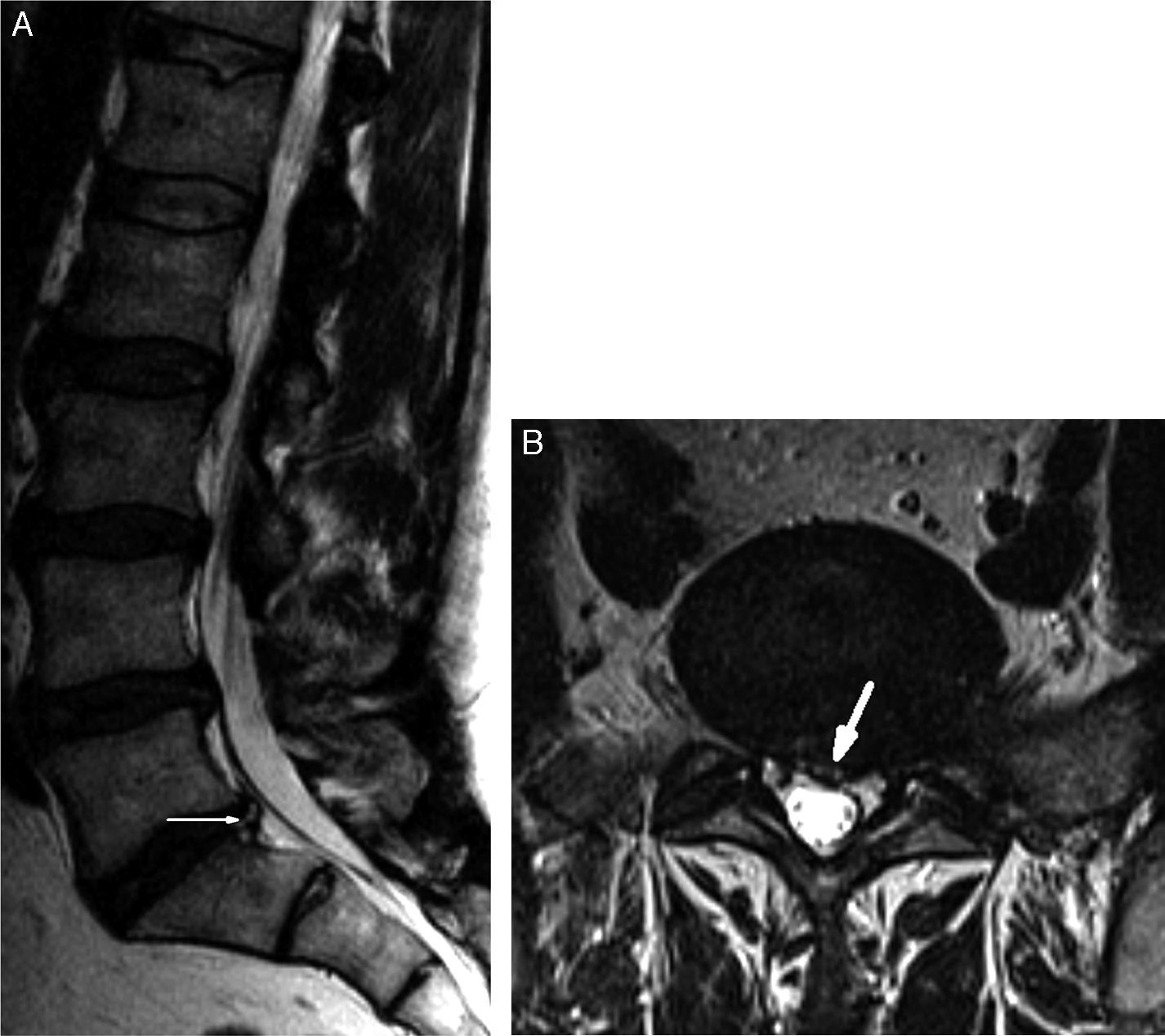
A) Imagen sagital potenciada en T2. Se aprecia hernia discal en L5S1, no secuestrada, emigrada caudalmente, en nivel discal y suprapedicular S1. B) Imagen axial potenciada en T2. Hernia discal centrolateral izquierda que comprime la raíz S1 homolateral. Produce estenosis de > 1/3 del conducto espinal en su porción central y completa del receso radicular.
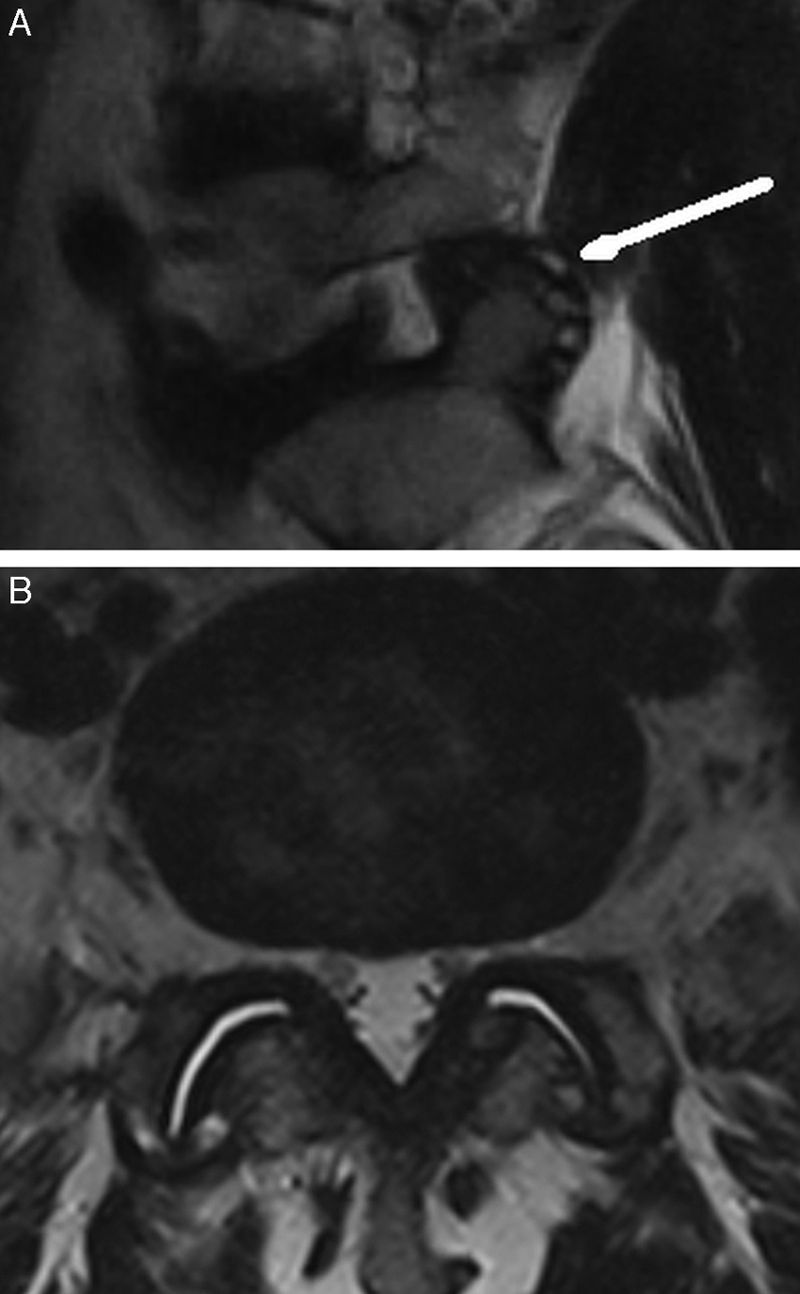
Las imágenes discales de fisura del anillo fibroso, consideradas antaño diagnósticas de dolor «discogénico», son igualmente frecuentes en sujetos asintomáticos y no deben informarse5 (fig. 3).
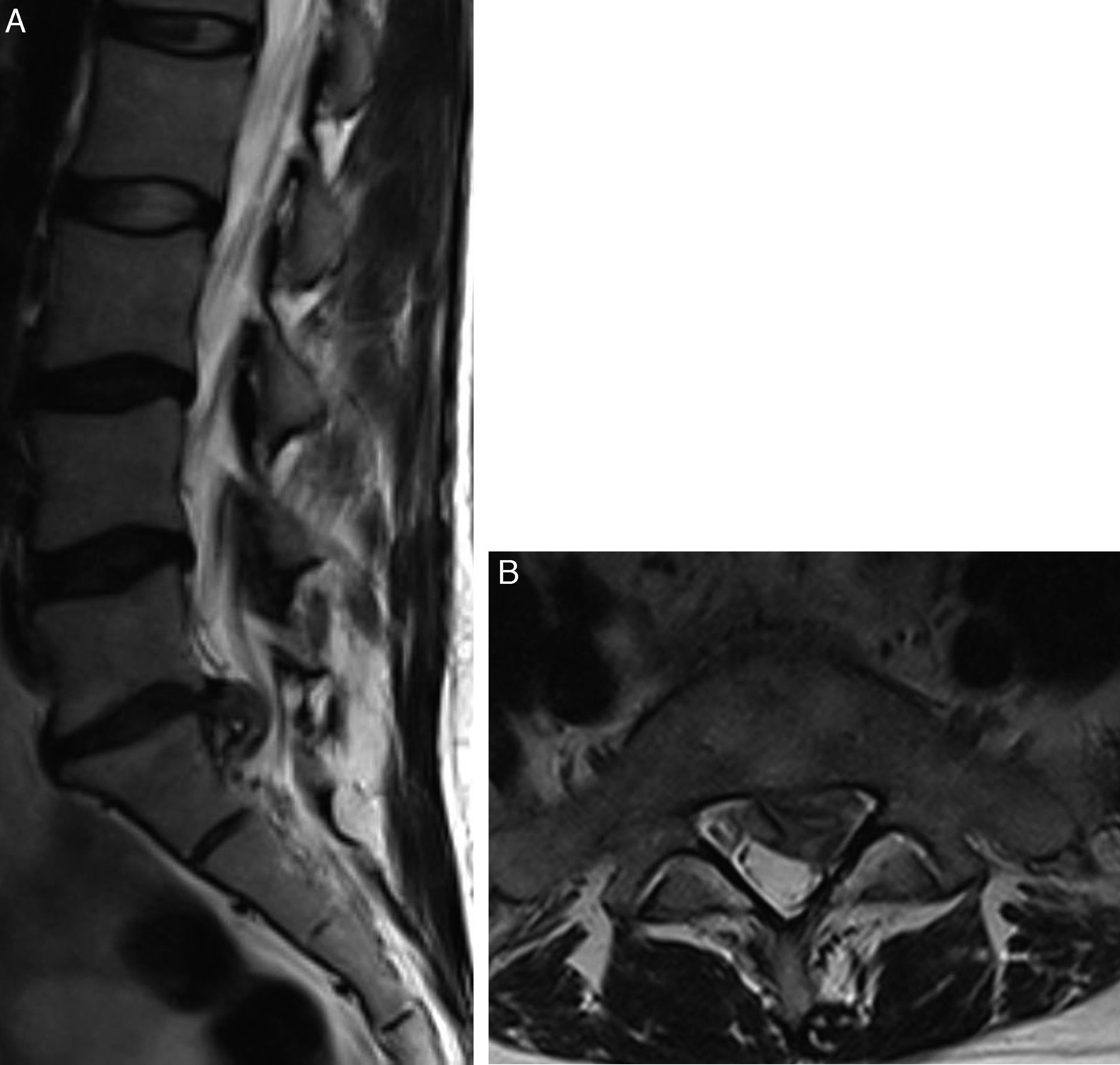
A) Imagen sagital potenciada en T2. Fisura del anillo fibroso en L5S1 (flecha). Nótense las protrusiones discales en los discos superiores, dentro del proceso involutivo fisiológico. B) Imagen axial potenciada en T2. Rotura del anillo fibroso (flecha). Nótense también los hallazgos normales involutivos en las articulaciones interapofisarias.
La estenosis espinal radiológica (conducto espinal <10mm de diámetro) es un hallazgo casual frecuente en personas asintomáticas (21% en mayores de 60 años)32. Sólo puede ser clínicamente relevante si existe claudicación neurógena o dolor irradiado en un trayecto concordante. El grado de estenosis central o de los recesos laterales debe describirse mediante una escala simple: leve, moderada y grave (1/3, 2/3 o todo el diámetro correspondiente)32. En caso de que las imágenes no concuerden con una sospecha clínica sólida de estenosis espinal, conviene considerar una RM dinámica, aunque su utilidad es controvertida33. La espondilolistesis sólo resulta relevante si causa o complica una estenosis espinal34,35; en ausencia de clínica de estenosis espinal, su presencia es irrelevante10,34.
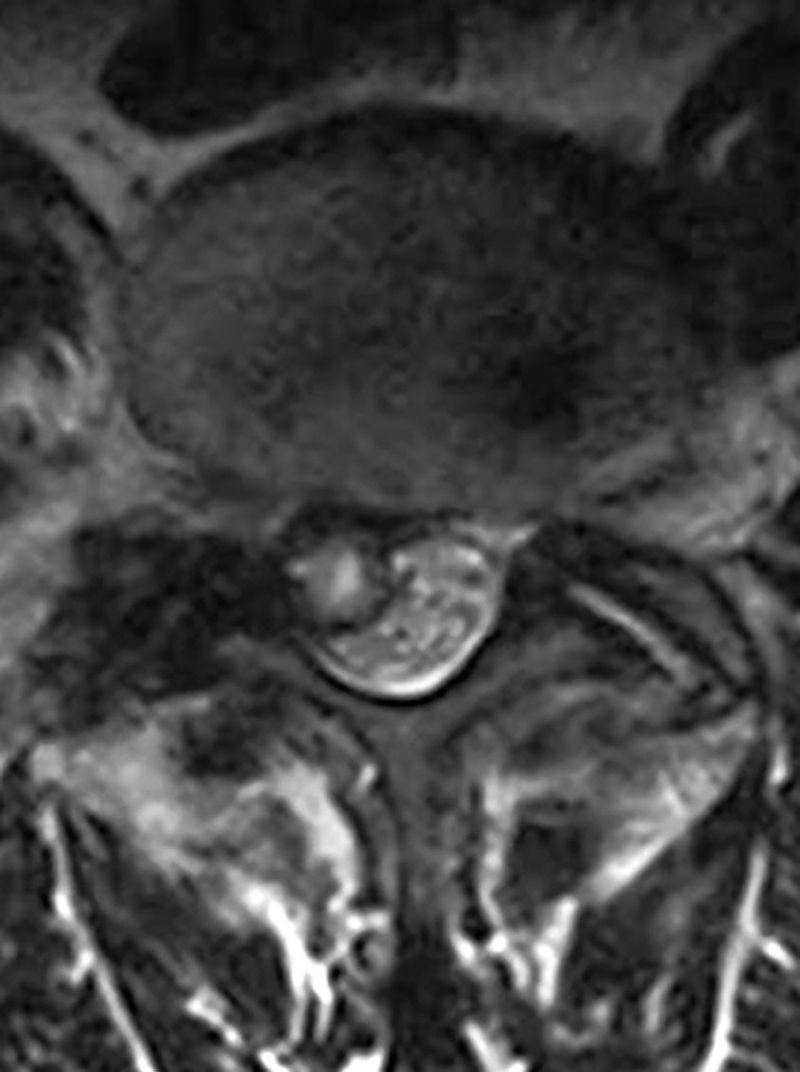
Respecto a la espondiloartrosis, aunque puede valorarse tanto por TC como por RM, ambas la infraestiman35. Sin embargo, su relevancia clínica también es escasa o nula5, además de que un 33% de los pacientes asintomáticos presentan estenosis foraminal debida a ella (fig. 4). Sólo deben señalarse las imágenes que muestren compresión mielorradicular, como por ejemplo un quiste interfacetario (fig. 5).
A) Detalle de una imagen sagital potenciada en T2 que muestra microquistes subcondrales interfacetarios en L5S1. B) Imagen axial potenciada en T2. Nótense el mínimo líquido en ambas articulaciones interfacetarias y los microquistes subcondrales. Estos hallazgos son igualmente prevalentes en población asintomática.
Imagen axial potenciada en T2. Se aprecia un quiste interfacetario en la articulación L4L5 derecha que provoca estenosis del conducto espinal de 2/3 y completa del receso radicular homolateral. Nótese la asimetría de la espondiloartrosis, pero el hallazgo relevante a mencionar es el quiste interfacetario.
No hay que realizar técnicas intervencionistas diagnósticas ni terapéuticas con inyección de fármacos, pues no han mostrado su eficacia36. Ninguna prueba científica sugiere que la «inestabilidad» (por la que en el pasado se prescribían radiografías dinámicas) tenga significación clínica ni definición por la imagen5,37. Los signos Modic están relacionados con la degeneración discal anexa5,10. De los tres que existen, el tipo I se ha asociado en determinadas poblaciones del norte de Europa con mayor sintomatología, aunque no influyen en el pronóstico a largo plazo37. Sin embargo, en nuestro medio es más prevalente el tipo II, pero ninguno de ellos se ha asociado con lumbalgia10 ni en ningún sitio del mundo existe evidencia de asociación con sintomatología38, por lo que todavía son analizados en estudios poblacionales5.
Por lo tanto, no deben informarse hallazgos que resultan clínicamente intrascendentes (como degeneración discal, signos Modic o espondilolistesis que no cause estenosis espinal) salvo que se indiquen de manera explícita su irrelevancia y la ausencia de importancia pronóstica, o que se aporten datos sobre su prevalencia en los sujetos sanos15,16.
Pruebas neurofisiológicasLo que puede modificar el tratamiento y el pronóstico del paciente son la duración y la relevancia clínica de la compresión radicular, no el resultado de las pruebas neurofisiológicas39. Por eso, resultan inútiles cuando los signos y los síntomas ya demuestran la existencia de una compresión nerviosa clínicamente relevante y no existen dudas sobre su origen y localización. Y también son inútiles cuando la exploración física descarta una compresión clínicamente relevante (pues el tratamiento y el pronóstico del paciente serían los mismos fueran cuales fueran los resultados del electromiograma)1,7,8.
Únicamente resultan útiles en aquellos casos en que la exploración física detecta signos que sugieren una afección neurológica independiente del dolor de espalda, o cuando los antecedentes dificultan discriminar qué parte de los hallazgos se debe a la posible compresión radicular y cuál a otras afecciones o secuelas (p. ej., paresia clínicamente perceptible en un paciente con secuelas de poliomielitis infantil). En estos casos, las pruebas neurofisiológicas ayudan a determinar el origen de los déficits y a distinguir las lesiones agudas de las crónicas1,7,8.
Incluso en los casos (infrecuentes) en que las pruebas neurofisiológicas ayudan en la valoración inicial del paciente, es excepcional que sea necesario repetirlas más adelante.
TratamientoEl «tratamiento» se refiere a la desaparición o la mejoría del episodio doloroso en curso. Las medidas destinadas a reducir el riesgo de recurrencias se consideran «prevención».
Se han propuesto más de 200 tratamientos distintos, incluyendo fármacos, procedimientos físicos, tecnologías mínimamente invasivas, y técnicas y dispositivos quirúrgicos. En la (tabla 2, online) se indican los tratamientos más habituales, identificando por separado aquellos cuya eficacia o efectividad ha sido comprobada científicamente. En el caso de los episodios agudos (de menos de 14 días), los principales tratamientos con ese respaldo científico son1,7,8 evitar el reposo en cama, mantener el mayor grado de actividad que el dolor permita, probablemente aplicar calor local y los antiinflamatorios no esteroideos. En los casos subagudos y crónicos (>14 o > 90 días de duración, respectivamente)4, en los que el uso de antiinflamatorios debe restringirse a los periodos en que el dolor es más intenso, los tratamientos7,8 consisten en el ejercicio, la intervención neurorreflejoterápica (que es el único que ha demostrado mejorar la resolución del episodio y, además, el pronóstico del paciente a medio plazo)10, la capsaicina tópica, los antiepilépticos y la cirugía descompresiva en los casos concretos de compresión radicular en que está indicada. Muy pocos de ellos cuentan con pruebas científicas sobre su eficiencia y sólo uno está sometido a mecanismos sistemáticos de vigilancia postimplantación en nuestro Sistema Nacional de Salud (SNS), que informan sobre su seguridad, su verdadero efecto clínico y su impacto económico en la práctica clínica7,8,40.
La alta prevalencia de las dolencias de la espalda genera enormes incentivos económicos, y la mayoría de los demás tratamientos se aplican asistencialmente sin haberse evaluado antes, o incluso después de haber demostrado ser inútiles, contraproducentes y hasta letales1,7,41,42. Esa falta de rigor y control causa un ingente derroche de recursos (públicos) y una morbimortalidad innecesaria42. El 60,12% de los pacientes a quienes se aplicaron tratamientos rehabilitadores costeados con fondos públicos en un servicio autonómico del SNS entre 2004 y 2007 recibieron tratamientos carentes de fundamento científico, incluyendo algunos comprobadamente inútiles en el 23,06%41. Tal vez el caso más paradigmático, por su frecuencia, agresividad, riesgos y costes, sea el de la cirugía en pacientes sin dolor irradiado ni signos de compresión radicular, cuyo dolor raquídeo se atribuye a «degeneración discal» pese a haberse demostrado que esta no es una causa verosímil de dolor5–8, y a quienes se realiza una artrodesis lumbar (típicamente instrumentada) o se coloca una prótesis discal, aunque se ha comprobado que estas técnicas no son más efectivas que el ejercicio intenso7,8,43–45.
Prevención primaria y secundariaLa prevención primaria pretende que el dolor no aparezca en quienes no lo han padecido previamente; la secundaria, que su duración sea tan breve y su impacto tan leve como resulte posible. También puede considerarse como prevención secundaria la adopción de medidas destinadas a reducir la repetición de los episodios dolorosos.
Hasta hoy, ninguna medida ha demostrado sólidamente ser efectiva para la prevención primaria del dolor de espalda. Las dos que cuentan con mayor soporte científico son el ejercicio (de cualquier tipo –no necesariamente centrado en la musculatura directamente implicada en el funcionamiento de la espalda–) y la educación en «manejo activo» (este se centra en transmitir al paciente que debe mantenerse tan físicamente activo como le sea posible y, en caso de dolor, evitar o reducir al máximo el reposo en cama y mantener el mayor grado de actividad física que permita el dolor)7,8,43. Por el contrario, la educación en «higiene postural» ha demostrado resultar inútil7,8,43.
Para la prevención secundaria también ha demostrado ser efectivo el ejercicio (de cualquier tipo, aunque algunos datos señalan que los ejercicios específicos podrían ser algo superiores)7,8,14, y la educación en manejo activo ha demostrado ser mucho más efectiva que la centrada en la higiene postural (cuyo efecto, si lo tiene, es nimio)43. La magnitud del efecto de la educación en manejo activo no aumenta significativamente si se añade un programa de fisioterapia que requiere ocho veces más tiempo43.
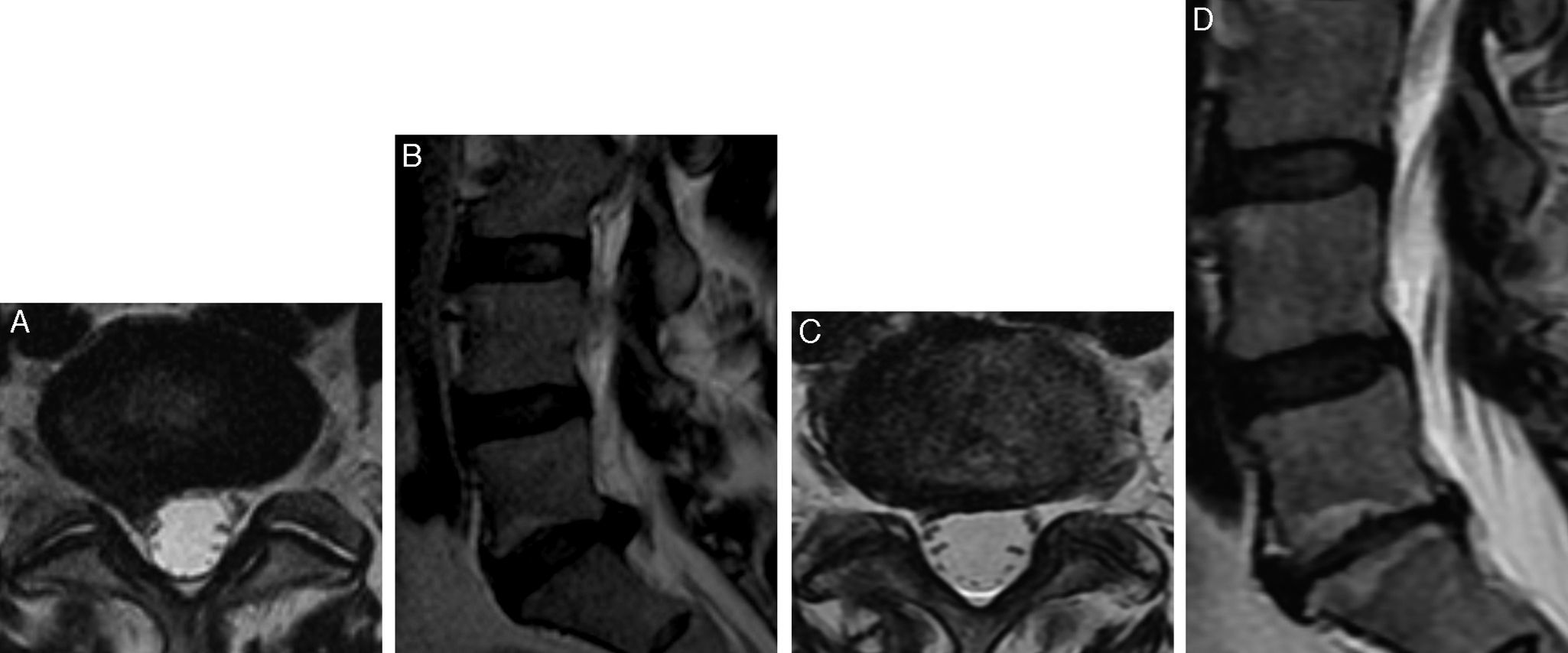
Los datos emanados de la vigilancia postimplantación de la intervención neurorreflejoterápica en el SNS sugieren que este es el único tratamiento médico-quirúrgico que mejora la resolución del episodio, y además influye de manera positiva en la evolución del paciente a medio plazo y en la reducción de las recurrencias10. Las pruebas científicas disponibles reflejan que la cirugía descompresiva tiene un efecto positivo en ciertos pacientes cuidadosamente seleccionados por presentar signos de compresión radicular persistente debida a hernia discal o estenosis espinal. A diferencia de lo que sucede en los casos de hernia discal sintomática, la evolución de los pacientes con compresión radicular debida a estenosis espinal sintomática que son operados es mejor que la de los no operados durante al menos 4 años (y tal vez 10 años)24,25. Asimismo, tenemos que recordar que en el 63% de los pacientes con hernia discal lumbar se produce una disminución espontánea de esta sin tratamiento46 (fig. 6). No obstante, la cirugía no ha demostrado tener ningún efecto preventivo, por lo que carece de sentido plantearla en un paciente que no tiene en ese momento criterios de indicación quirúrgica, por el temor a que estos aparezcan en el futuro, o que entonces operarlos sea más difícil o arriesgado.
Desaparición espontánea de una hernia discal. Paciente de 47 años de edad con lumbociatalgia derecha. Se le propuso tratamiento conservador y fue estudiado al año, con remisión completa de la sintomatología a los 6 meses tras el inicio. A) Imagen axial potenciada en T2. Hernia discal centrolateral derecha, que contacta con la raíz S1 homolateral. B) Imagen sagital potenciada en T2. Hernia discal centrolateral derecha, que contacta con la raíz S1 homolateral. C) Imagen axial potenciada en T2. Protrusión discal difusa con reabsorción de la hernia discal. D) Imagen sagital potenciada en T2. Desaparición de la hernia discal centrolateral derecha. Nótese la progresión de los cambios Modic II, correlacionados con la degeneración discal, pero no con la etiología del dolor.
El uso adecuado de las técnicas de imagen, fundamentalmente de la RM, debe hacerse en población con una indicación clínica seleccionada. Sólo así los radiólogos proporcionaremos la información en imagen, clínicamente adecuada, para la patología lumbar degenerativa (tabla 2). De esta forma daremos un servicio eficiente con un uso adecuado de los recursos, que son elementos decisivos en el tratamiento de estos pacientes.
Conflicto de interesesLos autores declaran no tener ningún conflicto de intereses.