INTRODUCCION
Ante un aplastamiento vertebral hemos de considerar que nos encontramos ante una fractura vertebral, estos dos términos han de considerarse sinónimos, aunque hay quien reserva el término de aplastamiento al colapso total del cuerpo vertebral.
CASO CLINICO
Se trata de un varón de 83 años con antecedentes de prostatismo, hipertensión arterial y ulcus duodenal, que es remitido por aplastamiento vertebral L3. El enfermo refiere debilidad progresiva de 3 meses de evolución con pérdida de fuerza y sensibilidad en pierna izquierda, con disestesias que le ocasionan dificultad para la deambulación y dolor de características inflamatorias en la zona lumbar, L3. A pesar del tratamiento con paracetamol y antiinflamatorios no presenta mejoría. No refiere síndrome febril ni sensación distérmica. En la exploración destaca palidez cutánea, delgadez con conservación del estado general, hiperreflexia rotuliana y aquilea izquierda, plantar izquierdo extensor, con disminución de sensibilidad en el tercio inferior de la pierna izquierda, dolor a la presión de apófisis espinosa lumbar nivel L3.
Los estudios complementarios realizados fueron: hemoglobina: 9,7; hematíes: 3,2; velocidad corpuscular media: 90; plaquetas: 272.000; leucocitos: 11.900 (N: 76%); glucemia: 96; urea: 118; creatinina: 1,7; Na: 140; K: 4,8; calcemia: 10; GOT: 27; GPT: 12; GGT: 148; FA: 131; beta2microg: 5,55; IQuick: 100%. Marcadores tumorales (antígeno carcinoembrionario, alfa-fetoproteína), PSA, y proteinograma dentro de la normalidad. La ecografía de abdomen destaca la presencia de hipertrofia de próstata. La cistoscopia con realización de biopsias vesicales estaba dentro de la normalidad. Gastroscopia y colnoscopia alcanzando válvula ileocecal: dentro de la normalidad. La radiología de columna lumbar muestra aplastamiento vertebral L3 (fig. 1). La imagen por resonancia magnética (IRM) de columna lumbar refleja aplastamiento vertebral L3 con gran componente de partes blandas que penetra en canal medular y provoca su estenosis (fig. 2). Se realiza biopsia de masa paravertebral guiada por tomografía que es informada como tumor mesenquimal pleomórfico maligno, los cultivos de la muestra en medios habituales y la tinción de Ziehl- Nielssen resultaron negativos. El enfermo desestima realización de nueva biopsia o cualquier otra actitud invasiva, decidiéndose tratamiento sintomático.
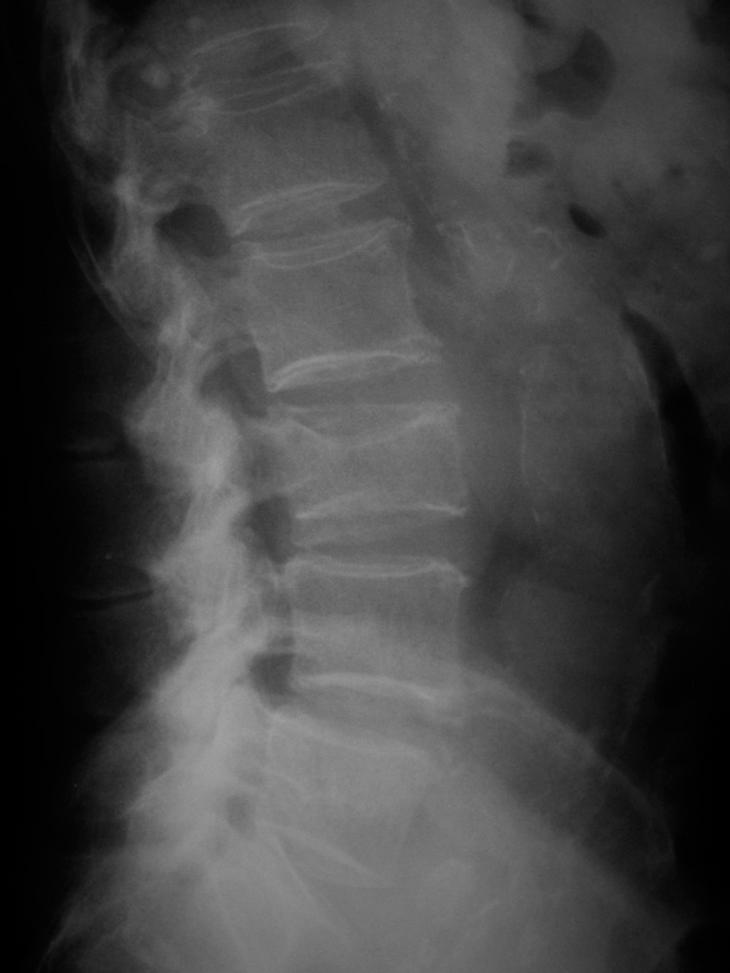
Fig. 1. Aplastamiento vertebral.
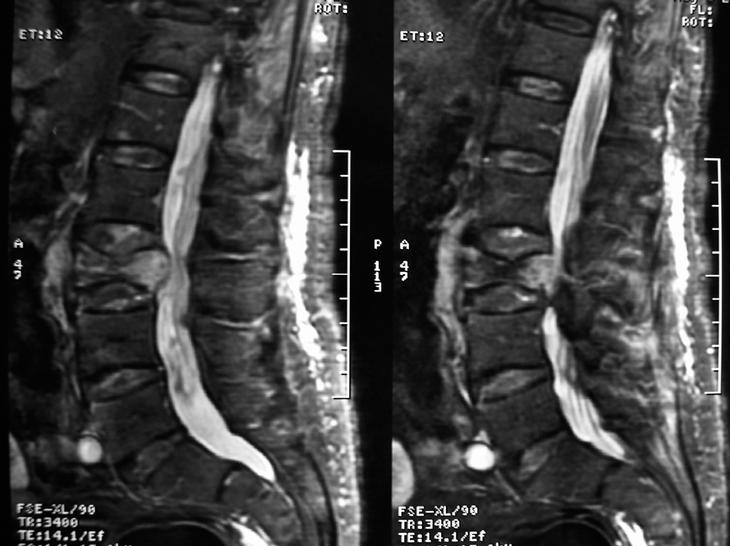
Fig. 2. Aplastamiento vertebral L3 con gran componente de partes blandas, que penetra en canal medular y provoca su estenosis.
DISCUSION
Entendemos por aplastamiento vertebral aquella pérdida de altura de la parte anterior del cuerpo vertebral o de su porción central en al menos un 20% con respecto a la altura de la porción posterior o con respecto a vértebras adyacentes. Otros criterios lo rebajan al 10% o a una diferencia de 2 mm de la altura de la pared anterior o central de la altura de la parte posterior; o como una disminución superior a tres desviaciones estándar de las medidas de referencia1-3.
Si agrupamos las causas de aplastamiento vertebral en función de su etiología tendremos: secundarias a traumatismo, secundarios a infección, debidas a alteraciones del metabolismo óseo, fracturas debidas a invasión neoplásica. El problema fundamental es establecer la diferencia entre las dos causas más frecuentes de las fracturas vertebrales: las osteoporóticas y las debidas a metástasis, aunque no debemos olvidar las otras causas de aplastamiento vertebral4.
Las vértebras son el elemento del esqueleto que se afecta con mayor frecuencia cuando hay diseminación ósea metastásica (hasta el 40% de las metástasis tienen lugar en la columna). Las localizaciones más frecuentes son las regiones dorsal y lumbar, al igual que las fracturas osteoporóticas. Las neoplasias sólidas que tienen más tendencia a metastatizar en el hueso son por orden las de próstata, mama, riñón, pulmón y tiroides, aunque por orden de incidencia son la mama, próstata y pulmón. Las neoplasias hematológicas también pueden ser causa de fractura, especialmente el mieloma múltiple o el plasmocitoma solitario; también se ha descrito en el curso de la leucemia aguda; al igual que las neoplasias óseas benignas (hemangioma, granuloma eosinófilo, quiste óseo aneurismático y tumor de células gigantes) o malignas (osteosarcoma, condrosarcoma y angiosarcoma)5.
Entre los antecedentes será importante reconocer si el paciente tiene alguna enfermedad de base o está tomando algún fármaco que pueda relacionarse con una enfermedad ósea metabólica o predisponga a infecciones.
En cuanto a la sintomatología, la afectación del estado general sugerirá una etiología neoplásica, la fiebre nos debe hacer pensar en procesos infecciosos; el dolor de la fractura osteoporótica suele ser agudo, intenso y con el tiempo suele disminuir de forma progresiva, a diferencia del neoplásico que es progresivo y refractario a la analgesia. En nuestro enfermo la refractariedad a la analgesia prescrita nos debía hacer sospechar el origen no osteoporótico del aplastamiento4.
Los datos analíticos deben incluir el hemograma, la velocidad de sedimentación globular (VSG), bioquímica completa, proteinograma y analítica de orina. El aumento de VSG nos sugiere la posibilidad de neoplasia o infección, pero su normalidad no la descarta.
La radiología simple proporciona gran cantidad de información, debe abarcar la totalidad de la columna vertebral siendo necesario practicar una proyección posteroanterior y otra lateral. Los signos de benignidad se basan en la integridad ósea (platillos, contornos y pedículos) y la inexistencia de afectación de masa de partes blandas; los signos de malignidad se basan en la demostración de destrucción del hueso (destrucción de estructuras corticales vistas tangencialmente, platillos vertebrales, contornos laterales, pedículos) y la afectación de partes blandas (de muy difícil valoración)6.
La valoración por tomografia computarizada (TC), tiene la ventaja de permitir la valoración individualizada del raquis sin superposiciones y de las partes blandas. Entre los signos de benignidad encontramos en las fracturas corticales sin destrucción ósea la visualización de todos los fragmentos aunque estén discontinuos (signo del puzzle), en la fractura del hueso medular la ausencia de destrucción ósea también es un signo de benignidad, son fracturas lineales, oblicuas o circulares; el pedículo no se afecta en las fracturas benignas. Entre los criterios de malignidad en las fracturas corticales encontramos la imposibilidad de recomponer la vértebra con abombamiento del muro posterior; en el hueso medular observamos áreas osteolíticas con rebordes mal definidos. La destrucción combinada córtico-medular o del pedículo es propia de malignidad. La afectación de partes blandas es propia de malignidad cuando es focal, no es uniforme, ni concéntrica, tiene un grosor superior a los 10 mm o está en el espacio epidural6-8.
La aportación de la IRM es la señal y afectación de la médula ósea y la proyección en múltiples planos. Entre los criterios morfológicos de malignidad encontramos convexidad del borde posterior, afectación del pedículo, presencia en otras vértebras de imágenes nodulares típicas de metástasis8,9.
Creemos que en los casos en que la historia clínica del paciente, los datos analíticos y la radiología simple no aclaren el diagnóstico, la siguiente exploración debería ser la resonancia magnética (capacidad para valorar la médula espinal y sus raíces, determinar características del aplastamiento) o tomografía (capacidad para estudiar en el plano axial la estructura ósea), requiriendo en casos de duda la biopsia ya sea quirúrgica o bajo control radioscópico.